环烷烃的结构环戊烷的构象
环烷烃1ppt课件

环辛烷 环壬烷 环癸烷
663.8 664.6 663.6
环十四烷 658.6 环十五烷 659.0
对比:开链烷烃每个CH2的燃烧热:658.6 KJ/mol
稳定性: 普通环 > 中环:> 小环
环的张力越小,相应的环烷烃越稳定。
环丙烷的结构: CH3
H
H
C
C H 2 1 0 9 .5 ° CH3
HC H
➢ 相同环连结时,可 用词头“联”开头。
顺反异构体:
由于环状结构,环烷烃有两个侧面:“上”方和“下” 方。因此,取代环烷烃可能存在同分异构现象。例如,有两 个1,3-二甲基环戊烷同分异构体:一个异构体的两个甲基在 环的同侧,另一个异构体的两个甲基在环的两侧。两个异构 体都是稳定的化合物。
CH3 CH3
➢ 了解三元和四元环化合物的活性,掌握相应的特殊化学性质。 ➢ 掌握环丙烷和环丁烷的结构特点(有角张力)和构象。 ➢ 了解并掌握环戊烷的构象。
➢ 掌握几种类型环烷烃(普通环烷烃、桥环烃和螺环烃)的命名
方法。
课后练习:p61 (一)、(十)
3 CH3CHCH2CH3
1
主要产物
H2 / Pt, 120oC or Ni, 200oC
CH3CH2CH2CH3
支链多 较稳定
➢ 小环化合物与卤素的反应
Br2 / r.t. Cl2 / FeCl3
Br2 / r.t.
Br Br CH2CH2CH2CH2
(离子型) 加成反应
不反应(难开环)
C H 4 + 2 O 2 C O 2 + 2 H 2 O + 燃 烧 热
环烷烃的燃烧热数据
小 C3 环 C4
普 C5 通 环 C7
第二章 第二节环烷烃
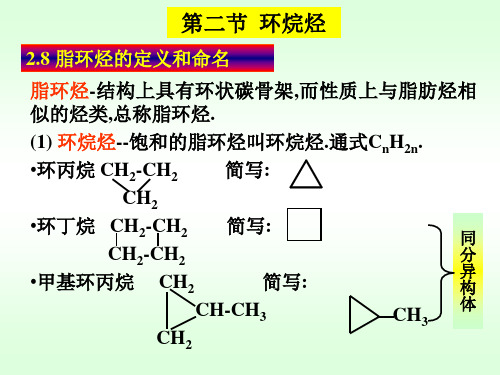
纽曼投影式
透视式
环己烷的椅型构象
(2) 船型构象
• 所有键角也接近 所有键角也接近109.5°,故也没有角 ° 故也没有角 张力.但相邻 但相邻C-H键却并非全是交叉 张力 但相邻 键却并非全是交叉 以及C-5和 的.C-2和C-3上的 C-H 键,以及 和 上的 以及 和 C-6上的 C-H键都是重叠式的 键都是重叠式的. 上的 键都是重叠式的 • C-1和 C-4上两个向内伸的 由于距 上两个向内伸的H由于距 和 上两个向内伸的 离较近而相互排斥,也使分子的能量 离较近而相互排斥 也使分子的能量 有所升高. 有所升高
取代基在e键上的构象较稳定 取代基在 键上的构象较稳定. 键上的构象较稳定 • 若有多个取代基 往往是 e 键取代基最多的构象最稳 若有多个取代基,往往是 取代基最多的构象最稳 定. • 若环上有不同取代基 则体积大的取代基连在 e键上 若环上有不同取代基,则体积大的取代基连在 键 的构象最稳定. 的构象最稳定 二甲基环己烷, 例1: 1,2-二甲基环己烷,顺式如下: 二甲基环己烷 顺式如下: •同一平面上的比较 同一平面上的比较. 同一平面上的比较 •在同侧为顺, a,e 在同侧为顺 在同侧为 •在异侧为反.a,a;e,e. 在异侧为反 在异侧为 •反式 反式(e,e)比顺式的稳定 (a,a)实际上不存在(能量太高) 比顺式的稳定. 反式 比顺式的稳定 )实际上不存在(能量太高)
5 2 3 4
1,2-二甲基环戊烷 二甲基环戊烷
• 例2:
例3:
1-甲基 乙基环己烷 甲基-3-乙基环己烷 甲基
1,1,4-三甲基环己烷 三甲基环己烷
**小取代基为 位. 小取代基为1位 小取代基为
环烷的顺反异构: 环烷的顺反异构 由于碳原子连接成环,环上 单键不能自由旋转. 由于碳原子连接成环 环上C-C单键不能自由旋转 环上 单键不能自由旋转 只要环上有两个碳原子各连有不同的原子或基团, 只要环上有两个碳原子各连有不同的原子或基团 就有构型不同的顺反异构体. 就有构型不同的顺反异构体 例: 1,4-二甲基环己烷 二甲基环己烷
第二章 烷烃和环烷烃

第二节 同系列和同分异构现象
一、同系列和同系物 • 烷 烃 的 分 子 通 式 为 CnH2n+2 , 环 烷 烃 的 分 子 通 式 为 CnH2n。 • 凡是具有同一分子通式和相同结构特征的一系列化合 物称为同系列(homologous series)。 • 同系列中的化合物互称同系物(homolog)。 • 同系物具有相似的化学性质,物理性质也随着碳链的 增长而表现出有规律的变化。
第 二 章 烷烃 环烷烃
exit
烃(hydrocarbons):
只含有C、H 两种元素的化合物 —— 碳氢化合物
碳原子之间均以C-C单键相连,其 余的价键均为H原子所饱和。 (saturated 烷烃 (alkanes) :甲烷、乙烷等; hydrocarbons) 环烷烃(cycloalkanes):
三级戊基 (Tert or t )
三级丁基 叔丁基
新戊基 (neo)
*3 有机化合物系统命名的基本格式
构型 +
R, S; D, L; Z, E; 顺,反
取代基
+
母体
官能团位置号 +名称
取代基位置号 + 个数 + 名称
(有多个取代基时,中文按顺 (没有官能团时 序规则确定次序,较优的在后。 不涉及位置号) 英文按英文字母顺序排列)
(1) 直链烷烃的命名: 含10个碳原子以内的直链烷烃, 从1-10依次用 天干名称甲、乙、丙、丁、戊、己、庚、辛、壬、 癸加上烷来命名; 而含碳原子10个以上的直链烷烃, 用数目加上烷来命名(P27) 。
(2) 支链烷烃的命名 *1 碳原子的级
CH3 H3C C CH3 CH2 CH3 CH
1oH 2oH 3oH
立体化学 第5章 环烷烃
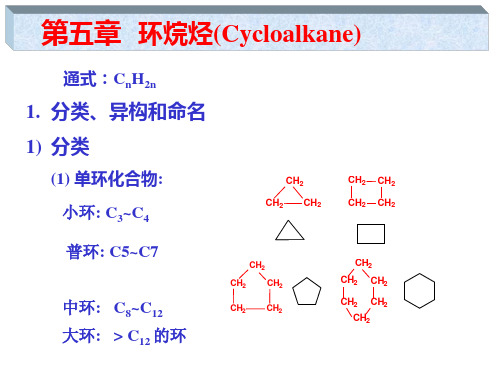
1,2,4-三甲基环己烷
C. 必要时须注明立体构型;
D. 复杂化合物也可将环的部分当作取代基。
顺-1,2-二甲基环丙烷 反-1,3-二甲基环丁烷
4-环戊基庚烷
(2) 多环化合物的命名:
(命名较为复杂, 以二环化合物为例). A. 参加成环的总碳原子数作为母体烃; 如有8个碳原子,则称为辛烷 B. 简单桥环可用“二环”、“三环”等作词头; C. 二环“连接”处的碳原子为桥头碳原子; D. 从桥头碳原子处,由大环开始编号;将各“桥”所含的碳原子 数写入方括号中(注意:桥头C原子都不可计入)。
2) 环戊烷的构象
环戊烷的结构是以拆叠的形式存在,四个C原子基本在一 平面上,另一个C则在平面之外,这种构象称为信封式构象。 环戊烷由于以“信封式”构象存在,使分子张力较小,化学性 质较稳定。
3) 环己烷的构象及构象分析
i) 椅式和船式构象
椅式
船式
船式构象相对能量较高, 不稳定,通过C-C键扭曲, 使其成为扭曲式(或称为扭 船型)。这种构象相对于船 式能量低。
角张力---由于键角偏离正常键角 而产生的张力。
环丙烷的三个C在同一平而上,相邻两个C上的C-H键都是重叠式构象, 相互拥挤,产生排斥,也具有较高的能量。
扭转张力---由于重叠式构象而产生的张力。
4. 环烷烃的构象和构象分析
1) 环丁烷的构象
环丁烷的四个C不在同一平面上,形如蝴蝶。即通过C-C键的扭转而以 一个拆叠的碳环存在。 环丁烷的三个C原子分布在同一平面,另一个C取于平面之外。 环丁烷的这种存在形式可使环的张力降低,但仍然是一个不稳定分子。
(1)分子中有两个平行的平面,C1、C3、C5和C2、C4、C6;
(2)12个氢原子分成两类:一类与分子对称轴平行,即垂直于环平面,称为
有机化学第三章环烷烃

※ 在不同的环烃中键角大于或小于 109o28’,而正常的 SP3 杂化轨道之间的夹角为 109°28′ 即 C - C 之间的电子云 没有达到最大程度的重叠。
1 (109° 28′-60° )= 24° 64′ 2 1 (109° 28′-90° )= 9° 44′ 2 1 (109° 28′-108° )= 0° 44′ 2 1 (109° 28′-120° )= -5° 16′ 2
两个环共用两个或两个以上碳原子的化合物称桥环化合物。
3、环戊烷的结构
C:sp3杂化,轨道夹角109.5o,五边形内角为108o角张力: 109.5-108=1.5o 可见,环戊烷分子中几乎没有什么角张力,故五元 比较稳定,不易开环,环戊烷的性质与开链烷烃相似。
事实上,环戊烷分子中的五个碳原子亦不共 平面,而主要是以“信封式”构象存在,使 五元环的环张力可进一步得到缓解。
二、化学性质
结构分析:C-C, C-H σ键牢固,化性稳定,似烷烃;
但C3—C4环易破,环可以加成,似烯烃。
1、取代反应
+ Cl2 光照 + HCl Cl Cl + HCl
+ Cl2
加热 300oC
反应条件加强, 反应程度减弱。
2、加成反应
小环烷烃,特别是环丙烷,和一些试剂作用时易发生开环。 A: 加氢(随碳原子数增加,环的稳定性增加;加氢反应条 件也愈苛刻)
7 6 5 4 3
9 1 2 8
10
1 2 5
7
6
5 4
3 2 1 CH3
7 CH3
6
4
3
8
9
螺[2, 4]庚烷
7-甲基螺[4, 5]癸烷
1-甲基螺[3,5]-5-壬烯
有机化学:第五章 环烷烃

? CH3 C CH3 CHC3H3
CH3 H3C CHC3H3
e, a构象
e, a构象
33
1,3-二取代环己烷的构象
CH3
CH3
CH3 CH3
CH3 CH3
e, a构象
CH3 CH3
H3C
CH3
a, a构象
e, e构象,优势
34
小结:
1°环己烷有两种极限构象(椅式和船式),椅式为优势构象。 2°一元取代基主要以e键和环相连。 3°多元取代环己烷最稳定的构象是e键上取代基最多的构象。 4°环上有不同取代基时,大的取代基在e键上构象最稳定。
1885年,Baeyer提出了张力学说(strain theory):
a. 形成环的C原子都在同一平面上,并排成正多 边形; b. 在不同环中C-C键之间的夹角小于或大于正四 面体所要求的角度:109°28′; c. 环中C-C键键角的变形会产生张力,键角变形 的程度越大,张力越大,环的稳定性低,反应活 性越大。
+
Cl2
+
Cl2
+
Cl2
+
Br2
+
Cl2
hv hv 300 oC hv hv
Cl Cl
Cl Br
Cl
10
氧化反应
KMnO4
O + CO2H
O3
( Z)
Zn/H2O
OHC
CHO
11
中小环的加成反应
加氢反应
+
H2
+
H2
+
H2
Ni 80 oC
Ni 100 oC
Pt 300 oC
环烷烃(环丙烷、环丁烷、环戊烷、环己烷)的构象

环烷烃的构象链状化合物的构象是由基团绕C—Cσ键旋转产生的;而环状化合物的构象至少涉及到两个C—Cσ键和其键角的转动和变化,有时还涉及到键长和键角的变化,比较复杂,常称环的翻转。
一、环丙烷的构象环丙烷是三个碳的环,只能是平面构象,即它的构型。
尽管只有一种构象,但这个环极不稳定,主要因为:1、所有C-H键都是重叠构象,扭转张力大。
2、C原子是不等性杂化或弯曲键,有“角张力”存在。
二、环丁烷的构象环丁烷有两种极限构象:动画演示:平面式构象:象环丙烷一样,不稳定,存在扭转张力和“角张力”。
蝶式构象:能缓解扭转张力和角张力,呈蝶式构象。
通过平面式构象,由一种蝶式翻转成为另一种蝶式构象,处于动态平衡。
蝶式是优势构象。
也有扭转能力和角张力存在。
三、环戊烷的构象环戊烷的构象主要是信封式和半椅式构象。
两者处于平衡。
因为平面构象能量较大,一般认为环戊烷采取这种构象可能性很少。
E相对=19kJ/mol 信封式半椅式四、环己烷的构象环己烷的构象经过近百年的努力才建立起来。
Baeyer 1885年提出张力学说,认为环状化合物是平面构型Sachse 1889年质疑张力学说只适合小环,提出环已烷有船式、椅式两种构象。
Hassel 1930年利用偶极矩测定法和电子衍射法研究环已烷构象,∠CCC=109.5°,气相、液相中环已烷几乎全是椅式构象。
Barton 1950年发展了构象理论,以甾族化合物为对象提出构象分析,把构象分析明确地引入有机化学中。
Hassel 和Barton获1969年Nobel化学奖1、椅式和船式构象环已烷保持碳原子的109.5°键角,提出了椅式和船式构象.1)椅式构象:C1、C2、C4、C5在一个平面上,C6和C3分别在平面的下面和平面的上面,很象椅脚和椅背,故称“椅式”。
2)船式构象:C1、C2、C4、C5在一个平面上,C3和C6在平面上面。
形状象只船,C3和C6相当船头和船尾,故称“船式”。
脂环烃的定义和命名
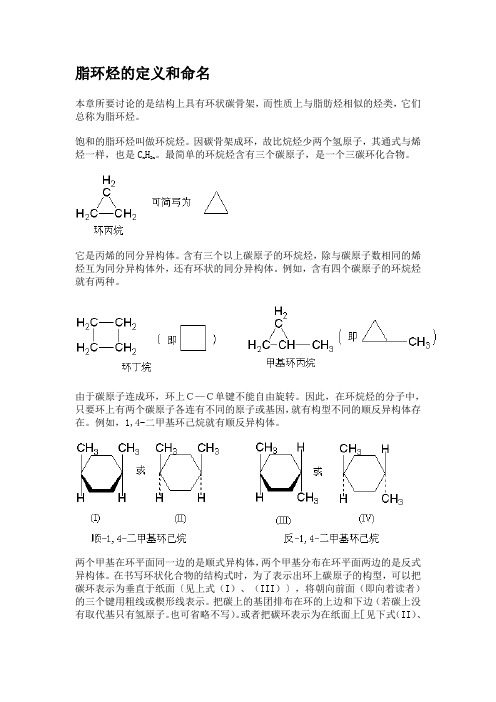
脂环烃的定义和命名本章所要讨论的是结构上具有环状碳骨架,而性质上与脂肪烃相似的烃类,它们总称为脂环烃。
饱和的脂环烃叫做环烷烃。
因碳骨架成环,故比烷烃少两个氢原子,其通式与烯烃一样,也是Cn H2n。
最简单的环烷烃含有三个碳原子,是一个三碳环化合物。
它是丙烯的同分异构体。
含有三个以上碳原子的环烷烃,除与碳原子数相同的烯烃互为同分异构体外,还有环状的同分异构体。
例如,含有四个碳原子的环烷烃就有两种。
由于碳原子连成环,环上C—C单键不能自由旋转。
因此,在环烷烃的分子中,只要环上有两个碳原子各连有不同的原子或基因,就有构型不同的顺反异构体存在。
例如,1,4-二甲基环己烷就有顺反异构体。
两个甲基在环平面同一边的是顺式异构体,两个甲基分布在环平面两边的是反式异构体。
在书写环状化合物的结构式时,为了表示出环上碳原子的构型,可以把碳环表示为垂直于纸面〔见上式(I)、(III)〕,将朝向前面(即向着读者)的三个键用粗线或楔形线表示。
把碳上的基团排布在环的上边和下边(若碳上没有取代基只有氢原子。
也可省略不写)。
或者把碳环表示为在纸面上[见下式(II)、(IV)],把碳上的基团排布在环的前方和后方,用实线表示伸向环平面前方的键,虚线表示伸向后方的键。
脂环烃的环上有双键的叫做环烯烃。
有两个双键和有一个叁键的则分别叫做环二烯烃和环炔烃。
它们的命名也与相应的开链烃相似。
以不饱和碳环作为母体,侧链作为取代基。
环上碳原子编号顺序应是不饱和键所在位置号码最小。
对于只有一个不饱和键的环烯(或炔)烃,因不饱和键总是在C(1)一C(2)之间,故双键(或叁键)的位置也可以不标出来。
例如:带有侧链的环烯烃命名时,若只有一个不饱和碳上有侧链,该不饱和碳编号为1;若两个不饱和碳都有侧链,或都没有侧链,则碳原子编号顺序除双键所在位置号码最小外,还要同时以侧链位置号码的加和数较小为原则。
例如:分子中含有两个碳环的是双环化合物。
其中两个环共用一个碳原子的叫做螺环化合物;共用两个或更多个碳原子的叫做桥环化合物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Ⅱ、芳香烃 > 一、单环芳香烃
当引入的烷基为三个碳以上时,引入的烷基会发生碳 链异构现象。
+ CH3CH=CH2
+ CH3CHCH3
OH
AlCl 3 H+
CH3 CH
CH3
CH3 CH
CH3
Ⅱ、芳香烃 > 一、单环芳香烃
酰基化反应:
O
+ CH3C
Cl
乙酰氯
AlCl 3
O
CH3 + HCl
甲基苯基酮 苯乙酮 97%
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象 3.一元取代环己烷的构象
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象
4、二元取代环己烷的构象
CH3 CH3 (顺式) CH3 CH3
(反式)
CH3
CH3 只能是e,a 构象
CH3
a,a
CH3 构象
CH3 CH3
e,e 构象 (优势构象)
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象
CH3
CH3
(反式)
CH3 CH3
CH3 H
H CH3
只有e,a 构象 (其中有大的基团时,则在 e键上)
CH3
CH3
H CH3
H CH3
(顺式)
a,a 构象
e,e 构象 (优势构象)
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象
小结: 1°环己烷有两种极限构象(椅式和船式),椅 式为优势构象。 2°一元取代基主要以e键和环相连。 3°多元取代环己烷最稳定的构象是e键上取代基 最多的构象。 4°环上有不同取代基时,大的取代基在e键上构 象最稳定。
COOH
SO3H
CHO
OH
NH2
苯甲酸
பைடு நூலகம்
苯磺酸
CH=CH 2
苯甲醛
苯酚
CH3
CH3-CH2-CH-C-CH 2-CH3 CH3
苯胺
苯乙烯
3,3-二甲基-4-苯基己烷
Ⅱ、芳香烃
二元取代苯的命名:
取代基的位置用邻、间、对或2、 3、 4表示。
CH3 H3C
CH3
CH3
CH3
CH3
邻二甲苯 (1,2-二甲苯) (o- 二甲苯)
Ⅱ、芳香烃 > 一、单环芳香烃
1、卤代反应历程
Br2
Br-Br FeBr3
H [FeBr4]-
Br
π 络合物
2、硝化反应历程
σ 络合物
HONO2 + HOSO2OH + NO2
[H2O+-NO2] + SO4H
NO2
- H2O
NO2
H
- H+
NO2
H+ + SO4H
π 络合物 H2SO4
σ 络合物
Br
Br
CH3 CH3
CH3 C-CH-CH2 Br Br
CH2-CH2-CH2-CH2
Br
Br
溴褪色 可用于 鉴别环 烷烃
Br2/CCl4
不起加成,而是取代反应
Ⅰ、脂环烃 〉三 、脂环烃的性质
普通脂环烃具有开链烃的通性,环烷烃主要 是起自由基取代反应。
300℃ Br2
CH3
光
Cl2
Br HBr
CH3
Cl
+ HCl
Br
+ HBr
Cl
+
Cl Cl
50%
Cl
+ 2HCl
45%
Ⅱ、芳香烃 > 一、单环芳香烃
(2)硝化反应
浓HNO3
浓H2SO4 55~60℃
NO2
H2O
硝基本(98%)
浅黄色液体,很毒,能与 血液中的血红素作用。
浓H2SO4的作用——促使+NO2离子(硝基正离子)的 生成。
HNO3
水中 H2SO4中
H
120°
H
0.1397nm
H
120°
0.1397nm
H
H
0.110nm H
正六边形结构 所有的原子共平面 C-C 键长均为 0.1397nm C-H 键长均为 0.110nm 所有键角都为 120°
Ⅱ、芳香烃 > 一、单环芳香烃 杂化轨道理论解释:
Ⅱ、芳香烃 > 一、单环芳香烃
(二)物理性质 芳香烃一般为无色有芳香味的液体,不溶于水, 但溶于有机溶剂,如乙醚、四氯化碳、石油醚等非极 性溶剂。一般芳香烃均比水轻,相对密度在0.860.93 ;是良好的溶剂,有一定的毒性;沸点随相对 分子量升高而升高;熔点除与相对分子质量有关外, 还与结构有关,通常对位异构体由于分子对称,熔点 较高。
Ⅰ、脂环烃 〉一、环烷烃的结构
环戊烷的构象:
0.05nm
这种构象的张力 很小,总张力能 25KJ/mol,扭转张力在 2.5KJ/mol 以 下 , 因此 , 环戊烷的化环戊烷的构 象学性质稳定。
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象 1.两种极限构象——椅式和船式
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象
Ⅰ、脂环烃 〉三 、脂环烃的性质
1.催化氢化
H2
Ni 80℃
H2
Ni 200℃
Pd H2 >300℃
2.与溴作用
CH3CH2CH3 CH3CH2CH2CH3 CH3CH2CH2CH2CH3
Ⅰ、脂环烃 〉三 、脂环烃的性质
Br2/CCl4
CH3 CH3 CH3
Br2/CCl4
Br2/CCl4
CH2-CH2-CH2
CH3
O
+ CH3C O
CH3C
O
乙酸酐
AlCl 3
O
CH3
CH3 + CH3COOH
甲基对苯基酮 对甲基苯乙酮 80%
Ⅱ、芳香烃 > 一、单环芳香烃
2、加成反应 苯环易起取代反应而难起加成反应,但并不是绝 对的,在特定条件下,也能发生某些加成反应。
Ni,P + 3H2
180~250 ℃
光 + 3Cl2
AlCl 3
Ⅱ、芳香烃 > 一、单环芳香烃
Ⅱ、芳香烃 > 一、单环芳香烃
(五)苯环上取代基的定位效应
混酸 60 ℃
CH3
混酸 30 ℃
NO2
NO2
发烟HNO3+H2SO4
95 ℃
NO2
93.2%
硝基苯的硝化比苯 困难,新引入的取代 基主要进入原取代 基的间位。
CH3 NO2
57%
CH3
NO2
甲苯的硝化比苯 容易,新引入的取 代基主要进入原 取代基的邻对位。
50℃
H Cl
H Cl
H Cl
Cl H
Cl H
H Cl
六六六 对人畜有害,世界禁用, 我国从83 年禁用。
Ⅱ、芳香烃 > 一、单环芳香烃 3、氧化反应
Ⅱ、芳香烃 > 一、单环芳香烃
若两个烃基处在邻位,氧化的最后产物是酸酐。
CH2CH3 CH(CH3)2
O2, V2O5 350~450 ℃
O O
O
Ⅱ、芳香烃
芳烃,也叫芳香烃,一般是指分子中含苯环 结构的碳氢化合物。
芳香二字的来由最初是指从天然树脂(香精 油)中提取而得、具有芳香气的物质。
现代芳烃的概念是指具有芳香性的一类环状 化合物,它们不一定具有香味,也不一定含有苯 环结构。
Ⅱ、芳香烃
Ⅱ、芳香烃 基的概念: 芳烃分子去掉一个氢原子所剩下的基团称为 芳基(Aryl)用Ar表示。重要的芳基有:
以减少可逆反应的发生。
磺化反应是可逆的,苯磺酸与稀硫酸共热时可 水解脱下磺酸基。
SO3H
+ H2O
180 ℃
+ H2SO4
Ⅱ、芳香烃 > 一、单环芳香烃
CH3
CH3
CH3
+ H2SO4
SO3H +
烷基苯比苯易磺化
邻甲基苯磺酸
SO3H
对甲基苯磺酸
反应温度不同 0℃
43%
53%
产物比例不同 25℃
32%
汪小兰《有机化学》第四版CAI教学配套课件
主讲:谢启明 教授
谢启明制作
第四章 环 烃 Ⅰ、脂环烃
Ⅱ、芳香烃 Ⅲ、煤焦油和石油
Ⅰ、脂环烃
一、环烷烃的结构 二、环已烷及其衍生物的构象 三 、脂环烃的性质
Ⅰ、脂环烃
Ⅰ、脂环烃
Ⅰ、脂环烃 当环状化合物上有支链时,支链不大,以环 作为母体化合物命名;支链较大,环作为取代基 而命名。
NO2 混酸 NO2
CH3 NO2
110℃
NO2
NO2
2,4,6-三硝基甲苯
(TNT)
Ⅱ、芳香烃 > 一、单环芳香烃
(3)磺化反应
80℃ + 浓 H2SO4
H2SO4, SO3 30~50℃
SO3H
+ H2O 反应可逆,生成的水
使 H2SO4 变稀,磺化速度
变慢,水解速度加快,故
SO3H
常用发烟硫酸进行磺化,
2.平伏键(e键)与直立键(a键)
对称轴
H
H
H
H
H H
H
H H
H H
H
环己烷的直立键和平伏键
直立键 平伏键
Ⅰ、脂环烃 〉二、环已烷及其衍生物的构象
在室温时,环己烷的椅式构象可通过C-C键的转动 (而不经过碳碳键的断裂),由一种椅式构象变为另一 种椅式构象,在互相转变中,原来的a键变成了e键,而 原来的e键变成了a键。
