分析光谱分析法之——红外吸收光谱法.
仪器分析3—红外吸收光谱法

傅立叶变换红外光谱仪
样品池
红外光源
摆动的 凹面镜
迈克尔逊 干扰仪
参比池
摆动的 凹面镜
检测器 干涉图谱 计算机 解析 还原
M1 II
同步摆动
I M2
红外谱图
BS
D
仪器组成
第五节 红外光谱法应用
红外光谱法由于操作简单,分析速度 快,样品用量少,不破坏样品,特征性 强等优点,在有机定性分析中应用广泛。 利用红外光谱可对化合物进行鉴定或结 构测定。 但由于吸收较复杂,在定量分析方面 应用受到一定限制。
第四章 红外吸收光谱分析法(IR)
Infrared Absorption Spectrometry
第一节
红外光谱基本知识
1、红外线波长范围: 光学光谱区域:10nm ~1000μm; 其中:10nm ~400nm为紫外光区 400nm ~760nm为可见光区, 760nm ~ 1000μm为红外光区。 为表示方便,红外光不用nm(纳米) 而用微米( μm)表示其波长。
由原理图可见,红外分光光度计也主要 由光源、样品吸收池、单色器、检测器、 记录仪等部件构成。 1、光源:能斯特灯或硅碳棒
红外光谱仪中所用的光源通常是一种惰性固体,用 电加热使之发射高强度的连续红外辐射。 常用的是Nernst灯或硅碳棒。 Nernst灯是用氧化锆、氧化钇和氧化钍烧结而成的 中空棒和实心棒。工作温度约为1700℃,在此高温下导 电并发射红外线。但在室温下是非导体,因此,在工作 之前要预热。它的特点是发射强度高,使用寿命长,稳 定性较好。 硅碳棒是由碳化硅烧结而成,工作温度在1200-1500℃ 左右。
ε>100 非常强峰(vs) 20<ε<100 强 峰(s) 10<ε<20 中强峰(m) 1<ε<10 弱 峰(w)
仪器分析-红外吸收光谱法

第 6 章红外吸收光谱法6.1 内容提要6.1.1 基本概念红外吸收光谱——当用红外光照射物质时,物质分子的偶极矩发生变化而吸收红外光光能,有振动能级基态跃迁到激发态(同时伴随着转动能级跃迁),产生的透射率随着波长而变化的曲线。
红外吸收光谱法——利用红外分光光度计测量物质对红外光的吸收及所产生的红外光谱对物质的组成和结构进行分析测定的方法,称为红外吸收光谱法。
振动跃迁——分子中原子的位置发生相对运动的现象叫做分子振动。
不对称分子振动会引起分子偶极矩的变化,形成量子化的振动能级。
分子吸收红外光从振动能级基态到激发态的变化叫做振动跃迁。
转动跃迁——不对称的极性分子围绕其质量中心转动时,引起周期性的偶极矩变化,形成量子化的转动能级。
分子吸收辐射能(远红外光)从转动能级基态到激发态的变化叫做转动跃迁。
伸缩振动——原子沿化学键的轴线方向的伸展和收缩的振动。
弯曲振动——原子沿化学键轴线的垂直方向的振动,又称变形振动,这是键长不变,键角发生变化的振动。
红外活性振动——凡能产生红外吸收的振动,称为红外活性振动,不能产生红外吸收的振动则称为红外非活性振动。
诱导效应——当基团旁边连有电负性不同的原子或基团时,通过静电诱导作用会引起分子中电子云密度变化,从而引起键的力常熟的变化,使基团频率产生位移的现象。
共轭效应——分子中形成大键使共轭体系中的电子云密度平均化,双键力常数减小,使基团的吸收频率向低波数方向移动的现象。
氢键效应——氢键使参与形成氢键的原化学键力常数降低,吸收频率将向低波数方向移动的现象。
溶剂效应——由于溶剂(极性)影响,使得吸收频率产生位移现象。
基团频率——通常将基团由振动基态跃迁到第一振动激发态所产生的红外吸收频率称为基团频率,光谱上出现的相应的吸收峰称为基频吸收峰,简称基频峰。
振动偶合一一两个相邻基团的振动之间的相互作用称为振动偶合。
基团频率区一一红外吸收光谱中能反映和表征官能团(基团)存在的区域。
红外吸收光谱法

).未知物结构的测定 ( 2 ).未知物结构的测定
基本方法: 基本方法:图谱解析 测绘样品的红外谱图 分析吸收峰的位置、形状、强度等要素 分析吸收峰的位置、形状、 确定分子中所含的基团或化学键 推断分子的结构
步骤1 步骤1: 准备工作 了解样品的来源、制备过程、外观、 了解样品的来源、制备过程、外观、 纯度、 纯度、经元素分析后确定的化学式以及熔 沸点、溶解性质等物理性质, 点、沸点、溶解性质等物理性质,取得对 样品有个初步的认识或判断
特点 光谱来源:分子振动和转动; 光谱来源:分子振动和转动; 样品:气态、液态、固态样品; 样品:气态、液态、固态样品; 应用:结构分析。 应用:结构分析。
一、
红外吸收光谱法的基本原理
1、红外光谱(IR)的产生 、红外光谱 的产生 样品受到的红外光照 射时, 射时,分子吸收其中 一些频率的辐射, 一些频率的辐射,发 生振-转能级的跃迁, 生振-转能级的跃迁, 分子的偶极矩发生变 即得红外光谱。 化,即得红外光谱。
3. 单色器
组成:色散元件、准直镜和狭缝。 组成:色散元件、准直镜和狭缝。 棱镜: 单晶。 棱镜:LiF、CaF2、NaF、KBr单晶。 、 、 单晶 光栅:可用几个光栅组合。 光栅:可用几个光栅组合。
三、
红外光谱法的应用
1
).已知物的鉴定 ( 1 ).已知物的鉴定 ).未知物结构的测定 ( 2 ).未知物结构的测定
二、色散型红外光谱仪
与紫外可见分光光度计对比 基本组成部件相似: 均有光源、吸收池、 基本组成部件相似: 均有光源、吸收池、单 相似 色器、检测器等。 色器、检测器等。 每个部件的结构、材料和性能不同: 每个部件的结构、材料和性能不同: 不同 如光源、吸收池等。 如光源、吸收池等。
仪器分析课件-第10章-红外光谱分析法

13:15:17
红外光谱分析基本原理
三、 分子的振动形式
两类基本振动形式:变形振动和伸缩振动。以甲烷为例:变形振动
13:15:17
红外光谱分析基本原理
五. 红外光谱峰的吸收强度 P297
这种方法适用于组分简单,样品厚度一定(一般在液体样品 池中进行),特征吸收谱带重叠较少,而浓度与吸光度不成线性 关系的样品。
13:15:17
红外光谱的应用
3 .吸收度比法 该发适用于厚度难以控制或不能准确测定其厚度的样品,例如厚度不均匀 的高分子膜,糊状法的样品等。这一方法要求各组分的特征吸收谱带相互 不重叠,且服从于郎伯 — 比尔定律。 如有二元组分 X 和 Y ,根据 朗伯 -比尔定律 ,应存在以下关系;
1.位置:由振动频率决定,化学键的力常数 K 越大,原子折合质量 m 越小, 键的振动频率越大,吸收峰将出现在高波数区(短波长区);反之,出现在低 波数区(高波长区); 2.峰数:分子的基本振动理论峰数,可由振动自由度来计算,对于由 n 个原子 组成的分子,其自由度为3 n
3n= 平动自由度+振动自由度+转动自由度 分子的平动自由度为3,转动自由度为:非线性分子3,线性分子2
13:15:17
红外光谱的应用
二、定性分析
定性分析大致可分为官能团定性和结构定性两个方面。 定性分析的一般过程: 1. 试样的分离和精制 2.了解与试样性质有关的其它方面的材料 3. 谱图的解析 4. 和标准谱图进行对照 5. 计算机红外光谱谱库及其检索系统 6. 确定分子的结构
13:15:17
红外光谱的应用
红外光谱分析法

例题: 由表中查知C=C键旳k=9.5 9.9 ,令其为 9.6, 计算波数值。
v 1 1 k 1307 k 1307 9.6 1650cm1
2c
12 / 2
正己烯中C=C键伸缩振动频率实测值为1652 cm-1
只合用于双原子分子和影响原因小旳多原子分子,实 际旳分子构造中,基团与基团间、基团旳化学键之间 都会有影响而造成振动波数旳变化
例:计算C-C、C=C、C≡C旳振动波数? 已知键旳力常数分别为5、10、15N·cm-1
某些键旳伸缩力常数(毫达因/埃)
键类型 力常数 峰位
—CC — > —C =C — > —C — C —
15 17 9.5 9.9
4.5 5.6
4.5m
6.0 m
7.0 m
化学键键强越强(即键旳力常数K越大)原子折合质量 越小,化学键旳振动频率越大,吸收峰将出目前高波数区。
1、红外光谱旳区域划分 常见旳化学基团在4000-670 cm-1范围内有
特征吸收。常将该波数范围提成四个区域 (1)X-H伸缩振动区 4000-2500 cm-1 (2)叁键和积累双键区 2500-1900 cm-1 (3)双键伸缩振动区 1900-1200 cm-1 (4)X-Y伸缩振动及X-H变形振动区
特征吸收:指基团在特定旳区域有吸收,且其他 部分对此吸收位置旳影响较小,并有较强旳吸收谱带。
最有分析价值旳基团频率在4000 cm-1 ~ 1300 cm-1 之间, 这一区域称为基团频率区、官能团区或特征区。区内旳峰是由 伸缩振动产生旳吸收带,比较稀疏,轻易辨认,常用于鉴定官 能团。
在1300 cm-1 ~600 cm-1 区域内,除单键旳伸缩振动外,还 有多数基团因变形振动产生旳谱带。这种振动与整个分子旳构 造有关。当分子构造稍有不同步,该区旳吸收就有细微旳差别, 并显示出分子特征,称为指纹区。
红外吸收光谱分析
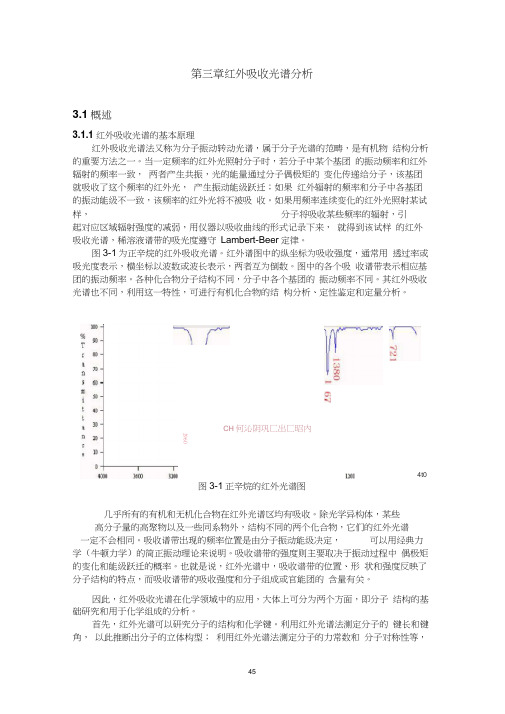
第三章红外吸收光谱分析3.1概述3.1.1红外吸收光谱的基本原理红外吸收光谱法又称为分子振动转动光谱,属于分子光谱的范畴,是有机物 结构分析的重要方法之一。
当一定频率的红外光照射分子时,若分子中某个基团 的振动频率和红外辐射的频率一致, 两者产生共振,光的能量通过分子偶极矩的 变化传递给分子,该基团就吸收了这个频率的红外光, 产生振动能级跃迁;如果 红外辐射的频率和分子中各基团的振动能级不一致,该频率的红外光将不被吸 收。
如果用频率连续变化的红外光照射某试样, 分子将吸收某些频率的辐射,引 起对应区域辐射强度的减弱,用仪器以吸收曲线的形式记录下来, 就得到该试样 的红外吸收光谱,稀溶液谱带的吸光度遵守 Lambert-Beer 定律。
图3-1为正辛烷的红外吸收光谱。
红外谱图中的纵坐标为吸收强度,通常用 透过率或吸光度表示,横坐标以波数或波长表示,两者互为倒数。
图中的各个吸 收谱带表示相应基团的振动频率。
各种化合物分子结构不同,分子中各个基团的 振动频率不同。
其红外吸收光谱也不同,利用这一特性,可进行有机化合物的结 构分析、定性鉴定和定量分析。
图3-1正辛烷的红外光谱图几乎所有的有机和无机化合物在红外光谱区均有吸收。
除光学异构体,某些高分子量的高聚物以及一些同系物外,结构不同的两个化合物,它们的红外光谱 一定不会相同。
吸收谱带出现的频率位置是由分子振动能级决定, 可以用经典力 学(牛顿力学)的简正振动理论来说明。
吸收谱带的强度则主要取决于振动过程中 偶极矩的变化和能级跃迁的概率。
也就是说,红外光谱中,吸收谱带的位置、形 状和强度反映了分子结构的特点,而吸收谱带的吸收强度和分子组成或官能团的 含量有关。
因此,红外吸收光谱在化学领域中的应用,大体上可分为两个方面,即分子 结构的基础研究和用于化学组成的分析。
首先,红外光谱可以研究分子的结构和化学键。
利用红外光谱法测定分子的 键长和键角, 以此推断出分子的立体构型; 利用红外光谱法测定分子的力常数和 分子对称性等,CH 何沁阴巩匚出匚昭內 4t02960根据所得的力常数就可以知道化学键的强弱;由简正频率来计算热力学函数等等。
仪器分析 第四章--红外吸收光谱法

章节重点:
分子振动基本形式及自由度计算;
红外吸收的产生2个条件;
各类基团特征红外振动频率;
影响红外吸收峰位变化的因素。
第八章 红外吸收光谱分 析法
第三节 红外分光光度计
1. 仪器类型与结构
2. 制样方法
3. 联用技术
1. 仪器类型与结构
两种类型:色散型 干涉型(傅立叶变换红外光谱仪)
弯曲振动:
1.4 振动自由度
多原子分子振动形式的多少用振动自由度标示。
三维空间中,每个原子都能沿x、y、z三个坐标方向独 立运动,n个原子组成的分子则有3n个独立运动,再除 掉三个坐标轴方向的分子平移及整体分子转动。
非线性分子振动自由度为3n-6,如H2O有3个自由度。 线性分子振动自由度为3n-5,如CO2有4个自由度。
某些键的伸缩力常数:
键类型: 力常数: 峰位:源自-CC15 2062 cm-1
-C=C10 1683 cm-1
-C-C5 1190 cm-1
-C-H5.1 2920 cm-1
化学键键强越强(即键的力常数K越大),原子折合 质量越小,化学键振动频率越大,吸收峰在高波数区。
1.2 非谐振子
实际上双原子分子并非理想的谐振子!随着振动量子 数的增加,上下振动能级间的间隔逐渐减小!
(1)-O-H,37003100 cm-1,确定醇、酚、酸 在非极性溶剂中,浓度较小(稀溶液)时,峰形尖锐 ,强吸收;当浓度较大时,发生缔合作用,峰形较宽。
注意区分: -NH伸缩振动:3500 3300 cm-1 峰型尖锐
(2)饱和碳原子上的-C-H -CH3 2960 cm-1 2870 cm-1 反对称伸缩振动 对称伸缩振动
第十四章 红外吸收光谱法

§14-1 红外吸收光谱基本原理
红外吸收光谱图
吸收带在光谱图中的位置可用波长(μ m)或波数(cm-1) 表示(横坐标)。光谱图的纵坐标,即吸收强度,可用百 分透光度或吸光度表示。
吸收峰出现的频率位置:由分子的振动能级差决定; 吸收峰的个数:由分子振动自由度的数目决定;
吸收峰的强度:取决于振动过程中偶极矩的变化以及 能级的跃迁几率。
它们主要包括X-H、C≡X和C=X的伸缩振动。
2、指纹区
1300 cm-1以下的区域
主要属C-X的伸缩振动和H-C的弯曲振动频
率区。由于这些化学键的振动容易受附近化学键的
振动的影响,因此结构的微小改变可使这部分光谱
面貌发生差异。就如同每人指纹有差别一样,故 1300-700cm-1区间称指纹区。利用指纹区光谱 可识别一些特定分子。
3N=平动自由度+转动自由度+振动自由度
分子的平动和转动自由度
线型分子
非线型分子
平动自由度:3个 转动自由度:3个
平动自由度:3个 转动自由度:2个
分子的振动自由度
线型分子振动自由度的数目: 振动自由度=3N-平动自由度-转动自由度 =3N-5; 非线型分子振动自由度的数目: 振动自由度=3N-6 任何一个复杂分子的振动,都可视作由3N-6或 3N-5个简正振动叠加而成。
二、 影响基团频率位移的因素
影响频率位移的因素有内部因素和外部因素:
(一)外部因素 样品的状态、测定温度及溶剂极性等外部因素均会影响振 动频率: 1、状态:气态时因分子间作用力小,可观察到振动及转 动光谱的精细结构,且频率高。液态、固态分子间作用力大, 且当有极性基团存在时可能发生分子间缔合或氢键而使频率、 形状、强度都有变化,一般频率较低; 温度:在低温下,吸收带尖锐,随温度升高,带宽增加, 带数减小; 溶剂:由于溶质和溶剂间相互作用,频率有所变化。极性 溶剂使吸收带向低频方向移动;溶液浓度不同,分子间作用 力不同,频率也有变化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2 L 2 3 L 3
合频峰 L 1 2 差频峰(即υ=1→υ=2,3- - -产生的峰) L 1 2 注:泛频峰强度较弱,难辨认→却增加了光谱特征性5
3 3
2. C-H弯曲振动
~ 2926cm (强) ~ 2853cm (强) 1 CH ~ 2870cm (中强,易淹没)
as CH 2 1 s CH 2 1
as CH 3
s 1 ~ 1375 cm (中 强) ~ 1460cm (中) CH 3
1
CH 2
1 ~ 720 cm (n 4) ~ 1465 20cm (中) CH 2
第四章 分子光谱分析法
之三、红外吸收光谱法
基本原理 傅立叶变换红外光谱仪
红外图谱的解析及应用
1
学习目的与要求
掌握红光吸收光谱产生的条件* 理解泛频、分子振动自由度、不饱和度的概念 了解基团特征频率的波数区域 掌握光谱解析的步骤和方法*# 掌握红外光谱峰位的影响因素* 了解傅立叶红外光谱的测量原理 了解红外光谱的应用范围
分子振动自由度 3N 分子(平动自由度 转动自由度)
非线性分子: F 3N 6
• • •
线性分子: F 3N 5
注: 振动自由度反映吸收峰数量 并非每个振动都产生基频峰 吸收峰数常少于振动自由度数
13
示例 CO2分子 ——线性分子
F 3 3 5 4
1
3. C-C骨架振动
1 C C 1250 ~ 1150cm (弱 中)
18
as CH 2960 3
as CH 2
2925
as CH 1460 3
s CH 3
2870
s CH 2
2850 CH 2 1465
s CH 3
1390
CH 723
2
庚烷
19
烯烃 1.C-H振动
11
问题
1、一个分子(n个原子)到底一共有多少振动? 2、每个基团的各个振动峰的峰位如何? 3、基团峰位受哪些因素影响?
第一节 基本原理
一、振动的自由度 二、基团特征频率 三、影响因素
12
一、振动的自由度
指分子独立的振动数目,或基本的振动数目
N 个原子组成分子,每个原子在空间具三个自由度 , 分子有3N个运动自由度。
1.双原子分子振动频率(回顾)
( 频率 )
1 2 k
.......... ....... 或 ( 波数 )
1 2c
k
m1 m2 m1 m2
k为化学键的力常数(N/cm = mdyn/Å),为双原子折合质量
k大,化学键的振动波数高,如 kCC(2222cm-1)>kC=C(1667cm-1)>kC-C(1429cm-1) 质量m大,化学键的振动波数低,如
as CH 3
2960
as CH 2
2925
as CH 3
1460
s s CH 2 1465 2850 CH 2870 CH 2 3
3、红外吸收光谱产生的条件(回顾)
满足两个条件:
(1) 辐射应具有能满足物质产生振动跃迁
所需的能量;
(2)辐射与物质间有相互偶合作用。
对称分子:没有偶极矩,辐射不能引起共振,无 红外活性。 如:N2、O2、Cl2 等。 非对称分子:有偶极矩,红外活性。
8
9
10
可用峰位, 峰形,峰强来描述。
定性:基团的特征吸收频率; 定量:特征峰的强度; 应用:有机化合物的结构解析。
倍频
红外光谱 (0.75~1000m)
中红外(振动区) (2.5~25 m)
4000~400/cm-1
分子振动转动 (常用区)
远红外(转动区) (25-1000 m)
400~10/cm-1
分子转动
分区及波长范围
跃迁类型
4
基频峰与泛频峰
基频峰:分子从基态跃迁至第一振动激发态产生的 吸收峰 (即υ=0 → 1产生的峰)
2
参考书目
中西香尔(美) 等,红外光谱分析100例,北京 -科学出版社,1984.08 杨南如,无机非金属材料测试方法,武汉工 业大学出版社,1990 翁诗甫,傅立叶变换红外光谱仪,化学工业 出版社,北京,2005年
3
红外光区划分(回顾)
近红外(泛 频) (0.75~2.5 m)
13158~4000/cm-1
16
基团特征频率
(一)脂肪烃类化合物 (二)芳香族化合物
► (三)含氧类化合物 ► (四)含氮化合物 ► (五) 含卤素的化合物 ► (六)无机化合物中的盐 (饱和) 3000 ~ 2750 cm (强) 烷烃 1. C-H伸缩振动 C H as 1 s 1 CH ~ 2962cm (很强) CH ~ 2872cm (很强)
mC-C(1430cm-1)<mC-N(1330cm-1)<mC-O(1280cm-1)
伸缩振动力常数大于弯曲振动力常数
6
2.
(回 顾)
弯曲振动(变形振动,变角振动) s 对称收缩 as 反对称收缩 面外变形振动 ( 面外摇摆 面外扭曲 ) 7 面内变形振动 ( 面内摇摆 面内剪式 )
as CH
3100 ~ 3000cm (弱 中强)
1
1 CH 1000 ~ 650cm (强)
2.C=C骨架振动
C C ~ 1660 ~ 1630cm (弱 不定)
1
20
烯烃
(面外)
1 CH 1010 ~ 650cm(强)
990和910两个峰
890
21
970
•
•
吸收峰数少于振动自由度的原因: 发生了简并——即振动频率相同的峰重叠 红外非活性振动
14
示例
水分子——非线性分子
F 3 3 6 3
15
二、基团特征频率
叁键和累积 双键区
双键区 氢键 区
OH、NH、CH等的弯曲振 动
特征谱带区(官能团区)4000~1500cm-1
1500~400cm-1,指纹区
