6 对映异构体的拆分
合集下载
6 对映异构体的拆分概述

Most of the important molecules to living systems are enantioenriched. Examples include: amino acids; sugars; proteins; nucleic acids; vitamins; terpenoids; alkaloids; and steroids.
Molecules with 2 or more chiral centers have more isomers.
• A mixture containing predominantly one enantiomer is termed as: Enantiomerically Enriched, or Enantioenriched.
Resolution of enantiomers • A collection containing equal amounts of
the two enantiomeric forms of a chiral molecule is called a: racemic mixture or racemate.
• They (diastereomeric derivatives) can be separated by conventional separation methods such as crystallization, or chromatography on silica or other conventional stationary phases.
转化方式: 一对对映体同时转化; 破坏或转化其中一个对映异构体。
• 手性层析分离
•外消旋体
羧基+光学活性碱 碱基+光学活性酸 差向异构体盐
Molecules with 2 or more chiral centers have more isomers.
• A mixture containing predominantly one enantiomer is termed as: Enantiomerically Enriched, or Enantioenriched.
Resolution of enantiomers • A collection containing equal amounts of
the two enantiomeric forms of a chiral molecule is called a: racemic mixture or racemate.
• They (diastereomeric derivatives) can be separated by conventional separation methods such as crystallization, or chromatography on silica or other conventional stationary phases.
转化方式: 一对对映体同时转化; 破坏或转化其中一个对映异构体。
• 手性层析分离
•外消旋体
羧基+光学活性碱 碱基+光学活性酸 差向异构体盐
对映异构体的性质

18
手性分子是指不能和它的镜像完全重叠的分子。 手性分子必定有旋光性,具有旋光的分子必定是手性。
18
手性分子(乳酸)
19
19
(2)对映体
COOH
COOH
COOH COOH
H
OH
HO
CH3 a
镜面
H
H
HO
CH3 b
OH H CCHH33
不能重叠
20
互呈物体和镜象的对映关系,互称对映异构体,简称为对映体。
L-构型:—OH在投影式中手性碳原子左边
24
COOH
COOH
H
OH
HO
H
COOH
H2N
H
CH3
L-(-)-丙氨酸
CH3
D-(–)-乳酸
CH3
L-(+)-乳酸
CHO
CHO
H
H
H
OH
H
OH
H
OH 25 H
OH
CH2OH
CH2OH
D-(-)- 赤藓糖 D-(-)-2-脱氧核糖
CHO H OH HO H H OH H OH
11
使偏振光的振动平面向顺时针旋转的物质称为右旋体,用d 或 (+)表示;逆时针旋转的物质称为左旋体,用l 或( – )表示。
11
(4)旋光仪 用于测定其旋光度的仪器称为旋光仪。
图5-4 旋光仪的结构示意图
12
由光源、2个尼可尔棱镜、旋光管(或 称盛液管)和刻度盘等主要部件组成
12
❖ 3.旋光度和比旋光度
(–) -乳酸
–3.8°
53
3.79
(±) -乳酸
0
18
3.79
手性分子是指不能和它的镜像完全重叠的分子。 手性分子必定有旋光性,具有旋光的分子必定是手性。
18
手性分子(乳酸)
19
19
(2)对映体
COOH
COOH
COOH COOH
H
OH
HO
CH3 a
镜面
H
H
HO
CH3 b
OH H CCHH33
不能重叠
20
互呈物体和镜象的对映关系,互称对映异构体,简称为对映体。
L-构型:—OH在投影式中手性碳原子左边
24
COOH
COOH
H
OH
HO
H
COOH
H2N
H
CH3
L-(-)-丙氨酸
CH3
D-(–)-乳酸
CH3
L-(+)-乳酸
CHO
CHO
H
H
H
OH
H
OH
H
OH 25 H
OH
CH2OH
CH2OH
D-(-)- 赤藓糖 D-(-)-2-脱氧核糖
CHO H OH HO H H OH H OH
11
使偏振光的振动平面向顺时针旋转的物质称为右旋体,用d 或 (+)表示;逆时针旋转的物质称为左旋体,用l 或( – )表示。
11
(4)旋光仪 用于测定其旋光度的仪器称为旋光仪。
图5-4 旋光仪的结构示意图
12
由光源、2个尼可尔棱镜、旋光管(或 称盛液管)和刻度盘等主要部件组成
12
❖ 3.旋光度和比旋光度
(–) -乳酸
–3.8°
53
3.79
(±) -乳酸
0
18
3.79
对映异构-有机化学

泳衣品牌
它们不同对映体
表现出相反作用。
对于含手性碳原子的药物,即便是同一药物,
产生的生物活性,有的强弱不一,有的甚至
这是因为生物大分子(如酶、受体、抗体等)或它的 活性部位具有手性,具有一定的立体构型和构象,所以 它要求和它相互作用的的生物活性分子(如神经递质、
激素、药物、毒物等)也要具有和它相适应的立体化学
二 含一个手性碳原子化合物的对映异构
手性碳原子:
泳衣品牌与四个不同的原子或原子团相
* CH CH CO O H 3 OH
连的碳原子。 例如:乳酸分子
(一) 对映异构体
COOH C CH3 H OH H HO COOH
对
互为实物与镜
影关系,不能 相互重叠的两
C CH3
映 体
S-(+)-乳酸
R-(-)-乳酸
5、迅猛增长的市场需求,刺激了手性药物的研究与开发。
§9.1 偏振光和旋光性
一、偏振光和物质的旋光性
光是一种电磁波,光波的振动方向与其前进方向垂直。
光束先进方向
光源
尼可尔棱镜 (偏振片)
与棱镜晶轴 平行的振动 平面
晶轴 b a c d
普通光
a 平面偏振光
有无数个振动平面,振动平面与光的前进方向 相垂直
-1 2 °
0° ( m) 酒 石 酸
0°
内消旋体(分子中有对称面)
内消旋体(meso):分子内部形成对映两半的化合物。
(有平面 对称因素)。内消旋体无旋光性。 具有两个手性中心的内消旋结构一定是(R、S)构 型。 外消旋体与内消旋体异同: 外消旋体与内消旋体的共同之处是:二者均 无旋光性,但本质不同。 外消旋体:是混合物,可拆分出一对对映体。 内消旋体:是化合物,不能拆分。
大学有机化学6对映异构

尼科尔棱镜 普通光 偏振光
旋光 度
旋光性物质
手性分子
偏振光的振动方向 发生旋转
上页 下页 返回 退出
6.3.1 物质对偏振光的作用
6.3.2 旋光仪工作原理示意图
上页 下页 返回 退出
6.3.3 比旋光度
比旋光度
[ ]
l C
-样品的旋光度
C-溶液的浓度 l- 管长
若被测物质是纯液体,则:
对称面
上页 下页 返回 退出
对称中心:设想分子中有一个点,从分子任何一个原
子出发,向这个点作一直线,再从这个点将直线延长 出去,则在与该点前一线段等距离处,可以遇到一个 同样的原子,这个点就是对称中心。
对称中心
动画 上页 下页 返回 退出
交替对称轴(旋转反映轴):设想分子中有一条直线,
当分子以此直线为轴旋转360/n后,再用一个与此直线 垂直的平面进行反映,如果得到的镜象与原来分子完 全相同,这条直线就是交替对称轴。
动画 上页 下页 返回 退出
R/S标记法:
COOH CH3 OH
优先次序: OH>COOH>CH3>H
命名为:(R)-2-羟基丙酸
HOOC H3 C HO H
优先次序: OH>COOH>CH3>H
命名为:(S)-2-羟基丙酸
上页 下页 返回 退出
在费歇尔投影式上进行R/S标记:
小基 在横 线上
COOH H CH3 OH
上页 下页 返回 退出
6.4 含有一个手性碳原子的化合物的对映异构
CH3C*HOHCOOH(乳酸)
H
*
H
*
HOOC
C CH3 HO
乳酸
旋光 度
旋光性物质
手性分子
偏振光的振动方向 发生旋转
上页 下页 返回 退出
6.3.1 物质对偏振光的作用
6.3.2 旋光仪工作原理示意图
上页 下页 返回 退出
6.3.3 比旋光度
比旋光度
[ ]
l C
-样品的旋光度
C-溶液的浓度 l- 管长
若被测物质是纯液体,则:
对称面
上页 下页 返回 退出
对称中心:设想分子中有一个点,从分子任何一个原
子出发,向这个点作一直线,再从这个点将直线延长 出去,则在与该点前一线段等距离处,可以遇到一个 同样的原子,这个点就是对称中心。
对称中心
动画 上页 下页 返回 退出
交替对称轴(旋转反映轴):设想分子中有一条直线,
当分子以此直线为轴旋转360/n后,再用一个与此直线 垂直的平面进行反映,如果得到的镜象与原来分子完 全相同,这条直线就是交替对称轴。
动画 上页 下页 返回 退出
R/S标记法:
COOH CH3 OH
优先次序: OH>COOH>CH3>H
命名为:(R)-2-羟基丙酸
HOOC H3 C HO H
优先次序: OH>COOH>CH3>H
命名为:(S)-2-羟基丙酸
上页 下页 返回 退出
在费歇尔投影式上进行R/S标记:
小基 在横 线上
COOH H CH3 OH
上页 下页 返回 退出
6.4 含有一个手性碳原子的化合物的对映异构
CH3C*HOHCOOH(乳酸)
H
*
H
*
HOOC
C CH3 HO
乳酸
06对映异构

手性:如果物质的分子和它的镜像不能重合,和我 们的左右手相像,那么把物质的这种特征称为手性。
如果分子是手性的,由于它的任何一分子的镜 象并不与其相同,而是它的对映体,对一种旋光性 物质来说,其分子引起的旋光就不会被抵消,结果 就表现出有旋光性。例如:
二. 比旋光度 物质的旋光度与旋光管的长度、溶液的浓度、溶 剂以及测定时的温度和光源的波长均有关系。条件不 同,不仅可改变旋光的度数,还可能改变旋光的方向。 当旋光管的长度是 ldm ,被测物质的浓度是 1g 溶质 /1mL溶剂时,测出的旋光度称为比旋光度,用[α] t 表示。它与旋光度的关系是: λ [α
对称中心
F
Cl
H
H H
F
H
Cl
一般地说,物质分子凡在结构上具有对称面或 对称中心的,就不具有手性,也就没有旋光性。 反之,同时不具有对称面和对称中心的,分子 就有手性和旋光性。分子的手性(而不是手性 碳)是其具有旋光性和对映异构现象的充分必 要条件。
苯或环己烷分子有多少个对称面?
提示:环烷烃分子的环骨架 可以看成是平面正多边形
第一节
物质的旋光性
一、平面偏振光和旋光性
1. 偏振光和旋光性的测定 光是一种电磁波,其振动方向与传播方向垂直。 普通光的光波可在垂直于其前进方向的所有平面内 振动,若使之通过一个尼科尔(Nicol)棱镜(其 作用像栅栏),则只有与棱镜晶轴平行平面上振动 的光线通过,这种只在一个平面上振动的光,称为 平面偏振光,简称偏振光或偏光。
CH2CH3 C CH3 H
H3C H
C Cl I
镜面
Cl II
O H H3C C CH2 H2C
O C H CH3
2. 构型的表示方法
第八章 对映异构
S HO R H CHO H OH CHO
H HO CHO OH R H S CHO
a
=
b
c
对体
d
内消旋体(meso)
内消旋体:有手性碳而没有旋光性的立体异构体
1、外消旋体与内消旋体的异同
(1)相同点:无旋光性(原因不同); (2)不同点:物理性质不同 外消旋体:混合物,可拆分; 内消旋体:单一化合物,不可拆分。 2、苏式构型和赤式构型
直观,但书写麻烦,不适用于复杂化合物
2、Fischer投影式
(1)投影原则
HOOC
COO H
H H3C
OH
HO
H CH 3
① 主C链竖置,且编号小者 置于上端
COOH H C CH3 OH
COOH HO C CH3 H
② 横前竖后
③ 横线与竖线交点:手性C 原子。
COOH H OH CH3
HO
COOH H CH3
l ——盛液管的长度(dm) C ——溶液的浓度(g.mL-1)
3、比旋光度是旋光性物质的一个物理常数
例如:葡萄糖:[α]D20 = +52.2°(水)
§8.2 对映异构体和手性分子
一、对映异构和手性
1、对映异构体
化合物互为实物和镜像,但它们不能重合,因此它们是一对异 构体,互为对映,称为对映异构体。
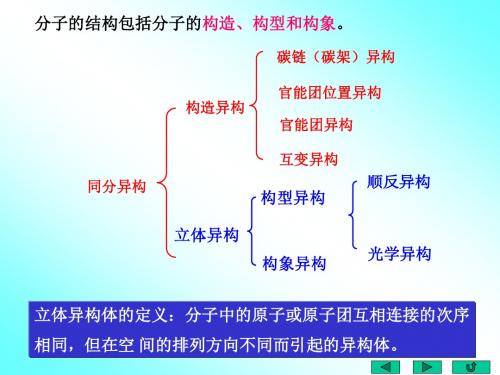
分子的结构包括分子的构造、构型和构象。
碳链(碳架)异构 官能团位置异构 构造异构 官能团异构 互变异构 同分异构
顺反异构
构型异构
立体异构
构象异构
光学异构
立体异构体的定义:分子中的原子或原子团互相连接的次序 相同,但在空 间的排列方向不同而引起的异构体。
§8.1 物质的旋光性
H HO CHO OH R H S CHO
a
=
b
c
对体
d
内消旋体(meso)
内消旋体:有手性碳而没有旋光性的立体异构体
1、外消旋体与内消旋体的异同
(1)相同点:无旋光性(原因不同); (2)不同点:物理性质不同 外消旋体:混合物,可拆分; 内消旋体:单一化合物,不可拆分。 2、苏式构型和赤式构型
直观,但书写麻烦,不适用于复杂化合物
2、Fischer投影式
(1)投影原则
HOOC
COO H
H H3C
OH
HO
H CH 3
① 主C链竖置,且编号小者 置于上端
COOH H C CH3 OH
COOH HO C CH3 H
② 横前竖后
③ 横线与竖线交点:手性C 原子。
COOH H OH CH3
HO
COOH H CH3
l ——盛液管的长度(dm) C ——溶液的浓度(g.mL-1)
3、比旋光度是旋光性物质的一个物理常数
例如:葡萄糖:[α]D20 = +52.2°(水)
§8.2 对映异构体和手性分子
一、对映异构和手性
1、对映异构体
化合物互为实物和镜像,但它们不能重合,因此它们是一对异 构体,互为对映,称为对映异构体。
分子的结构包括分子的构造、构型和构象。
碳链(碳架)异构 官能团位置异构 构造异构 官能团异构 互变异构 同分异构
顺反异构
构型异构
立体异构
构象异构
光学异构
立体异构体的定义:分子中的原子或原子团互相连接的次序 相同,但在空 间的排列方向不同而引起的异构体。
§8.1 物质的旋光性
第6章 对映异构
比旋光度 (Specific Rotation)
t
B l
:旋光度 B :质量浓度(g/ml) l :盛液管的长度(dm)
8
:光源的波长
t :测定时的温度
说明
•比旋光度[]:体现物质特性,可在手册中查到 •一般用钠灯(D)作光源,λ=589.3nm,t=20℃ •物质的旋光度,需要通过改变浓度或者改变盛液管长度 的方式测定两次,才能确定。 •溶液一般为稀溶液,否则测出的α值不准 •若溶剂不是水,则要在后面标出溶剂及相应浓度 右旋酒石酸: (乙醇, 5%)
25
CH3 C HO H CH2CH3 HO
CH3 C CH2CH3 H HO
CH2CH3 C H CH3
S
R
R
S
≡ ≡
A B C
≡
B
B
A
C
D
D
R
D A C
≡
A
D B
26
C
Fischer投影式中R、S的简便确定法: •若最小基团d在竖线上,则a,b,c顺时针旋转为R型, 逆时针为S型; •若最小基团d在横线上,则a,b,c顺时针旋转为S型, 逆时针为R型。 使用费歇尔投影式应注意的问题: •在纸面上转动180°或偶数倍,构型不变。
n
﹡
﹡
I
≡
II
III
IV
关系:对映体:III和IV
内消旋体:I和II
非对映体:I和III,II和III,I和IV,II和IV
33
内消旋体(meso):分子内部形成对映两半的化合物 (有) 内消旋体无旋光性(抵消), 不能分离成光活性物质
mp
(+)-酒石酸 (-)-酒石酸 170oc 170oc
第五章 立体化学
四、判断对映体的方法
有三种方法可以用来判断一个分子是否 存在对映体: 1.建造一个分子和它的镜像的模型,如果 两者不能重合,就存在对映体。 2. 如果分子有对称面,那么它和其镜像 就能重合,就不存在对映体。 3.如果一个分子有一个手性碳原子,它就 具有对映异构现象,有一对对映体。
第二节 费歇尔(Fischer)投影式
D-(-)-甘油酸
D-(-)-乳酸
D.L命名法的使用有一定的局限性,它只适用与甘油醛结构 类似的化合物.目前,仍用于糖类和氨基酸的构型命名
二、 R.S构型命名法
R/S 构型标记法分为两步:
(1) 按次序规则确定与手性碳相连的四个原子 或基团的优先次序(或称为“大小” 次序)
3
CH3 C H4 Br1
对称面
内消旋酒石酸分子
问题:内消旋体是否显旋光性?为什么? 答案:不显旋光性。因为内消旋体有一对 称面,互为对称的两部分对偏振光的影响 相互抵消,使整个分子不表现旋光性。
第六节 构型命名
一、D.L命名法 规则:以甘油醛为标准,Fischer投影式中C* 上羟基处于右侧的为D-构型;反之为L-构型
CH3 H C6H5
S构型
CH3
Br
HO H
S构型
C6H5
COOH HO H
R构型
COOH H3C Cl C6H5
R构型
CH2OH
问题:判断下列手性碳的R、S构型。
R
HO COOH C H
R
H H
CO2H OH OH CH3
CH3
R
R-乳酸
2R,3R-2,3-二羟基丁酸
实物与镜像不重合
不含 对称中心 对称面
CO2H H HO C C OH H HO H
6章-对映异构10.4
COOH
楔形式
COOH H C CH3 OH
COOH C H OH
H OH
C CH3 H3C
COOH
COOH HO H CH3
H
OH CH3
Fischer投影式的立体含义: 横外竖里” Fischer投影式的立体含义:“横外竖里” 投影式的立体含义
纸面上转动1800 纸面上转动180
COOH H OH CH3
第六章 对 映 异 构
构造异构体:分子式相同, 构造异构体:分子式相同,但分子构造不同的化合物
同分异构
碳干异构 构造异构 官能团位置异构 互变异构 构型异构 立体异构 构象异构 顺反异构 对映异构
立体异构:具有相同分子构造, 立体异构:具有相同分子构造,但空间排列方式 不同产生的异构现象
第一节 物质的旋光性
(1) Br C (2) CH3 H CH3 H (1) = Br Br H
H CH3
二、加成反应立体化学解释
Br H CH3
CH3 = Br H H Br CH3
Br CH3
Br CH3 = Br
H
Br CH3 = Br
CH3 H Br H CH3
(2)
H H Br CH3
H CH3
应用
O
H C C H
Cl
H
H
i P
H
Cl
F
F H
Cl H F H H Cl
H F
H F H Cl
Cl H F H
3. 对称轴(Cn) 对称轴(
H
H
Cl H C C H Cl C2
H H H H H H C4
H H Cl
C2
H H Cl Cl H H
6 第六章 对映异构
第六章 对映异构 (一)、教学要求
1、掌握偏振光、旋光性、比旋光度、摩尔比旋光度的概念。 2、理解对称元素和对称操作,识别指定结构中的对称元素, 掌握手性和手性碳的概念。 3、掌握费歇尔投影规则和使用费歇尔投影式的原则, 以及费歇尔投影式、纽曼投影式与锯架式的转换。 4、掌握含一个手性碳化合物的对映异构现象,对映异构体、 外消旋体。 5、掌握含二个手性碳化合物的立体异构,非对映异构体、 内消旋体,画出上述异构体的纽曼投影式。 6、理解丙二烯型、螺环和有位阻联苯的对映异构的特征。 7、构型标记法,R/S标定法,D/L系。 8、理解对映异构体混合物的化学拆分基本原理。
返回教学内容
第三节
含一个手性碳原子化合物的对映异构
一.对映体(Enantiomers) 乳酸是含一个手性碳原子的典型代表:
COOH COOH
H CH3 OH H3C OH
H
-
构造相同,构型相反,互为物象关系叫对映异构体 (简称对映体) 其中一个是右旋体: []20D = + 3.8º 一对乳酸: 另一个是左旋体: []20D = - 3.8º
H
CH3
HO CH 3
H
投影
使用费歇尔投影式时应注意的操作: 1.不能离开纸面翻转——否则会改变原来的构型。 2.在纸面上转动180º ,不改变原来构型。 3.在纸面上旋转90º 或90º 的奇数倍,则改变原来构型。 4.把其中一个基团固定,其他三个基团按顺时钟方向 或反时 钟方向改变相对位置,则构型不变。 5.任何两个基团互相调换位置,则改变原来构型。
(Enantiotropy or Enantiomorphism) (旋光异构)
(Conformers or rotational isomers)
1、掌握偏振光、旋光性、比旋光度、摩尔比旋光度的概念。 2、理解对称元素和对称操作,识别指定结构中的对称元素, 掌握手性和手性碳的概念。 3、掌握费歇尔投影规则和使用费歇尔投影式的原则, 以及费歇尔投影式、纽曼投影式与锯架式的转换。 4、掌握含一个手性碳化合物的对映异构现象,对映异构体、 外消旋体。 5、掌握含二个手性碳化合物的立体异构,非对映异构体、 内消旋体,画出上述异构体的纽曼投影式。 6、理解丙二烯型、螺环和有位阻联苯的对映异构的特征。 7、构型标记法,R/S标定法,D/L系。 8、理解对映异构体混合物的化学拆分基本原理。
返回教学内容
第三节
含一个手性碳原子化合物的对映异构
一.对映体(Enantiomers) 乳酸是含一个手性碳原子的典型代表:
COOH COOH
H CH3 OH H3C OH
H
-
构造相同,构型相反,互为物象关系叫对映异构体 (简称对映体) 其中一个是右旋体: []20D = + 3.8º 一对乳酸: 另一个是左旋体: []20D = - 3.8º
H
CH3
HO CH 3
H
投影
使用费歇尔投影式时应注意的操作: 1.不能离开纸面翻转——否则会改变原来的构型。 2.在纸面上转动180º ,不改变原来构型。 3.在纸面上旋转90º 或90º 的奇数倍,则改变原来构型。 4.把其中一个基团固定,其他三个基团按顺时钟方向 或反时 钟方向改变相对位置,则构型不变。 5.任何两个基团互相调换位置,则改变原来构型。
(Enantiotropy or Enantiomorphism) (旋光异构)
(Conformers or rotational isomers)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.差异性吸附( Differential absorption ) • 手性固定相层析:纸层析、柱层析、气相色 谱、液相色谱。 例:外消旋扁桃酸( mandelic acid ):淀粉 OH 柱层析,完成拆分。
C COOH H
• 手性吸附剂( chiral absorbents)层析柱: 气相色谱、液相色谱。
Me Ph R H + H Ph S Me NH2 Cl C O NH2 OMe C H Ph Ph Ph
Me
H N
OMe C O C H OMe C O C H Ph Ph
H H H N
Me
对映体→测NMR:R、S所有对映体信号重叠 对映体: ①在一般非手极性溶剂中,具相同的NMR谱图, ②在手性溶剂或添加手性试剂环境下,具不同的 NMR谱图,混合物中哪个信号属哪个对映体?
4.生物化学处理( Biochemical processes ) • 微生物:有的可能只对对映体中一个异构 体发生作用。 • 寻找适合的微生物是问题关键。
5. 机械分离( Mechanical separation ,手工分 离) • Pasteur 首创 • Racemic acid——(+)和(-)tartaric acid • Racemic solution ammonium tartrate (外消旋 酒石酸胺钠) • (+)成一种晶体;(-)成一种晶体 非重 叠晶体.
• Classically, enantiomers have been separated by forming diastereomeric salts or derivatives with enantioenriched chiral pool reagents. Since these diastereomeric derivatives are no longer enantiomers.
• 7. 去外消旋化 (Deracemization ) :将对 映体之一转化成另一异构体,得到单一 对映体纯或相对含量多的产物 • 例: O
O2 N N NO 2 H O racemer S Bu
NEt3 (R)- isomer 89% optically active amide 产物 28 days (S)- isomer 11%
3.手性识别( Chiral recognition ) • 手性宿主(chiral host ):与对映体形成 差向异构包合物。常只与客体对映体混 合物中一种异构体结合; 或与一种异构体 比与另外一种形成包合物稳定。 • 手性宿主腔穴 ( Chiral host cavity )
• 手性冠醚( chiral crown ether )
5. Classical resolution & chromatographic enantioseparation (对映性分离).
6. Spontaneous(自发的)resolution.
Classical Resolution • Enantiomers have identical physical properties, and consequently cannot be directly separated by conventional methods such as distillation(蒸馏), crystallization, sizing(定量), or chromatography on conventional stationary phases. • Physical separation of the enantiomers comprising a racemic mixture requires the use of some external enantiopure, enantioenriched material, or device.
升华( Sublimation )拆分 • 例:
H OH H (+) crystal same crystal form (-) crystal
6.动力学拆分( Kinetic resolution ) • 对映体与手性化合物以不同速度进行反应, 可在完全反应前中止反应,达到部分分离。
• 例 1 : 对 映 体 烯 烃 与 光 学 活 性 diisopinocampheylborane(二异松蒎醇硼烷) 反应。
Molecules with 2 or more chiral centers have more isomers.
• A mixture containing predominantly one enantiomer is termed as: Enantiomerically Enriched, or Enantioenriched.
Resolution of enantiomers • A collection containing equal amounts of the two enantiomeric forms of a chiral molecule is called a: racemic mixture or racemate.
• They (diastereomeric derivatives) can be separated by conventional separation methods such as crystallization, or chromatography on silica or other conventional stationary phases.
• The seeding of a racemic solution with something that will cause only one enantiomer to crystallize——引入晶种
• 例 2 : heptahelicene, 其 一 异 构 体 具 []=+1200°,在苯中易结晶。 • 例3:Polycrystalic racemic samples of () 1,1’-binaphthyl (双萘)——加热到 76- 150C 发生晶型转化,从一种晶型转化成 另外一种晶型——光学活性晶体产生。 • 例4.在手性添加物(chiral additive)存 在下,对映选择性结晶。
Method of resolution (拆分)
• Resolution( 拆 分 ) : to separate a pair of enantiomers into the single isomer.
• 常用方法:将对映体混合物转化为差向 异 构 体 , 再 进 行 分 步 结 晶 ( fractional crystallization),再还原为原结构。 转化方式: 一对对映体同时转化; 破坏或转化其中一个对映异构体。 • 手性层析分离
• 外消旋体
羧基+光学活性碱 差向异构体盐 碱基+光学活性酸
• 差向异构体:不同的物化性质。 • 差向异构体盐:不同的结晶特性,适合的溶 剂中可进行分步结晶。 • 缺点:常不能够经一步结晶达到完全分离; 长时间的分离过程。
COOH H C CH3 OH + (S)-Brucine OH H
COOC CH3 OH Brucine-H (S)
Most of the important molecules to living systems are enantioenriched. Examples include: amino acids; sugars; proteins; nucleic acids; vitamins; terpenoids; alkaloids; and steroids.
Quantitating Enantiopurity (对映纯度) • Enantiomeric Excess (%e.e.) : Enantiopurity is usually reported in terms of “enantiomeric excess”
Most of chiral compounds are unavailable in enantioenriched form
•
• 例2:allylic alcohols (烯丙基醇)与手 性环氧化试剂(对映体之一)反应
手性环氧 化试剂 O
OH OH OH
(R)-enantiomer
(S)-enantiomer
获得另外一个对映体或相应产物方法:
(1)选用另外一个对映体试剂
(2)保持立体化学中心构型不变情况下, 从产物转化为起始物。
Methods for obtaining enantioenriched compounds
1. Directly from chiral pool(手性源)
2. Synthesis from enantioenriched chiral pool starting products.
3. Synthesis using enantioenriched chiral pool auxiliaries(辅助物). 4. Enantioselective catalysts(催化剂).
去外消旋化的两个条件: (1)对映体与不同光学活性物形成复合物 (2)在实验条下须能互为转化
Optical Purity []obs • Percent optical purity= ———— 100 []max []与化合物浓度一般成线性关系。 • Optical purity= percent enantiomeric excess [(R)]-[(S)’] = 100
+
(R) COOH OH C H
(R) COOC CH3
H Brucine-H+ (S) (S)
CH3 (S)
对映体
差向异构体盐
• 天然存在的生物碱:好的光学活性碱试剂,如 brucine, ephedrine,strychnine, morphine。 • 非羧酸:转化为羧酸,再成为差向异构体盐进行拆 分 • 碱:用羧酸,成为盐 • 醇:转化为酯 • 醛:转化为腙(hydrazone) • 烷烃:转化为包合物( inclusion compound),常 用urea(尿素,笼状化合物)。 • 手性冠醚(chiral crown ether):拆分直链烷胺、 芳香胺,形成差向异构化的复合物(complexes) 。
