卤素期末考试必考点.doc
卤素知识点

卤族元素第一节氯气一、分子式、电子式、结构式二、物理性质黄绿色有刺激性气味的气体,比空气重(分子量大于29),有毒,易液化,能溶于水(1:2.26),但难溶于饱和食盐水。
(1)色、味、态(介绍毒性)(2)密度:比空气大(3)水溶性:可溶(体积比1:2)常温下,1体积水约能溶解2体积氯气)(4)熔、沸点:-101 C;-34.6 C (与氧气-218 C;-183 C和氢气-259 C;-252 C比较)常压,-34.6 C易液化:氯气液氯观察一瓶氯气,闻味(注意方法”扇”和”飘”),再到入水振荡.用手轻轻地在瓶口扇动,仅使极少量的气体飘进鼻孔。
三、化学性质(强氧化剂)①与金属反应(将金属氧化为高价态...)2Na + Cl2点燃2NaCl(白烟) Cu + Cl2点燃CuCl2(棕黄色烟)2Fe + 3Cl2点燃2FeCl2(棕色烟)注意:●干燥的氯气与铁不反应,故工业上把液氯储存在钢瓶中●CuCl2固体加水后,浓溶液呈绿色,稀溶液呈蓝色CuCl2溶液的颜色随溶液浓度的不同而略有不同。
CuCl2溶液浓溶液稀溶液黄色黄绿色绿色蓝色②与非金属反应点燃H2 + Cl2 === 2HCl(苍白色火焰,工业制HCl原理)光照H2 + Cl2 === 2HCl(爆炸)点燃2P + 3Cl2 === 2PCl3(液体)三氯化磷(白色烟雾)PCl3 + Cl2 === PCl5(固体)五氯化磷磷在氯气中燃烧时,两个反应同时发生产生白色烟雾燃烧(广义定义):指任何发热发光的剧烈的化学反应。
③与水反应Cl 2 + H 2O = HCl + HClO注意:氯水为淡黄绿色,主要成分为Cl 2、H 2O 、 HClO 、H + 、Cl - 、ClO - 、OH - 。
并且2HClO= 2HCl + O 2↑,故久置氯水为稀盐酸,新制氯水在保存时应该棕色瓶,密封保存。
另HClO 是一种一元弱酸,具有强氧化性和不稳定性,可以做漂白剂、杀菌剂。
卤素的知识点归纳总结

卤素的知识点归纳总结一、卤素的性质1. 物理性质卤素的物理性质各异,如氟气为浅黄色气体,氯气为黄绿色气体,溴为红褐色液体,碘为紫黑色晶体,烷为暗紫色晶体。
卤素的沸点和熔点逐渐升高,原子量增大。
2. 化学性质卤素在化学性质上也有很多相似之处,例如:(1)卤素的电负性逐渐减小,化活性逐渐减弱;(2)卤素能与氢形成卤化氢,如氟与氢结合为氢氟酸、氯可与氢结合为盐酸,溴合氢结合为溴化氢,碘与氢结合为碘化氢;(3)卤素与金属反应,形成卤化物,如氟与钠反应形成氟化钠,氯与钾反应形成氯化钾,溴与钙反应形成溴化钙,碘与铝反应形成碘化铝。
3. 卤素的氧化性和还原性卤素可以表现出比较复杂的氧化性和还原性。
例如,氟气能与水蒸气反应生成氢氟酸和氧气;氯气与水反应生成盐酸和电子;溴与水反应生成溴化氢和氧气。
二、卤素在生活和工业中的应用1. 卤素在医疗和药物工业中的应用卤素及其化合物在医疗和药物工业中有着广泛的应用。
例如,碘和氯制成的药物可用于消毒和杀菌;氟化合物可用于制作药物和牙膏等。
2. 卤素在农业中的应用卤素及其化合物在农业中也有着重要的应用,例如氯化钠、氯化钾和氯化镁可用于土壤改良和植物生长;氯气可制成杀虫剂和杀菌剂。
3. 卤素在化工生产中的应用卤素及其化合物在化工生产中也有着广泛的应用,比如氯和氯化物可用于橡胶生产、塑料制造和合成纤维等;氟和氟化物可用于制作冷冻剂和高分子化合物。
三、卤素的环境影响1. 卤素对环境的影响卤素及其化合物对环境有着重要的影响,比如氯氟烃类气体和氟化物等对臭氧层和温室气体的破坏,对生态系统的影响;氯化物和碘化物等对水体和土壤的污染。
2. 卤素的环境保护为了减少卤素对环境的影响,需要加强卤素的环境保护工作,采取科学的措施进行处理和利用,减少对环境的影响。
四、卤素元素的发现及历史1. 卤素元素的发现卤素元素的发现可追溯到古代。
人类在早期,就发现了一些卤素原素。
比如,古埃及人用氯化钠制成各种药品,古希腊人发现了碘元素。
(完整版)卤素知识点总结

1•氯气 [氯气的物理性质](1)常温下,氯气为黄绿色气体•加压或降温后液化为液氯,进一步加压或降温则变成固态氯.(2)常温下,氯气可溶于水(1体积水溶解2体积氯气).(3)氯气有毒并具有强烈的刺激性,吸入少量会引起胸部疼痛和咳嗽,吸入大量则会中毒 死亡.因此,实验室闻氯气气味的正确方法为:用手在瓶口轻轻扇动,仅使少量的氯气飘进鼻孔.[氯气的化学性质]画出氯元素的原子结构示意图: ___________________________ 氯原子在化学反应中很容易获得1个电子.所以,氯气的化学性质非常活泼,是一种强氧化剂.注意 ①在不同的条件下,H 2与C12均可发生反应,但反应条件不同,反应的现象也不同.点燃时,纯净的 H 2能在 C12中安静地燃烧,发出苍白色的火焰,反应产生的气体在空气中形成白雾并有小液滴出现;在强光照射下,H 2与C12的混合气体发生爆炸.② 物质的燃烧不一定要有氧气参加.任何发光、发热的剧烈的化学反应,都属于燃烧.如金属铜、氢气在氯气中燃烧 等.③ “雾”是小液滴悬浮在空气中形成的物质; “烟”是固体小颗粒分散到空气中形成的物质.要注意“雾”与“烟”的区别.④ H 2与Cl 2反应生成的HCI 气体具有刺激性气味,极易溶于水. HCI 的水溶液叫氢氯酸,俗称盐酸. ⑶与水反应.C12 + H 2O = HCI + HCIO离子方程式:CI 2 + H 2O = H + + CI — + HCIO说明 ①C1 2与H 20的反应是一个C12的自身氧化还原反应.其中, CI 2既是氧化剂又是还原剂,H 20只作反应物.②在常温下,1体积水能溶解约 2体积的氯气,故新制氯水显黄绿色.同时,溶解于水中的部分C12与H 20反应生成HCI 和HCIO ,因此,新制氯水是一种含有三种分子(C12、HCIO 、H 2O )和四种离子(H +、Cl —、CIO —和水电离产生的少量OH —)的混合物.所以,新制氯水具有下列性质:酸性(H + ),漂白作用(含HCIO ) , Cl —的性质,C12的性质.卤素(1)与金属反应: Cu + C1 2 八 CuCl 2实验现象:铜在氯气中剧烈燃烧,集气瓶中充满了棕黄色的烟.一段时间后,集气瓶内壁附着有棕黄色的固体粉 末.向集气瓶内加入少量蒸馏水,棕黄色固体粉末溶解并形成绿色溶液,继续加水,溶液变成蓝色.2Na + CI 2丄一2NaCI实验现象:有白烟产生.说明 ①在点燃或灼热的条件下,金属都能与氯气反应生成相应的金属氯化物.其中,变价金属如 应时呈现高价态(分别生成CuCl 2、FeCl 3).② 在常温、常压下,干燥的氯气不能与铁发生反应,故可用钢瓶储存、运输液氯.③ “烟”是固体小颗粒分散到空气中形成的物质.如铜在氯气中燃烧,产生的棕黄色的烟为 氯气中燃烧,产生的白烟为NaCI 晶体小颗粒;等等.(Cu 、Fe )与氯气反CuCl 2晶体小颗粒;钠在(2)与氢气反应. H 2 + Cl 2 2HCl③新制氯水中含有较多的CI2、HCIO,久置氯水由于C12不断跟H20反应和HCIO不断分解,使溶液中的C12、HCIO逐渐减少、HCI逐渐增多,溶液的pH逐渐减小,最后溶液变成了稀盐酸,溶液的pH V 7.④C12本身没有漂白作用,真正起漂白作用的是C12与H20反应生成的HCIO .所以干燥的C12不能使干燥的有色布条褪色,而混有水蒸气的C12能使干燥布条褪色,或干燥的C12能使湿布条褪色.⑤注意“氯水”与“液氯”的区别,氯水是混合物,液氯是纯净物.(4)与碱反应.常温下,氯气与碱溶液反应的化学方程式的通式为:氯气+可溶碱T金属氯化物+次氯酸盐+水.重要的反应有:C12 + 2NaOH = NaCI + NaCIO + H 2O 或CI2 + 2OH-= CI-+ CIO-+ H2O 该反应用于实验室制C12时,多余CI2 的吸收(尾气吸收).2CI2 + 2Ca(OH) 2 = Ca(C1O)2 + CaCb + 2H2O说明①CI2与石灰乳[Ca(OH)2的悬浊液]或消石灰的反应是工业上生产漂粉精或漂白粉的原理•漂粉精和漂白粉是混合物,其主要成分为Ca(CIO)2和CaCb,有效成分是Ca(C1O)2②次氯酸盐比次氯酸稳定.③漂粉精和漂白粉用于漂白时,通常先跟其他酸反应,如:Ca(CIO)2+2HCI = CaCI2+2HCIO④漂粉精和漂白粉露置于潮湿的空气中易变质,所以必须密封保存.有关反应的化学方程式为:Ca(CIO) 2 + CO2 + H2O =CaCO3 J + 2HCIO 2HCIO由此可见,漂粉精和漂白粉也具有漂白、消毒作用.[氯气的用途]①杀菌消毒;②制盐酸;⑧制漂粉精和漂白粉;④制造氯仿等有机溶剂和各种农药.[次氯酸]①次氯酸(HCIO)是一元弱酸(酸性比H2CO3还弱),属于弱电解质,在新制氯水中主要以HCIO分子的形式存在,因此在书写离子方程式时应保留化学式的形式.②HCIO不稳定,易分解,光照时分解速率加快.有关的化学方程式为:2HCIO = 2H + + 2CI - + O2 f,因此HCIO是一种强氧化剂.③HCIO能杀菌.自来水常用氯气杀菌消毒(目前已逐步用C1O2代替).④HCIO能使某些染料和有机色素褪色.因此,将CI2通入石蕊试液中,试液先变红后褪色.[氯气的实验室制法](1) 反应原理:实验室中,利用氧化性比C12强的氧化剂[如MnO2、KMnO 4、KCIO 3、Ca(CIO)2等]将浓盐酸中的CI-氧化来制取C12。
(完整word版)卤族元素知识点详细总结,

卤族元生性质复习要点1。
卤素单质在物理性质和化学性质上的主要差别及递变规律;2。
卤族元素的化合物性质的递变性;3。
卤化银的性质、用途及碘与人体健康的关系。
4。
要点察看卤生性质的变化规律。
1。
氯气[ 氯气的物理性质 ](1)常温下,氯气为黄绿色气体。
加压或降温后液化为液氯,进一步加压或降温则变为固态氯。
(2)常温下,氯气可溶于水( 1 体积水溶解 2 体积氯气)。
(3)氯气有毒并拥有激烈的刺激性,吸入少许会惹起胸部悲伤和咳嗽,吸入大批则会中毒死亡。
所以,实验室闻氯气气味的正确方法为:用手在瓶口轻轻扇动,仅使少许的氯气飘进鼻孔。
[ 氯气的化学性质 ]氯原子在化学反响中很简单获取 1 个电子。
所以,氯气的化学性质特别开朗,是一种强氧化剂。
(1)与金属反响: Cu + C12CuCl2实验现象:铜在氯气中激烈焚烧,集气瓶中充满了棕黄色的烟。
一段时间后,集气瓶内壁附着有棕黄色的固体粉末。
向集气瓶内加入少许蒸馏水,棕黄色固体粉末溶解并形成绿色溶液,连续加水,溶液变为蓝色。
2Na + Cl22NaCl实验现象:有白烟产生。
说明:①在点燃或灼热的条件下,金属都能与氯气反响生成相应的金属氯化物。
此中,变价金属如( Cu、Fe)与氯气反响时表现高价态(分别生成 CuCl2、FeCl3)。
②在常温、常压下,干燥的氯气不可以与铁发生反响,故可用钢瓶储存、运输液氯。
③“烟”是固体小颗粒分别到空气中形成的物质。
如铜在氯气中焚烧,产生的棕黄色的烟为CuCl2晶体小颗粒;钠在氯气中焚烧,产生的白烟为NaCl 晶体小颗粒;等等。
(2)与氢气反响。
H2+ Cl22HCl注意:①在不一样样样的条件下, H2与 C12均可发生反响,但反响条件不一样样样,反响的现象也不一样样样。
点燃时,纯净的 H2能在 C12中安静地焚烧,发出苍白色的火焰,反响产生的气体在空气中形成白雾并有小液滴出现;在强光照耀下, H2与 C12的混淆气体发生爆炸。
卤素背记知识点

第一章 物质结构 元素周期律
栏目导引
2.递变性
具体情况如下: (1)与 H2 反应越来越难,对应氢化物的稳定性逐渐减弱,还原性逐渐增强, 其水溶液的酸性逐渐增强,即: 稳定性:HF>HCl>HBr>HI; 还原性:HF<HCl<HBr<HI; 酸性:HF<HCl<HBr<HI。(其中 HF 为弱酸,HCl、HBr、HI 为强酸) (2)最高价氧化物对应的水化物的酸性逐渐减弱,即 HClO4>HBrO4>HIO4。
F Cl Br I
1.相似性:易得一个电子,单质具有氧化性, 2.递变性:从上到下原子核外电子层数依次增多,原子半径逐渐增大 ,得电子能力逐渐减弱,非金属性逐渐减弱 氧化性: F2> Cl2> Br2>I2
1.两组规律 (1)碱金属元素随着原子序数的递增,①元素的金属性逐渐增强;②与水反应 程度越来越剧烈;③氢氧化物的碱性逐渐增强。 (2)卤族元素随着原子序数的递增,①元素的非金属性逐渐减弱;②与 H2 化 合越来越难;③对应氢化物的稳定性逐渐减弱。 2.卤素单质物理性质的记忆口诀 氟气淡黄绿,氯气黄绿色,溴液深红棕,碘是紫黑固,液溴挥发碘升华,单 质有色也有毒。
第一章 物质结构 元素周期律
栏目导引
3.卤族元素的原子结构与性质的关系 卤族元素的原子结构的相同点是最外层电子数都是 7,由此决定了卤素单质 的主要化学性质具有很强的氧化性,易与氢气反应。 卤族元素随着核电荷数的增多,原子的电子层数增多,原子半径逐渐增大, 因此,卤素单质的氧化性逐渐减弱。 4.特殊性 (1)氟元素无正价,无含氧酸。 (2)Br2 在常温下是唯一的一种液态非金属单质。 (3)碘为紫黑色固体,易升华,淀粉遇 I2 变蓝色。
卤素复习补充知识
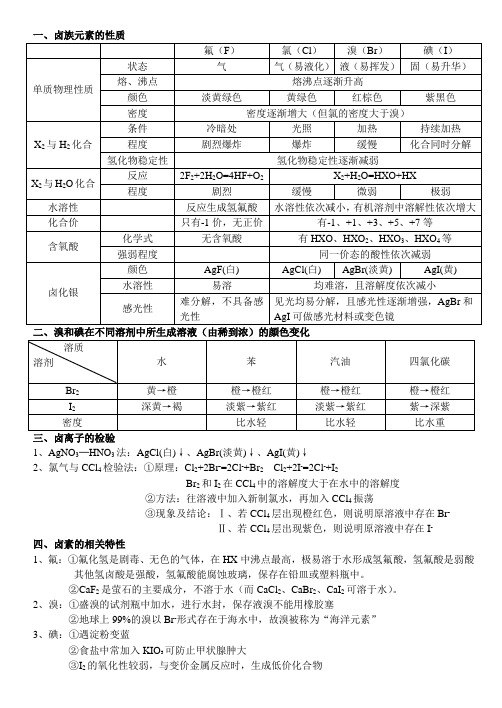
三、卤离子的检验
1、AgNO3─HNO3法:AgCl(白)↓、AgBr(淡黄)↓、AgI(黄)↓
2、氯气与CCl4检验法:①原理:Cl2+2Br-=2Cl-+Br2Cl2+2I-=2Cl-+I2
Br2和I2在CCl4中的溶解度大于在水中的溶解度
②方法:往溶液中加入新制氯水,再加入CCl4振荡
③现象及结论:Ⅰ、若CCl4层出现橙红色,则说明原溶液中存在Br-
Ⅱ、若CCl4层出现紫色,则说明原溶液中存在I-
四、卤素的相关特性
1、氟:①氟化氢是剧毒、无色的气体,在HX中沸点最高,极易溶于水形成氢氟酸,氢氟酸是弱酸
其他氢卤酸是强酸,氢氟酸能腐蚀玻璃,保存在铅皿或塑料瓶中。
②CaF2是萤石的主要成分,不溶于水(而CaCl2、CaBr2、CaI2可溶于水)。
2、溴:①盛溴的试剂瓶中加水,进行水封,保存液溴不能用橡胶塞
②地球上99%的溴以Br-形式存在于海水中,故溴被称为“海洋元素”
3、碘:①遇淀粉变蓝
②食盐中常加入KIO3可防止甲状腺肿大
③I2的氧化性较弱,与变价金属反应时,生成低价化合物。
卤素高考考点
卤素高考考点:考点1:卤素单质及其化合物的主要化学性质是什么?金非水碱盐两硫考点2:氯气的强氧化性和氯水的四大作用的主要内容是什么 ?()漂白、杀菌消毒、与碘化钾考点3:卤化物的俗名具体有哪些?考点4:卤素单质及其化合物的主要用途有哪些?考点5:氯气的实验室制法应注意的八个问题是什么?从原理、原料、装置、除杂质、干燥、检验、收集、吸收八个方面考虑。
考点6:氯化氢的实验室制法中应注意的八个问题是什么?考点7 :卤素物理性质及其递变规律的主要内容是什么?引导学生从颜色、状态、气味、密度、溶解性、熔沸点等方面列表比较。
考点8:卤素化学性质的递变规律有哪些?要求学生从单质的氧化性、卤离子的还原性、气态氢化物的稳定性、气态氢化物的还原性、最高氧化物及其对应水化物的酸性等方面列表比较。
考点9:卤离子的鉴定方法有几种?考点10:正确判断氧化剂和还原剂,物质的氧化性和还原性以及氧化产物和还原产物的方法——十二字方针是什么 ?要求学生从氧化还原反应里的化合价升降、电子转移、氧化剂、还原剂、氧化产物、还原产物的关系等方面画图比较(图略)。
根据图表的关系可以概括成12个字,简称氧化还原反应十二字方针“升—失—氧—还—还—氧;降—得—还—氧—氧—还”。
具体内容可引导学生思考、分析。
考点11:判断物质氧化性和还原性相对强弱的10种方法是什么?考点12:过量计算的方法和具体实例。
在给学生复习过量问题和多步反应的计算时,我给学生归纳总结了这样几句话:化学方程式要配平,换算纯量代方程,左右单位要相应,上下单位须相同,遇到两个已知量,应找不足来进行,遇到多步反应时,关系式法有捷径,关系式来关系量,对准计算细完成。
在学生搞清掌握这几句话的实质后,只讲一个例题,再给学生针对过量或多步反应编选一个练习题,学生就会做到触类旁通,举一反三。
基本概念,基础理论,元素的单质及其化合物,有机化合物,化学实验和化学计算。
卤素的知识点总结
教学目标掌握卤素的性质和制备重点、难点重点:卤素的性质难点:卤素的性质和掌握考点及考试要求主要考察基础及简单应用教学内容一、氯水与次氯酸1、次氯酸的化学性质①次氯酸(HClO)是一元弱酸(酸性比H2CO3还弱),属于弱电解质,在新制氯水中主要以HClO分子的形式存在,因此在书写离子方程式时应保留化学式的形式.②HClO不稳定,易分解,光照时分解速率加快.有关的化学方程式为:2HClO =2H+ + 2Cl- + O2↑,因此HClO是一种强氧化剂.③HClO能杀菌.自来水常用氯气杀菌消毒(目前已逐步用C1O2代替).④HClO能使某些染料和有机色素褪色.因此,将Cl2通入石蕊试液中,试液先变红后褪色.涉及的化学方程式:(1)强氧化性:①漂白作用②杀菌消毒作用(2)不稳定性:见光分解:2HClO 2HCl+O2↑(3)很弱的酸性:HclO H+ + ClO-注:比较次氯酸和碳酸的酸性强弱:Ca(ClO)2+2H2O+2CO2→Ca(HCO3)2+2HCl2、新制氯水和久置氯水的区别?新制久置颜色浅黄绿色无色气味刺激性无味成分 Cl 2 H 2O HCl HClOH 2O HCl 微粒 H 2O Cl 2 HClO H +Cl - ClO - OH -H 2O H +Cl - OH -性质更强的氧化性更强的酸性小结:氯水的性质 1、酸性:HCl HClO 2、Cl -的性质:加AgNO 3溶液有白色沉淀 二、漂粉精和水的消毒1、制取 ⑴原理:氯气与碱反应生成次氯酸盐;⑵原料:氯气和消石灰⑶反应式:2Ca(OH)2+2Cl 2 CaCl 2+Ca(ClO)2+2H 2O2、成分:Ca(ClO)2 与CaCl 2 (因此,漂粉精是混合物) 有效成分:Ca(ClO)23、杀菌、消毒、漂白原理: 次氯酸盐与酸作用生成次氯酸Ca(ClO)2 + 2HCl → CaCl 2 + 2HClO 空气中:Ca(ClO)2 + H 2O + CO 2→ CaCO 3 + 2HClO 三、卤素1、[卤族元素] 简称卤素.包括氟(F)、氯(C1)、溴(Br)、碘(I)和放射性元素砹(At).在自然界中卤素无游离态,都是以化合态的形式存在. [卤素单质的物理性质]颜色状态(常态)熔点、沸点溶解度(水中)密度F 2 浅黄绿色 浅深气体 低高降低小大Cl 2 黄绿色气体 部分溶于水,并与水发生不同程度反应Br 2深红棕色 液体易挥发 I 2紫黑色固体升华说明 (1)实验室里,通常在盛溴的试剂瓶中加水(即“水封”),以减少溴的挥发.(2)固态物质不经液态而直接变成气态的现象,叫做升华.升华是一种物理变化.利用碘易升华的性质,可用来分离、提纯单质碘.(3)Br 2、I 2较难溶于水而易溶于如汽油、苯、四氯化碳、酒精等有机溶剂中.医疗上用的碘酒,就是碘(溶质)的酒精(溶剂)溶液.利用与水互不相溶的有机溶剂可将Br 2、I 2从溴水、碘水中提取出来(这个过程叫做萃取). 2、卤素单质的化学性质递变规律:随着核电荷数的增大,因原子半径增大,得电子能力(即氧化性)减弱,其离子还原性增强,卤化氢稳定性减弱,对应的酸酸性增强。
卤素知识点重点总结
卤素知识点重点总结
1. 卤素的性质和特点
卤素的原子结构非常稳定,它们的电子排布为ns^2np^5(n为能级数),因此它们都是
单原子分子,具有较高的电子亲和能和电负性。
卤素的物理性质有色、味道和气味,随着
原子序数的增加,颜色逐渐加深,味道逐渐变苦,气味逐渐加重。
除氟气外,其他卤素均
为二原子分子。
2. 卤素的化学性质
卤素的化学性质非常活泼,它们可以和大多数元素发生化学反应。
卤素和金属反应时,会
生成卤化物,如NaCl(氯化钠)、KBr(溴化钾)等。
卤素和非金属反应时,则会生成酸
类物质,如HCl(盐酸)、HBr(溴酸)等。
卤素也可以和氢气反应,生成氢卤酸。
3. 卤素的应用
卤素在生活和工业中有着广泛的应用。
氯代烃是重要的有机溶剂,可用于化工、医药等行业;氯气用于漂白剂的生产;溴化物可以用作防腐剂和杀菌剂;碘化物可用于药品和影像
学领域;氟化物广泛应用于非金属冶炼和陶瓷工业。
4. 卤素的环境影响
卤素具有强烈的毒性和腐蚀性,对环境和生物造成严重危害。
大量的卤素排放会导致土壤
和水体的污染,对植物和动物的生长和繁殖产生不利影响,甚至引发严重的环境灾害。
因此,对卤素的排放和应用必须严格控制,采取有效的环境保护措施。
总的来说,卤素是一类具有重要化学性质和广泛应用的元素,但也具有较强的毒性和腐蚀性,需要引起足够重视。
在今后的科研和生产中,应当更加深入地研究卤素的性质和影响,寻求更加有效的解决方案,以保护人类和环境的健康。
卤素(复习)正式版
第三节 氧化还原反应(一)
一.知识要点: 1.氧化还原反应的实质是_电__子__转__移___.表观现象是_化__合_价__升__降_____.
通常用_化__合_价__的变化 来作为判断氧化还原反应的依据.
2.以化合价升降与电子得失的关系来理解有关概念:
+2e Zn+2HCl=ZnCl2+H2
a.尾气(Cl2)处理 NaOH + Cl2==NaCl+H2O b.制取漂白粉 Ca(OH)2 + 2Cl2==CaCl2+Ca(ClO)2+H2O
版权所有:深圳华人教育有限公司
3、氯气的实验室制法
(1)原浓理盐酸HC的l 代+ 氧替化品剂为-:-_-浓_C_lH_2(_2氧_S_O化_4_.剂N__a:_MC_ln_O_ 2
5.有关物质的量的计算
版权所有:深圳华人教育有限公司
第三节 氧化还原反应(二)
一.知识要点
1.氧化还原方程式的配平
(1)方法: (2)原则: (3)遵循:
化合价升降法 化合价升高和降低总数相等 质量守恒定律,电荷守恒
2.氧化还原反应的应用
(1)定性判断: a.概念的理解,b.排列顺序(氧化性,还原性),
Cl2<--------HCl---------->H2 (3)Cl-的检验:(AgNO3+HNO3)
(三) HCl 的实验室制法. 可溶性氯化物+浓H2SO4(或H3PO4)---------->HCl
(1)此原理利用了浓H2SO4及H3PO4的__________性.据此原理, 能否制取 HBr.HI?为什么?
(1)与氢气反应渐难 表现为 (2)与变价金属 (金属的化合价) 版权所有:深圳华人教育有限公司
