弱电解质电离度及电离常数
实验一 电导法测定弱电解质的电离平衡常数

实验一电导法测定弱电解质的电离平衡常数实验目的:通过电导法测定弱电解质的电离平衡常数,探究电导法测定电离平衡常数的原理和操作方法。
实验原理:弱电解质的电离平衡常数K为:K=α²C/(1-α) (其中,α表示电离度,C表示弱电解质的浓度)。
由于弱电解质的电离度很小,可以近似认为它的电离度是常数。
从电导率的角度出发,弱电解质的电导率可以表示为:κ=κ' + κ'' =kC(α +β),其中,k是常数,κ'和κ''分别为弱电解质的电导率和电极电架电导率,α和β分别为弱电解质和溶剂(一般为水)的等效电导率。
通常实验中只能测量到总电导率,但是可以通过电导率对浓度和电离度的关系进行分析,进而计算出弱电解质的K值。
实验步骤:1.将所需量的KCl、NaCl和HCl等指定量的不同浓度的溶液加入电导池中。
在每次测量前,用去离子水清洗电导池。
2.打开电导计电源开关,选择对应的测量范围,将电导池放入电导计的电极架内。
3.读取电导计显示的电导率值,将其记到实验记录表中。
4.根据所加入的某一种量浓度的水溶液电离平衡常数的已知值,计算α和K值。
将计算结果记录到实验记录表中。
5.重复以上步骤,测定其他浓度水溶液的电导率和计算α和K值。
6.将α和K值以绘制α和C的曲线等形式呈现。
通过分析α和C的曲线,确定弱电解质的电离平衡常数K。
实验注意事项:1.电导池在使用前需清洗,以保证测量结果的准确性。
2.一定要记录所有测量数据,保证测量结果的可重复性。
3.将实验结果以图表等形式呈现,进行分析和论证。
实验结果:所得结果表明,电导法测定弱电解质的电离平衡常数是可靠准确的。
通过实验,还可以得到弱电解质电离度与浓度的变化规律,进一步了解了电解质溶液中的离子平衡关系。
电离度和电离平衡常数

湖北省黄石市第七中学
探究实验:
利用数字化传感器探究升高温度情况下醋酸溶液的PH值的变化情况? 升温有利于电离平衡正向还是逆向移动? PH减小,平衡向电离方向移动。
湖北省黄石市第七中学
湖北省黄石市第七中学
探究实验:
保持温度不变,稀释0.1mol/L醋酸溶液至 0.001mol/L浓度过程中,PH值的变化情况。 讨论曲线的变化趋势并分析原因。
湖北省黄石市第七中学
体验数据之美
——探究弱电解质的电离平衡(第二课时)
主讲人: 陈雄伟 参赛学校:湖北省黄石市第七中学 使用教材:化学(拓展型课程)
上海科学技术出版社出版
湖北省黄石市第七中学
湖北省黄石市第七中学
了解大纲: 一、认识弱电解质在水溶液中存在电离程度 二、了解电离平衡常数的含义。 三、从定量的角度建立对弱电解质电离平衡 及条件改变后平衡的移动的认识。
湖北省黄石市第七中学
湖北省黄石市第七中学
自学:
课本P60有关电离平衡常数的相关 内容,并完成课堂练习T1、2。
湖北省黄石市第七中学
湖北省黄石市第七中学
湖北省黄石市第七中学
拉
居
瓦
里
锡
夫
和
人
他
的
夫Байду номын сангаас
人
湖北省黄石市第七中学
湖北省黄石市第七中学
电离度:弱电解质在溶液里达到电离平衡时,已 电离的电解质分子数占原来总分子数的百分数。
电离度(α)= 已电离的电解质分子数 ×100% 溶液中原有电解质总分子数 = 已电离的电解质物质的量 ×100% 溶液中原有电解质总物质的量 = 已电离的电解质浓度 ×100% 溶液中原有电解质总浓度
常见弱电解质电离平衡常数表
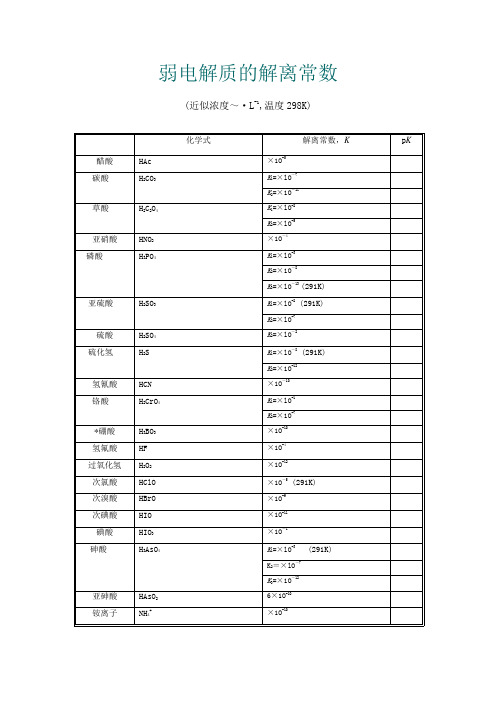
弱电解质的解离常数(近似浓度~·L-1,温度298K)名称化学式解离常数,K p K 醋酸HAc×1O-5碳酸H2CO3K1=×lO-7K2=×1O-11草酸H2C2O4K1=×lO-2K2=×lO-5亚硝酸HNO2×1O-4磷酸H3PO4K1=×lO-3K2=×1O-8K3=×lO-13 (291K)亚硫酸H2SO3 K1=×lO-2 (291K)K2=×lO-7硫酸H2SO4K2=×lO-2硫化氢H2S K1=×lO-8 (291K)K2=×1O-12氢氰酸HCN×1O-1O铬酸H2CrO4K1=×lO-1K2=×1O-7*硼酸H3BO3×1O-1O氢氟酸HF×1O-4过氧化氢H2O2×1O-12次氯酸HClO×1O-5 (291K)次溴酸HBrO×1O-9次碘酸HIO×1O-11碘酸HIO3×1O-1砷酸H3AsO4 K1=×lO-3 (291K)K2=×lO-7K3=×1O-12亚砷酸HAsO26×1O-1O铵离子NH4+×1O-1O氨水NH3·H2O×1O-5联胺N2H4×1O-7羟氨NH2OH×1O-9氢氧化铅Pb(OH)2×1O-4氢氧化锂LiOH×1O-1氢氧化铍Be(OH)2×1O-6BeOH+×1O-9氢氧化铝A1(OH)3×1O-9Al(OH)2+×1O-1O氢氧化锌Zn(OH)2×1O-7氢氧化镉Cd(OH)2×1O-11*乙二胺H2NC2H4NH2K1=×lO-5K2=×lO-8*六亚甲基四胺(CH2)6N4×1O-9 *尿素CO(NH2)2×1O-14*质子化六亚甲基四胺(CH2)6N4H+×1O-6甲酸HCOOH ×1O-4 (293K)氯乙酸ClCH2COOH×1O-3氨基乙酸NH2CH2COOH×1O-1O*邻苯二甲酸C6H4(COOH)2K1=×1O-3K2=×1O-6柠檬酸(HOOCCH2)2C(OH)COOH K1=×1O-4K2=×1O-5 (293K)K3=×1O-7-酒石酸(CH(OH)COOH)2K1=×1O-3K2=×1O-5*8-羟基喹啉C9H6NOH K1=8×lO-6K2=1×1O-9苯酚C6H5OH ×1O-1O (293K)*对氨基苯磺酸H2NC6H4SO3H K l=×lO-lK2=×1O-4*乙二胺四乙酸(EDTA) (CH2COOH)2NH+CH2CH2NH+(CH2COOH)2K5=×1O-7K6=×1O-11。
电离度和电离平衡常数

H++HCO3-
K1 C(H ) C(HCO3 ) C(H 2CO3)
HCO3-
H++CO32-
K 2 C(H ) C(CO32 ) C(HCO3 )
每步电离都各有电离常数,分别用K1、K2表示。在 25℃时,K1=4.2×10-7,K2=5.6×10-11,K1>>K2, 一般说,多元弱酸溶液的酸性主要由第一步电离决定。
方法一、取同浓度的HCl和CH3COOH,进行溶液导 电性实验
方法二、测定CH3COONa的水溶液应呈碱性。 方法三、测定0.1mol/L CH3COOH 的pH值。 方法四、相同浓度的HCl 和 CH3COOH 和相同大
小颗粒的锌粒比较反应速率。
方法五、相同 pH值,相同体积 的HCl 和 CH3COOH, 和足量的锌粒反应, CH3COOH产生的氢气多。
越热温越度。电离, 越稀越电离(电离过程吸热)
用电离度比较弱电解质的相对强弱时必须在同 温同浓度条件下 一般不注明温度是指25℃
表 不同浓度HAc的电离度α和[H+]
c/(mol.L-1) 0.020 0.100 0.200
α(%) 2.95 1.32 0.932
[H+]/(mol.L-1)
5.90×10-4 1.32×10-3 1.86×10-3
酸 HA
K
水溶液
中的酸
(25 oC )
稀磷酸溶液中C(H+)>>C(PO43-) 而非C(H+)=3C(PO43-)
H3PO4+H2O
H2PO4 - +H3O+
Ka1
[H2PO4][H3O] 6.92103 [H3PO4]
弱电解质的电离平衡

稀释相 同倍数 后pH 小 大
相同pH、相同体积时 pH、 同体积时 比较 C(H+) 项目 HA HB 相同 相同 C(酸 C(酸) 中和碱 与活泼金 与金属反 的能力 属反应产 应的开始 生H2的量 速率 小 大 小 大 相同 相同 稀释相 同倍数 后pH 大 小
小 大
四、强电解质和弱电解质的证明方法
冰醋酸加水溶解并不断稀释过程中, 1、冰醋酸加水溶解并不断稀释过程中,溶 液导电能力与加入水的体积有如下变化关系: 液导电能力与加入水的体积有如下变化关系 : 试回答: 试回答: 点导电能力为0 ⑴“0”点导电能力为0的理由是: 冰醋酸中只 0 点导电能力为 的理由是: 存在醋酸分子,无离子。 存在醋酸分子,无离子。 ⑵a、b、c三点对应溶液的PH值由大到小的 顺序是 a﹥c﹥ b ⑶a、b、c三点中电离程度最大的是 C 。电 离平衡常数的关系 相等 . 若使c点溶液中C(Ac ⑷若使c点溶液中C(Ac-)、PH 值均增大,可采取的措施有: 值均增大,可采取的措施有: ①加碱②加碳酸钠③加镁或锌 加碱②加碳酸钠③
下表是常见弱酸的电离平衡常数(25℃) 下表是常见弱酸的电离平衡常数(25℃)
酸 醋酸 碳酸 氢硫酸 电离方程式 电离平衡常数K 电离平衡常数K
CH3COOH ⇌ CH3COO-+H+
H2CO3 ⇌ H++HCO3HCO3- ⇌ H++ CO32H2S ⇌ H++HSHS- ⇌ H++ S2H3PO4 ⇌ H++H2PO4H2PO4— ⇌ H++HPO42HPO42— ⇌ H++PO43-
回答下列各问题: 回答下列各问题:
弱酸电离度与电离常数的测定实验报告

弱酸电离度与电离常数的测定实验报告弱酸电离度与电离常数的测定试验报告范文1一、试验目的1、测定醋酸电离度和电离平衡常数。
2、学习使用pH计。
3、把握容量瓶、移液管、滴定管基本操作。
二、试验原理醋酸是弱电解质,在溶液中存在下列平衡:HAc+H+?Ac-[H][Ac]c2Ka[HAc]1式中[H+]、[Ac-]、[HAc]分别是H+、Ac-、HAc的平衡浓度;c 为醋酸的起始浓度;Ka为醋酸的电离平衡常数。
通过对已知浓度的醋酸的pH值的测定,按pH=-lg[H+]换算成[H+],[H]依据电离度,计算出电离度α,再代入上式即可求得电离平衡常数Ka。
三、仪器和药品仪器:移液管(25mL),吸量管(5mL),容量瓶(50mL),烧杯(50mL),锥形瓶(250mL),碱式滴定管,铁架,滴定管夹,吸气橡皮球,Delta320-SpH计。
药品:HAc(约0、2mol?L-1),标准缓冲溶液(pH=6、86,pH=4、00),酚酞指示剂,标准NaOH溶液(约0、2mol?L-1)。
四、试验内容用移液管吸取25mL约0、2mol?L-1HAc溶液三份,分别置于三个250mL锥形瓶中,各加2~3滴酚酞指示剂。
分别用标准氢氧化钠溶液滴定至溶液呈现微红色,半分钟不褪色为止,记下所用氢氧化钠溶液的体积。
从而求得HAc溶液的精确浓度(四位有效数字)。
用移液管和吸量瓶分别取25mL,5mL,2、5mL已标定过浓度的HAc溶液于三个50mL容量瓶中,用蒸馏水稀释至刻度,摇匀,并求出各份稀释后的醋酸溶液精确浓度(cc,210c)的值(四位有效数字)。
用四个干燥的50mL烧杯分别取30~40mL上述三种浓度的'醋酸溶液及未经稀释的HAc溶液,由稀到浓分别用pH计测定它们的pH值(三位有效数字),并纪录室温。
依据四种醋酸的浓度pH值计算电离度与电离平衡常数。
五、数据纪录和结果1、醋酸溶液浓度的标定滴定序号标准NaOH溶液的浓度/mol?L-1所取HAc溶液的量/mL标准NaOH 溶液的用量/mL试验测定HAc测定值溶液精确浓度/mol?L-1?平均值2、醋酸溶液的pH值测定及平衡常数、电离度的计算?t=℃HAc溶液编号1?(c/20)2?(c/10)3?(c/2)4?(c)cHAc/mol?L-1pH[H+]/mol?L-1α/%Ka六、预习要求及思考题(1)专心预习电离平衡常数与电离度的计算方法,以及影响弱酸电离平衡常数与电离度的因素。
弱电解质电离常数的测定实验报告

弱电解质电离常数的测定实验报告实验报告:弱电解质电离常数的测定摘要:本实验采用了电导法和pH法,测定了弱电解质乙酸的电离常数。
实验结果表明,在本实验条件下,乙酸的电离常数(K)为1.42×10^-5。
引言:弱电解质的电离常数是描述其电离程度的重要参数。
而弱电解质的电离程度又对其化学性质和物理性质的表现产生重要影响。
因此,测定弱电解质的电离常数是化学实验中非常重要的一项内容。
本实验采用了两种方法测定弱电解质电离常数:电导法和pH 法。
电导法是通过测量溶液电导率的方式,求出电离度,再根据电离度求出电离常数。
而pH法则是引入指示剂,通过观察溶液酸碱指示剂的颜色变化,来测定溶液的pH值,再根据酸碱平衡理论求出电离常数。
两种方法各具特点,都有其适应性较广的实验条件。
实验方法:1. 电导法:实验准备:分别将乙酸(CH3COOH)和氯化钠(NaCl)粉末称取适量加入两个干燥的量筒中。
在称量过程中,要求精确且取样量应相同。
将两个量筒分别加入水后摇匀,使其完全溶解,制成1 mol/L的标准溶液。
实验过程:(1)实验前,使用电导仪对电极进行标定,并检查仪器应用状态是否正常。
(2)将不同体积的乙酸溶液加入电导池中,测定每个体积下的电导率,记录数据。
(3)将不同体积的氯化钠溶液加入电导池中,测定每个体积下的电导率,记录数据。
实验准备:分别将pH值各不相同的缓冲溶液制备好,乙酸和氯化钠的标准溶液也需要提前制备好。
实验过程:(1)将乙酸标准溶液倒入盛有相同体积缓冲溶液的比色皿中,然后将一定体积的NaOH溶液导入其中,观察pH值变化,并记录所导入NaOH溶液的体积。
这样做是为了制备满足pH值要求的乙酸缓冲溶液。
(2)当制作好乙酸缓冲溶液后,将其与NaCl混合制成一定浓度的混合溶液,并在其中加入酸碱指示剂,以观察其pH值的变化,并记录所导入NaOH溶液的体积。
(3)根据获得的数据,计算出乙酸的电离度和电离常数。
实验结果:1. 电导法:可计算出不同体积下的溶液电导率,进而计算出溶液的电离度。
弱电解质电离平衡常数

能力由强到弱的顺序为
。
一、电离平衡常数应用(只受温度影响,)
酸 醋酸
次氯酸
碳酸
亚硫酸
K K=1.75×10- K=2.98×10-8 K1=4.30×10-7 K1=1.54×10-2
5
K2=5.61×10-11 K2=1.02×10-7
3、判断反应能否发生:强酸制弱酸
①2CH3COOH + CO32—=2 CH3COO—+H2O+CO2 ↑ ②Ca(ClO)2中通入少量SO2: H2O+SO2+2ClO-+Ca2+=CaSO3↓+2HClO 因氧化还原反应,产物不正确
1.判断:①电离常数大的酸溶液中c(H+) 一定比 电离常数小的酸溶液大。 错,浓度不确定
追问:相同温度和浓度时,电离常数大的酸溶 液中c(H+) 一定比电离常数小的酸溶液大。 正确
②相同温度下,0.1mol/L CH3COOH溶液比 0.01mol/L CH3COOH溶液的电离常数大。 错,Ka只与温度有关。
判断下列反应能否发生
A
A. CO2+H2O+ ClO-=HClO+ HCO3-
B. CO2+H2O+ 2ClO-=2HClO+ CO32-
②比较HR和HR1的酸性强弱
NaR+CO2+H2O=HR+NaHCO3
2NaR1+CO2+H2O=2HR1+Na2CO3
HR1弱
弱电解质电离平衡常数
1.衡量化学反应进行程度用化学平衡常数
对于一般的可逆反应 mA(g)+nB(g) pC(g)+qD(g),在一定温
度下,K=
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
弱电解质电离度及电离常数
电离度是指物质电子分子电量比值的度量,也就是电子分子强弱的度量,衡量物质压强,又称为离子容量。
电离常数也称为电解质常数,是指在特定温度、压强和其他影响因素下,水受到强电场刺激时电离成H+和OH-的比例,理想情况下,通常在25℃的常数是1.0,
H+和OH-的数量相等。
弱电解质电离度是指弱电解质在某特定条件下,将溶液及其他分解成其他离子,电荷等产
物的能力。
它能反映出弱电解质在电解过程中的离子分布以及电性质的变化程度。
电解质
的电离度要比无电解质的溶液高得多,离子形成的电位也高得多,因此说电解质是一种强
离子溶液。
此外,电解质的电离度不同,电离常数也不尽相同,同样电解质的电离常数也
随温度的变化而变化。
因此,电离度和电离常数对于合成试剂等物质的运转至关重要。
如果电离度不合格,会影
响物质的分解效果,电离常数过高,也会导致试剂过度分解,从而降低整体性能,所以重视电离度和电离常数的维护非常重要。
