2018届中考化学压轴题揭秘专题16综合计算(中考题,无答案)(优选.)
2018中考化学:计算压轴题总结

2018中考化学:计算压轴题总结各位读友大家好,此文档由网络收集而来,欢迎您下载,谢谢1.用氯酸钾和二氧化锰的混合物16g,加热制取氧气,待完全反应,冷却后称量,得到固体物质,计算原混合物中二氧化锰的质量。
2.刘彬同学的姑父从三峡搬迁到我们家乡后,准备兴建一座碳酸钙精粉厂。
为检测当地石灰石中碳酸钙的纯度,他在实验室用6g石灰石样品与19g稀盐酸恰好完全反应,测得残留物为。
求:依椐质量守恒定律,生成二氧化碳_______g;样品中碳酸钙的质量分数;所用稀盐酸溶液中溶质的质量分数。
3.由硫元素和铜元素组成的一种化合物,高温条件下在空气中充分煅烧,只得到气体SO2和固体CuO。
要使煅烧后的固体CuO完全溶解,可加入适量稀硫酸。
计算至少需要溶质质量分数为10%的稀硫酸多少克?运用所学知识和上述数据进行分析,这种硫化物的化学式为_____。
4.曲酸是一种新型添加剂,它具有广泛的抗菌作用,作为防腐剂添加于食品中,具有非常好的效果.曲酸的相对分子质量是,曲酸中碳、氢、氧三种元素的质量比是某工厂的废料中含铁和铜,需回收此废料中的铜.现取铁和铜的混合物样品l0g,向其中加入废弃的稀硫酸50g恰好完全反应,产生。
求:①废料中铜的质量分数。
②废弃稀硫酸中硫酸的质量分数。
5.侯德榜是我国著名的化学家。
由他发明的侯氏制碱法制得的纯碱中可能含有少量氯化钠。
现取仅含氯化钠杂质的纯碱样品,加入130g稀盐酸中,恰好完全反应,得氯化钠溶液150g。
求:该纯碱样品中Na2CO3的质量;反应后所得溶液中溶质的质量分数。
6.某矿井采出的食盐中含有CaCl2,为设计除杂方案需测定CaCl2的含量;取上述井盐,向其中加入100g质量分数为%的Na2CO3溶液恰好完全反应。
若样品检测过程在露℃的恒温下进行,此时NaCl的溶解度为36g。
取样检测后的溶液中,Na+与Cl-的数量比为。
求检测后的溶液中NaCl的质量及井盐中CaCl2的质量分数。
2018中考化学压轴计算题解题分析

2018中考化学压轴计算题解题分析
化学计算常考题介绍
中考化学试卷的最后一题计算是中考中的压轴计算题,它考
查学生对质量守恒定律、方程式计算、溶质质量分数的计算
以及酸碱盐部分的知识,考查知识综合,难度较大。
题目主
要分为文字叙述型计算、表格计算、图像计算、探究实验计
算。
以下详细地进行介绍:
文字叙述型计算
主要考察学生归纳整理题目中隐含信息的能力,难点往往在
于“题目文字过多,流程过于复杂,读不懂题,找不到已知,不会列有效的等式求出未知数”。
考题经常将溶液和化学方
程式结合在一起进行计算,对学生的题目分析理解能力较
高,情景比较复杂。
解题时,应首先明确所求溶液中溶质是
什么,溶质的质量可以通过化学方程式得出。
其次,应明确
所求溶液的质量如何计算。
最后运用公式计算出溶液的质量
分数。
最终溶液的质量=反应前各物质的质量总和-难溶性杂质(反应前混有且不参加反应)-生成物中非溶液(生成沉淀
或气体)。
决胜2018中考化学压轴题揭秘 专题16 综合计算(中考题,无答案)
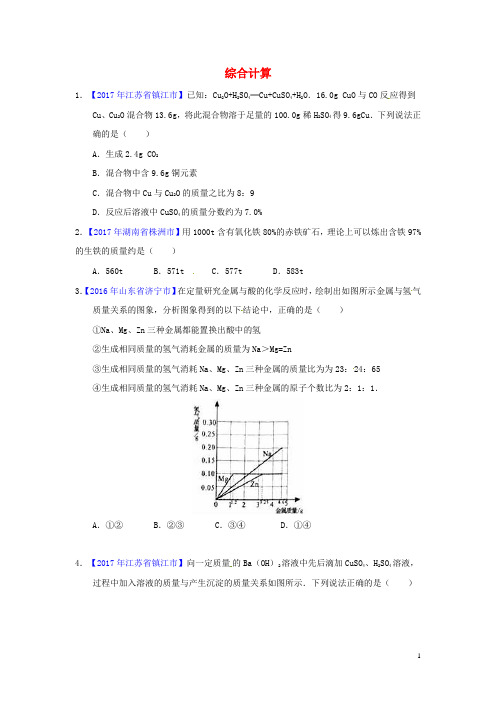
综合计算1.【2017年江苏省镇江市】已知:Cu2O+H2SO4═Cu+CuSO4+H2O.16.0g CuO与CO反应得到Cu、Cu2O混合物13.6g,将此混合物溶于足量的100.0g稀H2SO4得9.6gCu.下列说法正确的是()A.生成2.4g CO2B.混合物中含9.6g铜元素C.混合物中Cu与Cu2O的质量之比为8:9D.反应后溶液中CuSO4的质量分数约为7.0%2.【2017年湖南省株洲市】用1000t含有氧化铁80%的赤铁矿石,理论上可以炼出含铁97%的生铁的质量约是()A.560t B.571t C.577t D.583t3.【2016年山东省济宁市】在定量研究金属与酸的化学反应时,绘制出如图所示金属与氢气质量关系的图象,分析图象得到的以下结论中,正确的是()①Na、Mg、Zn三种金属都能置换出酸中的氢②生成相同质量的氢气消耗金属的质量为Na>Mg=Zn③生成相同质量的氢气消耗Na、Mg、Zn三种金属的质量比为为23:24:65④生成相同质量的氢气消耗Na、Mg、Zn三种金属的原子个数比为2:1:1.A.①② B.②③ C.③④ D.①④4.【2017年江苏省镇江市】向一定质量的Ba(OH)2溶液中先后滴加CuSO4、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图所示.下列说法正确的是()A.a点对应溶液pH>7 B.b点对应溶液中溶质有2种C.m=3.31 D.取c点对应溶液,滴加NaOH溶液,立刻产生沉淀5.【2017年广西省桂林市】小甜利用石灰石和稀盐酸进行如下实验,操作过程和数据如图所示(样品中的杂质不与酸反应也不溶于水).(1)20g石灰石样品中CaCO3的质量为 g.(2)列式计算不饱和溶液A的溶质质量分数(结果准确到0.1%).6.【2017年山东省潍坊市】实验室有一部分被氧化成氧化镁的镁粉样品、未知浓度盐酸和40%的氢氧化钠溶液。
兴趣小组同学为分析样品中金属镁的质量百分含量和计算盐酸的质量分株,进行如下探究:(1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。
化学中考压轴题及答案2018

化学中考压轴题及答案2018
宇宙是由物质组成的,化学则是人类认识和改造物质世
界的主要方法和手段之一。
查字典化学网为大家准备了化学
中考压轴题及答案,快来练习。
化学中考压轴题及答案2018
一、选择题(每题各有一个正确答案,共16道小题,每题1分,共16分)
1.(1分)(2018?青岛)厨房里发生的下列变化中,不涉及化学变化的是( )
A. 菜刀生锈
B. 葡萄酿酒
C. 食品发霉
D. 瓷盘摔碎
考点:化学变化和物理变化的判别.
专题:物质的变化与性质.
分析:化学变化是指有新物质生成的变化,物理变化是指
没有新物质生成的变化,化学变化和物理变化的本质区别是。
2018年中考化学答题技巧:计算压轴题篇-文档资料

2018中考化学答题技巧:计算压轴题篇
计算题是中考化学考试的一个难点,主要分布在选择题24或25题和最后一个大题。
一般技巧型的计算题,一般可以用守恒法、极限、平均值法、差量法、假设数据法来解答。
以下,小编就给大家一一介绍。
1、守恒法
守恒法解题的核心就是质量守恒定律中的六不变。
除此之外,化学中的等量关系还表现为同一物质中的电荷守恒、化合物中化合价守恒、同一化合物等量关系。
学生对于挖掘题目中隐含的等量关系的能力较弱,对于物质和元素质量关系不能很好地建立联系。
2、极限、平均值法
在处理复杂的模糊题型的选择题时,此方法可以直接求解出设定的参量(平均值或极值),然后用此参量与各选项做比较确定符合题意的选项。
学生的思维误区一般是不能准确确定设定的参量。
3、差量法
化学反应都遵循质量守恒定律,有些反应在遵循质量守恒定律的同时,会出现固、液、气体质量在化学反应前后有所改变的现象,同一状态的物质的质量遵循化学反应中各物质之间的固定的质量关系,因此,在根据方程式的计算引入差量,根据变化值可以求出反应物或生成物的质量。
差量法的难点
在于学生找不到计算的差量,而且不知道同一状态的物质质量的差与物质的质量也成比例。
4、假设数据法
根据题目中涉及的化学反应中物质的相对质量结合题意假设适合计算的数据进行计算。
学生的思维误区一般是质量分数计算、物质的质量的计算、元素的质量计算,粒子个数的计算不能很好的进行迁移。
专题16 综合计算(中考题)-决胜2019中考化学压轴题全揭秘精品(原卷版)

决胜2019中考化学压轴题全揭秘之中考题专题16 综合计算1.【2018年甘肃省平凉市】用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸碱度变化如下图所示。
请计算:(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水__________克.(2)当a为80g时,所得溶液中溶质的质量分数是___________(结果精确到0.1%)?2.【2018年四川省德阳市】某工厂利用废硫酸与废铁屑反应制取硫酸亚铁。
现取废硫酸4.9 t 与足量的废铁屑反应,得到FeSO4 1.52 t。
计算废硫酸中H2SO4的质量分数为_______________。
3.【2018年四川省达州市】实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g 碳酸钠溶液,将150g氯化钙溶液分四次加入,充分反应,四次测量所得数据如下表所示:次数累计加入氯化钙溶液的质量/g 烧杯中溶液的总质量/g一40 134二80 168三120 202四150 232(1)恰好完全反应时,生成沉淀的总质量为____g(2)第四次测量时,所得溶液中的溶质有_______(填化学式)。
(3)计算氯化钙溶液的溶质质量分数为______________(写出计算过程)。
4.【2018年四川省巴中市】小华有一只银手镯(银锌合金),她想用实验探究手镯中银的含量。
先用电子秤称得手镯的质量是25.00克,再用稀盐酸分多次与此手镯充分反应。
实验数据如下表:第1次第2次第3次第4次第5次加入烯盐酸的质量(克) 10.00 10.00 10.00 10.00 10.00充分反应后剩余固体的质量(克) 24.35 23.70 23.05 23.00 23.00根据上表中数据分析,完成下列问题:(1)手镯中银的质量是________克。
(2)所用稀盐酸中溶质的质量分数是多少________?5.【2018年山东省威海市】向20g,铜锌合金中不断加入一定溶质质量分数的稀盐酸,加入稀盐酸的质量与固体质量的关系如图所示。
2018年中考化学真题分类汇编计算题含解析

2018年中考化学真题分类汇编:综合计算题(一)1.(18安徽)尿素[CO(NH2)2]是一种常见的氮肥,工业上制备反应如下:CO2+2NH3CO(NH2)2+H2O,请计算:(1)尿素中氮元素的质量分数。
(2)生产6t尿酸理论上需要氨气的质量是多少?化学试题参考答案及评分标准【答案】(1)46.7%;(2)3.4t。
【解析】(1)尿素中氮元素的质量分数为:×100%=46.7%(2)设理论上需要氮气的质量为x。
CO2+2NH3CO(NH2)2+H2O3460x6tx=3.4t答:生产6t尿酸理论上需要氨气的质量是3.4t。
2.(18福建)一种新型“人造树叶”可吸收二氧化碳并转化为乙醇(C2H5OH)燃料,化学方程式为2CO2+3H2OC2H5OH+3O2。
研究显示,一升“人造树叶”每天可从空气中吸收968gCO2。
(1)一升“人造树叶”工作一天可得到乙醇的质量是________?(2)若每天一棵树平均可吸收48.4gCO2,则一升“人造树叶”吸收的CO2相当于_______棵树吸收的CO2。
【答案】(1).506g(2).20【解析】根据反应的化学方程式计算解答。
(1)设一升“人造树叶”工作一天可得到乙醇的质量为x。
2CO2+3H2O C2H5OH +3O28846968gxx=506g(2)968g÷48.4g=20答:(1)一升“人造树叶”工作一天可得到乙醇的质量是506g;(2)若每天一棵树平均可吸收48.4gCO2,则一升“人造树叶”吸收的CO2相当于20棵树吸收的CO2。
3.(18甘肃)用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸碱度变化如下图所示。
请计算:(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水__________克.(2)当a为80g时,所得溶液中溶质的质量分数是___________(结果精确到0.1%)?【答案】(1)50(2)3.8%【解析】(1)设需要水的质量为x,根据溶质在稀释前后质量不变。
<合集试卷3套>2018届广州市中考化学终极压轴试题

中考化学模拟试卷一、选择题1.如图表示的是物质A~G相互间的关系(“ →” 表示物质间存在的转化关系,“—”表示两端的物质能发生化学反应)A、F都是单质;F是使用最多的金属材料;B是导致温室效应的主要气体;在工业上,C广泛用于玻璃、造纸、纺织和洗涤剂的生产等;E是一种蓝色溶液。
D与E反应的生成物均为沉淀。
结合信息判断下列叙述正确的是A.C是Ca(OH)2B.G一定是盐酸C.F是铜D.D物质可能是Ba(OH)2【答案】D【解析】F是使用最多的金属材料,可得F是铁;B是导致温室效应的主要气体、B是二氧化碳;在工业上,C广泛用于玻璃、造纸、纺织和洗涤剂的生产等、C是碳酸钠;E是一种蓝色溶液,E可能是硫酸铜,由图示可知A可能是碳或氧气,G能够与碳酸钠和铁反应,则G是酸可以是盐酸或硫酸,D既能与碳酸钠反应又能与硫酸铜反应,D与E反应的生成物均为沉淀,则D可以是氢氧化钙,也可以是氢氧化钡。
【详解】A、由分析可知,C为碳酸钠,故选项错误;B、由分析可知,G是酸,可以是盐酸,也可以是硫酸,故选项错误;C、由分析可知,F是铁,故选项错误;D、由分析可知,D可以是氢氧化钙,也可以是氢氧化钡,故选项正确;故选:D。
【点睛】本题考查了常见物质的推断,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可。
2.下列实验操作或结论合理的是A.区分两种常见氮肥氯化铵和硫酸铵,可以通过取样,分别加入少量熟石灰,研磨分辨B.除去二氧化锰中的氯化钾,可以通过加水溶解、过滤、蒸发的实验操作达到目的C.Ca(NO3)2、Na2CO3、NaCl、HNO3不另加试剂就不能将它们区别开来D.在如下图所示的几个实验操作中,错误的操作为②③④①探究酸碱中和②过滤操作③测某浓度浓硫酸的pH④探究反应物接触面积对反应速率的影响【答案】D【解析】A、氯化铵和硫酸铵都能与氢氧化钙反应生成有刺激性气味的氨气,因此无法通过取样,分别加入少量熟石灰,研磨分辨,不符合题意;B、氯化钾溶于水,二氧化锰不溶于水,通过加水溶解、过滤即可达到目的,不符合题意;C、将四种试剂两两混合,有一次沉淀生成,一次气泡产生的是碳酸钠,只有沉淀产生的是硝酸钙,只有气泡产生的是硝酸,无现象的是氯化钠,不另加试剂可以将它们区分,不符合题意;D、①无色酚酞试液遇碱变红,向烧杯中逐渐滴加稀硫酸,稀硫酸与氢氧化钠反应生成硫酸钠和水,酚酞在中性和酸性条件下不变色,红色逐渐消失,故可以探究酸碱中和,操作正确;②过滤操作需“一贴、二低、三靠”,另外还要用玻璃棒引流,操作错误;③浓硫酸具有脱水性,使试纸变黑,不能用pH试纸测定浓硫酸的pH值,操作错误;④稀盐酸的浓度不同,变量不唯一,不能探究反应物接触面积对反应速率的影响,操作错误。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
综合计算
1.【2017年江苏省镇江市】已知:Cu2O+H2SO4═Cu+CuSO4+H2O.16.0g CuO与CO反应得到Cu、Cu2O混合物13.6g,将此混合物溶于足量的100.0g稀H2SO4得9.6gCu.下列说法正确的是()
A.生成2.4g CO2
B.混合物中含9.6g铜元素
C.混合物中Cu与Cu2O的质量之比为8:9
D.反应后溶液中CuSO4的质量分数约为7.0%
2.【2017年湖南省株洲市】用1000t含有氧化铁80%的赤铁矿石,理论上可以炼出含铁97%的生铁的质量约是()
A.560t B.571t C.577t D.583t
3.【2016年山东省济宁市】在定量研究金属与酸的化学反应时,绘制出如图所示金属与氢气质量关系的图象,分析图象得到的以下结论中,正确的是()
①Na、Mg、Zn三种金属都能置换出酸中的氢
②生成相同质量的氢气消耗金属的质量为Na>Mg=Zn
③生成相同质量的氢气消耗Na、Mg、Zn三种金属的质量比为为23:24:65
④生成相同质量的氢气消耗Na、Mg、Zn三种金属的原子个数比为2:1:1.
A.①② B.②③ C.③④ D.①④
4.【2017年江苏省镇江市】向一定质量的Ba(OH)2溶液中先后滴加CuSO4、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图所示.下列说法正确的是()
A.a点对应溶液pH>7 B.b点对应溶液中溶质有2种
C.m=3.31 D.取c点对应溶液,滴加NaOH溶液,立刻产生沉
淀
5.【2017年广西省桂林市】小甜利用石灰石和稀盐酸进行如下实验,操作过程和数据如图所示(样品中的杂质不与酸反应也不溶于水).
(1)20g石灰石样品中CaCO3的质量为 g.
(2)列式计算不饱和溶液A的溶质质量分数(结果准确到0.1%).
6.【2017年山东省潍坊市】实验室有一部分被氧化成氧化镁的镁粉样品、未知浓度盐酸和40%的氢氧化钠溶液。
兴趣小组同学为分析样品中金属镁的质量百分含量和计算盐酸
的质量分株,进行如下探究:
(1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。
实验数据如下表所示:
实验序号所取样品质量(g)所加盐酸质量(g)生成氢气质量(g)Ⅰ16.0 60.0 0.5
Ⅱ16.0 130.0 1.0
Ⅲ16.0 150.0 1.0 镁粉样品中金属镁的质量百分含量为_________________。
(2)向实验Ⅲ后的溶液中加入40%的氢氧化钠溶液,生成沉淀的质量随加入氢氧化钠
溶液质量的变化关系如图所示。
计算盐酸的质量分数。
(写出计算过程)
7.【2016年江西省】小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”
(杂质不参加反应)。
操作过程如下:请计算:
(1)20g样品中碳酸钠的质量为 g;
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩制成“叶脉书签”所需质量分数为10%的氢氧化钠溶液,
需蒸发水 g.
8.【2017年山东省滨州市】小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5g 珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),
记录数据如下:
操作次序第一次第二次第三次第四次剩余固体质量/g 10.8 9.6 8.1 8.1 试计算:
(1)完全反应后生成二氧化碳的质量为____________g;
(2)求该珍珠粉中碳酸钙的质量分数。
9.【2017年湖南省益阳市】如图所示,往水电解器中加入96g蒸馏水和2g Na2SO4(Na2SO4不参与反应,仅起增加水的导电性的作用)组成的混合物,然后进行电解,当负极得到
2g气体时,停止实验(所需相对原子质量:H﹣1、O﹣16).
计算:
(1)停止实验时,电解消耗水的质量是多少?
(2)停止实验后,剩余溶液中Na2SO4的质量分数是多少?
10.【2017年湖北省荆州市】某腐蚀印刷电路板的废液经处理后只含有CuCl2和FeCl2两种溶质,为了分析处理后废液的组成,取200g该废液加入40g废铁屑(杂质不溶于水,也不参与反应),恰好完全反应,过滤经处理得到16g铜,往滤液中加入足量的硝酸银溶液,经过滤、干燥、称量,最终得到114.8gAgCl固体。
回答下列问题:
(1)往废液中加入废铁屑发生反应的化学方程式为___________________________,往滤液中加入硝酸银溶液发生反应的化学方程式为
________________________________。
(2)求滤液中溶质的质量分数(精确到1%)。
(3)求200g废液中FeCl2的质量分数(精确到1%)。
给生活足够的热量,让他充满温度,虽说一份情会随着时间而平淡,但一颗心却可以铭记到永恒,时光可以带走美丽的曾经,却难以覆盖一份心念。
岁月的风沙可以苍老面容,但绝不可以让它石化我们的温情,心暖情自在,时光就不会老去,莫忘给心灵加温。
生活承受着岁月的打磨,一路踩着旅途的平仄,虽不能尽数完善自己的梦想,却也燃起了生命的火热。
心若懂得,一切得失就无关风月,心若明媚,又何惧季节的沧桑。
当血脉涟漪,奔放的节拍就不会搁浅在岁月的泥流中,一束心花也会随时光生成,绽放在尘世的枝头上,悠远着醉人的醇。
——《一抹浅念,岁月留香》
最新文件---------------- 仅供参考--------------------已改成-----------word文本
--------------------- 方便更改赠人玫瑰,手留余香。
