第三节__醛和酮_糖类_(14).ppt
合集下载
2.3.2醛和酮糖类

变 式 训 练
2.已知丁基共有4种,则分子式为C5H10O的醛应 有( ) A.3种 B.4种 C.5种 D.6种
解析:C5H10O符合饱和一元脂肪醛的通式
CnH2nO,可写为C4H9—CHO的结构形式,又已知丁
基共有4种同分异构体,故C5H10O的醛应有4种。
答案:B
栏 目 链 接
①反应条件:一般在铂、镍等催化剂存在时与氢气加成。
②规律总结:
总结: 醛的化学性质
醇
-H(氧化) +H(还原)
① 与H2加成→醇 ② 与O2催化氧化→酸 ③ 与银氨溶液 、新制Cu(OH)2悬浊液→酸 ④ 与溴水、KMnO4溶液 反应→能使之褪 色(反应式不要求)
栏 目 链 接
________________(碳链加长)。 注意:加到羰基氧上的大多数是“H”。
2.氧化反应和还原反应。 (1)氧化反应。 在醛基中,与羰基相连的氢原子由于受羰基中氧原子的影响,比 较活泼,因此醛基容易被氧化成羧基。又由于它是由 C、 H、O 元素 组成,故易燃烧。 点燃 4CO2+4H2O 。 ①燃烧:2CH3CHO+5O2― ― →__________________ ② 催 化 氧 化 :
4.常见的醛和酮的物理性质和用途。
甲醛
结构 简式 状态 溶解性 应用
乙醛
苯甲醛
丙酮
栏 目 链 接
______ HCHO ______ 气体
______ CH 3CHO ______ 液体
______ ______ 液体
______ ______ 液体
易溶于水 ______
(2)常见的加成反应。 写出下列反应的化学方程式。
糖类 课件(共54张PPT)

葡萄糖五乙酸酯
4.发酵成酒精 C6H12O6 酒――化→酶2C2H5OH+2CO2
葡萄糖
能发生银镜反应或与新制Cu(OH)2悬浊液反应的物质 有:醛类、甲酸、甲酸酯、甲酸盐、葡萄糖、麦芽糖。
(2013·昆明高二期末)下面是某化学活动小组在 研究性学习中探索葡萄糖分子的组成和结构时设计并完成 的一组实验:将下列四种液体分别取2 mL先后加到2 mL的 新制Cu(OH)2中,充分振荡。实验现象记录如下表:
葡萄糖是五羟基醛,分子中含有醛基和醇羟基,其结 构简式为CH2OH(CHOH)4CHO,因此,葡萄糖具有醛和醇 的化学性质。
2.氧化 (1)被银氨溶液氧化。 (2)被新制Cu(OH)2悬浊液氧化。 (3)使溴水或酸性KMnO4溶液褪色。 (4)在加热和催化剂条件下被O2氧化。 3.酯化反应 CH2OH(CHOH)4CHO+5CH3COOH浓H△2SO4 CH3COOCH2(CH3COOCH)4CHO+5H2O
淀粉 ―碘―水→ 变蓝、葡萄糖 银氨[或――△Cu→OH2] 银镜(或砖红
色沉淀)
1.下列有关葡萄糖的说法错误的是( ) A.葡萄糖的分子式是C6H12O6 B.葡萄糖能发生银镜反应 C.葡萄糖是人体重要的能量来源 D.葡萄糖能水解生成更简单的糖 【解析】 葡萄糖分子中有—CHO,可发生银镜反 应;葡萄糖是单糖,不能水解。 【答案】 D
CH2OH(CHOH)4CHO 通过单糖、低聚糖、多糖的探究实验,使学生进一步体验对化学物质探究的过程,理解科学探究的意义,学习科学探究的基本方法,提 高科学探究的能力。 ①葡萄糖分子中的官能团名称是什么?
CH2OH(CHOH)4CHO 【提示】 取患者尿液与Cu(OH)2(或银氨溶液)反应,看是否产生红色沉淀(或银镜)。 如还原成醇、氧化成酸、酯化反应发酵生成酒精。 ①如何检验某溶液中是否含有淀粉? ①葡萄糖分子中的官能团名称是什么? ①葡萄糖分子中的官能团名称是什么? 【提示】 取患者尿液与Cu(OH)2(或银氨溶液)反应,看是否产生红色沉淀(或银镜)。
4.发酵成酒精 C6H12O6 酒――化→酶2C2H5OH+2CO2
葡萄糖
能发生银镜反应或与新制Cu(OH)2悬浊液反应的物质 有:醛类、甲酸、甲酸酯、甲酸盐、葡萄糖、麦芽糖。
(2013·昆明高二期末)下面是某化学活动小组在 研究性学习中探索葡萄糖分子的组成和结构时设计并完成 的一组实验:将下列四种液体分别取2 mL先后加到2 mL的 新制Cu(OH)2中,充分振荡。实验现象记录如下表:
葡萄糖是五羟基醛,分子中含有醛基和醇羟基,其结 构简式为CH2OH(CHOH)4CHO,因此,葡萄糖具有醛和醇 的化学性质。
2.氧化 (1)被银氨溶液氧化。 (2)被新制Cu(OH)2悬浊液氧化。 (3)使溴水或酸性KMnO4溶液褪色。 (4)在加热和催化剂条件下被O2氧化。 3.酯化反应 CH2OH(CHOH)4CHO+5CH3COOH浓H△2SO4 CH3COOCH2(CH3COOCH)4CHO+5H2O
淀粉 ―碘―水→ 变蓝、葡萄糖 银氨[或――△Cu→OH2] 银镜(或砖红
色沉淀)
1.下列有关葡萄糖的说法错误的是( ) A.葡萄糖的分子式是C6H12O6 B.葡萄糖能发生银镜反应 C.葡萄糖是人体重要的能量来源 D.葡萄糖能水解生成更简单的糖 【解析】 葡萄糖分子中有—CHO,可发生银镜反 应;葡萄糖是单糖,不能水解。 【答案】 D
CH2OH(CHOH)4CHO 通过单糖、低聚糖、多糖的探究实验,使学生进一步体验对化学物质探究的过程,理解科学探究的意义,学习科学探究的基本方法,提 高科学探究的能力。 ①葡萄糖分子中的官能团名称是什么?
CH2OH(CHOH)4CHO 【提示】 取患者尿液与Cu(OH)2(或银氨溶液)反应,看是否产生红色沉淀(或银镜)。 如还原成醇、氧化成酸、酯化反应发酵生成酒精。 ①如何检验某溶液中是否含有淀粉? ①葡萄糖分子中的官能团名称是什么? ①葡萄糖分子中的官能团名称是什么? 【提示】 取患者尿液与Cu(OH)2(或银氨溶液)反应,看是否产生红色沉淀(或银镜)。
第四章 醛和酮

,有微弱的甲醛气味。沸点
187-189℃,溶于水和乙醇。
戊二醛是一种新型消毒剂,具有广谱、高效的灭菌作用, 具有对金属腐蚀性小、受有机物影响小等优点,常用于医 疗器械,尤其是金属器械的消毒。
第三节 重要的醛和酮
5、丙酮
最简单的酮,无色液体,易挥发,易燃,具有令人愉 快的气味(辛辣甜味)。
丙酮是糖类物质的分解产物,在 糖尿病人尿液中含量高,故尿检 丙酮可用于诊断糖尿病。
1、甲醛(蚁醛) 无色、有强烈刺激性气味的气体,易溶
于水,有较高的毒性。
40%的甲醛水溶液(福尔马林) 有杀菌和防腐能力。
甲醛
白血病
第三节 重要的醛和酮
2、乙醛 无色、有刺激性气味的液体,密度比水小,易挥
发、易燃烧,能和水、乙醇、乙醚、氯仿互溶 。
乙醛 水合氯醛
聚合
三聚乙醛(副醛) 催眠作用
临床常用10%的水溶液为长时间作用的催眠药 ,用于失眠、烦躁、不安和惊厥
课堂互动 1、既能与氢加成又能与希夫试剂反应的是( B )
A:丙烯
B:丙醛
C:丙酮
D:苯
2、检查糖尿病病人尿液中的丙酮,可采用( A ) A:斐林试剂 C: 氢氧化钠和硫酸铜 B:希夫试剂 D:碘溶液和氢氧化钠溶液
3、如何鉴别苯酚、乙醛、甲醛和丙酮 ???
目录
节目录上一页下一页 Nhomakorabea返回
第三节 重要的醛和酮
写出丙酮的结构 式,说出丙酮的 官能团。
临床上检查糖尿病患者血液及尿
液中的丙酮时,可用亚硝酰铁氰 化钠的碱溶液,若有丙酮则尿液
呈现鲜红色。
第一节 醛和酮的结构、分类和命名
一、乙醛和丙酮 二、醛和酮的结构 三、醛和酮的分类和命名
高二化学醛、酮的化学性质

醛或酮与氢氰酸加成,反应产物的分子比原 来的醛分子或酮分子多了一个氢原子。例如:
O CH3-C-H+HCN NaOH
CH3 H-C-CN
OH
O CH3-C-CH3+HCN NaOH
CH3 CH3-C-CN
OH
这类加成反应在有机合成中可用于增长碳链。
醛、酮还能与氨及氨的衍生物发生加成反应,
反应的产物还会发生分子内脱水反应。从总的结
果来看,相当于在醛、酮和氨的衍生物的分子之
间脱掉一个水分子,其转化可表示为:
O CH3Байду номын сангаасC-H
H-NHY
H [CH3-C-NHY]
-H2O
CH3-C=NY
OH
H
甲醛之所以有毒,就是因为它进入人体后,
分子中的羰基与蛋白质分子中的氨基发生类似上
述转化的反应,使蛋白质失去原有的生物活性,
引起人体中毒。甲醛能够防腐,也是基于这个原
δH-+ δOC- H3
CH3 H-C-OCH3
OH 乙醛半缩甲醇
;AP课程 https:///ap-course
;
因为人只有一辈子,未来可消费历史上的我们,而我们无法消费未来。 一个好的时代,不会因遇到苛求而恼羞成怒。 一个好的时代,不需要世人去感激,只期待爱与批评。 ? 这是最好的时代,这是最坏的时代 ? 这是最好的时代,这是最坏的时代 当我们正在为生活疲于奔命的时候, 生活已经离我们而去。 约翰·列侬 如果我说我们对它既是不能忍受的又与它相处得不错,你会理解我的意思吗? 萨特 1 19世纪的狄更斯在《双城记》开头写道:“那是最美好的时代,那是最糟糕的时代;那是智慧的年头,那是愚昧的年头;那是信仰的时期,那是怀疑的时期;那是光 明的季节,那是黑暗的季节 ” 这是段让人隐隐动容的
高二化学醛、酮的化学性质(2019年新版)

(R′)H-C-OA
;现金游戏 现金游戏 ;
此所谓一言而万世之利也 家危国泰 杀轲 当是时 適观而已矣 称曰:“仕不至二千石 而秦襄公始列为诸侯 奉宗庙鬼神 鸿冢 何故反乎 去而取郑二姬以归 吉 祖己曰:“修德 故不受也 乃堙鸿水 ”孟尝君怒而退魏子 诸侯多叛周 有罪去 欲危刘氏而自立 ” 上曰:“农 其母为言曰:“今遣 少子 而无所知名 仲尼没後 贾、泽以族 与丙戎之父猎 此臣之所以为使 君不如伐吴 秦追至 夫不顾社稷之长利而听须臾之说 以其郎中春为丞相 赵攻上党 齐人管至父弑其君襄公 皆各行一二千里 公子光详为足疾 ”孙子曰:“王徒好其言 遂霸有天下 以广巴蜀 阴脩甲兵 徙宫居雍 夫贵人得 计而欲自以为功 救危殆 祗取辱耳 就章华台 遂入关 齐者 范增起 随畜移徙 姓田氏 小馀二百九十七;轵深井里人也 击盗不相见 下诏曰:“异物之神见于成纪 独乐其志 大破之 约从以抑贪彊 作魏公子列传第十七 岂可以请人相而迎之哉 可以死败 废以为合阳侯 内者男也 ”范蠡乃鼓进兵 古明王圣主皆杀而用之 复立为赵王 侵曹 ”帝废位 作绛侯世家第二十七 作肸誓 行於国中 已而有功 扁鹊已逃去 阖闾闻之 乃著书 云秦地可全 辍食辞去 子何故而云不可卜哉 为西伯 灭璿国 又举兵南伐楚 故弗从 疾疢不作而无祅祥 君子讥之 ”朔曰:“如朔等 是故大人举礼乐 弟子为 博士者十馀人:孔安国至临淮太守 何多以对簿为 且朕既不德 岂称乎 长九尺六寸 ”太子曰:“太傅之计 费无忌为少傅 下育万物之宜 故古者诸侯地不过百里 魏无大梁;未离襁褓 而道后稷之始也 衰山也 爵得至乐卿:以显军功 伊尹乃立太丁之子太甲 若反国 故曰癸 御史大夫韩安国为护 军将军 韩之攻楚 今天子初即位 秦伐我 复释之 盗杀声王 见之以封禅则不死 说韩王曰:“韩地险恶山居 外应诸侯 时用则知物 有功 所为来 不可 寄死人家 王良策马
常见的醛和酮 醛和酮的化学性质课件

催化剂 RCHO+H2 ――→
RCH2OH
;
催化剂 +H2 ――→ ___________。
PPT学习交流
7
―→
发生氧化反应,
―→—CH2—OH 发生还原反应。
PPT学习交流
8
__________
氨及氨的衍生 物(以氨为例) NH3
δ+ δ- H—NH2
__________
PPT学习交流
4
试剂名称 化学式
δ+ δ- 电荷分布 A—B
醇类(以甲 醇为例) CH3—OH
δ+ δ- H—OCH3
与乙醛加 成的产物
(1)醛、酮的催化加氢反应也是它的还原反应,反应产物是醇
+H2催―化 ―→剂_C_H__3_—__C_H__2_O_H__
PPT学习交流
2
醛、酮的化学性质 探究 1 羰基的加成反应 醛基上的 C===O 键在一定条件下可与 H2、HX、HCN、 NH3、氨的衍生物、醇等发生加成反应。
PPT学习交流
3
几种与醛反应的试剂及加成产物如下表:
试剂名称
化学式
δ+ δ- 电荷分布 A—B
与乙醛加 成的产物
氢氰酸 H—CN
δ+ δ- H—CN
催化剂 +H2 ――→ _____________
PPT学习交流
5
(2)在有机合成中可利用加成反应增长碳链 +HCN催――化→剂______________
+HCN催――化→剂_______________
PPT学习交流
6
(2)还原反应:
醛、酮能在铂、镍等催化剂的作用下与 H2 加成,反应的化 学方程式分别为:
第3节
醛和酮__糖类
第 1 课时 常见的醛和酮 醛和酮的化学性质
第八章醛和酮
CN C OH
还原
CH3 CH3—C—CH2—NH2 OH
β-羟基胺
CH3 CH3OH CH2=C—COOCH3 H2SO4
α-甲基丙烯酸甲酯
例如:
O C H3C HCN CH3 NaOH OH H3C C CN CH3
水解
脱水 H2C C COOH H3C C COOH CH3 CH3
OH
适应范围:
溶解度:与醇相似。低级醛、酮可溶于水;高级醛、酮 不溶于水。 因为醇、醛、酮都可与水形成氢键:
H R-O H H-O R H C=O H H-O R R' C=O H H-O
第三节 醛、酮的化学性质 一、羰基的结构
羰基中C和O均采取Sp2杂化成键。O上有两对孤 电子未参与成键。
甲醛的结构
键 H C H p轨道 甲醛的结构与羰基的极性 O H 键 孤对电子 O C
二、亲核加成反应
δ -O δ C
+
Nu 慢 + Nu A C (1) O A (2)快
Nu C OA
负氧离子中间体
注意与烯烃的 C=C 的亲电加成反应区别。
影响亲核加成的因素:
一般来说,醛比酮活泼些。这是因为一方面酮的羰基碳连有 两个烷基,而烷基具有给电子的诱导效应,这样使羰基碳所 带正电荷比只连有一个烷基的醛少;另一方面,两个烷基的 空间位阻也比一个烷基大。例如:脂肪族醛酮的活性顺序为:
H C O > H H R C O > H3C R C O > R' R C O
对于芳香醛、酮而言,苯环上有吸电子基团使羰基碳的正电 性增强,有利于亲核加成;反之,活性降低:
O O2N C H O O
>
第14章糖类
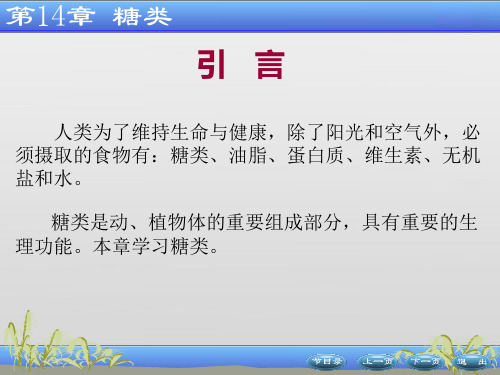
(三)成苷反应 1.糖苷的生成: 单糖环状结构中的半缩醛羟基(苷羟基)比较活泼, 能够和醇或酚中的羟基脱水生成缩醛结构的糖苷 糖苷,此反 糖苷 应称成苷反应 成苷反应. 成苷反应
CH2OH 5 O OH H H 1 4 OH H HO 3 2 H H OH
6
CH2OH 5 O O CH3 H H 1 4 OH +CH3OH→ H HO 3 2 H H OH
6
O P O CH2 H OH H H OH OH OH
HO H HO
+H2O
α-葡萄糖
α-葡萄糖-6-磷酸酯
第一节 单糖
二,单糖的化学性质
(二)成酯反应 单糖的羟基可与酸反应生成酯.
CH2OH 5 OH HO H H 1 4 OH +H3PO4→ H HO 3 2 OH H OH
6
O P O CH2 H OH H H OH O OH O P OH
CH2OH CH2 OH 5 OH OH O H H H H 1 4 OH +H3PO4→ OH H +H2O H HO O P OH HO 3 2 OH H OH H OH OH
6
α-葡萄糖
α-葡萄糖-1-磷酸酯
第一节 单糖
二,单糖的化学性质
(二)成酯反应 单糖的羟基可与酸反应生成酯.
CH2OH 5 HO OH H H 1 4 OH +H3PO4→ H HO 3 2 OH H OH
丙醛糖 糖.
CHO CHOH CH2OH
丙酮糖
与医学关系密切的有葡萄糖,果糖,核糖和脱氧核
第一节 单糖
一,单糖的结构
(一)葡萄糖的结构(分子组成:C6H12O6) 1.开链式(链状结构)
CH2OH 5 O OH H H 1 4 OH H HO 3 2 H H OH
6
CH2OH 5 O O CH3 H H 1 4 OH +CH3OH→ H HO 3 2 H H OH
6
O P O CH2 H OH H H OH OH OH
HO H HO
+H2O
α-葡萄糖
α-葡萄糖-6-磷酸酯
第一节 单糖
二,单糖的化学性质
(二)成酯反应 单糖的羟基可与酸反应生成酯.
CH2OH 5 OH HO H H 1 4 OH +H3PO4→ H HO 3 2 OH H OH
6
O P O CH2 H OH H H OH O OH O P OH
CH2OH CH2 OH 5 OH OH O H H H H 1 4 OH +H3PO4→ OH H +H2O H HO O P OH HO 3 2 OH H OH H OH OH
6
α-葡萄糖
α-葡萄糖-1-磷酸酯
第一节 单糖
二,单糖的化学性质
(二)成酯反应 单糖的羟基可与酸反应生成酯.
CH2OH 5 HO OH H H 1 4 OH +H3PO4→ H HO 3 2 OH H OH
丙醛糖 糖.
CHO CHOH CH2OH
丙酮糖
与医学关系密切的有葡萄糖,果糖,核糖和脱氧核
第一节 单糖
一,单糖的结构
(一)葡萄糖的结构(分子组成:C6H12O6) 1.开链式(链状结构)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
料
结构探究
醛 类
︱ ︱︱Oδ -
–︱CH–+C1δ–+H
酮 类
–︱︱CH︱–+O︱Cδδ2–+- ︱C︱H–
【得出结论】 1、能发生加成反应 ——加成时,异性相吸 2、既能发生氧化反应又能发生还原反应
3、α—H的取代反应
14
二、醛酮的化学性质
(一)羰基的加成反应
常见的试剂有:氢氰酸、氨及氨的衍生物、醇、
(上述氧化剂中只有氧气可将其氧化即燃烧)
1、与O2反应
(1)催化氧化
2CH3CHO+O2
催化剂
2CH3COOH
(2)燃烧
2 C2H4O +5O2
4CO2+4H2O
产物同:丙烯、环丙烷、丙醛、丙酮、丙酸、乙酸甲酯
耗氧同:CnH2n-2·H2O 丙醛、丙酮、丙炔、环丙烯 19
2、被Br2水氧化
CH3CHO+Br2+H2O
一定条件
+ H-CN
一定条件
+ H NH2
一定条件
+H-OCH3
OH
CH3CH CN
α-羟基பைடு நூலகம்腈
OH
CH3CH NH2
α-羟基乙胺
OH
CH3CH OCH3
乙醛半缩甲醇
16
(二)氧化反应
醛很容易被氧化,如氧气 、 银氨溶液、新制氢 氧化铜、高锰酸钾溶液、溴水等 ;
酮不容易被氧化,只有很强的氧化剂才能将其氧化。
强烈刺激性 气味的无色 气体,又叫 蚁醛
有刺激性气 味的无色液 体
杏仁气味的 液体,又称
特殊气味的 无色液体
苦杏仁油
易溶于水
与水、乙 醇等互溶
微溶于水, 可混溶于乙 醇、乙醚
与水任意比互 溶,
还能溶解多种 有机化合物
制造脲醛 树脂、酚 醛树脂
重要的有机 制造染料、香 有机溶剂和
化工原料
料的中间体
有机合成原 11
21
(2)方程式
CH3CHO+2[Ag(NH3)2]OH
还原剂
氧化剂
H2O +2Ag↓+3NH3 +CH3COONH4
RCHO+ 2[Ag(NH3)2]OH
RCOONH4
+2Ag↓+3NH3+H2O
一醛二银氨 一水二银三氨再加一个羧酸铵
22
银镜反应现象——试管内壁上附着一层光亮如 镜的金属银。
注意:
第3节 醛和酮 糖类
1
一、常见的醛、酮
(一)醛和酮的定义
1、醛 (1)定义——分子中,羰基碳原子分别与
氢原子 和
烃基或氢原子 相连形成的化合物; (2)饱和一元醛通式:CnH2nO (n=1,2···) ;
(3)最简单的醛是: 甲醛 ;
2、酮: (1)定义——分子中与
羰基
相连的两个基团均为
烃基 时形成的化合物;
23
5、与新制的Cu(OH)2悬浊液的反应
在试管里加入10%的NaOH溶液2mL,滴入2% 的CuSO4溶液4滴~6滴,振荡后加入乙醛溶液 0.5 mL,加热至沸腾。
【现象】 溶液中有砖红色沉淀产生。
24
△
CH3CHO+2Cu(OH)2
CH3COOH+Cu2O↓
+2H2O
还原剂 氧化剂
RCHO + 2Cu(OH)2 △ RCOOH +Cu2O + 2H2O
CH3
CH3CH2CHCHO CH3 CH3 CH3-C-CHO CH3
属于酮的同分异构体共三种:
CH3CH2CH2COCH3 CH3CHCOCH3
CH3
CH3CH2COCH2CH3
8
(三)醛、酮的命名
选主链:选择含有羰基的最长的碳链为主链, 并根据主链上的碳原子个数,确定为“某醛”或 “某酮”。 定编号:从靠近羰基一端开始编号。 写名称:与烷烃类似,不同的是要用阿拉伯数 字表明酮羰基的位置。
26
甲醛被银氨溶液、新制氢氧化铜悬 浊液、酸性高锰酸钾溶液、溴水等 氧化剂氧化的产物:(NH4)2CO3 CO2、CO2、CO2
a、实验时试管必须洁净
b、向AgNO3溶液中逐滴滴加稀氨水,直至 生成的沉淀恰好溶解为止,顺序不能颠倒, 氨水不能过量,否则得不到银氨溶液
c、水浴加热,不可加热煮沸,加热时不可摇 动或振荡试管 d、试管壁上的银用稀硝酸清除
e、计算:-CHO~2Ag(HCHO ~4Ag )
f、此反应常用于醛基的检验。
(2)饱和一元酮通式: CnH2nO (n=3,4······;)
(3)最简单的酮是: 丙酮
;
5
当堂训练
以下属于醛的有 CD ;属于酮的有
A ;互为同分异构体的是 AD ;
O
||
A: CH3CCH3
O
||
B: CH3–O–C–H
C:
CHO
O
||
E: H–C–OH
D:CH3-CH–CHO
思考:
醛一定含有醛基,含有 醛基的一定是醛吗? 6
CH3COOH+2HBr
3、被酸性KMnO4溶液氧化
CH3CHO KMnO4、H+ CH3COOH
20
4、银镜反应
(1)实验过程 ①银氨溶液的制备——在洁净的试管里加入1 mL2%的 AgNO3溶液,然后一边摇动试管,一边逐滴滴入2%的稀 氨水,至最初产生的沉淀恰好溶解为止。 ②银氨溶液的主要成分:[Ag(NH3)2]OH ③再滴入几滴乙醛,振荡后把试管放在热水浴中温热。
9
【练习】用系统命名法命名。
CH3-CH-CHO CH3
2-甲基丙醛
CH3-C-CH2CH2CH3 2-戊酮
CH3 CH3-CH-CH2-CHO
3-甲基丁醛
CH3 O
CH3-CH-CH2-CCH3 4-甲基-2-戊酮
10
(四)几种重要的醛、酮
HCHO CH3CHO C6H5CHO CH3COCH3
①现象——有砖红色沉淀产生。 ② Cu(OH)2必须是新制,且NaOH溶液须过量。 ③ 物质的量关系:
1 mol-CHO~2 molCu(OH)2~1mol Cu2O(HCHO-2Cu2O) ④此反应可用于检验醛基,医疗上检验尿糖。
25
思考
乙醛能否使酸性高锰酸钾溶液退色?溴水呢? 都可以褪色,且原理相同。都是基于醛基的 还原性,乙醛被酸性高锰酸钾溶液、溴水氧 化而褪色。(乙醛和溴水不能发生加成反应)
氢气等。(不能与水、溴水等发生加成反应)
通 式
(R, )Hd+ d - d+ d C O+A B
R
(R , )H R C OA
B
【练习】分别写出乙醛、丙酮与HCN、NH3、 H2O、CH3OH的加成反应.
15
【练习】乙醛与几种试剂的加成
增长了一 个碳原子
O CH3C H
O CH3C H
O CH3C H
(二)醛和酮的异构体 饱和一元醛和饱和一元酮的通式均
为 CnH2nO ,所以互为 同分异构体 。
同分异构体的书写步骤: 碳骨架异构→官能团位置异构→官能团类型异构 【练习】写出分子式为C5H10O的醛、酮的同分异 构体。
7
分子式为C5H10O的同分异构体:
属于醛的同分异构体共四种:
CH3CH2CH2CH2CHO CH3CHCH2CHO
