有机物之间的相互转化
有机物和无机物在环境中的迁移和转化

有机物和无机物在环境中的迁移和转化地球上的物质可以分为有机物和无机物两大类,它们在环境中的迁移和转化过程非常复杂,也是人们长期以来关注的重点。
本文将从多个方面探讨有机物和无机物在环境中的迁移和转化过程。
一、有机物和无机物的定义与特点有机物指的是含碳并且大部分都是由生物合成的化合物。
它们广泛存在于大气、水体和土壤中,包括生物体、死亡的生物体和其代谢产物等。
与之相对的是无机物,它们是不含碳的化合物,由天然矿物和非生物合成物质构成。
有机物和无机物的存在形式、化学性质和环境行为都有所不同。
有机物通常是复杂的化合物,分子量较大,且包含不同的官能团,因此在水体和土壤中非常容易被吸附、降解、迁移和转化。
相对于有机物而言,无机物的特点则是化学反应相对简单,降解速度较慢,同时在环境中存在的形式比较单一,如酸和碱等。
二、有机物和无机物在土壤中迁移和转化土壤是地球上最重要的有机物和无机物存储介质,其中包含大量的微生物和有机化合物。
有机物在土壤中的迁移和转化受到多种因素的影响,如土壤pH值、温度、水分、氧气含量等。
一般情况下,有机物主要是通过微生物代谢、吸附和溶解等方式在土壤中降解和转化的。
无机物在土壤中的迁移和转化则更加复杂。
它们可以与土壤中的有机物、水和气体发生化学反应,而这些反应通常是非常缓慢的。
此外,无机物还可以被吸附到土壤团粒和孔隙中,防止其扩散到土壤深层和地下水中。
三、有机物和无机物在水环境中迁移和转化水是地球上最重要的资源之一,其中含有大量的有机物和无机物。
水环境中的有机物通常存在于溶解态和颗粒态两种形式。
当溶解的有机物在水中浓度过高时,会影响水体中的生物物种多样性和稳定性。
一些水体富含的有机物也可能在缺氧条件下会发生反硝化作用,产生氮氧化物等污染物,对人类和生物体产生危险。
在水环境中,无机物主要是通过沉积物和悬浮物的方式存在,但也可能传输到大气中。
各种因素如水流、波浪和水深等都会影响无机物在水环境中的迁移和转化。
高三有机化学中有机物间相互转化关系图

一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3 + 2FeBr 36FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 32FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2⑷ Zn 、Mg 等单质 如 ⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O HBrO + Na 2CO 3 = NaBrO + NaHCO 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(CCl 4、氯仿、溴苯等)、CS 2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 Mg + Br 2 === MgBr 2 (其中亦有Mg 与H +、Mg 与HBrO 的反应)△2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的Fe (亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
重要有机物之间的相互转化

重要有机物之间的相互转化汇报人:日期:contents •脂肪烃的转化•脂环烃的转化•芳香烃的转化•卤代烃的转化•有机化合物的氧化还原反应•有机化合物的官能团转换目录脂肪烃的转化03烷基化反应01裂解反应02脱氢反应氧化反应聚合反应氧化反应聚合反应加氢反应脂环烃的转化环扩大环缩小环烷烃的加成030201环氧化环烯烃可以通过催化氧化或化学氧化反应,转化为环氧化物。
环加成环烯烃可以与炔烃、烯烃等发生Diels-Alder反应或 ene 反应,生成新的环状化合物。
开环反应在酸或碱催化下,环烯烃可以开环转化为链状烃。
1 2 3环加成末端加成开环反应芳香烃的转化氧化反应磺化反应硝化反应苯的转化磺化反应烷基化反应氧化反应氧化反应磺化反应烷基化反应卤代烃的转化氧化反应还原反应水解反应消去反应01加成反应02氧化反应03多卤代烃的转化裂解反应多卤代烃在无氧或缺氧的条件下,可发生裂解反应,生成多个小分子卤代烃或烯烃。
聚合反应多卤代烃可在催化剂的作用下,发生聚合反应,生成高分子化合物。
有机化合物的氧化还原反应氧化反应醇的氧化酮的氧化01羧酸的还原02醛的还原03酮的还原还原反应既有氧化又有还原的反应烯烃的环氧化烯烃的氢化有机化合物的官能团转换醇到醚通过醇和卤代烃发生取代反应得到醚。
醇到醛通过醇和醛发生氧化反应得到醛。
醇到羧酸通过醇和羧酸发生酯化反应得到羧酸。
030201醛到醇醛到酮酮到羧酸羧酸到酯羧酸到酰胺羧酸到酮感谢观看。
有机物间的相互转化

例2:用化合物A和乙醇可制备某种新型材料W,W的表示式为:
下列是有关的各步转化关系(其中所有的无机产物已略去):
回答下列问题: (1)化合物D与H中含有的官能团是_______________(写名称)。
③卤代烃的水解(碱性) C2H5Br+NaOH ④酯的水解 CH3COOC2H5 + H2O
C2H5OH + NaBr CH3COOH+C2H5OH
△
⑷引入醛基或羰基
①醇催化氧化 2CH3CH2OH+O2
Cu
△
2CH3CHO+2H2O
②烯烃与O2反应
③炔烃与水加成
催化剂 2CH2=CH2+O2 △
CH3COOCH2CH3 + H2O
转化方法之—官能团性质
官能团性质
具有酸性
官能团
—COOH、酚羟基
C=C
—C C—
官能团性质
与新制
Cu(OH)2反应
官能团
—CHO —COOH —CHO —OH —COOH
—X、 —COO—、 —COOH、酚羟基
能发生加成 反应
能发生消去 反应 能发生水解 反应 KMnO4(H ) 溶液褪色 溴水褪色
有机化合物之间的转 化关系
CH3CH3 加成 CH2=CH2 加成
取代
CH3CH2Br
消去 水解 取代 氧化 氧化
加成
消去
CH3CH2OH
加成
CH3CHO
酯化
CH3COOH
还原
CH≡CH
CH3COOCH2CH3
烃复习09.2

同系物的性质: 3、随碳原子个数增加H%有规律的变化 ①烷烃随碳原子数的增加H%减少,燃烧等质量的烷烃 耗氧量减少,生成水减少,生成CO2增多。烷烃C%最大值 =85.7%。 ②烯烃随碳原子数的增加H%不变,燃烧等质量烯烃耗 氧量相等,生成水相等,生成CO2相等。烯烃C%=85.7%。 ③炔烃随碳原子数的增加H%增大,燃烧等质量的炔烃 耗氧量增大,生成水增多,生成CO2减少。炔烃中H的百 分含量最大H%=14.3%。 7、同分异构体
例1.写出醋酸的最简式_______________;分子式________; C2H4O2 CH2O
HO .. H .. . .∶O∶H . . H-C-C-O-H .. 电子式 H∶C∶C∶∶O∶ _____________________________;结构式____________; H H 结构简式____________________;球棍模型_____________。 CH3COOH
5、表示有机物组成和结构的方法
最简式(实验式)---表示有机物组成原子的最简整数比 分子式---表示有机物分子组成的式子(是最简式的整数倍)
电子式---用元素符号和原子最外层电子表示分子结构的式子 结构式—由简化电子式而来,用短线表示共用电子对。表示 分子内原子间的连接顺序和方式(C-C、C=C、 = C 、C=O C 能团不能省去 键线式—省去结构简式中的碳原子和氢原子,以线示键表示有机 物结构的式子。CH2=CHCH=CH2键线式结构:= - = 比例模型、球棍模型、立体结构示意图和结构式的区别。 结构式只表示分子内原子间的连接顺序和方式,不表示分子 的空间构型,而比例模型、球棍模型、立体结构示意图既表示 结构式的含义,又表示分子的空间构型。
化合物分子式相同, 结构不同的现象叫同分异构现象。 分子式相同,结构不同的化合物互称同分异构体。
重要有机物的相互转化

– 有机物一般都可以发生氧化反应,此过程发生 了碳碳键或碳氧键的断裂
– 醇氧化的规律:
伯醇氧化生成醛,如CH3CH2OH 仲醇氧化生成酮,如(CH3)2CHOH 叔醇不能被氧化,如(CH3)3COH – 多官能团物质被氧化的顺序看信息
有机反应类型——还原反应
• 原理:有机物得氢或去氧 • 包括:烯、炔、苯环、醛、油脂等和氢气加成,
有机反应类型——消去反应
• 说明: – 消去反应的实质:—OH或—X与所在碳相邻 的碳原子上的-H结合生成H2O或HX而消去 – 不能发生消去反应的情况:—OH或—X所在 的碳无相邻碳原子,或相邻碳原子上无氢 (注意区分不能消去和不能氧化的醇)
– 有不对称消去的情况,由信息定产物 – 消去反应的条件:醇类是浓硫酸+加热;
有机反应类型——显色反应
• 包括 – 苯酚遇FeCl3溶液显紫色 – 淀粉遇碘单质显蓝色 – 含苯环的蛋白质遇浓硝酸凝结显黄色 – 多羟基物质(甘油、葡萄糖)与新制 Cu(OH)2悬浊液生成绛蓝色物质
有机反应类型——酯化反应拓展
• 机理:一般为羧酸脱羟基,醇脱氢
• 类型
– 一元羧酸和一元醇反应生成普通酯
制乙炔,烯与炔加溴,烯、炔及苯的同系 物被KMnO4氧化,苯酚的溴代,卤代烃的 水解
有机反应类型——知识归纳
反应条件
反应类型
NaOH水溶液、加热 卤代烃或酯类的水解反应
NaOH醇溶液、加热 卤代烃的消去反应
稀H2SO4、加热 浓H2SO4、加热 浓H2SO4、170℃ 浓H2SO4、140℃ 溴水
酯和糖类的水解反应 酯化反应或苯环上的硝化反应 醇的消去反应 *醇生成醚的取代反应 不饱和有机物的加成反应
浓溴水
4-6重要有机物之间的相互转化关系
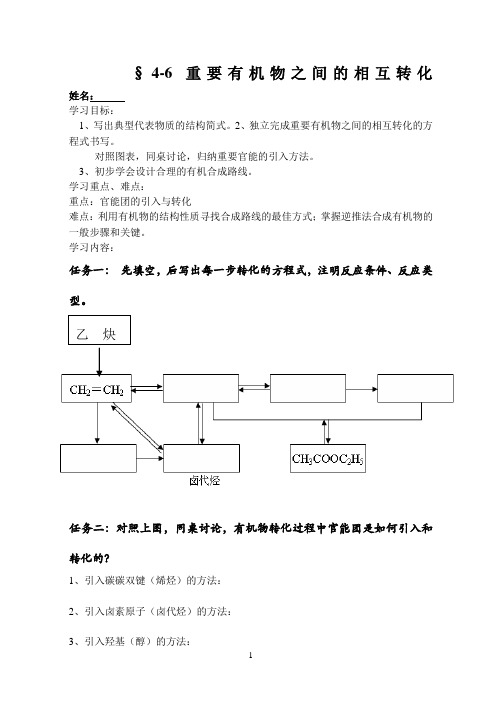
§4-6重要有机物之间的相互转化姓名:学习目标:1、写出典型代表物质的结构简式。
2、独立完成重要有机物之间的相互转化的方程式书写。
对照图表,同桌讨论,归纳重要官能的引入方法。
3、初步学会设计合理的有机合成路线。
学习重点、难点:重点:官能团的引入与转化难点:利用有机物的结构性质寻找合成路线的最佳方式;掌握逆推法合成有机物的一般步骤和关键。
学习内容:任务一:先填空,后写出每一步转化的方程式,注明反应条件、反应类型。
任务二:对照上图,同桌讨论,有机物转化过程中官能团是如何引入和转化的?1、引入碳碳双键(烯烃)的方法:2、引入卤素原子(卤代烃)的方法:3、引入羟基(醇)的方法:500℃-600℃4、引入醛基(醛)的方法5、引入羧基(酸)的方法:方法指导:逆向分析法:目标产物 中间物质 中间物质 原始材料例:CH ≡CH 为原料合成聚氯乙烯。
例:以乙烯为原料,其它无机试剂自选,合成乙二酸乙二酯,结构简式如图所示巩固练习2:从丙醇合成丙三醇,可采用下列四步反应:CH 3CH=CH 2 CH 2ClCH=CH 2 1,2,3-三氯丙烷丙三醇综合提高:写出各步反应的化学方程式,并分别注明反应类型:1、已知有机物A 是具有水果香味的液体,其分子式是C 4H 8O 2,在一定条件下有下列转化关系:乙酸乙酯乙醇 乙醛 乙酸 溴乙烷 乙烯写出A、B、C各物质的结构简式A_______B_______C________2:A、B、C、D、E五种有机物的转化关系如下图所示已知液体B能发生银镜反应,气体D对H2的相对密度为14。
请回答:(1)A、B、C、的结构简式分别是________ _________ ________(2)D中官能团的名称是______________(3)A→D的化学方程式是_________________________________(4)在一定条件下,A与E反应可生成一种具有香味的物质。
官能团的性质和有机物相互间的转化

KMnO4 侧链与苯环相连的碳 不反应,溶液分层, 不反应,溶液分层,上层无色 上有氢, (H+) (苯层),下层紫色(水层) 上有氢,侧链一律被 苯层),下层紫色(水层) ),下层紫色
+3H2
Ni
苯环上加成
苯与苯的同系物化学性质对比: 苯与苯的同系物化学性质对比: 侧链影响苯环, (1)侧链影响苯环,使苯环上的氢原子比苯更易被取代 苯环影响侧链, (2)苯环影响侧链,使侧链能被强氧化剂氧化 有机物分子中基团之间存在相互影响。《步步高》p187(典例1) 有机物分子中基团之间存在相互影响。 步步高》p187(典例1 思考】如何鉴别苯和苯的同系物? 【思考】如何鉴别苯和苯的同系物? 酸性高锰酸钾,若褪色为苯的同系物。 酸性高锰酸钾,若褪色为苯的同系物。
二、烷烃
通式: 饱和) 1、通式: CnH2n+2 (饱和) 不饱和度: 2、不饱和度: 0 官能团: 3、官能团: 无 4、空间结构特点:链状单键 空间结构特点: CH4:正四面体 【思考】二氯甲烷的空间结构?有多少种同分异构体? 思考】二氯甲烷的空间结构?有多少种同分异构体? 四面体结构,只有一种结构。 四面体结构,只有一种结构。 思考】 含有的共价键数目是多少? 【思考】1mol CnH2n+2含有的共价键数目是多少? (3n+1)NA 3n+1)
通式: 1、通式: CnH2n 不饱和度: 2、不饱和度: 1 官能团: 3、官能团: 碳碳双键 空间结构特点: 4、空间结构特点:链状双键 C2H4:平面四边形 【思考】丙烯有多少个原子处于同一平面? 思考】丙烯有多少个原子处于同一平面? 7个 。 5、主要化学性质
(1) 氧化反应 燃烧:火焰明亮, ①燃烧:火焰明亮,伴有黑烟
