2019年中考化学复习专项突破4溶解度及溶解度曲线
中考化学专题练习溶解度(含解析)

2019中考化学专题练习-溶解度(含解析)一、单选题1.在t℃时,A%的硝酸钾饱和溶液,冷却使其析出晶体,过滤后,将剩下的溶液再回升到t℃时(假定水量不变),剩下的溶液是()A.不饱和溶液,浓度小于A%B.饱和溶液,浓度小于A%C.不饱和溶液,浓度等于A%D.饱和溶液,浓度大于A%2.60℃时,100g水溶解20.94g氢氧化钡恰好饱和,则氢氧化钡属于()A.易溶物质B.可溶物质C.微溶物质D.无法确定3.如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是()A.a、b两种物质都属于微溶性物质B.分别降温t2℃时a、b的饱和溶液到t1℃时,析出的a比b多C.t2℃时,恒温蒸发a、b饱和溶液中等质量的水,析出a比b多D.当a中含有少量b时,可以用降温结晶法提纯b4.如图是甲、乙两种物质的溶解度曲线,下列说法错误的是()A.t1℃时,甲、乙两种物质的溶解度相等B.甲物质的溶解度随温度的升高而增大C.将t2℃时甲、乙两种物质的饱和溶液降温到t1℃,溶液仍然饱和D.t1℃时,将50g甲物质加入100g水中,充分搅拌,能得到甲物质的饱和溶液5.下列变化中,溶液中原溶质的溶解度和溶质分量分数都发生变化的是()A.常温下密闭容器中硝酸钾稀溶液升温10°CB.氯化铁溶液中加入少量生石灰C.硫酸锌溶液中加入少量铜粉D.稀释硫酸钠溶液6.甲、乙两种物质的溶解度曲线如图所示。
下列叙述正确的是()A.t1℃时,甲和乙饱和溶液中溶质的质量分数相同B.依据溶解度曲线可判断,甲的溶解度比乙的大C.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大D.将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法7.下列措施中:℃加热,℃振荡,℃搅拌,℃将溶质的大颗粒粉碎.可以加快固体在水中的溶解速率的是()A.℃℃B.℃℃C.℃℃℃D.℃℃℃二、多选题8.如图所示为硝酸钾和氯化钠两种物质的饱和溶液的质量分数随温度变化的曲线,M、N分别是50℃时硝酸钾和氯化钠质量分数随温度变化曲线上的点.分析曲线得到的以下结论中,正确的是()A.50℃时,其他条件不变,降温至40℃,N点向左平移,氯化钠的溶解度降低B.50℃时,向两饱和溶液添加溶质,M和N点竖直向上移动,硝酸钾和氯化钠的溶解度不变C.50℃时,M、N之间任一点表示的溶液一定是硝酸钾和氯化钠的饱和溶液D.50℃时,其他条件不变,升温至60℃,M点向右平移,硝酸钾的溶解度增大9.在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.下列说法正确的是()A.室温时,乙溶液可能是不饱和溶液B.图2中能表示甲物质的溶解度曲线的是cC.t1℃时,甲、乙、丙三种物质的等质量的饱和溶液中水的质量由大到小的顺序是a=b>cD.t2℃时,a的饱和溶液中含有少量b,要得到较纯净的a晶体,可采用降温结晶、过滤等操作三、填空题10.目前市场上销售的汽水饮料大多数是碳酸饮料,其中溶有二氧化碳气体.打开汽水瓶盖时,汽水会自动喷出来,这说明气体在水中的溶解度与________有关.喝了汽水后,常常会打嗝,这说明气体的溶解度还与________有关.由此可见,有利于气体溶解的条件是________温________压.11.下图是A、B、C三种物质的溶解度曲线,回答下列问题:(1)________℃时,A、C的溶解度相等.(2)如果A物质中混有少量B物质,可用________ 的方法得到较纯的A物质。
中考化学《溶解度及溶解度曲线》专项练习题(附答案解析)

中考化学《溶解度及溶解度曲线》专项练习题(附答案解析)1. 甲、乙、丙三种固体物质的溶解度曲线如右图所示。
下列说法不正确的是()A. T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙B. T2℃时,将甲、乙的饱和溶液均降温到T1℃,得到的溶液仍饱和C.若甲中混有少量的丙,可采用降温结晶的方法提纯甲D. T2℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液2. 下图是甲、乙两种固体物质的溶解度曲线。
下列说法中错误的是( )A. 20℃时,甲、乙饱和溶液中溶质质量分数相等B. 40℃时,甲的溶解度大于乙的溶解度C. 40℃时,乙的饱和溶液中溶质的质量分数为40%D. 将40℃甲的饱和溶液降温到20℃,会有晶体析出3. KNO3与KCl的溶解度曲线如右图所示。
下列说法正确的是( )A. KNO3的溶解度比KCl的溶解度大B. t1温度下的KCl的饱和溶液升温至t2,有晶体析出C. A点所表示的KCl饱和溶液溶质的质量分数为29%D. 冷却热的KNO3饱和溶液可获得KNO3晶体4. ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。
下列说法正确的是( )A. N点对应的ZnSO4溶液升温或降温均都可能析出晶体B. M点对应的ZnSO4溶液是不饱和溶液C. ZnSO4饱和溶液的溶质质量分数随温度升高而增大D. 40℃时,ZnSO4的溶解度为41g5. 下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )A. 甲的溶解度大于乙的溶解度B. 降温可使接近饱和的丙溶液变为饱和溶液C. 将t2°C甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数℃乙>甲=丙D. P点表示t1℃时甲、丙两种物质的溶解度都是25g6. 下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )A. 乙中含有少量甲,可用冷却热饱和溶液的方法提纯甲B. t3℃时,甲的溶液溶质质量分数一定大于乙的溶液溶质质量分数C. t3℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t2℃,析出晶体的质量甲一定大于乙D. t1℃时,乙的不饱和溶液只有通过蒸发溶剂的方法才能转变成饱和溶液7.甲、乙、丙三种固体物质的溶解度曲线如图所示。
河南中考化学基础知识复习:04专题四溶液及溶解度曲线

专题四溶液及溶解度曲线命题点1溶解与乳化1. (2020重庆B)下列饮料中,不属于溶液的是()A. 汽水B. 白酒C. 酸奶D. 苏打水2. (2020泰州)下列物质溶于水,能形成溶液的是()A. 蔗糖B. 泥土C. 粉笔灰D. 食用油3. (2020丹东)溶液在生产生活中有着广泛的应用,下列溶液中溶剂不是水的是()A. 碘酒B. 盐酸C. 氯化钠溶液D. 酒精溶液4. (2020湘西)关于溶液,下列说法正确的是()A. 将20毫升汽油放入烧杯中,加50毫升水搅拌,得到溶液B. 溶液中的溶质可以是气体、液体和固体C. 凡是均一的、稳定的液体一定是溶液D. 氢氧化钠溶于水形成溶液时,温度下降5. (2019青岛)下列与洗涤有关的做法不合理的是()A. 用洗洁精洗去餐具上的油污B. 用汽油洗去沾在衣服上的油渍C. 用白醋洗去水壶中的水垢(水垢的主要成分是碳酸钙和氢氧化镁)D. 用纯碱溶液洗去铁制品表面的铁锈命题点2溶解时的吸热、放热现象6. (2020宜宾)取某固体物质5 g加入20 mL水中,测得溶液的温度随时间变化曲线如图所示。
该固体物质可能是()第6题图A. NaClB. NaOHC. NH4NO3D. CaCO37. (2020郴州)下列物质溶于水因发生化学反应放出热量的是()A. NaOHB. NH4NO3C. NaClD. CaO8. (2020锦州)向液体X中加入固体Y,观察到U形管内红墨水左侧液面上升。
下列液体X 和固体Y的组合,符合题意的是()第8题图A.X是水,Y是氧化钙B. X是水,Y是氢氧化钠C. X是水,Y是硝酸铵D. X是水,Y是氯化钠9. (2020毕节)关于如图所示实验的相关判断错误的是()第9题图A.固体X可能是NaOHB. 固体X可能是NH4NO3C. Ca(OH)2溶解度:①>②D. Ca(OH)2质量分数:①=③命题点3溶解度、饱和溶液与不饱和溶液10. (2020张家界)在20 ℃时,将40 g氯化钠固体加入100 g水中,充分搅拌后,有4 g固体未溶解。
中考化学经典题型专题练习之溶解性、溶解度和溶解度曲线
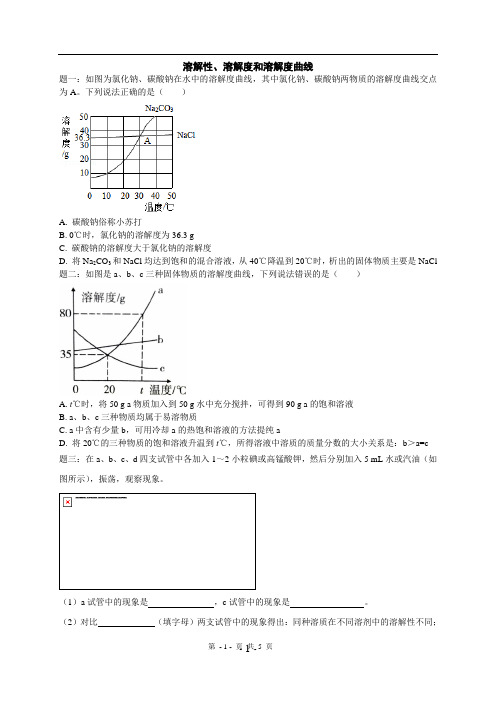
溶解性、溶解度和溶解度曲线题一:如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A。
下列说法正确的是()A. 碳酸钠俗称小苏打B. 0℃时,氯化钠的溶解度为36.3 gC. 碳酸钠的溶解度大于氯化钠的溶解度D. 将Na2CO3和NaCl均达到饱和的混合溶液,从40℃降温到20℃时,析出的固体物质主要是NaCl 题二:如图是a、b、c三种固体物质的溶解度曲线,下列说法错误的是()A. t℃时,将50 g a物质加入到50 g水中充分搅拌,可得到90 g a的饱和溶液B. a、b、c三种物质均属于易溶物质C. a中含有少量b,可用冷却a的热饱和溶液的方法提纯aD. 将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a=c题三:在a、b、c、d四支试管中各加入1~2小粒碘或高锰酸钾,然后分别加入5 mL水或汽油(如图所示),振荡,观察现象。
(1)a试管中的现象是,c试管中的现象是。
(2)对比(填字母)两支试管中的现象得出:同种溶质在不同溶剂中的溶解性不同;对比a、c试管中的现象得出的结论是;(3)【提出问题】物质的溶解性除与溶质、溶剂的性质有关外,还与什么有关?【作出猜想】。
【设计方案】。
【观察现象】。
【得出结论】。
题四:小明陪妈妈到医院输液,不小心将护士手中的盘子打翻,其中的棉球落在了小明的白色衬衣上,白色衬衣上立即出现了一大片紫黑色痕迹。
为找到去掉白衬衣上的痕迹的最好方法,几位同学进行了讨论,提出了以下几个方案并进行实验:①用水洗;②用无水酒精洗;③用汽油洗;④用四氯化碳洗;⑤用肥皂水洗;⑥用淀粉溶液洗。
(1)你认为留在白色衬衣上的紫黑色物质是什么?(2)如果用白色布条进行实验,为使实验结果更加准确,你认为该实验中需要控制哪些实验条件?(3)一位同学按如图所示方法进行实验:结果是⑤、⑥几乎完全褪色;②略带颜色;③、④略微变浅;①几乎不变。
专题20 溶解度及溶解度曲线的应用-2019年中考化学大题狂做系列(解析版)

专题20 溶解度及溶解度曲线的应用1.【广东省广州市天河区思源学校2019届九年级下学期月考】如表是NaCl、KNO3在不同温度时的溶解度:温度/℃0 10 20 30 40 50 60NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 溶解度/gKNO313.3 20.9 31.6 45.8 63.9 85.5 110(1)若要比较KNO3与NaCl在水中的溶解能力,需要控制的变量是水的质量和______。
(2)60℃时,在100 g水中加入100 g KNO3固体,充分搅拌后得到______(填“饱和”或“不饱和”)溶液,此时该溶液中溶质的质量分数为______。
若将温度冷却到20℃,烧杯中析出晶体的质量为______g,此时溶液的溶质质量分数为______(精确到0.01%)。
(3)在10℃时,NaCl饱和溶液的溶质质量分数______(填“大于”“等于”或“小于”)KNO3饱和溶液的溶质质量分数。
在50℃时,12g水中最多能溶解______ gNaCl。
【答案】温度不饱和50% 68.4 24.01% 大于 4.4【解析】(1)影响固体溶解度的外界因素主要是温度,因此要比较KNO3与NaCl在水中的溶解能力,需要控制的变量是水的质量和温度。
(2)由表中的数据可知,60℃时,硝酸钾的溶解度是110g,由溶解度的含义可知,在100 g水中加入100 gKNO3固体,充分搅拌后得到不饱和溶液,此时该溶液中溶质的质量分数为:=50%,若将温度冷却到20℃,由于在20℃时硝酸钾的溶解度是31.6g,所以在烧杯中析出晶体的质量为:100g-31.6g=68.4g,此时溶液的溶质质量分数为:24.01%。
(3)由于在10℃时,氯化钠的溶解度大于硝酸钾的溶解度,所以在10℃时,NaCl饱和溶液的溶质质量分数大于KNO3饱和溶液的溶质质量分数。
在50℃时,氯化钠的溶解度是37g,由溶解度的含义可知,12g水中最多能溶解4.4gNaCl。
2019年中考化学试题分类汇编:.溶液及溶解度曲线

课时5 溶液及溶解度曲线一、选择题8.(2019湖北省宜昌,8,1)把少量下列物质分别放入水中充分搅拌,不能得到溶液的是A.纯碱B. 蔗糖C.酒精D.面粉【答案】D【解析】纯碱、蔗糖、酒精均能溶于水,形成均一、稳定的溶液,故ABC选项不符合题意;面粉难溶于水,将面粉放入水中会形成悬浊液,而不能形成溶液,故D选项符合题意。
【知识点】溶液的形成14.(2019湖南省郴州市,14,2)将下列物质放入水中,其中一种物质的能量变化与其他三种物质不同的是A. CaOB. NaOHC.浓H2SO4D. NH4NO3【答案】D【解析】能与水反应生成氢氧化钙,并释放大量的热,使水温度升高,NaOH溶于水后使水温度升高,浓H2SO4放入水中,使水温度升高,NH4NO3固体溶于水使水温度降低,故D选项符合题意。
【知识点】固体物质溶于水后温度的变化1.(2019四川省泸州市,7,3)下列物质不溶于水的是A.酒精B.硝酸C.蔗糖D.铁锈【答案】B【解析】A.酒精与水能以任意比互溶,故A选项不符合题意;B.硝酸易溶于水,故B选项不符合题意;C.蔗糖易溶于水,故C选项不符合题意;D.铁锈不溶于水,故D选项符合题意;【知识点】物质的溶解性强弱3.(2019山东省潍坊市,3,2)下列物质不属于溶液的是()A.生理盐水B. 白醋C. 医用酒精D. 冰水混合物【答案】D【解析】A.生理盐水是氯化钠溶于水形成的均一稳定的混合物,属于溶液,故A错;B.白醋是乙酸溶于水形成的均一稳定的混合物,属于溶液,故B错;C.医用酒精是酒精溶于水形成的均一稳定的混合物,属于溶液,故C错;D.冰水混合物是由水一种物质组成,属于纯净物,不属于溶液,溶液必须属于混合物,故D正确。
【知识点】溶液的形成3.(2019湖南衡阳,3,2)溶液在我们生活中有着广泛的用途。
下列物质不属于溶液的是()A.碘酒B.食醋C.生理盐水D.牛奶【答案】D【解析】碘酒属于均一稳定的混合物,属于溶液,A错误;食醋属于均一稳定的混合物,属于溶液,B错误;生理盐水属于均一稳定的混合物,属于溶液,C错误;牛奶不均一不稳定,属于乳浊液,D 正确。
中考化学考点专训:溶解度及溶解度曲线
1. X 、Y 、Z三种物质的溶解度曲线如图所示。
将t2℃时三种物质的饱和溶液降温至t1℃,溶液中溶质质量分数大小关系正确的是 ( )A.X>Y>ZB.Y>Z>XC.Z>Y>XD.X=Y>Z【答案】B2.我国古代劳动人民常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白丝帛。
清液的主要成分及溶解度如图所示。
(1)t1℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是。
(2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充分溶解。
4组实验数据如下:由上述实验数据可知:①所得溶液是不饱和溶液的是(填序号);②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。
【答案】(1)Ca(OH)2 KOH K2CO3 (2) ①AB ② 283.下表是Ca(OH)2 和NaOH的溶解度数据。
请回答下列问题:温度/℃0 20 40 60 80 100溶解度/gCa(OH)2 0.19 0.17 0.14 0.12 0.09 0.08NaOH 31 91 111 129 313 336(1)依据上表数据,绘制Ca(OH)2 和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是(填“A”或“B”)。
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有(填序号)。
①蒸发水②升高温度③降低温度④加入水⑤加入氢氧化钙实验序号 A B C D加入氢氧化钾的质量/g7 14 56 70溶液质量/g 57 64 106 106(3)现有60 ℃时含有Ca(OH)2 和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是。
(4)现有20 ℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20 ℃,得到乙溶液,溶液中溶质的质量分数的关系为甲乙(填“>”、“<”或“=”)。
中考化学复习第一模块分类复习3.4溶解度和溶解度曲线
12/13/2021
第一页,共三十一页。
-2-
科学内容
目标
1.饱和溶液的含义 认识
2.溶解度的含义 认识
3.溶解性表或溶解 度曲线
知道
4.结晶现象
知道
中考概况
广东近年中考中,对本节知识的考查 主要集中在:①对溶解度的理解、大 小的比较、变化趋势及相关计算;② 从溶解度表中提取有效信息推断物 质的溶解度;③以溶解度曲线入题, 考查溶解度随温度的变化、溶液的 转化方法判断、两饱和溶液溶质质 量分数的比较、结晶方法的选用等; ④饱和溶液与不饱和溶液的转化
温度/℃ 10 30
50
70
90
溶解度/g 27.7 39.3
12/13/2021
第六页,共三十一页。
-7-
命题解读该考点的命题方向主要是根据溶解度数据考查①固体溶解度随温 度的变化规律;②结晶方法的选择;③利用某温度时的溶解度判断一定量水中 最多可溶解的溶质质量或计算(jìsuàn)此时的溶质质量分数;④找出两物质 溶解度相等的温度区间;⑤计算结晶析出晶体质量等。
A.②中溶液是饱和洛液 B.③中溶液一定是不饱和溶液 C.②③中溶液的溶质质量分数不相同 D.③中溶液的溶质质量大于②中溶液的溶质质量
12/13/2021
第十九页,共三十一页。
-20-
2.(2017·来宾(láibīn))20℃时氯化钾的溶解度为34g。下列是四位同学在20℃时配 制的氯化钾溶液,其中一定达到饱和的是 ( B )
饱和溶液;若 没有剩余固体
,则不一定为不饱和溶液
(可能是恰好饱和)
12/13/2021
第十页,共三十一页。
中考复习溶解度及溶解度曲线(20张)
中考复习 溶解度及溶解度曲线(20页)-PPT执 教课件 【推荐 】
2.溶质的质量分数
(1)基本公式。
溶质的质量分数=溶质质量 溶液质量
100%
饱和溶液中溶质的质量分数=
S 100g+S
100%
( S表示溶解度)
(2)溶液稀释的计算。 ①依据:溶液稀释前后,溶质的质量不变 ②公式:m浓×w浓=m稀×w稀(w表示溶质的质量分数)
分数为 _____ (精确到0.1 %) 。
(4)向饱和食盐水中加入足量的碳酸氢钱固体,会有溶解度较小的碳酸氢钠晶体析出,该 反应的化学方程式是NaCl+NH4HCO3=NaHCO3↓+NH4Cl,请根据以上信息和图中物 质的溶解度曲线,简述以硫酸铵_
溶液 分子或离子
乳浊液 小液滴
悬浊液 固体小颗粒
特点 实例
均一、稳定
不均一、不稳定
葡萄糖溶液、NaOH溶液 油水混合物 泥水、石灰乳
(1)物质以分子形式向水中扩散时,形成的溶液不具有导电性;若以离子形式向水中扩散时,形 成的溶液具有导电性,如酸、碱、盐的水溶液都能导电。
(2)物质溶于水时,往往会伴随能量的变化,如NaOH、浓硫酸溶于水放热,使溶液温度升 高;NH4 NO3溶于水吸热,使溶液温度降低。
中考复习 溶解度及溶解度曲线(20页)-PPT执 教课件 【推荐 】
中考复习 溶解度及溶解度曲线(20页)-PPT执 教课件 【推荐 】
2.饱和溶液与不饱和溶液 (1)二者之间的转化。
饱和溶液与不饱和溶液转化过程中,对溶液组成的 影响 说明:若是溶解度随温度升高而减小的物质(如熟石灰),将 饱和溶液变成不饱和溶液时应降温,将不饱和溶液变成饱 和溶液时应升温。 (2)一般来说,溶液的浓稀与溶液是否饱和没有必然的 联系,即饱和溶液不一定是浓溶液,不饱和溶液也不一定 是稀溶液。但是,在相同温度下,同种溶质的饱和溶液一 定比不饱和溶液浓。
人教版化学中考专题复习:溶解度曲线共28页
文 家 。汉 族 ,东 晋 浔阳 柴桑 人 (今 江西 九江 ) 。曾 做过 几 年小 官, 后辞 官 回家 ,从 此 隐居 ,田 园生 活 是陶 渊明 诗 的主 要题 材, 相 关作 品有 《饮 酒 》 、 《 归 园 田 居 》 、 《 桃花 源 记 》 、 《 五 柳先 生 传 》 、 《 归 去来 兮 辞 》 等 。
人教版化学中考专题复习:溶解度曲 线
6
、
露
凝
无
游
氛
,
天
高
风
景
澈
。
7、翩翩新 来燕,双双入我庐 ,先巢故尚在,相 将还旧居。
8
、
吁
嗟
身
后
名
,
于
我
若
浮
烟
。
Hale Waihona Puke 9、 陶渊 明( 约 365年 —427年 ),字 元亮, (又 一说名 潜,字 渊明 )号五 柳先生 ,私 谥“靖 节”, 东晋 末期南 朝宋初 期诗 人、文 学家、 辞赋 家、散
1
0
、
倚
南
窗
以
寄
傲
,
审
容
膝
之
易
安
。
6、最大的骄傲于最大的自卑都表示心灵的最软弱无力。——斯宾诺莎 7、自知之明是最难得的知识。——西班牙 8、勇气通往天堂,怯懦通往地狱。——塞内加 9、有时候读书是一种巧妙地避开思考的方法。——赫尔普斯 10、阅读一切好书如同和过去最杰出的人谈话。——笛卡儿
