重庆大学大学化学第一章思考题答案
重庆大学大学化学习题答案

习题答案11.△f H m(298.15K)=44.01 kJ·mol-12mol时,△H(298.15K)=88.02kJ吸热Q p=△H=88.02kJ做功W=83.06 kJ2.νA= -3,νB= -1,νc= 2,△ξ(1)=0.5mol3.(1)△ξ(1)=4mol△r H m(298.15K)= -92.30kJ·mol-1△r H(298.15K)= -369.2kJ(2)△ξ(2)=2mol△r m(298.15K)= -184.6kJ·mol-1△r H (298.15K)= -369.2kJ4.△f m(298.15K)= -157kJ·mol-15.A.△r m(298.15K)分别为-2599kJ·mol-1,-890.3kJ·mol-1,-566.0kJ·mol-1B.△c H 分别为-1299.5kJ·mol-1,-890.3kJ·mol-1,-283.0kJ·mol-1 C.发热量排队C2H2>CH4>CO D.发热量排队CH4>C2H2>CO 6.(1)C,(2)B 7.(1)31.7kJ,(2)1.91×103kJ·mol-1 8.△= -626.6kJ·mol-110.△r m(298.15K)=173.14kJ·mol-1,有11. △f m(298.15K)= -1015kJ·mol-1 12.B13.T<1.24×103K,建议不可行,因为任何温度下,△r G(T)>0 14.D<A<C<B<E15.(1)△r m(298.15K)=689.94kJ·mol-1△r S m(298.15K)=0.360kJ·K-1·mol-1(2)△r m(298.15K)=582.2·mol-1,否(3)△r(1 000K)=329.0kJ·mol-1,否(4)T>1912K16.T<463.7K21. νA=0.5mol·dm-3·s-1,νB=0.5mol·dm-3·s-1,νC=0.5mol·dm-3·s-1,3. ν=kc2A c B三级反应4.9.36 5,75kJ·mol-1 6.k=3×1012s–17.Ea=1.0×105J·mol-1,A=1.1×1013s-18. k=1.2×10-2s–1 9.20% 10.4.69×106倍11. k=4.9×10-4s–112.k1(平均值)=2.15×10-4s–1,t1/2=3223.9s13.(1)v0(蔗糖)=6.43×10-5 mol·dm-3·s-1(2)n(葡萄糖)=n(果糖)=0.128mol(3)α(蔗糖)=0.3214.1.8×10-11 mol·dm-3·s-1 15.4600年31.p总=3.9×104pa2.n(O2)=2.0×10-2mol3.p(N2)=4.6×105pa,P(O2)=105pa5.K =2.0×10-106.K =2.3×10-29,K p=8.9×10-32pa7.(1)△r G(298K)=173.1kJ·mol-1,K =5.01×10-31(2)△r m(298K)=208.4kJ·mol-1,K =3.16×10-37(3)△r G m(298K)= -33.0kJ·mol-1,K =6.03×1058.(1)△r G(298K.15K)=37kJ·mol-1,K =3.3×10-7(2)K (800K)≈1.4×1039. K (500K)=1.47×101010.K2×104,△r G m(292K)= -27.2kJ·mol-111.△r m(298K)=86.55kJ·mol-1,K(298K)=6.8×10-16△r(1 573K)≈70.7kJ·mol-1,K(1 573K)≈4.5×10-312.(1)pH=5.15(2)pH=3.8814. pH= 4.7515. pH=9.25,α=9.0×10-516.(1)1.3×10-5mol·dm-3(2)1.8×10-10mol·dm-317.(1)无沉淀生成(2)c(Cl-)=8.9×10-3mol·dm-3(3)2.2%45.(Ni2+/Ni)= -0.257V6.(1)E,△r G m= -98.4kJ·mol-1,反应能自发。
大学化学课后习题答案解析..

第一章化学反应热教学内容1.系统、环境等基本概念; 2. 热力学第一定律; 3. 化学反应的热效应。
教学要求掌握系统、环境、功、热(恒容反应热和恒压反应热)、状态函数、标准态、标准生成焓、反应进度等概念;熟悉热力学第一定律;掌握化学反应标准焓变的计算方法。
知识点与考核点1.系统(体系)被划定的研究对象。
化学反应系统是由大量微观粒子(分子、原子和离子等)组成的宏观集合体。
2.环境(外界)系统以外与之密切相关的部分。
系统和环境的划分具有一定的人为性,划分的原则是使研究问题比较方便。
系统又可以分为敞开系统(系统与环境之间既有物质交换,又有能量交换);封闭体系(系统与环境之间没有..能量交换);..物质交换,只有孤立系统(体系与环境之间没有物质交换,也没有能量交换)系统与环境之间具有边界,这一边界可以是实际的相界面,也可以是人为的边界,目的是确定研究对象的空间范围。
3.相系统中物理性质和化学性质完全相同的均匀部分。
在同一个系统中,同一个相可以是连续的,也可以是不连续的。
例如油水混合物中,有时水是连续相,有时油是连续相。
4.状态函数状态是系统宏观性质(T、p、V、U等)的综合表现,系统的状态是通过这些宏观性质描述的,这些宏观性质又称为系统的状态函数。
状态函数的特点:①状态函数之间往往相互制约(例如理想气体状态方程式中p、V、n、T之间互为函数关系);②其变化量只与系统的始、末态有关,与变化的途径无关。
5*.过程系统状态的变化(例如:等容过程、等压过程、等温可逆过程等)6*.途径完成某过程的路径。
若系统的始、末态相同,而途径不同时,状态函数的变量是相同的。
7*.容量性质这种性质的数值与系统中的物质的量成正比,具有加合性,例如m(质量)V、U、G等。
8*.强度性质这种性质的数值与系统中的物质的量无关,不具有加合性,例如T、 (密度)、p(压强)等。
9.功(W)温差以外的强度性质引起的能量交换形式 [W=W体+W有]。
大一有机化学答案
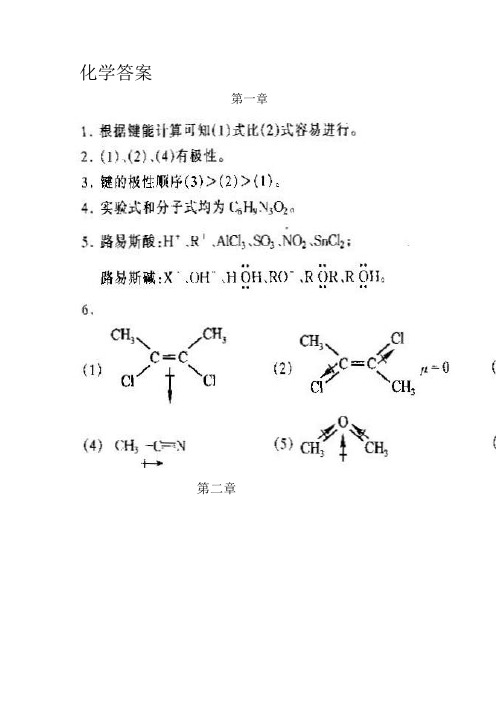
化学答案第一章第二章•3-甲基戊烷(3) 2,4-二甲基-3-乙基戊烷•2,2,3-三甲基丁烷(5) 2,3,4-三甲基己烷(6) 2,2,5-三甲基-6-异丙基壬烷(4)5. (1) .(2)都是等同的6. (1)第三章7. 属于同分异构体的是(1) (2),(3) (4) 属于同种物质的是(3) (5)属于同系物的是(1)(3), (2)(3), (1)(4), (2)(4)第三章 习题参考答案•(1) 3,4-二甲基-1,3-戊二烯 (2)5-甲基-3-己烯-1-炔(3) (E)-3-甲基-2-戊烯 (4)(Z)-2-甲基-3-乙基-3-己烯(5)2,6-二甲基-2-庚烯 (6) 丙炔银 (7) 3,3-二甲基-1-戊烯 (8) 4-甲基-2-戊炔2. (3)(4) (5)(2) CH 2C HCCH+Br 2BrH 2CC H Br C CH3. (2) ,(3)有顺反异构体。
结构式略。
4.(6) C H3C C H2C H2C H2C H2C CH3O O(8) (9)(10) (11)(12 )CH3CH3(13)CH3CH2CH2Br(14) (15) OHOH 5.(1)(2)1-丁炔2-丁炔丁烷[Ag(NH3)2+]白色沉淀无现象无现象溴水褪色无变化(C H3C H2C H2)3B,C H3C H2C H2OH6.7. 其结构式为:8. (2) > (3) > (1)9. 其结构式为:10. A,B的结构式分别为:第四章•(1) 1,1-二甲基-2-异丙基环丙烷(2) 5-甲基螺[2,4]庚烷(3) 2-甲基-3-环丙基丁烷(4) 1-甲基-3-乙基环己烷(5) 2-硝基苯磺酸(6)1,7-二甲基萘(7) 双环[3,2,1]辛烷(8)1-甲基-1,3-环戊二烯(9) 4-硝基-2-氯甲苯(10)1,2-二苯乙烯3. (3),(5),(6) 有芳香性,因为其结构为平面共轭的,且 电子数符合(4n+2)(1),(2),(4) ,(7),(8)无芳香性。
分析化学第1章思考题答案

第1章 绪论【思考题解答】4. 标定碱标准溶液时,邻苯二甲酸氢钾(KHC 8H 4O 4,M = 204.23 g·mol -1)和二水合草酸(H 2C 2O 4·2H 2O,M = 126.07 g·mol -1)都可以作为基准物质,你认为选择哪一种更好?为什么? 答:选择邻苯二甲酸氢钾更好。
因为邻苯二甲酸氢钾的摩尔质量较大,称量误差较小5.基准物Na 2CO 3和Na 2B 4O 7·10H 2O 都可用于标定HCl 溶液的浓度。
你认为选择哪一种更好? 为什么?答:选择Na 2B 4O 7·10H 2O 更好。
因为Na 2B 4O 7·10H 2O 的摩尔质量较大,称量误差较小6. 用基准Na 2CO 3标定HCl 溶液时,下列情况会对HCl 的浓度产生何种影响(偏高,偏低或没有影响)?a. 滴定时速度太快,附在滴定管壁的HCl 来不及流下来就读取滴定体积;b. 称取Na 2CO 3时,实际质量为0.1834 g ,记录时误记为0.1824 g ;c. 在将HCl 标准溶液倒入滴定管之前,没有用HCl 溶液荡洗滴定管;d. 锥瓶中的Na 2CO 3用蒸馏水溶解时,多加了50 mL 蒸馏水;e. 滴定开始之前,忘记调节零点,HCl 溶液的液面高于零点;f. 滴定官活塞漏出HCl 溶液;g. 称取Na 2CO 3时,撒在天平盘上;h. 配制HCl 溶液时没有混匀。
答:据2323Na CO HCl Na CO HCl m c M V =⨯a 由于V HCl 偏高,c HCl 偏低;b 由于23Na CO m 偏低,c HCl 偏低;c 由于V HCl 偏高,c HCl 偏低;d 无影响;e 因为V HCl 偏低,c HCl 偏高;f 因为V HCl 偏高,c HCl 偏低;g 由于Na 2CO 3易吸湿,应用减量法称量。
称取Na 2CO 3时,撒在天平盘上,Na 2CO 3会 吸湿,使23Na CO m 偏低,最终导致c HCl 偏低;h 溶液没有混匀时,很可能的情况是上层较稀,因此c HCl 偏低的可能性较大。
大学化学实验_重庆大学中国大学mooc课后章节答案期末考试题库2023年

大学化学实验_重庆大学中国大学mooc课后章节答案期末考试题库2023年1.能相互反应产生有毒气体的废液,不得倒入同一收集桶中,应分类存放,并贴上标签。
答案:正确2.实验用过的仪器应及时清洁干净,放回指定位置,化学药品归还实验室,实验成品可自行带走。
答案:错误3.对强酸灼伤,应立即用水冲洗,再用20%-50%的碳酸钠或碳酸氢钠,肥皂水或淡石灰水冲洗,最后用水冲洗。
答案:错误4.倾注药剂或加热液体时,不要俯视容器,以防溅出。
试管加热时,切记不要使试管口向着自己或别人。
答案:正确5.酒精起火时,应立即用湿布或沙土等灭火,如火势较大,也可用泡沫灭火器灭火。
答案:正确6.对于无机酸类废液,实验室可以收集后进行如下处理:将废酸慢慢倒入过量的含碳酸钠或氢氧化钙的水溶液中(或用废碱)互相中和,再用大量水冲洗。
答案:正确7.含Pb等重金属的废液需要将重金属转化为难溶的氢氧化物,离子含量达标后方可排放。
答案:正确8.关于金属腐蚀,下列说法错误的是答案:发生吸氧腐蚀是由于金属表面氧气分布浓度不同而引起的_钢铁在大气中的腐蚀只有析氢腐蚀9.电镀结束后,对工件表面形状进行认真观察和仔细记录。
答案:正确10.下列关于试剂的取用描述正确的是答案:往试管中滴加试剂时,切勿使滴管伸入滴管中_所有取出的液体试剂和固体试剂都不能再倒入原试剂瓶中_从滴瓶中取用试剂时,需用滴瓶中的滴管11.下列关于学生实验守则描述正确的是答案:实验完毕,须清洗玻璃仪器,放回原位_随时保持实验台面的整洁_节约试剂,按规定用量取用12.采用EDTA滴定法测定水的硬度时,如何判断滴定的终点答案:溶液恰好由红色变成蓝色13.测定水的硬度时,采用EDTA进行配位滴定,所用指示剂为答案:铬黑T14.在进行电抛光前不需要的操作是答案:打磨工件15.在金属铜片上电镀镍时,下列操作正确的是答案:铜片做阴极,镍片做阳极16.在电抛光过程中,关于电化学除油操作的正确描述是答案:工件做阴极,钢板做阳极17.在进行减压过滤时,下列操作错误的是答案:抽滤前应用同一溶剂润湿滤纸18.影响反应速率常数的因素有答案:催化剂_反应温度_反应活化能19.用外推法确定∆T时,首先要在坐标纸上绘制反应温度随时间的变化曲线,坐标系的横轴是反应时间,纵轴是反应温度,单位是K。
重庆大学大学化学()期末考试试卷

重庆⼤学⼤学化学()期末考试试卷重庆⼤学⼤学化学(Ⅰ)期末考试试卷(B)试卷号:B070005学院___________ 专业___________姓名___________ 学号___________(请考⽣注意:本试卷共5页)⼀、对的在题末括号内填“+”、错的填“-”。
(本⼤题分9⼩题, 每⼩题1分, 共9分)1、⼀个反应如果是放热反应,当温度升⾼时,表⽰补充了能量,因⽽有助于提⾼该反应进⾏的程度。
答:()2、现有H2CO3、H2SO4、NaOH、NH4Ac 四种溶液,浓度均为0.01 mol?dm-3,同温度下在这四种溶液中,c(H+) 与c(OH-) 之乘积均相等。
答:()3、⽤两条相同的锌棒,⼀条插⼊盛有0.1 mol?dm-3 ZnSO4溶液的烧杯中,另⼀条插⼊盛有0.5 mol?dm-3ZnSO4溶液的烧杯中,并⽤盐桥将两只烧杯中溶液联接起来,便可组成⼀个原电池。
答:()4、冰与⼲冰相⽐,其熔点和沸点等物理性质有很⼤的差异,其重要原因之⼀是由于冰中H2O 分⼦间⽐⼲冰中CO2分⼦间多了⼀种氢键作⽤的缘故。
答:()5、已知HCN 是直线形分⼦,所以它是⾮极性分⼦。
答:()6、升⾼温度,使吸热反应的反应速率提⾼,放热反应的反应速率降低,从⽽使平衡向吸热的⽅向移动。
答:()7、析氢腐蚀与吸氧腐蚀的不同点在于阴极处的电极反应不同:析氢腐蚀时,阴极上H+放电析出H2;⽽吸氧腐蚀时,阴极上是O2得电⼦变成OH-。
答:()8、实验测得CS2是直线型结构的分⼦,则分⼦中共有4 个σ键。
答:()9、螯合物的稳定性⼤于⼀般配合物。
答:()⼆、将⼀个或两个正确答案的代码填⼊题末的括号内。
若正确答案只有⼀个,多选时,该题为0分;若正确答案有两个,只选⼀个且正确,给1分,选两个且都正确给2分,但只要选错⼀个,该⼩题就为0分。
(本⼤题分14⼩题, 每⼩题2分, 共28分)1、真实⽓体⾏为接近理想⽓体性质的外部条件是答:()(1) 低温⾼压(2) ⾼温低压(3) 低温低压(4) ⾼温⾼压2、温度⼀定,在BaSO4饱和溶液中,加⼊⼀定量0.1mol?dm-3BaCl2溶液,则BaSO4的溶解度可能发⽣的变化是答:()(1) 不变(2) 增⼤(3) 降低(4) 不确定3、已知下列各电对的标准电极电势:E(Fe3+/Fe2+)=+0.77V E(Cu2+/Cu)=+0.34VE(Mg2+/Mg)= -2.83V E(Cl2/Cl-)=+1.36V则在标准条件下,最强的还原剂是答:()(1)Fe2+(2)Cu(3)Mg(4)Cl-(5)Mg2+4、4f 轨道的⾓量⼦数为答:()(1)0 (2)1(3)2 (4)35、下列元素中电负性最⼤的是答:()(1)Na(2)Ca(3)S(4)I(5)Cl6、已知K(HAc)=1.76?10-5,若⽤HAc 和NaAc 溶液配制pH=4.0 的缓冲溶液,则所需两种溶液浓度之⽐c(HAc)/c(NaAc) 为答:()(1) 5:8.8(2) 50:8.8(3) 8.8:50(4) 8.8:57、对于反应:2MnO4-+10Fe2++16H+=2Mn2++10Fe3++8H2O,有?r G= -nFE。
重庆大学有机化学习题答案

习题答案第一章1.(1)有机化合物:含碳化合物(一氧化碳、二氧化碳、碳酸盐、金属碳化物等少数简单含碳化合物除外)或碳氢化合物及其衍生物的总称。
有机物是生命产生的物质基础。
(2)共价键:共价键(covalent bond)是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定的化学结构叫做共价键。
(3)同分异构:同分异构是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物的现象。
(4)杂化:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化。
(5)偶极矩:正、负电荷中心间的距离r和电荷中心所带电量q的乘积,叫做偶极矩μ=r×q。
它是一个矢量,方向规定为从负电荷中心指向正电荷中心。
(6)诱导效应:诱导效应是指在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects)。
(7)异裂:共价键断裂时,共用电子对完全转移给成键原子中的某个原子,形成了正、负离子,这种断键方式称为异裂。
(8)范德华力:在化学中通常指分子之间的作用力。
(9)键角:分子中和两个相邻化学键之间的夹角。
(10)Lewis酸:路易斯酸(Lewis Acid,LA)是指电子接受体,可看作形成配位键的中心体。
(11)疏水作用:非极性分子间或分子的非极性基团间的吸引力。
导致这些基团在水性环境中的缔合。
(12)官能团:决定有机物性质的原子或原子团称为官能团。
2.(1)(2)(3)(4)(5)(6)(7)(8)(9)3.具有偶极的分子:(1)两H原子中心指向O原子方向;(2)又H原子指向Br原子;(4)H原子指向三个Cl原子的中心方向;(5)乙基指向羟基方向4.(1)正庚烷;(2)异丁烷;(3)异己烷;(4)新戊烷5.(1)(2)(3)(4)6.酸:Cu2+ FeCl3 CH3CN碱:NH3 CH3NH2 C2H5OC2H5加合物:CH3COOH CH3OH7.(1)CH3COOH/CH3COO- H3O+/ H2O(2)H2SO4/HSO4- CH3OH2+/CH3OH(3)HNO3/NO3- (CH3)3NH+/(CH3)3N8. (3) CH3Cl > (2) CH3F >(4)CH3Br >(5)CH3I > (1) CH49. 单键最长,双键次之,叁键最短.单键中两个原子间的电子云密度小,叁键两个原子间的电子云密度最大,共同的电子把两个原子吸引得最近.所以说,叁键最短,单键最长,双键处于中间.10. C5H12O11. C 8H 10N 4O 2第二章1. ⑶>⑵>⑴>⑸>⑷3. 2-甲基丁烷较稳定的构象是:3H 33CH3CH 3⑴⑵⑶其中⑴和⑵更稳定。
第一章 化学热力学基础思考题与习题答案

第二章化学键与分子结构同步练习、思考题与习题答案同步练习P50:1.(A)2.(D)P57:1.(B)2.(C)P64:1.(D)2.(D)3.(C)P71:1.(C)2.平面三角形、三角锥形、平面三角形;sp2、不等性sp3、sp23.(D)P78:1.(B)2.(A)3.(C),(A)与(D)4.(C)、(F)P86:1.(B)2.(C)3.SbH3> AsH3> PH3,高,取向力、诱导力、色散力,氢键作用力思考题1.(1)B (2)C (3)D (4)C 、E (5)C、D (6)B (7)A、D (8)A 2.(1)×(2)×(3)√(4)×(5)×(6)×3.略4.(1)(2)大多数分子中以色散力为主。
(3)(4)水分子间易形成氢键,导致分子间作用力加强,因此水蒸气易液化。
而氮气分子间以及氢气分子间都只有色散力,且分子量较小,因此分子间作用力相对较弱,故通常条件下不易液化。
(5)CF4、CCl4、CBr4和CI4四化合物均为非极性分子,分子间只存在色散力,随分子量增大,分子间作用力逐渐加强,因此状态由气态到液态再到固态,同时熔点也依次升高。
习题1.Be2+:2电子构型Fe2+、Cu2+:9~17电子构型Zn2+、Sn4+:18电子构型Pb2+:18+2电子构型S2--、Br–:8电子构型2.非极性分子:CH4、BCl3、CS2;极性分子:CHCl3、NCl3、H2S3.(1)色散力(2)取向力、诱导力、色散力、氢键(3)诱导力、色散力(4)取向力、诱导力、色散力4.5.6.不等性sp 3,角形,H 2O 偶极矩大,χΔ大。
7.O 2分子轨道电子排布式为:O 2 :(σ1s )2(σ*1s )2(σ2s )2(σ*2s )2(σ2p x )2(π2p y )2(π2p z )2(π*2p y )1(π*2p z )1 O 2+、O 2-、O 22-分子轨道电子排布式分别为:O 2+ :(σ1s )2(σ*1s )2(σ2s )2(σ*2s )2(σ2p x )2(π2p y )2(π2p z )2(π*2p y )1 O 2- :(σ1s )2(σ*1s )2(σ2s )2(σ*2s )2(σ2p x )2(π2p y )2(π2p z )2(π*2p y )2(π*2p z )1 O 22-:(σ1s )2(σ*1s )2(σ2s )2(σ*2s )2(σ2p x )2(π2p y )2(π2p z )2(π*2p y )2(π*2p z )2O 2+、O 2、O 2-、O 22-单电子数分别为1、2、1和0,分别具有顺磁、顺磁、顺磁和反磁性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
重庆大学大学化学第一章思考题答案
1、下列生物碱碱性最强的是()[单选题] *
APkA=22
BPkA=5(正确答案)
CPkA=13
DPkA=58
2、苯丙素类化合物的生物合成途径是()[单选题] *
A醋酸-丙二酸途径
B丙二酸途径
C莽草酸途径(正确答案)
D氨基酸途径
3、下列方法中哪一个不是按照色谱法的操作形式不同而进行分类的()[单选题] * A离子交换色谱(正确答案)
B薄层吸附色谱
C纸色谱
D吸附柱色谱
4、由两个C6-C3单体聚合而成的化合物称()[单选题] * A木质素
B香豆素(正确答案)
C黄酮
D木脂素
5、木脂素母核结构中的C6-C3单体数目为()[单选题] * A1个
B2个(正确答案)
C3个
D4个
6、阿托品是莨菪碱的()[单选题] *
A左旋体
B右旋体
C同分异构体
D外消旋体(正确答案)
7、香豆素衍生物最常见的羟基取代位置是()[单选题] * AC7位(正确答案)
BC5位
CC3位
DC6位
8、香豆素及其苷发生异羟肟酸铁反应的条件为()[单选题] *
A在酸性条件下
B在碱性条件下
C先碱后酸(正确答案)
D在中性条件下
9、适用于队热及化学不稳定的成分、低极性成分的提取()[单选题] * A渗漉法
B超声提取法
C回流提取法
D超临界流体提取法(正确答案)
10、沉淀法的分类不包括以下哪一种方法()[单选题] *
A水提醇沉法
B碱提酸沉法
C铅盐沉淀法
D结晶法(正确答案)
11、苯丙素类的基本母核是具有一个或数个()单元的天然化合物()[单选题] * AC6-C3基团(正确答案)
BC6-C6基团
CC5-C3基团
DC8-C8基团
12、黄酮母核具有的下列何种结构特点在碱液中不稳定()[单选题] *
A邻二酚羟基(正确答案)
B3-羟基
C5-羟基
D7-羟基
13、检识黄酮类化合物首选()[单选题] *
A盐酸-镁粉反应(正确答案)
B四氢硼钠反应
C硼酸显色反应
D锆盐-枸橼酸反应
14、大黄素型蒽醌母核上的羟基分布情况是()[单选题] *
A一个苯环的β位
B苯环的β位
C在两个苯环的α或β位(正确答案)
D一个苯环的α或β位
15、属于二萜的化合物是()[单选题] *
A龙脑
B月桂烯
C薄荷醇
D穿心莲内酯(正确答案)
16、纸色谱是分配色谱中的一种,它是以滤纸为(),以纸上所含的水分为固定相的分配色谱。
()[单选题] *
A固定相
B吸附剂
C展开剂
D支持剂(正确答案)
17、二萜的异戊二烯单位有()[单选题] *
A5个
B6个
C3个(正确答案)
D4个
18、萃取法是利用混合物中各成分在两相溶剂中的分配.系数不同而到达分离的方法,所谓两相溶剂是指()[单选题] *
A两种相互接触而又不相溶的溶剂(正确答案)
B两种不相互接触而又互相溶的溶剂
C两种不相互接触而又不相容的溶剂
D两种互相接触而又互相溶的溶剂
19、挥发油的溶解性难溶于()[单选题] *
A水(正确答案)
B乙醇
C石油醚
D乙醚
20、从香豆素类的结构与分类看,下列属于简单香豆素类的是()[单选题] *
A龙脑
B七叶内酯(正确答案)
C薄荷醇
D西瑞香素
21、淀粉含量多的药材提取时不宜用()[单选题] *
A浸渍法
B渗漉法
C煎煮法(正确答案)
D回流提取法
22、从香豆素类的结构看,香豆素是一种()[单选题] * A内酯(正确答案)
B羧酸
C酰胺
D糖
23、与明胶反应生成沉淀的成分是()[单选题] *
A强心苷
B皂苷
C有机酸
D鞣质(正确答案)
24、香豆素母核为()[单选题] *
A苯骈-A-吡喃酮(正确答案)
B对羟基桂皮酸
C反式邻羟基桂皮酸
D顺式邻羟基桂皮酸
25、羟基蒽醌类化合物中,大黄素型和茜草素型主要区别于()[单选题] *
A羟基位置
B羟基数目
C羟基在不同苯环上的分布(正确答案)
D羟基数目
26、以下哪种方法是利用成分可以直接由固态加热变为气态的原理()A [单选题] * A升华法(正确答案)
B分馏法
C沉淀法
D透析法
27、挥发油可析出结晶的温度是()[单选题] *
A0~-20℃(正确答案)
B0~10℃
C0~20℃
D0~15℃
28、萜类化合物在化学结构上的明显区别是()[单选题] *
A氮原子数不同
B碳原子数不同(正确答案)
C碳环数不同
D硫原子数不同
29、在脱铅处理中,一般通入的气体为()[单选题] *
A氯化氢
B二氧化硫
C硫化氢(正确答案)
D二氧化碳
30、以葛根素为指标成分进行定性鉴别的中药是()[单选题] * A葛根(正确答案)
B黄芩
C槐花
D陈皮。
