广东省惠州市2014届高三4月模拟考试化学试题(WORD版)
广东省惠州市铁场中学高三化学模拟试卷含解析

广东省惠州市铁场中学高三化学模拟试卷含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色排列的正确顺序是①金属钠在氧气中燃烧;②FeSO4溶液滴入NaOH溶液中并在空气中放置一段时间;③FeCl3溶液滴入KSCN溶液;④无水硫酸铜放入医用酒精中。
A.②③①④ B.③②①④C.③①②④ D.①②③④参考答案:B略2. 有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是()A.氧化剂与还原剂的物质的量之比为1∶8B.该过程说明Fe(NO3)2溶液不宜加酸酸化C.若有1 mol NO3-发生氧化反应,则转移8 mol e-D.若把该反应设计为原电池,则负极反应为Fe2+-e-===Fe3+参考答案:C略3. 下列有机物命名正确的是参考答案:B4. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )A、pH=l的溶液中:Ca2+、Fe2+,NO3-B、的溶液中:Na+、NH4-.Cl-C、c(Fe3+)=0.1 mol L-1的溶液中:K+、SCN-、SO42-D、由水电离的c(H+)=1×10-14 mol L-1的溶液中;Na+、AlO2-、CO32-参考答案:B略5. (2010·全国卷Ⅰ)下列判断错误的是A.沸点: B.熔点:C.酸性: C.碱性:参考答案:AB考查不同类型晶体的熔沸点高低,2008年高考全国卷I第8题已经考过,一般认为是:原子晶体>离子晶体>分子晶体,所以B正确; C项正确,一般元素非金属性越强,对应最高价氧化物的水化物的酸性越强;D正确,一般元素金属性越强,对应最高价氧化物的水化物的碱性越强。
A项错误,2009年高考全国卷I第29题已经考过,NH3分子间存在氢键,故最高,AsH3、PH3分子间不存在氢键,只有范德华力,组成和结构相似的分子相对分子质量越大,其分子间作用力越大,熔沸点越高故应该为:NH3>AsH3>PH3;6. 如图是课外活动小组同学设计的4个喷泉实验方案.下列有关操作不可能引发喷泉现象的是A. 挤压装置①的胶头滴管使CCl4全部进人烧瓶,片刻后打开止水夹B. 挤压装置②的胶头滴管使NaOH溶液全部进人烧瓶.片刻后打开止水夹C. 用鼓气装置从装置③的a处不断鼓人空气并打开止水夹D. 向装置④的水槽中慢慢加人足量浓硫酸并打开止水夹参考答案:B略7. (2分)能正确表示下列反应的离子方程式是()DA.FeCl3溶液与Cu反应生成氯化亚铁和氯化铜,离子方程式两边正电荷不相等,正确的离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故A错误;B.NH4HCO3溶液与足量Ba(OH)2溶液混合,反应生成碳酸钡沉淀、一水合氨和水,正确的离子方程式为:NH4++HCO3﹣+Ba2++2OH﹣=BaCO3↓+H2O+NH3?H2O,故B错误;C.将过量的CO2通入Ca(ClO)2溶液中,反应生成碳酸氢钙,正确的离子方程式为:CO2+H2O+ClO﹣=HClO+HCO3﹣,故C错误;D.设溶液体积为1L,1L 0.2 mol?L﹣1的KAl(SO4)2溶液中含有0.2mol铝离子、0.4mol 硫酸根离子,1L 0.3 mol?L﹣1的Ba(OH)2溶液中含有0.3mol钡离子、0.6mol氢氧根离子,两溶液等体积混合后生成0.2mol氢氧化铝沉淀、0.3mol硫酸钡沉淀,反应的离子方程式为:2Al3++3SO42﹣+3Ba2++6OH﹣=2Al(OH)3↓+3BaSO4↓,故D正确;8. 常温下,用0.1000mol?L﹣1NaOH溶液滴定20.00mL 0.1000mol?L﹣1CH3COOH溶液所得滴定曲线如图.下列说法不正确的是()A.点①所示溶液中:c(CH3COO﹣)+c(CH3COOH)=2c(Na+)B.点②所示溶液中:c(Na+)=c(CH3COO﹣)C.点③所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO﹣)D.滴定过程中可能出现:c(CH3COOH)>c(H+)>c(CH3COO﹣)>c(Na+)>c (OH﹣)参考答案:D考点:酸碱混合时的定性判断及有关ph的计算..专题:电离平衡与溶液的pH专题.分析:A、根据点①反应后溶液是CH3COONa与CH3COOH物质的量之比为1:1的混合物,所以c(CH3COO﹣)+c(CH3COOH)=2c(Na+);B、点②pH=7,即c(H+)=c(OH﹣),由电荷守恒可知:c(CH3COO﹣)+c(OH﹣)=c (Na+)+c(H+),所以c(Na+)=c(CH3COO﹣);C、点③体积相同,则恰好完全反应生成CH3COONa,根据物料守恒可知:c(Na+)=c (CH3COOH)+c(CH3COO﹣);D、在滴定中当加入碱比较少时,可能出现c(CH3COOH)>c(CH3COO﹣)>c(H+)>c(Na+)>c(OH﹣)的情况.解答:解:A、根据点①反应后溶液是CH3COONa与CH3COOH物质的量之比为1:1的混合物,所以c(CH3COO﹣)+c(CH3COOH)=2c(Na+),故A正确;B、点②pH=7,即c(H+)=c(OH﹣),由电荷守恒知:c(Na+)+c(H+)=c(CH3COO ﹣)+c(OH﹣),故c(Na+)=c(CH3COO﹣),故B正确;C、点③说明两溶液恰好完全反应生成CH3COONa,物料守恒可知:c(Na+)=c(CH3COOH)+c(CH3COO﹣),故C正确;D、如果出现c(CH3COOH)>c(H+)>c(CH3COO﹣)>c(Na+)>c(OH﹣)这个关系,则溶液中电荷不守恒,故D错误;故选:D.点评:本题考查NaOH与CH3COOH的反应,涉及盐类的水解和溶液离子浓度的大小比较,注意利用电荷守恒的角度做题.9. 下列溶液中,微粒浓度关系正确的是()A.含NH、Cl-、H+、OH-的溶液,其离子浓度一定是:c(Cl-)>c(NH+4)>c(H+)>c(OH-)B.pH=7的氨水与氯化铵的混合溶液中,Cl-与NH的浓度关系:c(Cl-)>c(NH)C.0.1 mol·L-1的Na2S溶液中粒子浓度关系:c(OH-)=c(HS-)+2c(H2S)+c(H+)D.pH=3的一元酸和pH=11的一元强碱等体积混合:c(OH-)=c(H+)参考答案:C略10. 下列说法正确的是A.稀释Na2CO3溶液时,增大B.常温下,反应C.用0.1mol·L1 CH3COOH溶液滴定0.lmol·L-1 NaOH至中性时:c(CH3COO—)+ c(CH3COOH)=c(Na+)D.向纯水中加入盐酸或氢氧化钠都能使水的电离平衡逆向移动,水的离子积减小参考答案:B略1.2013年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行。
【化学】广东省惠东高级中学2014届高三入学摸底考试试题

化学试题第一部分选择题一、单项选择题:本大题共6小题,每小题4分,共24分。
在每小题给出的四个选项中,只有一个选项符合题目要求,选对的得4分,选错或不答的得0分。
7.化学与生产、生活密切相关。
下列叙述正确的是A.淀粉、油脂和蛋白质都是天然高分子化合物B.14C可用于文物年代的鉴定,14C与12C互为同素异形体C.葡萄糖注射液不能产生丁达尔效应现象,不属于胶体D.从海水中可以得到NaCl,电解饱和NaCl溶液可以得到金属Na8.设n A为阿伏加德罗常数的数值,下列说法正确的是A.1L 1mol·L-1的氯化铵溶液中有n A个NH4+B.常温常压下,8g O2含有0.5n A个氧原子C.标准状况下,22.4LSO2含有n A个O2D.1molNa被完全氧化生成Na2O2,失去2n A个电子9.在含1molHCl的水溶液中能大量共存的一组离子是A.Na+、K+、Cl-、HCO3-B.Ca²⁺、Na+、Fe2+、NO3-C.K+、NH4+、Ag⁺、SO42-D.K+、Ca2+、Cl-、NO3-10.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图1所示。
下列说法正确..的是A.元素X与元素Z的最高正化合价之和的数值不等于8B.离子Y2-和Z 3+的核外电子数和电子层数都不相同C.元素Y的氢化物的稳定性比W的氢化物强D.Z单质只能和酸反应生成氢气11.反应产物除与反应物的结构、性质有关,还与反应的条件有关。
下列各组物质反应时:①Cu与HNO3溶液②Cu与FeCl3溶液③Na与O2中,由于浓度或条件不同得到不同产物的是:A.①②B.①②③C.②③D.①③12.下列离子方程式中正确的是A.过量氨水加入AlCl3溶液中:Al3++4NH₃·H₂O= [Al(OH) 4]-+4NH₄⁺B.实验室用Ca(OH)2和NH4Cl制取氨气:OH-+NH4+NH3↑+ H2OC.金属钠溶于水中:2Na+2H2O = 2Na++2OH-+H2↑D.足量氯气通入FeI2溶液中:Cl2+2Fe2+= 2Fe3+ + 2Cl-二、双项选择题:本大题共2小题,每小题6分,共12分。
广东省惠州市2014届高三4月模拟考试数学文理试题 Word版含答案

广东省惠州市2014届高三4月模拟考试数 学 试 题(文科) 2014.04本试卷共5页,21小题,满分150分。
考试用时120分钟。
一、选择题:本大题共10小题,每小题5分,满分50分.在每小题给出的四个选项中,只有一项是符合题目要求的.请在答题卡上填涂相应选项. 1.函数3)(+=x x g 的定义域为( )A .{}3-≥x xB .{}3->x xC .{}3-≤x xD .{}3-<x x2.已知向量)3,2(),5,1(=-=,则向量+2的坐标为( )A .)3,1(B .)4,2(C .)4,5(D .)13,0( 3.不等式021≥+-xx的解集为( ) A .]1,2[- B .]1,2(- C .),1()2,(+∞--∞ D .),1(]2,(+∞--∞4.i 是虚数单位,若i i z )1(+=,则z 等于( )A .2B .2C .1D .22 5.如图,一个空间几何体的主视图、左视图、俯视图为全等 的等腰直角三角形,如果学科网直角三角形的直角边长为1,那么这 个几何体的体积为 ( ) A .1 B .21 C .31D .61 6.用二分法求方程x x -=3lg 的近似解,可以取的一个区间是( ) A .)1,0( B .)2,1( C .)3,2( D .)4,3(7. 已知椭圆110222=-+-my m x 的长轴在x 轴上,焦距为4,则m 等于 ( ) A .8 B .7 C .6 D .58.设n m 、是两条不同的直线,βα、是两个不同的平面。
下列四个命题正确的是( ) A.ββαα//,//,m m 则若⊂ B.βαββα//,//,//,则、若n m n m ⊂ C.n m n m ⊥⊥⊥则若,//,,ββαα D.βαγβγα⊥⊥⊥则若,, 9.已知1123456(1)n n s n +=-+-+-++-⋅,则61015s s s ++等于( )A .5-B .1-C .0D .6左视图主视图 俯视图P10.设命题p :函数)32sin(π+=x y 的图象向左平移6π个单位长度得到的曲线关于y 轴对称; 命题q :函数13-=xy 在[)+∞-,1上是增函数.则下列判断错误..的是( ) A .p 为假 B .q ⌝为真 C .q p ∧为假 D .q p ∨为真 二、填空题:本大题共5小题,考生作答4小题,每小题5分,满分20分. (一)必做题(11~13题)11.已知点),(y x 满足⎪⎩⎪⎨⎧≤+≥≥100y x y x ,则x y u -=的最小值是 .12. 程序框图(即算法流程图)如下图所示,其输出结果是 . 13.设一直角三角形的两条直角边长均是区间)1,0(上 的任意实数,则斜边长小于43的概率为 . (二)选做题(14~15题,考生只能从中选做一题)14.(坐标系与参数方程选做题)在平面直角坐标系下,曲线)(22:1为参数t ty a t x C ⎩⎨⎧-=+=,曲线)(sin 22cos 2:2为参数θθθ⎩⎨⎧+==y x C .若曲线21,C C 有公共点,则实数a 的取值范围是____________.15.(几何证明选讲选做题)如右图所示,P 是圆O 外一点,过P 引圆O 的两条割线,PABPCD 、PA AB ==3CD PC ==,则 . 三、解答题:本大题共6小题,满分80分.解答须写出文字说明、证明过程和演算步骤. 16. (本小题满分12分)已知函数R x x x x x f ∈+=,cos sin cos )(2(1)求)6(πf 的值; (2)若53sin =α,且),2(ππα∈,求)242(πα+f .第12题图17.(本小题满分12分)某校高三(1)班共有40名学生,他们每天自主学习的时间全部在180分钟到330分钟之间,按他们学习时间的长短分5个组统计,得到如下频率分布表:(1)求分布表中s ,t 的值;(2)王老师为完成一项研究,按学习时间用分层抽样的方法从这40名学生中抽取20名进行研究,问应抽取多少名第一组的学生?(3)已知第一组学生中男、女生人数相同,在(2)的条件下抽取的第一组学生中,既有男生又有女生的概率是多少?18.(本小题满分14分)如图1,在直角梯形ABCD 中,CD AB //,AD AB ⊥,且121===CD AD AB . 现以AD 为一边向梯形外作正方形ADEF ,然后沿边AD 将正方形ADEF 翻折,使平面ADEF 与平面ABCD 垂直,M 为ED 的中点,如图2. (1)求证:AM ∥平面BEC ; (2)求证:BDE BC 平面⊥; (3)求点D 到平面BEC 的距离.FE D CBA图1ABCDFE 图2M19.(本小题满分14分)已知正项数列{}n a 中,31=a ,前n 项和为n S )(*N n ∈,当2≥n=. (1)求数列{}n a 的通项公式;(2)记n T 是数列{}n b 的前n111,n n a a +的等比中项,求n T .20.(本小题满分14分)已知椭圆)0(12222>>=+b a b y a x 的左右顶点分别为)0,2(),0,2(B A -,离心率23=e .(1)求椭圆的方程;(2)若点C 为曲线E :422=+y x 上任一点(C 点不同于B A ,),直线AC 与直线2=x 交于点R ,D 为线段RB 的中点,试判断直线CD 与曲线E 的位置关系,并证明你的结论.21.(本小题满分14分)已知函数).(ln )(R a x ax x f ∈+=(1)若2=a ,求曲线)(x f y =在1=x 处的切线方程; (2)求)(x f 的单调区间;(3)设22)(2+-=x x x g ,若对任意),0(1+∞∈x ,均存在]1,0[2∈x ,使得)()(21x g x f <,求a 的取值范围.广东省惠州市2014届高三4月模拟考试文科数学答案 2014.04一. 选择题题号 1 2 3 4 5 6 7 8 9 10 答案A DB B DC A A C D1.【解析】选A ,.303-≥≥+x x 可得 2.【解析】选D ,)13,0(2=+b a . 3.【解析】选B ,12020)2)(1(021≤<-⇔⎩⎨⎧≠+≥+-⇔≥+-x x x x x x.4.【解析】选B ,.2=Z 两边同时取模可得5.【解析】选D, 由三视图还原几何体可知11111326V ⨯=⨯⨯=.6.【解析】选C , 设3ln )(-+=x x x f ,当连续函数.,0)(0)()()()上有解在(时,满足b a x f b f a f x f =<7.【解析】选A ,8,4102,610102020102==+--=>>⎪⎩⎪⎨⎧->->->-m m m c m m m m m 由得8.【解析】选A ,有面面平行的性质可知A 正确.9.【解析】选C,相邻两项依次结合可得:0,81577,5,3151061515106=++∴=+-=+-=-=-=S S S a S S S 10. 【解析】选D ,[)..1-13),322sin(6)32sin(D q y p x y x y x 所以错误的命题为假上不单调,故,的图像可知其在由函数假;不是偶函数,故得到向左平移∞+-=+=+=πππ 二.填空题 11.1- 12. 127 13.649π14. 22a ≤( 或[2 ) 15. 211.【解析】,11 1.y x u u y u =+-≤≤为斜率为的平行直线系在轴上的截距,由数形结合可知 12.【解析】连续递推可得.12763==a a 输出时,再一次进入循环, 13.【解析】设两条直角边长为,a b ,222213()013944,(),0141164a a b p b ππ<<⎧+<==⎨<<⨯⎩由已知可知构造面积模型:子事件为所以其概率 14.【解析】化为普通方程后,圆心到直线的距离小于或等于圆的半径(r d ≤),解不等式即可.15.【解析】由割线定理可得,2PA PB PC PD PC ⋅=⋅=得G M AFBCD EN三.解答题16. (本小题满分12分) 解:(1)2213()cossincos()6666224f x πππ+=+=+⨯=…………………2分 (2) 21cos 21()cos sin cos sin 22x f x x x x x +=+=+ …………4分111(sin 2cos 2))22224x x x π=++=++ ……………………6分1())2422124f πππαα+=+++ ……………………8分111)(sin )2322πααα=++=++ …………10分 因为3sin 5α=,且(,)2παπ∈,所以4cos 5α=- ………11分所以1134()()242255f πα+=+⨯-=………12分 17.(本小题满分12分)解:(1)80.240s ==,10.10.30.250.15t s =----=. …………4分 (2)设应抽取x 名第一组的学生,则20440x =20,440x =得2x =. 故应抽取2名第一组的学生. …………6分(3)在(2)的条件下应抽取2名第一组的学生,记第一组中2名男生为12,a a ,2名女生为12,b b . 按时间用分层抽样的方法抽取2名第一组的学生共有6种结果,列举如下:121112212212,,,,,a a a b a b a b a b b b . ……………9分其中既有男生又有女生被抽中的有11122122,,,a b a b a b a b 这4种结果, ……10分 所以既有男生又有女生被抽中的概率为4263P ==.…………12分 18.(本小题满分14分)(1)证明:取EC 中点N ,连结BN MN ,. 在△EDC 中,,M N 分别为,EC ED 的中点,所以MN ∥CD ,且12MN CD =.由已知AB ∥CD ,12AB CD =,所以MN ∥AB ,且MN AB =. …………………………3分所以四边形ABNM 为平行四边形.所以BN ∥AM . …………………………4分 又因为⊂BN 平面BEC ,且⊄AM 平面BEC ,所以AM ∥平面BEC . ………………………5分 (2)在正方形ADEF 中,ED AD ⊥.又因为平面ADEF ⊥平面ABCD ,且平面ADEF 平面ABCD AD =,所以⊥ED 平面ABCD .所以ED BC ⊥. ………………………7分 在直角梯形ABCD 中,1==AD AB ,2=CD ,可得2=BC .在△BCD 中,2,2===CD BC BD , 所以222CD BC BD =+.所以BC BD ⊥. …………………………8分 所以BC ⊥平面BDE . …………………………10分(3)解法一:因为BC ⊂平面BCE , 所以平面BDE ⊥平面BEC . …………11分 过点D 作EB 的垂线交EB 于点G ,则⊥DG 平面BEC所以点D 到平面BEC 的距离等于线段DG 的长度 ………………………12分 在直角三角形BDE 中,DG BE DE BD S BDE ⋅=⋅=∆2121 所以3632==⋅=BE DE BD DG 所以点D 到平面BEC 的距离等于36. ………………………14分 解法二:BE ⊂平面BDE ,所以BC BE ⊥ 所以,1222121=⋅⋅=⋅=∆BC BD S BCD .26322121=⋅⋅=⋅=∆BC BE S BCE ………………………12分 又BCE D BCD E V V --=,设点D 到平面BEC 的距离为.h 则⋅=⋅∆3131DE S BCD h S BCE ⋅∆,所以 36261==⋅=∆∆BCE BCD S DE S h 所以点D 到平面BEC 的距离等于36. ………………………14分 19. (本小题满分14分)解析: (1)n s s -=d ∴===数列公差……………1分(1)n =-=, ……………2分 23n s n =即 …………………………………………3分 163(2)n n n a s s n n -∴=-=-≥………………………………………4分1n =当时,上式也成立*63()n a n n N ∴=-∈……………6分(2)111,n n nb a a +是的等比中项, 111(63)(63)n n n b a a n n +∴==-+ …………………………………7分 111()66363n n =--+ …………………………………9分 1111111()()...()6399156363n T n n ⎡⎤=-+-++-⎢⎥-+⎣⎦……………11分 111()6363n =-+ ……………………………………13分 9(21)nn =+ ………………………………………14分20.(本小题满分14分)解析:(1)由题意可得2a =,c e a==, ∴ c = …………2分 ∴2221b a c =-=, …………………3分所以椭圆的方程为2214x y +=. …………………4分 (2)曲线E 是以(0,0)O 为圆心,半径为2的圆。
广东省惠州市高考理综-化学4月模拟考试试卷
广东省惠州市高考理综-化学4月模拟考试试卷姓名:________ 班级:________ 成绩:________一、单选题 (共7题;共14分)1. (2分)(2011·铁岭) 生产、生活离不开各种化学物质,下列说法正确的是()A . 纳米材料是指一种称为“纳米”的新物质制成的材料B . 光导纤维是由高纯度的硅制成的通信材料C . 王水是浓硝酸和浓盐酸的混合物D . 绿色食品是指不含任何化学物质的食品2. (2分) (2015高二上·宁波开学考) 下列有关实验的选项正确的是()A.配制0.10mol•L﹣1NaOH溶液B.除去CO中的CO2C.苯萃取碘水中I2 ,分出水层后的操作D.记录滴定终点读数为12.20mLA . AB . BC . CD . D3. (2分)下列有机化合物分子中,所有碳原子一定处于同一平面的是()A .B .C .D . HC≡C﹣CH2﹣CH34. (2分) (2018高一下·嘉定期中) 下列气体中,既不能用浓硫酸干燥,也不能用碱石灰干燥的是()A . NH3B . H2SC . SO2D . H25. (2分) (2016高二上·承德期中) 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是()A . 两烧杯中铜片表面均无气泡产生B . 两烧杯中溶液的pH均增大C . 甲中铜片是正极,乙中铜片是负极D . 产生气泡的速度甲比乙慢6. (2分) (2016高一下·安阳期中) 下列物质的性质递变规律正确的是()A . O,S,Na的原子半径依次增大B . LiOH,KOH,CsOH的碱性依次减弱C . H2CO3的酸性比H3BO3的酸性弱D . Cl﹣, Br﹣, I﹣的还原性依次减弱7. (2分)(2020·梅县模拟) 已知电解质溶液电导率越大导电能力越强。
常温下用溶液分别滴定10.00mL浓度均为的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。
惠州市高三第三次调研考试化学试题和参考答案

2014惠州高三第三次调研考试化学试题和参考答案(7-12单选题,22-23双选题)7.下列说法中,不正确的是A.NH3的水溶液可以导电,说明NH3是电解质B.明矾水解形成的Al(OH)3胶体有吸附性,可用于水的净化C.二氧化硅可用于制造光导纤维D.向淀粉KI溶液中加入溴水,溶液变蓝色,说明Br2的氧化性强于I28. 下列实验不能达到预期目的的是A.用饱和NaHCO3溶液除去CO2中少量的HClB.用醋和澄清石灰水验证蛋壳中含有碳酸盐C. 在试管中煮沸液体时,加碎瓷片可以防止暴沸D. 用硝酸酸化的氯化钡溶液检验某溶液中是否含有SO42-9. 下列有关说法不正确的是A.干馏煤可以得到甲烷、苯和煤焦油等重要化工原料B.淀粉、纤维素和脂肪在一定条件下都可发生水解反应C.用大米酿的酒在一定条件下密封保存,时间越长越香醇D.“乙醇汽油”是在汽油中加入乙醇生成的一种新化合物10 .下列离子方程式中正确的是A.碳酸钙溶于醋酸:CaCO3 + 2H+=Ca2+ + CO2 + H2OB.Fe3O4溶于稀盐酸:Fe3O4 + 8H+=3Fe3+ + 4H2OC.用烧碱溶液吸收氯气:Cl2 + 2OH-= Cl-+ ClO-+ H2OD.向硫酸亚铁溶液中加入用硫酸酸化的H2O2溶液Fe2++ 2H+ + H2O2=Fe3+ + 4H2O11. 相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应,二者相比较,相等的是A.铜片完全消耗时所需要的时间B.反应中转移的电子总数C.反应所消耗硝酸的物质的量D.反应生成气体的体积(标准状况)12.用如图装置实验,下列叙述不正确的是A.K与N连接时,组成原电池装置B.K与N连接时,石墨电极产生气泡C.K与M连接时,一段时间后溶液的pH变小D.K与M连接时,石墨电极反应为:2 Cl-- 2e- = Cl2↑22. 常温下,Na2CO3溶液中有:CO32-+H2O HCO3-+OH-,下列说法正确的是A.Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(H+)B.加入NaOH固体,溶液pH减小C.Na2CO3溶液中:c(Na+)+ c(H+) =2c(CO32-)+c(OH-)D.升高温度,平衡向正反应方向移动23. 据下表信息,判断以下叙述正确的是A.GOH溶液和M(OH)3可以相互反应B.非金属性:T<QC.气态氢化物的稳定性:R >T D.L2+与T2-的核外电子数相等30.(16分)化合物Ⅴ是具有抗氧化和抗肿瘤作用的药物成分。
广东省惠州市2014届高三4月模拟考试语文试题(WORD版)

广东省惠州市2014届高三高考模拟试题语文一、本大题4小题,每小题3分,共12分。
1.下列词语中加点的字,每对读音都不相同....的一组是A.鏖.战/麇.集安抚./果脯.萎靡./奢靡.B.悖.逆/蓬勃.麦茬./检查.兴.奋/高兴.C.巨擘./玉璧.惆怅./倜傥.应.承/呼应.D.颦.蹙/濒.临嗔.怪/称.呼俭省./反省.2.指出下面一段话中用词不当的一项城市管理涉及面广,从空中到地下,有些是宏大构建,比如摩天大楼,有些则具体而微....,比如地下管线。
事无巨细....才不影响人们正常的生产生活。
可是,现实中,....,应该管得滴水不漏管得一塌糊涂或者监管真空..的情况占了不少。
A.具体而微 B.事无巨细 C.滴水不漏 D.真空3.指出下面句子没有语病的一项A.美国新任国务卿就职后首次对民众公开演讲时,将吉尔吉斯斯坦和哈萨克斯坦两个国家合并到一起,读成了“吉尔萨克斯坦”,令人贻笑大方。
B.什么是幸福?这个在田园农耕时代似乎很易寻得的答案,在当代繁复的经济、社会和文化背景下,却显得日益模糊和多元。
C.嗜甜的饮食习惯会加速锌的流失,而锌就是怂恿味觉逃亡的主犯。
这样一来,在不断的恶性循环中,重口味日渐加剧。
D.与泰戈尔不同,鲁迅的散文诗中的哲理不是追求宗教式的光明、和谐,而是充满了对人生、对自我的无情的严酷的解剖,对人心黑暗的正视和孤独的战斗的坚持。
4.在文中横线处填入下列语句,衔接最恰当的一项是在李商隐以前,诗人运用典故,___,不会句句都用典故。
而且一般的用典故,都是明用,读者看得出,这一句中包含着一个典故。
只要注明典故,___。
但是,李商隐的诗,___,即使都注明白了,诗意还是不易了解。
因为在运用典故的艺术手法上,他也有所独创。
他在诗中运用典故,___。
___,常常不是李商隐企图在他的诗中所显示的意义。
①诗意也就明白了②典故本身所代表的意义③常常是暗用、借用或活用④往往是逐句都用典故⑤不过偶尔用一二处A.⑤①④③② B.③①②④⑤ C.③②④①⑤ D.⑤①②④③二、本大题7小题,共35分。
广东省惠州市2014届高三4月模拟考试理综试题及参考答案(不全)

广东省惠州市2014届高三4月模拟考试理科综合化学试题7. 下列有关物质的性质与应用不相对应的是A.明矾能水解生成Al(OH)3胶体,可用作净水剂B.FeCl3溶液能与Cu反应,可用于腐蚀铜制印刷电路C.SO2具有氧化性,可用于漂白纸浆D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料8. 下列有关物质的性质和应用正确的是A.油脂在酸性条件下水解生成高级脂肪酸和甘油B.福尔马林可防腐,可用它保存海鲜产品C.乙醇、糖类和蛋白质都是人体必需的营养物质D.合成橡胶与光导纤维都属于有机高分子材料9. 北大和中科院已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。
有关分析正确的是A. K3C60中只有离子键B. K3C60中碳元素显-3价C. 该晶体在熔融状态下能导电D. 该晶体熔点较低10.下列各组离子,在碱性条件下能大量共存,在强酸性条件下发生氧化还原反应的是A.Mg2+、Na+、SO42-、HCO3—B.Na+、K+、NO3—、SO32—C.K+、Na+、SiO32—、ClO—D.NH4+、Na+、SO42—、NO3—11.甲醇、氧气和强碱溶液做电解质的手机电池中的反应为:2CH3OH+3O2+4OH-2CO32-+6H2O,有关说法正确的是A.放电时,CH3OH参与反应的电极为正极B.放电时,负极电极反应:CH3OH+8OH--6e- =CO32-+6H2OC.标况下,通入11.2LO2完全反应有1mol电子转移D.充电时电解质溶液的pH逐渐减小12. 设N A为阿伏加德罗常数的值,下列叙述正确的是A.标况下,11.2L乙烷中含有共价键的数目为3N AB.标况下,22.4LO2和CO2组成的混合物中含有氧原子数为2N AC.常温下,22.4L甲烷中含有的电子数为10N AD.常温下,1 L 0.1mol·L-1的Na2CO3溶液中含OH-离子数为0.1N A22.下列说法不正确的是A.NaHCO3和Na2CO3混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO-3) +2c(CO2-3) B.常温下,浓度均为0.1 mol·L-1下列各溶液的pH:NaOH>Na2CO3> NaHCO3> NH4Cl C.向冰醋酸中逐滴加水,醋酸的电离程度、pH均先增大后减小D.常温下,pH=1的稀硫酸与醋酸溶液中,c (SO42-)与c(CH3COO-)之比为2∶123.短周期元素X、Y、Z、W在周期表中的相对位置如图,W原子的最外层电子数是其最内层电子数的3倍。
惠州市2014届高三第三次调研考试(化学答案)
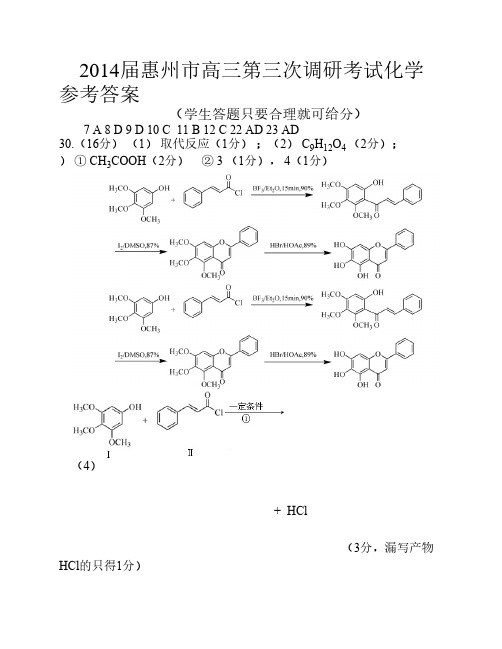
2014届惠州市高三第三次调研考试化学参考答案(学生答题只要合理就可给分)7 A 8 D 9 D 10 C 11 B 12 C 22 AD 23 AD30.(16分)(1)取代反应(1分);(2) C9H12O4 (2分);(3)① CH3COOH(2分)② 3 (1分), 4(1分)(4)+ HCl(3分,漏写产物HCl的只得1分)(5)CD ( 全对得4分,选一个对的得2分)(6)( 2分,合理的可给分)31、(16分)(1)、10-3 (2分);(2)、c2NO2/ c N2O4(或0.122/0.04)(2分),<(2分)(3)、A (4分)(4)、B(3分)(5)、-1079.6(3分,未写“-”号扣1分)32.(16分)(1)第五周期(1分);(2)蒸发浓缩、冷却结晶(2分);(3)抑制Sn2+ 的水解(2分);(4)防止Sn2+ 被氧化(2分);(5)Sn Cl2 + Na2CO3= SnO↓+ CO2↑+ 2NaCl(3分,未写↓和↑符号共扣1分,未配平扣1分)(6)Sn2+ + H2O2 +2H+ = Sn4 + + 2H2O (3分,未配平扣1分)(7)③ 6 1 14 6 2 2 7 H2O(3分,化学式H2O给1分,系数全对2分)33、(1)SO32- + Br2 + 2 OH- = H2O + SO42- + 2Br- (3分,未配平扣1分)(2)(8分)实验操作预期现象与结论步骤②方法1:取少量步骤①中上层清液于试管中,加入少量氯水,观察溶液的颜色。
(2分)(若再加入CCl4,振荡,静置观察颜色也可)溶液呈橙黄色,证明待测液中含Br-。
(2分)(下层液体呈橙红色,证明待测液中含Br-。
)方法2:另取少量待测液于试管中,加入足量的2 mol·L-1盐酸直到不产生气泡为止,再加入少量氯水,观察溶液的颜色。
(2溶液呈橙黄色,证明待测液中含Br-。
(2分)(下层液体呈橙红色,证明待测液中含Br-。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
广东省惠州市2014届高三4月模拟考试理科综合化学试题7. 下列有关物质的性质与应用不相对应的是A.明矾能水解生成Al(OH)3胶体,可用作净水剂B.FeCl3溶液能与Cu反应,可用于腐蚀铜制印刷电路C.SO2具有氧化性,可用于漂白纸浆D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料8. 下列有关物质的性质和应用正确的是A.油脂在酸性条件下水解生成高级脂肪酸和甘油B.福尔马林可防腐,可用它保存海鲜产品C.乙醇、糖类和蛋白质都是人体必需的营养物质D.合成橡胶与光导纤维都属于有机高分子材料9. 北大和中科院已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。
有关分析正确的是A. K3C60中只有离子键B. K3C60中碳元素显-3价C. 该晶体在熔融状态下能导电D. 该晶体熔点较低10.下列各组离子,在碱性条件下能大量共存,在强酸性条件下发生氧化还原反应的是A.Mg2+、Na+、SO42-、HCO3—B.Na+、K+、NO3—、SO32—C.K+、Na+、SiO32—、ClO—D.NH4+、Na+、SO42—、NO3—11.甲醇、氧气和强碱溶液做电解质的手机电池中的反应为:2CH3OH+3O2+4OH-2CO32-+6H2O,有关说法正确的是A.放电时,CH3OH参与反应的电极为正极B.放电时,负极电极反应:CH3OH+8OH--6e- =CO32-+6H2OC.标况下,通入11.2LO2完全反应有1mol电子转移D.充电时电解质溶液的pH逐渐减小12. 设N A为阿伏加德罗常数的值,下列叙述正确的是A.标况下,11.2L乙烷中含有共价键的数目为3N AB.标况下,22.4LO2和CO2组成的混合物中含有氧原子数为2N AC.常温下,22.4L甲烷中含有的电子数为10N AD.常温下,1 L 0.1mol·L-1的Na2CO3溶液中含OH-离子数为0.1N A22.下列说法不正确的是A.NaHCO3和Na2CO3混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HCO-3) +2c(CO2-3) B.常温下,浓度均为0.1 mol·L-1下列各溶液的pH:NaOH>Na2CO3> NaHCO3> NH4Cl C.向冰醋酸中逐滴加水,醋酸的电离程度、pH均先增大后减小D.常温下,pH=1的稀硫酸与醋酸溶液中,c (SO42-)与c(CH3COO-)之比为2∶123.短周期元素X、Y、Z、W在周期表中的相对位置如图,W原子的最外层电子数是其最内层电子数的3倍。
下列判断正确的是A .原子半径:X >Y >Z >WB .含Y 元素的盐溶液有的显酸性,有的显碱性C .最简单气态氢化物的热稳定性:Z >WD .X 的氢化物能与其最高价氧化物对应的水化物反应生成盐30. (16分)中学化学常见有机物A (C 6H 6O )能合成紫外线吸收剂BAD 和某药物中间体F ,合成路线为:已知:BAD 的结构简式为:F 的结构简式为:(1)C 中含氧官能团的名称 ,W 的结构简式 。
(2)反应类型 A →B 。
(3)1mol C 充分反应可以消耗 mol Br 2 ;C 和过量 NaOH 溶液反应的化学方程式 。
(4)C →D 的过程中可能有另一种产物D 1,D 1的结构简式 。
(5)E 的结构简式为 。
反应类型 E →F 。
(6)W 的同分异构体有多种,写出一种符合以下要求的W 的同分异构体的结构简式: ① 遇FeCl 3溶液呈紫色; ② 能发生银镜反应;③ 苯环上的一氯代物只有两种。
。
31.(16分)氨的合成是最重要的化工生产之一。
I .工业上合成氨用的H 2有多种制取的方法:① 用焦炭跟水反应: C(s) + H 2O(g)CO(g) + H 2(g);② 用天然气跟水蒸气反应:CH 4(g) + H 2O(g) ========高温催化剂CO (g)+ 3H 2(g) 已知有关反应的能量变化如下图,则方法②中反应的ΔH =_____________。
Ⅱ.在3个1L 的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H 2(g) + N 2(g) 高温高压催化剂2NH 3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:(1) 下列能说明该反应已达到平衡状态的是a .容器内N 2、H 2、NH 3的浓度之比为1︰3︰2b .v (N 2)正=3v (H 2)逆c .容器内压强保持不变d .混合气体的密度保持不变(2) 甲容器中达到平衡所需要的时间t 5min (填>、< 或=)(3) 乙中从反应开始到平衡时N 2的平均反应速率 (注明单位)。
(4) 分析上表数据,下列关系正确的是________.a .2c 1 =3mol/Lb .ω1 = ω2c . 2ρ1 = ρ2(5) 该温度下,容器乙中,该反应的平衡常数K =____ __(用分数表示)(mol/L )-2。
32.(16分)铬铁矿的主要成分的化学式为FeO ·Cr 2O 3,还含有SiO 2、Al 2O 3等杂质。
工业上常采用固体碱熔氧化法用铬铁矿粉制备重铬酸钾,流程为:已知:① NaFeO 2遇水强烈水解;② 重铬酸钾为橙红色针状晶体,溶于水,不溶于乙醇,有强氧化性;③2CrO42-+ 2H+Cr2O72-+ H2O(1)灼烧操作一般在坩埚中进行,下列物质适合用来制作此实验坩埚材料的是A. 铁B. 氧化铝C. 石英D. 陶瓷(2)①铬铁矿经粉碎处理的目的是。
②写出Cr2O3和纯碱、氧气反应生成Na2CrO4的化学方程式为;③NaFeO2水浸时强烈水解生成氢氧化铁沉淀,离子方程式为___ ___。
(3)滤液1的成分除Na2CrO4、NaOH外,还含有(填化学式),(4)通过途径I从Na2CrO4溶液获得K2Cr2O7晶体,操作步骤有:“酸化”→加KCl固体→蒸发浓缩→操作a→过滤→洗涤→干燥。
①②操作a的名称。
33. (16分)牙膏中的摩擦剂一般由CaCO3、Al(OH)3或SiO2组成。
某小组对几种牙膏中摩擦剂成分及其含量进行探究:(1)根据上述信息,推测摩擦剂应具备的性质有A. 易溶于水B. 难溶于水C. 颗粒较大D.颗粒较小(2)已知A牌牙膏的摩擦剂是Al(OH)3,取少量牙膏样品,加水充分搅拌、过滤:①往滤渣中加入过量NaOH溶液,Al(OH)3与NaOH溶液反应的离子方程式____ __。
②往①所得滤液先通入过量CO2,再加入过量稀盐酸,观察到的现象是。
(3)已知B牌牙膏中摩擦剂可能含有一或两种物质,将此牙膏的摩擦剂溶于盐酸时,发现有不溶性物质。
①对B品牌牙膏摩擦剂的成分提出合理假设:假设1:只有SiO2假设2:可能有SiO2和CaCO3假设3:可能有________________。
②请设计方案对B品牌牙膏摩擦剂的成分进行验证。
填写下表。
限选..试剂:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水(4)已知C牌牙膏中的摩擦剂为CaCO3,为测定CaCO3的质量分数,取20.0g牙膏样品溶于水后过滤,将所得沉淀溶于100mL1mol/L的盐酸(假设所得溶液体积不变),从所得的溶液中取20.00mL,用1mol/L NaOH溶液进行滴定,消耗NaOH溶液5.00mL,则C品牌牙膏中CaCO3的质量分数为_(保留四位有效数字)。
.理科综合化学参考答案7. C 8. A 9. C 10. B 11. B 12.B 22. CD 23. BD(第30-33题中的解答只要合理即可给分)30.(16分)(1)羧基、羟基(2分)(2分);(2)加成反应(1分)(3)3 mol(1分)+ 2 NaOH →2 H2O+(3分,未配平扣1分)(4)(2分)(5)(2分);取代反应(或酯化反应)(1分)(6)(2分,写出其中一种即可)31.(16分)I.ΔH =(a+3b-c)( 3分)Ⅱ.(1) c(3分);(2) t > 5 (2分);(3) 0.2 mol·L-1·min-1(2分,数据1分,单位1分)(4) c(3分);(5) K= 4/81(3分)32.(16分)(1) A ( 3分)(2)①增大反应物的表面积,加快反应速率(2分)②2Cr2O3 + 3O2+4Na2CO3 4Na2CrO4+4CO2↑(3分,未配平扣1分)③FeO2-+2H2O=Fe(OH)3↓+OH-(3分,未配平扣1分)(3)Na [Al(OH)4](或NaAlO2 )、Na2SiO3(2分)(4)①使2CrO42-+ 2H+Cr2O72-+ H2O 的平衡向正反应方向移动,尽量将CrO2-转化为Cr2O72-(2分)4②冷却结晶(1分,只写冷却或只写结晶不得分)33.(16分)(1)B D(3分,选1个对的得1分,全对3分)(2)①Al(OH)3+OH-=AlO2-+2H2O(3分,未配平扣1分)(或Al(OH)3+OH-=[Al(OH)4]-)②通入CO2气体有白色沉淀生成;加入盐酸有气体生成、沉淀溶解;(2分)(或:通入CO2气体有白色沉淀生成;加入盐酸沉淀溶解)(3)①SiO2和Al(OH)3(或二氧化硅和氢氧化铝)(1分,少一种不得分)②(4分)(4)18.75% (或0.1875)( 3分)。
