第一节 晶体的常识(第1课时)
选修二3.1.1晶体的常识
第一节 晶体的常识 第一课时
物质的聚集状态
物质的三态变化是物理变化,变化时克服分子间作用力或破坏 化学键,但不会有新的化学键形成。
固态
凝固
凝华
(放热)
(放热)
融化 升华
(吸热)(吸热)
液态
气化 (吸热) 气态
液化 (放热)
物质的聚集状态
物质的聚集状态
气态 等离子体
通常物质有三种存在状态,这
课堂练习4:计算下列晶胞中原子数目,确定化学式。
晶胞1 X:6/12=1/2 化学式:
Y:6/4+3/6=2 Z:1
X2ZY4
晶胞2
Mg:12/6+2/2=3 B:(在体内) 6
化学式: MgB2
课堂练习5:科学家发现了一种由钛原子和碳 原子构成的气态团簇分子。如图所示,顶角和 面心的原子是钛原子,棱的中心和体心的原子
Cl-数=8×
1 8
+6 × 12=4
一个晶胞含4个NaCl
氯化钠的化学式为NaCl
应用:根据晶胞确定化学式。
思考与讨论:
(1)晶胞有几套平行棱?有几套平行面? 晶胞有三套各4根平行棱,有3套各两个平行面
(2)数一数,它们分别平均含有几个原子?
金属钠(Na)
1+8 1 =2 8
金属锌(Zn)
1+8 1 =2 8
外层冷却快,内层冷却慢;晶体生长速率适当 是保持自范性的条件之一。
晶体自范性的条件之一是生长的速率适当 玛瑙
水晶
天然水晶球里的玛瑙和水晶
玛瑙是熔融态SiO2快速冷却形成——没有规则外形 水晶是熔融态SiO2缓慢冷却形成——有规则外形 思考:除了冷却的方法,还有没有其它途径得到晶体 内部:1
第一节-晶体的常识

(3)晶体具有固定的熔点
二、晶胞
1.晶胞:描述晶体结构的基本单元 2.晶胞的结构
晶胞都是平行六面体,上下左右前后无隙 并置排列着无数晶胞。
3.确定晶胞化学式的方法——均摊法
顶点占1/8
面占1/2
棱占1/4
氯化钠晶体
一个Na+吸引多少个 Cl- ? 6个
一个Cl-吸引多少个 Na+ ? 6个 NaCl晶体中Na+ 与Cl-的离 子个数比为多少?︰1 1 与Na+等距离且距离最近的Na+为多少个? 12个
与Cl-等距离且距离最近的Cl-为多少个? 12个
二氧化碳结构模型
与二氧化碳距离最近且等距离的二氧化碳 有多少个? 12个
第一节 晶体的常识
一、晶体与非晶体
1.晶体与非晶体的本质差异 自范性 晶体 有(能自发呈现多 面体外形) 没有(不能自发呈 现多面体外形)
具有规则的几何外 形的固体叫晶体
微观结构 原子在三维空间 里呈周期性有序 排列 原子排列相对无 序
非晶 体
2.晶体呈现自范性的条件
晶体生长的速率适当Fra bibliotek3.得到晶体的一般条件
(1)熔融态物质凝固
固体粉末仍是晶体, 只因晶粒太小,肉眼 看不到而已
(2)气体物质凝华
(3)溶质从溶液中析出
4.晶体的特点
(1)晶体的外形和内部质点排列高度有序
晶体SiO2与非晶体SiO2的投影示意图
(2)晶体具有各向异性
在晶体中,不同晶面和晶面上原子排列的方式不 同和密度不同,它们之间结合力的大小也不相同, 这种性质叫做晶体的各向异性
晶体的常识第一课时

Cu晶体结构示意图
3.晶体的特性:
(1)自范性:晶体能自发地呈现多面体外形的性质, (2)各向异性, 如强度、导热性、导电性、光学性质等,同样 反映了晶体内部粒子排列的有序性。
(3)晶体具有固定的熔点,非晶体没有确定的熔点。
(4)晶体具有均一性:晶体的化学组成、密度等性质在晶体 中各部分都是相同的。 (5)晶体具有对称性:晶体的外形和内部结构都具有特 有的对称性,在外形上,常有相等的晶面、晶棱和顶角 重复出现。
猫 眼 石
猫眼石又称东方猫眼,是珠宝中稀有而名贵的品种。由于猫眼石表
现出的光现象与猫的眼睛一样,灵活明亮,能够随着光线的强弱而变化, 因此而得名。这种光学效应,称为“猫眼效应”。 具有猫眼效应的宝石很多。宝石学界把具有猫眼效应的金绿宝石称之 为猫眼石,一般所说的猫眼石指的是金绿猫眼宝石,而其它具有猫眼效应 的宝石,必须在“猫眼”二字之前加上宝石的名称,如海蓝宝石猫眼、电 气石猫眼等。
晶体自范性的条件之一是生长速率适当
天然水晶球里的玛瑙和水晶 思考: 得到晶体的途径,除了冷却的方法,还有没有 其它途径?你能列举哪些?
4. 晶体形成的途径
(1)熔融态物质凝固
(2)气态物质冷却不经液态直接凝固(凝华)
(3)溶质从溶液中析出
学与问
1.某同学在网站上找到一张玻璃的结构示意图,如右 图,这张图说明玻璃是不是晶体?为什么?
第一课时
水 晶 石
紫水晶
紫水晶(amethyst)是一种宝石,水晶的一种,呈紫色,一般被
用于装饰之用。摩氏硬度7级,成分以二氧化硅为主,其紫色早期认为是 由于含锰所造成的,其晶体加热后会呈黄色。最早在古埃及时代即被用作 装饰宝石之用,在中古欧洲仅有教皇或大主教才能配戴。
高中化学第三章第一节晶体的常识第一课时新人教版选修3
"四川省德阳五中高中化学第三章-第一节-晶体的常识-第一课时新人教版选修3 "课题晶体的常识(第一课时)课型新知识课授课人授课班级教材分析学生分析本节内容是安排在原子结构、分子结构以及结构决定性质的内容之后来学习,对于学生的学习有一定的理论基础。
结合前两章已学过的有关物质结构知识,学生能够比较全面地认识物质的结构及结构对物质性质的影响,提高分析问题和解决问题的能力。
运用观察、分析、对比、讨论等教学策略引导学生自主学习,让学生主动参与学习活动。
教学目标【知识与技能】(1)知道获得晶体的几种途径(2)理解晶体的特点和性质及晶体与非晶体的本质区别【过程与方法】(1)收集生活素材,结合已有知识和生活经验对晶体与非晶体进行分类(2)学生通过观察、实验等方法获取信息(3)学会运用比较、分类、归纳、概括等方法对获取的信息进行加工【情感态度与价值观】(1)培养学生科学探究的方法(2)培养学生的动手能力、观察能力、自主学习的能力,保持对生活中化学的好奇心和探知欲,增强学生学习化学的兴趣。
教学重点1、晶体与非晶体的区别2、晶体的特征教学难点晶体与非晶体的区别教学媒体多媒体教学策略观察、分析、对比、讨论教学过程学习任务教师活动学生活动设计意图板块1:引出晶体与非晶体的概念任务1.1:认识晶体与非晶体板块2:晶体的特点之一:自范性任务2.1:掌握“自范性”和“自范性条件”板块3:晶体的形成途径任务3.1:途径之一:凝固任务3.2:途径之二:凝华任务3.3:途径之三:结晶板块4:晶体的其他特点任务4.1:微观世界去探究一下晶体的微观结构任务4.2:其他的物理性质任务4.3:介绍X—射线衍射实验板块5:新课导入上课前,我已经请同学们收集了一些身边的固体物质,大家都带来了吗?你们都带来了哪些固体呢?同学们带来的固体物质可真是琳琅满目啊!但是,我们每个人可能只带了几样,想知道别人收集了哪些固体物质吗?指导学生分类请前后四个同学组成一个小组,然后互相交流一下收集的各种固体物质,并讨论如何将这些固体物质进行分类呢?教师进行巡视提问你们为什么会这样分呢?总结同学收集的物品很丰富,并通过组内讨论确定了分类依据,然后进行了恰当的分类。
《第一节 晶体的常识》PPT课件第一课时)
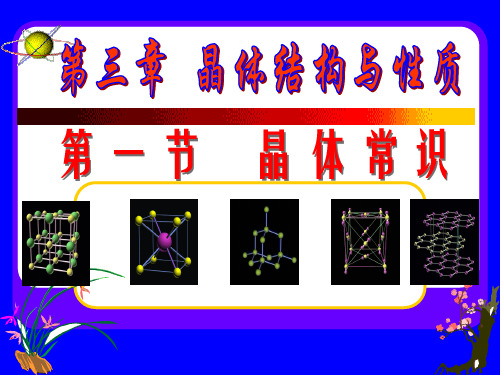
看图写化学式 C
B A
A:B:C=1:1:3
练习1:根据离子晶体的晶胞结构,判断下列 离子晶体的化学式:(A表示阳离子)
A
B
化学式: AB
练习2:根据离子晶体的晶胞结构,判断下 列离子晶体的化学式:(A表示阳离子)
A B
化学式: A2B
练习4:根据离子晶体的晶胞结构,判断下 列离子晶体的化学式:(A表示阳离子)
1、定义:晶体——具有规则几何外形的固体 非晶体——没有规则几何外形的固体 又称玻璃体 2、分类 思考
晶体
离子晶体 原子晶体 分子晶体 金属晶体
为什么晶体呈现规则 的几何外形,而非晶体 没有规则的几何外形呢? 你认为可能和什么因素 有关?
3、晶体与非晶体的本质差异
自范性 微观结构 原子在三维空间里 呈周期性有序排列 原子排列相对无序
经不同途径得到的晶体
(见教材P61图3~2)
4、晶体形成的途径
(1)熔融态物质凝固 (2)气态物质冷却不经液态直接凝固(凝华)
(3)溶质从溶液中析出
--
许多固体粉末用肉眼看不到晶体外形,但在光 学显微镜下可观察到规则的晶体外形
那么怎样判断固体是晶体还是非晶体呢?
5、晶体的特性
<1>.有规则的几何外形 (晶体内部质点和外形质点排列的高度有序性) <2> .有固定的熔沸点 <3> .各向异性(强度、导热性、光学性质等) <4>.当一波长的x-射线通过晶体时,会在记录仪上 看到分立的斑点或者普线. (教材63页图3-6)
雪 花
冰糖
金刚石
石墨
水晶石
观察图片,下列固体在外形上有什么区别?
明 矾
雪 花
《晶体的常识》完美课件1

• 自范性
有
无
•熔 点
固定 不固定
• 各向异性
有
无
• X-衍射(粉末)明锐线条 漫峰
人教版高中化学选修三第三章第一节 晶体的常识
2. 晶体自范性的条件之一:生长速率适当 3.晶体形成的途径: ①熔融态物质凝固. ②气态物质冷却不经液态直接凝固(凝华). ③溶质从溶液中析出.
1.下列关于晶体与非晶体的说法正
人教版高中化学选修三第三章第一节 晶体的常识
3.晶体形成的途径
• 熔融态物质凝固. • 气态物质冷却不经液态直接凝固(凝华). • 溶质从溶液中析出.
人教版高中化学选修三第三章第一节 晶体的常识
人教版高中化学选修三第三章第一节 晶体的常识
• 1.石墨(C)和蓝宝石(Al2O3·SiO2)是常见的 晶体,其中石墨的结构呈层状,在与层垂直方 向的导电率为与层平行方向上导电率的 1/10000;蓝宝石在不同方向上的硬度是不 同的.
人教版高中化学选修三第三章第一节 晶体的常识
黄黄水水晶晶
人教版高中化学选修三第三章第一节 晶体的常识
人教版高中化学选修三第三章第一节 晶体的常识
NaCl晶体结构示意图:
人教版高中化学选修三第三章第一节 晶体的常识
ClNa+
人教版高中化学选修三第三章第一节 晶体的常识 人教版高中化学选修三第三章第一节 晶体的常识
人教版高中化学选修三第三章第一节 晶体的常识 人教版高中化学选修三第三章第一节 晶体的常识
人教版高中化学选修三第三章第一节 晶体的常识
1.从外形看,晶体与非晶体有何不同? 2.构成晶体的微粒在空间的排列有何特点?
晶体与非晶体比较
自范性
微观结构
晶体 有(能自发呈现多面 粒子在三维空间呈
晶体的常识优质课件1

NaCl晶体结构和晶胞
1.上述铜晶体、金刚石、CO2晶体、NaCl晶 体面的心晶立胞方的正空四间面构体形网状呈结什构么形面心状立?方 简单立方
2.在上述晶体中,晶胞是如何排列的?晶胞
之间是否存在空隙?
8/5/2020
二﹑晶胞
无隙并置
平行六 面体
2、特点:晶胞都是
平行六面体.晶胞在
晶体中“无隙并
8/5/2020
晶体的结构
一、晶体和非晶体
Cu晶 体结 构示 意图
NaCl晶 体结构 示意图
观察图片:构成晶体与非晶体的微粒在空间的排列有 何不同?
晶体内部粒子 排列的有序性
非晶体内部粒子 排列的无序性
8/5/2020
一、晶体和非晶体
3、特点和性质: (1)自范性:晶体能自发地呈现多面体外形的 性质——是晶体中粒子在微观空间里呈现周期 性有序排列的宏观表现
(2)物理性质表现各向异性(强度、导热性、 光学性质)——同样反映了晶体内部粒子排列 的有序性
(3)晶体具有固定的熔点
8/5/2020
一、晶体和非晶体
(4)规则的晶体外形 许多固体粉末用肉眼看不到晶体外形,但在 光学显微镜下可观察到规则的晶体外形
8/5/2020
一、晶体和非晶体
4、晶体自范性的条件之一是生长的速率适当
CaTiO3
8/5/2020
4、在碳单质的成员中还有一种混合型晶体 ——石墨,如图所示。它是层状结构,层与层 之间依靠作用力相结合。每层内部碳原子与碳 原子之间靠作用力相结合,其键角为120ْ。
分析图中每个六边形含有2 个碳原子。
8/5/2020
5、下列是NaCl晶胞示意图,晶胞中 Na+和Cl¯的个数比是多少?
《第一节 晶体的常识》PPT课件(部级优课)

第一课时
【观察·讨论】观察以下几种固体的外形特点?
海波
石蜡
食盐 有规则多面体外形
松香 没有规则多面体外形
【观察·交流】
观察CuSO4 ·5H2O晶体的形成过程及外形特征
【CuSO4 ·5H2O晶体的制备】:
将少量热饱和CuSO4溶液迅速倒入培养皿
观察培养皿中CuSO4溶液的变化
一、晶体与非晶体 1、晶体的形成途径
(1)溶质从溶液中析出
(2)熔融态物质凝固
(3)气态物质冷却不经液态 直接凝固(凝华)
2、晶体的特点 (1)自范性:自发呈现多面体外形的性质
第五天
第一天
第二天
第三天
玛瑙
水晶
晶体呈现自范性 的重要条件: 适当的生长速率
物质
玛瑙 水晶
冷却速率
快
慢 快 慢
石膏
晶体 有(能自发呈现多面 粒子在三维空间里呈周期
体外形)
性有序排列
非晶体 没有(不能自发呈 现多面体外形)
粒子排列相对无序
玻璃的平面透视图
NaCl晶体微观结构示意图
Cl
Na
最小重复单元 8个最小重复单元并置 18个最小重复单元并置
晶体的自范性是晶体中粒子在微观空间里 呈现周期性有序排列的宏观表象
CaCO3的微观结构示意图
Ca
C
O
正面
侧面
Байду номын сангаас顶面
【探究·交流】
1、分别旋转方解石和玻璃片, 透过方解石和玻璃片观察白纸上横线的影像变化。
2、用小刀在方解石和玻璃片沿相互垂直的方向上刻划, 感受不同方向上的硬度。
(2)各向异性: 晶体的不同方向上光学性质、硬度、 导电性、导热性等某些物理性质不同。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章 晶体结构与性质
第一节 晶体的常识(第1课时)
【教学目标】
1、通过实验探究理解晶体与非晶体的差异。
2、学会分析、归纳和总结的逻辑思维方法,提高发现问题、分析问题和解决问题的能力。
3、了解区别晶体与非晶体的方法,认识化学的实用价值,增强学习化学的兴趣。
【教学重点、难点】
1、晶体与非晶体的区别
2、晶体的特征
【教学过程】
[新课引入]:前面我们讨论过原子结构、分子结构,对于化学键的形成也有了初步的了解,
同时也知道组成千万种物质的质点可以是离子、原子或分子。
又根据物质在不同温度和压强下,物质主要分为三态:气态、液态和固态,下面我们观察一些固态物质的图片。
[讲述]:像上面这一类固体,有着自己有序的排列,我们把它们称为晶体;而像玻璃这一
类固体,本身原子排列杂乱无章,称它为非晶体,今天我们的课题就是一起来探究晶体与非晶体的有关知识。
一、晶体与非晶体
1、晶体与非晶体的概念
⑴晶体:内部粒子(原子、离子或分子)在空间按一定规律呈 构成的固
体物质,如食盐、干冰、金刚石等
⑵非晶体:内部原子或分子的排列呈 的分布状态的固体物质。
如橡胶、
玻璃、松香等
【提问】:在初中化学中,大家已学过晶体与非晶体,你知道它们之间有没有差异? 食单质硫
2、晶体的特性
⑴具有规则的几何外形――晶体的自范性
在适宜的条件下,晶体能自发的呈现的性质,称为晶体的自范性。
非晶体就没有这个特性。
晶体与非晶体的本质差异
注意:
a、晶体自范性的本质:是晶体中粒子微观空间里呈现周期性的有序排列的宏观表象.
b、自范性需要一定的条件,其中最重要的条件是晶体的生长速率适当。
⑵晶体在不同的方向上表现出不同的物理性质即
⑶晶体具有特定的
【思考】:请列举得到晶体有哪些途径?
3、晶体形成的一段途径:
(1)熔融态物质凝固;
(2)气态物质冷却不经液态直接凝固(凝华);
(3)溶质从溶液中析出。
观察教材P63页图3-2:1、从熔融态结晶出来的硫晶体;
2、凝华得到的碘晶体;
3、从硫酸铜饱和溶液中析出的硫酸铜晶体。
【探究实验】:完成教材实验3-1,请同学们认真观察,观察到什么现象?
【过渡】许多固体的粉末用肉眼是看不见晶体的,但我们可以借助于显微镜观察,这也证明固体粉末仍是晶体,只不过晶粒太小了!
观察教材P63页图3-3
【思考】:观察教材P64页图3-4晶体二氧化硅和非晶体二氧化硅的示意图。
小组讨论,通过比较,可以得出什么样结论。
【总结】晶体的三大特点:
(1)有固定的几何外形;
(2)有固定的熔沸点;
(3)有各向异性(强度、导热性、光学性质等)
例如:蓝晶石(Al2O3·SiO2)在不同方向上的硬度不同;石墨在与层垂直的方向上的导电率与层平行的方向上的导电率1∕104。
【小结】可以根据晶体特点区别某一固体属于晶体还是非晶体。
然而,得出区别晶体与非晶体最可靠的方法是利用x-射线衍射实验。
【学与问】
一些不法商人制造假宝石来牟取暴利,你能否根据晶体物理性质的各向异性的特点,列举出一些可能有效鉴别假宝石的方法?
随堂练习:
1、下列关于晶体与非晶体的说法正确的是:()
A、晶体一定比非晶体的熔点高
B、晶体有自范性但排列无序
C、非晶体无自范性而且排列无序
D、固体SiO2一定是晶体
2、区别晶体与非晶体最可靠的科学方法是:()
A、熔沸点
B、硬度
C、颜色
D、x-射线衍射实验
3、下列不属于晶体的特点是:()
A、一定有固定的几何外形
B、一定有各向异性
C、一定有固定的熔点
D、一定是无色透明的固体
4、下列过程可以得到晶体的有:()
A、对NaCl饱和溶液降温,所得到的固体
B、气态H2O冷却为液态,然后再冷却成的固态
C、熔融的KNO3冷却后所得的固体
D、将液态的玻璃冷却成所得到的固体
5、晶体具有各向异性。
如蓝晶石(Al2O3·SiO2)在不同方向上的硬度不同;又如石墨在
与层垂直的方向上的导电率与层平行的方向上的导电率1∕104。
晶体的各向异性主要表现在是:()
①硬度②导热性③导电性④光学性质
A、①③
B、②④
C、①②③
D、①②③④
6、在我们的生活中遇到许多固体,通过今天这节课的学习,我们知道固体可以分为晶体与非晶体。
请你举出常见的晶体与非晶体的实例。
