原花青素的含量正丁醇测定方法
葡萄籽原花青素液相检测方法

原花青素原花青素原花青素原花青素HPLC初步方案初步方案初步方案初步方案一.实验目的:分析样品原花青素纯度,了解其中杂质成分。
二.实验方案:1. 方案一:Waters 公司高效液相色谱,C18柱(4.6 ×250 mm) , 检测波长为280 nm,进样量10μL ,柱温为室温。
待测液均经0.45μm 孔径的滤膜过滤。
流动相及流速见下表(A —10 %乙酸,B —重蒸水):2. 方案二:(间接法定量)(原理类似铁盐催化比色法)(1) 标准曲线:称取前花青素标准品10mg 溶于10ml甲醇中,吸取该溶液0、0.1、0.25、0.5、1.0、1.5ml 置于10ml 容量瓶中,加甲醇至刻度,摇匀。
各取1ml 测定。
(2) 试样测定: 将正丁醇与盐酸按95 :5的体积比混合后,取出6.0ml 置于具塞锥瓶中,再加入0.2ml硫酸铁铵[NH4Fe(SO4) 2·12H2O]溶液(用浓度为2mol/L 盐酸配成2%(w/v)的溶液)和1.0ml 经0.45μm滤膜过滤的试样溶液,混匀,置沸水浴回流,精确加热40min后,立即置冰水中冷却,待进行高效液相色谱分析。
(3)液相色谱参考分析条件: 色谱柱Shimadzu Shim –pak CLC –ODS 4.6 ×150mm;柱温35 ℃;检测器:紫外检测器,检测波长525nm流动相: 水:甲醇:异丙醇:10 %甲酸= 73 :13 :6 :8 流速0.9ml/min。
注:该方法使用的水解方法与我们当前使用的铁盐催化水解原花青素方法稍有差异,哪种效果更好,可进行预实验加以比较。
3.方案三:(反相高效液相色谱)标样:原花青素标准品色谱柱:Hypersi ODS-2 ,150 × 4.6mm 5μm;流动相:A:0 . 2%(V/V) 乙酸;B:乙腈;流量:1ml /min;进样量:5μl;柱温:30℃;检测波长:280nm.洗脱梯度:以乙腈的百分比浓度表示(B液溶于A液)0 ~5 % ,10min;5%~20%,10~20min;20%~40%,20~40min;40%~50%,40~50min;50%~5%,45~50min;5%~0,50~60min。
正丁醇的测定

正丁醇的测定正丁醇是一种常见的醇类化合物,化学式为C4H10O。
它是四碳醇的一种,由一个直链四碳骨架和一个羟基组成。
正丁醇在工业生产和实验室中广泛应用,因此准确测定正丁醇的含量对于许多应用场景来说非常重要。
正丁醇的测定方法有多种,下面将介绍两种常见的方法:比重法和气相色谱法。
比重法是一种简单直观的测定正丁醇含量的方法。
它基于正丁醇的比重与其浓度之间存在一定的关系。
首先,需要准备一台电子天平和一个比重瓶。
将比重瓶称重,记录下空瓶的质量。
然后,向比重瓶中加入一定量的正丁醇样品,再次称重,记录下瓶中含有正丁醇的质量。
通过比较两次称重的结果,可以计算出正丁醇的质量。
最后,通过质量与体积的比值,可以得到正丁醇的比重。
根据已知正丁醇的比重和样品的比重,可以计算出正丁醇的浓度。
气相色谱法是一种精确测定正丁醇含量的方法。
它基于正丁醇在气相色谱柱中的保留时间与其浓度之间存在一定的关系。
首先,需要准备一台气相色谱仪和一根适合分析正丁醇的色谱柱。
将正丁醇样品注入气相色谱仪的进样口,通过适当的气流和温度条件,使样品中的正丁醇被蒸发并进入色谱柱。
在色谱柱中,正丁醇会与柱内的固定相发生相互作用,从而延长其在柱中的滞留时间。
根据正丁醇的保留时间和已知浓度的对照样品的保留时间,可以通过标准曲线计算出待测样品中正丁醇的浓度。
除了上述两种方法,还有许多其他测定正丁醇含量的方法,比如红外光谱法、核磁共振法等。
每种方法都有其适用的场景和优缺点,选择合适的方法需要根据具体的实验目的和条件来确定。
正丁醇的测定对于许多领域来说都是非常重要的。
比重法和气相色谱法是常用的测定方法,它们分别基于正丁醇的比重和保留时间与其浓度之间的关系。
选择合适的测定方法需要根据实验目的和条件来确定。
无论使用哪种方法,都需要严格控制实验条件,以保证测定结果的准确性和可靠性。
希望本文对正丁醇的测定提供了一些基本的了解和参考。
葡萄籽提取物中原花青素含量的最佳测定方法
葡萄籽提取物中原花青素含量的最佳测定方法葡萄籽提取物-原花青素被誉为“最强效的自由基清除剂”,其抗氧化能力是VC的20倍,VE的50倍。
也是唯一能透过血脑屏障的抗氧化剂,因此在促进皮肤新陈代谢,分解黑色素,以及提高机体免疫力,延缓衰老方面的应用极为广泛。
葡萄籽提取物由原花青素、儿茶素、表儿茶素、没食子酸等多酚类物质组成的,由于原花青素的成分极其复杂,目前的研究实验中还无法提供原花青素的标准品,因此Bate-Smith 和Porter法只能测定葡萄籽提取物中原花青素的相对含量。
一、Bate-Smith法、Porter法测定葡萄籽原花青素含量西安源森生物实验室对Bate-Smith法和Porter法测定原花青素相对含量实验进行了研究:(一)Bate-Smith法测定葡萄籽原花青素含量【实验目的】由于目前没有原花青素的标准品,因此此方法测定的只是葡萄籽提取物中原花青素的相对值,其含量用原花青素指数(procyanidolic index)来表示。
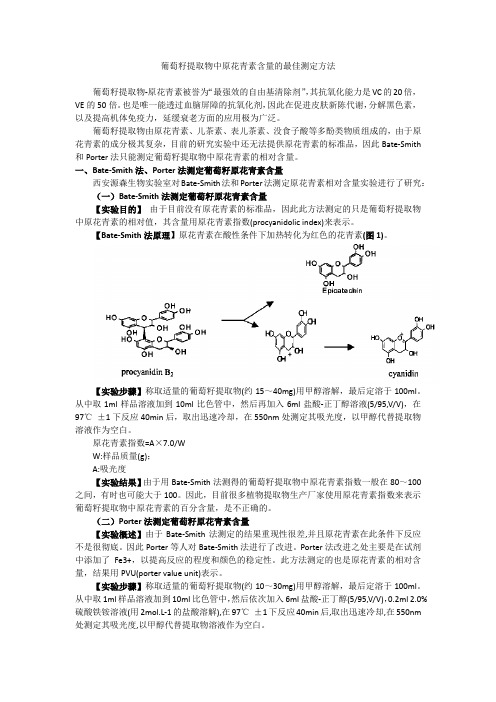
【Bate-Smith法原理】原花青素在酸性条件下加热转化为红色的花青素(图1)。
【实验步骤】称取适量的葡萄籽提取物(约15~40mg)用甲醇溶解,最后定溶于100ml。
从中取1ml样品溶液加到10ml比色管中,然后再加入6ml盐酸-正丁醇溶液(5/95,V/V),在97℃±1下反应40min后,取出迅速冷却,在550nm处测定其吸光度,以甲醇代替提取物溶液作为空白。
原花青素指数=A×7.0/WW:样品质量(g);A:吸光度【实验结果】由于用Bate-Smith法测得的葡萄籽提取物中原花青素指数一般在80~100之间,有时也可能大于100。
因此,目前很多植物提取物生产厂家使用原花青素指数来表示葡萄籽提取物中原花青素的百分含量,是不正确的。
(二)Porter法测定葡萄籽原花青素含量【实验概述】由于Bate-Smith法测定的结果重现性很差,并且原花青素在此条件下反应不是很彻底。
前花青素含量测定方法(UV)

编号:TCD0150 原花青素(Proanthocyanidin)含量测定方法
一、仪器与试剂
1.仪器:UV-2101 PC紫外-可见光分光光度计
2.试剂:2%NH4Fe(SO4)2·12H2O的2N盐酸水溶液:量取浓盐酸17mL,加水至100mL,加入2gNH4Fe(SO4)2·12H2O,振摇溶解,即得。
(两周内有效) 酸性正丁醇溶液:95mL正丁醇中加入5mL浓盐酸,混匀。
(当日使用)
二、溶液制备
1.样品溶液制备精密称取葡萄籽提取物样品约100mg,置50mL容量瓶中,加甲醇溶解定容。
精密吸取2mL于50mL容量瓶中,用甲醇定容至刻度,即为供试液。
精密吸取该供试液1mL于10mL具塞试管中,加入2% NH4Fe(SO4)2·12H2O 的2N盐酸水溶液0.2mL,酸性正丁醇溶液6mL,拧紧密封盖,摇匀,拧松密封盖。
置95℃水浴中加热反应60min,取出,在冰水浴中快速冷却,即得待测样品溶液。
2.标准品溶液制备以标准样品代替样品,按样品溶液制备方法,处理即得标准品溶液。
3.样品空白溶液制备以甲醇代替样品供试液,按样品溶液处理,即得空白溶液。
三、样品测定
打开仪器电源,预热20min,待仪器自检通过后,在546nm处以样品空白溶液作为空白,测定标准品溶液和样品溶液吸收度。
四、结果计算
A×Ws
C%= ×S
As×W
As、A:标准样品、样品吸收值
Ws、W:标准样品、样品称样量(mg)
S:标准样品含量(%)
注:所用器皿均需干燥处理。
除甲醇外,其余均需平行显色三份。
原花青素简介

原花青素(Proantho Cyanidins,PC),又名缩合鞣质,可视作花青素( cyanidin)类物质的聚合物,是自然界中广泛存在的一类多酚类化合物。通常将从植物中分离得到的一切无色的、在无机酸存在和加热处理下能产生红色花青素( cyanidin)的一类多酚化合物统称为原花青素(赵平2011)。最初是在20世纪40年代从花生仁的包衣中提取出来,在50年代又被法国科学家从海松树皮中发现并提取出来,并将其提取率提高到达85%。近来,研究证明原花青素是很强的抗氧化剂,可以清除自由基,其抗氧化、清除自由基的能力是维生素E的50倍、维生素C的20倍,能防治80多种因自由基引起的疾病,包括心脏病、关节炎等,还具有改善人体微循环功能(张长贵2009)。目前,原花青素作为营养强化剂、天然防腐剂、天然抗氧化剂、DNA保护剂等,被广泛应用于食品、药品、化妆品等领域。
4.3 pH示差法
pH示差法是利用原花青素在不同pH下呈色不同的性质进行检测。pH 1.0时,原花青素颜色最深; pH 4.5时,以无色的半缩酮形式存在。pH示差法是基于此反应来快速准确地测量花青素含量的方法(Clifford et al 2000)。pH示差法是一种简便的测定原花青素含量的方法,能很好地消除溶液中杂质对测定结果的影响,可信度较高。
2化学结构及分类
原花青素是以黄烷-3-醇为结构单元通过C-C键聚合而形成的化合物,起初称为黄烷醇类或归于缩合鞣质。其结构分类主要取决于五方面:(1)黄烷-3-醇单元的类型;(2)单元之间的连接方式;(3)聚合程度(组成单元的数量);(4)空间构型;(5)羟基是否被取代(如羟基的酯化、甲基化等)。根据原花青素的聚合程度可分为单倍体(monomer)、寡聚体(oligomer)和多聚体(polymer)(Alan et al 2008)。其中单倍体是基本结构单元,寡聚体由2~10个单倍体聚合而成,多聚体则由10个以上的单倍体聚合而成(张慧文2015)。
原花青素含量检测的概述

原花青素含量检测的概述【摘要】对目前原花青素常用的检测方法进行了对比并阐述了各种方法的优缺点,为探索更好的原花青素的测定方法奠定基础。
【关键词】原花青素;检测;含量原花青素是一类广泛存在于植物中的黄烷醇单体及其聚合体的多酚类混合物,具有抗氧化和自由基清除能力等生物活性。
自20世纪60年代以来,在保健品、医药和化妆品领域获得了广泛应用。
研究表明[1],儿茶素和表儿茶素是构成原花青素的结构基础,继而形成缩合成二聚体、三聚体至高聚体。
且单体具有旋光性,因此要想测定每一种成分的含量非常困难。
目前国内外对原花青素含量的测定方法尚未统一,现介绍几种常用的方法。
1.可见分光光度法[2]原花青素最常用的测定方法是可见分光光度法,它分为KMnO4法[3]、正丁醇-盐酸法、香草醛-强酸法、铁盐催化比色法、和pH示差法等。
正丁醇-盐酸法、香草醛-强酸法两种方法是目前普遍采用的相对专一、灵敏的、简单迅速测定原花青素的方法。
1.1 Porter法(Bate-smith法)又叫盐酸-正丁醇法,是依据原花青素在无机酸和加热的条件下被降解,产生红色花青素,在546nm处有最大吸收,原花青素的含量与吸光度值符合朗伯-比尔定律[4]。
在强酸作用下,聚合原花青素单元间的连接键易被打开,上部单元生成黄烷-3-醇,下部单元生成花色素。
而对于黄烷3,4-二醇单体原花青素来说,C-4位有极强的亲电性,其醇羟基与C-5,C-7上的酚羟基形成了一个苄醇系统,使得4位碳易于生成正离子。
在强酸作用下,正碳离子失去质子,生成花色素[5]。
对于黄烷-3-醇单体,不会有正离子形成,因此与儿茶素和表儿茶素的单体不发生显色反应。
此法对原花青素具有专一选择性,儿茶素、黄酮类、棓酸类及水解单宁类化合物皆不具备此反应,不适宜于低聚原花青素的测定,它与原花青素的高聚体反应也不完全。
随后,Porter等对该法的反应条件进行了探索,并认为Fe3+、Co2+、Cu2+等金属离子可催化加速自氧化过程,提高转化率,其中以Fe3+的催化效果最好。
葡萄籽原花青素含量检测方法

杭州尼诺生物科技有限公司葡萄籽原花青素一目的:建立葡萄籽原花青素含量测定法。
二仪器:紫外可见分光光度UV—UNIC7200。
三责任者:QC检验员。
四原理:原花青素在酸性条件下加热水解产生色素,产生色素的过程是定量反应。
通过检测水解产物的最大吸收波长下的吸光度对原花青素进行定量。
在吸光度0.2-0.7纳米范围内浓度和吸光度呈线性关系。
五试剂和对照品:甲醇(分析纯)正丁醇(分析纯)盐酸(分析纯)硫酸铁铵(分析纯)葡萄籽对照品(公司自制)六试剂配制及溶液配制:1 试剂配制:50%甲醇溶液:量取50毫升甲醇溶于50毫升纯化水中。
盐酸正丁醇溶液:量取5毫升盐酸溶于95毫升正丁醇,置阴凉处避光保存。
硫酸铁铵盐酸溶液:称取2克,NH4F e (SO4)212H2O溶于100毫升2摩尔/升的盐酸水溶液中。
2 溶液配制:对照品溶液:称取10毫克葡萄籽对照品,精密称定,用50%甲醇溶解并定容到100毫升容量瓶中。
供试品溶液:称取10毫克葡萄籽供试品,精密称定,用50%甲醇溶解并定容到100毫升容量瓶中。
七测定步骤:在一系列10毫升具塞硼硅酸玻璃刻度试管中,各加0.2毫升硫酸铁铵盐酸溶液,6毫升正丁醇盐酸溶液,再逐个加1毫升待测样品溶液,1毫升对照品溶液,1毫升甲醇(空白),记录试管体积V A。
加塞,振荡混匀。
于98。
C沸水浴中反应45分钟,取出试管于冰水中迅速冷却,记录试管的体积V B。
在546纳米处用紫外分光光度计检测相对于空白的吸光度。
八计算:此方法受环境因素影响,操作中用对照品来定量待测样,其计算公式如下:原花青素%=K×A1×M2×V1/(A2×M1×V2)式中:A1 为供试品吸收度A2 为对照液吸收度M1 为供试品称样量M2 为对照品称样量V1 为供试品最终体积V A-V BV2 为对照品液最终体积K 为对照品的含量。
原花青素的含量正丁醇测定方法
原花青素含量1.材料和仪器主要试剂:提取液,原花青素标样,盐酸正丁醇溶液、NH4Fe(SO4)2、95% 乙醇。
主要仪器:UV2100 型紫外分光光度计、恒温水浴锅。
溶液配制: 2%NH4Fe(SO4)2 称取3.66g七水合硫酸亚铁固体,溶于100ml水中后即得95%乙醇移取5ml的蒸馏水至100ml容量瓶中用无水乙醇定容盐酸正丁醇移5ml浓HCL 至100ml容量瓶正丁醇定容2.实验步骤a.标准曲线的制备:准确称取原花青素标准样品0.010g,用95% 乙醇溶解并定容于10mL 容量瓶中,所得浓度为1mg/mL 作标样。
吸取标样溶液0mL、0.5mL、1.0mL、1.5mL、2.0mL、2.5mL、3mL分别于25mL 具塞试管中,加95%乙醇定容为3mL, 然后分别加入0.2mL 2%NH4Fe(SO4)2 溶液和6mL盐酸正丁醇(5:95)溶液,盖塞,摇匀,于微沸的水浴中加热反应40min 取出,于冷水中迅速冷却,溶液显红色,以0mL 溶液作为空白对照,于546nm 处测定其吸光度。
采用最小二乘法作原花青素浓度(C)与吸光度( A ) 线性回归方程。
结果见表取得标样体0 0.5 1.0 1.5 2.0 2.5 3.0 积(/ml)对应标样浓度(mg/ml)测的吸光度值Ab.样品测定分别精确吸取10mL 样品,用95%乙醇定容于50mL 容量瓶。
吸取上述样品待测液3mL 于25mL 具塞试管中,按标准曲线制作项下的操作步骤,依次分别加入0.2mL 2%NH4Fe(SO4)2 溶液、6mL 盐酸正丁醇溶液。
根据标准曲线计算出结果,按其稀释倍数求得各样品中原花青素含量。
3.单因素实验1 .料液比: 1:6 1;7 1:8 1:9温度室温超声波时间10min 乙醇浓度 95%2. 超声波时间: 10min 20min 30min 40min温度室温料液比:1:8 乙醇浓度 95%3.乙醇浓度 35% 55% 75% 95%温度室温料液比:1:8 超声波时间30min4.正交试验1 2 3A A AA B BA C CB A BB B CB C AC A CC B AC C B1为单因素中第1项(以此类推2...)A为单因素中第1项第2类 B为第3类(如3 C 指乙醇浓度95%) A B C 为单因素测定中最优3选项。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原花青素含量
1.材料和仪器
主要试剂:提取液,原花青素标样,盐酸正丁醇溶液、NH4Fe(SO4)2、95% 乙醇。
主要仪器:UV2100 型紫外分光光度计、恒温水浴锅。
溶液配制: 2%NH4Fe(SO4)2 称取3.66g七水合硫酸亚铁固体,溶于100ml水中后即得
95%乙醇移取5ml的蒸馏水至100ml容量瓶中用无水乙醇定容
盐酸正丁醇移5ml浓HCL 至100ml容量瓶正丁醇定容
2.实验步骤
a.标准曲线的制备:准确称取原花青素标准样品0.010g,用95% 乙醇溶
解并定容于10mL 容量瓶中,所得浓度为1mg/mL 作标样。
吸取标样溶液0mL、0.5mL、1.0mL、1.5mL、2.0mL、2.5mL、3mL分别于25mL 具塞试管中,加95%乙醇定容为3mL, 然后分别加入0.2mL 2%NH4Fe(SO4)2 溶液和6mL盐酸正丁醇(5:95)溶液,盖塞,摇匀,于微沸的水浴中加热反应40min 取出,于冷水中迅速冷却,溶液显红色,以0mL 溶液作为空白对照,于546nm 处测定其吸光度。
采用最小二乘法作原花青素浓度(C)与吸光度( A ) 线性回归方程。
结果见表
取得标样体
0 0.5 1.0 1.5 2.0 2.5 3.0 积(/ml)
对应标样浓
度(mg/ml)
测的吸光度
值A
b.样品测定
分别精确吸取10mL 样品,用95%乙醇定容于50mL 容量瓶。
吸取上述样品待测液3mL 于25mL 具塞试管中,按标准曲线制作项下的操作步骤,依次分别加入0.2mL 2%NH4Fe(SO4)2 溶液、6mL 盐酸正丁醇溶液。
根据标准曲线计算出结果,按其稀释倍数求得各样品中原花青素含量。
3.单因素实验
1 .料液比: 1:6 1;7 1:8 1:9
温度室温超声波时间10min 乙醇浓度 95%
2. 超声波时间: 10min 20min 30min 40min
温度室温料液比:1:8 乙醇浓度 95%
3.乙醇浓度 35% 55% 75% 95%
温度室温料液比:1:8 超声波时间30min
4.正交试验
1 2 3
A A A
A B B
A C C
B A B
B B C
B C A
C A C
C B A
C C B
1为单因素中第1项(以此类推2...)
A为单因素中第1项第2类 B为第3类(如3 C 指乙醇浓度95%) A B C 为单因素测定中最优3选项。
