(完整版)初中化学推断题专题
完整)初中化学推断题专题附答案

完整)初中化学推断题专题附答案1.化学反应推断题1) A的化学式为未知。
2) 反应②的化学方程式为:Fe2O3 + 3CO → 2Fe + 3CO2.C物质固态时的名称为氯化钙,它在实际生活中用作融雪剂。
3) 反应③中生成红色固体的化学方程式为:FeCl3 +3NaOH → Fe(OH)3 ↓ + 3NaCl。
4) 产生无色气体G的原因是A和G在加热条件下反应生成氯气:2HCl + 2NaCl → 2NaCl + Cl2↑ + H2↑。
2.钠盐混合物实验题1) D的化学式为CO2,E的化学式为Na2CO3,B的化学式为BaCl2.2) 原混合物中含有的三种易溶于水的钠盐的化学式分别为NaCl、Na2CO3和NaHCO3.3.食盐样品除杂题1) 沉淀甲是氢氧化铁(III),滤液C中的溶质是氯化镁,操作⑤中加入过量盐酸的作用是将滤液C中的氢氧化铁(III)转化为FeCl3.2) 固体丁中NaCl的质量不变,如果在操作②中改为加过量的KOH溶液,则固体丁中可能含有的杂质是氢氧化铜(II)。
4.文章没有问题5.物质化学式推测题1) B的化学式为未知,D的化学式为CuSO4,F的化学式为Fe。
2) C→A转化的化学方程式为:2Al + 6HCl → 2AlCl3 + 3H2↑。
6.无色气体转化关系推断题A为氧气,B为氮气,C为氯气,D为二氧化碳,E为一氧化碳。
7.无色溶液鉴别题A为稀HCl溶液,B为NaOH溶液,C为MgSO4溶液,D为未知溶液。
通过加入BaCl2溶液,若产生白色沉淀,则D 为SO4 2-离子的溶液。
1.根据实验结果,可以确定溶液A中的溶质为Cu2+离子,溶质为MgSO4的溶液是C溶液,呈酸性。
在B溶液中滴加硝酸银溶液,可以观察到无明显反应。
2.根据题目所给信息,可以列出以下物质的化学式:A为元素Cu,C为Fe2O3,D为H2,E为氧气。
3.根据转换关系,可以得知A为NaOH,G为Na2CO3.4.原白色固体中一定不含有CuSO4,一定含有BaCl2.实验①得到的无色溶液B中一定含有Na+离子。
中考化学初中化学推断题(各种题型答案完整版)

中考化学初中化学推断题(各种题型答案完整版)一、文字叙述型推断题:1、有一包固体粉末,可能由碳酸钙、硫酸钾、硝酸钠、氯化铁、氯化钡中的一种或几种组成,做实验得以下结论:(1)将此固体粉末加到水中,得到白色沉淀,上层溶液为无色。
(2)该白色沉淀部分溶于稀硝酸,且有气体放出。
从实验可判断出,该粉末中一定含有,一定不含有。
答案;(1)中“上层溶液为无色”可推得无“氯化铁”;“白色沉淀”有两种可能:碳酸钙或硫酸钾与氯化钡反应生成的硫酸钡。
(2)中“白色沉淀部分溶于稀硝酸”中的“部分溶于”可知既有“碳酸钙”,又有“硫酸钡”;而有硫酸钡时,则一定含有硫酸钾与氯化钡。
但整个推断过程中,始终无法确定硝酸钠的存在与否。
所以,原固体粉末中一定含有碳酸钙、硫酸钾和氯化钡,一定不含有氯化铁,可能含有硝酸钠。
2、某固体混合物可能含有氯化钙、碳酸钠、硫酸铜、硫酸钾和硝酸钡。
现进行以下实验:(1)将该混合物放入足量水中,产生白色沉淀,得无色透明溶液;(2)再加入足量的稀硝酸,沉淀全部溶解,逸出无色气体,所得溶液澄清透明;(3)最后加入稀硫酸,又立刻出现白色沉淀。
据上可推断原混合物中肯定有,肯定没有,用化学方程式表示上述实验中肯定发生的反应答案;(1)由该固体溶于水,得白色沉淀,静置后上层溶液呈无色.可推出混合物中一定没有硫酸铜,可能是沉淀为:碳酸钠和氯化钙、碳酸钠和硝酸钡、硫酸钾和硝酸钡反应都能生成沉淀;(2)由向(1)所得白色沉淀中加入足量稀硝酸,沉淀全部溶解,可推出出混合物中一定没有硫酸钾,因为硫酸钡沉淀不能溶于稀硝酸;(3)向(2)中的溶液中加入稀硫酸产生了白色沉淀,说明在溶液中含有钡离子,则说明原混合物中含有硝酸钡.(1)由该固体溶于水,得白色沉淀,静置后上层溶液呈无色,可推出混合物中一定没有硫酸铜(铜离子在溶液中呈蓝色),可能的沉淀是由碳酸钠和氯化钙反应生成的碳酸钙,或者是碳酸钠和硝酸钡反应生成的碳酸钡或者硫酸钾和硝酸钡反应生成的硫酸钡沉淀或者三者两两结合甚至三者兼有.(2)由向(1)所得白色沉淀中加入足量稀硝酸,沉淀全部溶解,可推出该沉淀一定不是硫酸钡,因为硫酸钡沉淀不能溶于稀硝酸.则沉淀可能是能够溶解于硝酸的碳酸钡或者碳酸钙,可以判断一定含有碳酸钠;(3)向(2)中的溶液中加入稀硫酸产生了白色沉淀,说明在溶液中含有钡离子,则说明原混合物中含有硝酸钡,而(1)中的沉淀一定有碳酸钡,可能有碳酸钙.故答案为:硝酸钡,碳酸钠;硫酸钾,硫酸铜;氯化钙.二、方程式叙述型推断题:1、已知A、B、C、D、E、F6种物质的转化关系如下:(1)A+B→C+H2O (2)C+KOH→D↓(蓝色)+E (3)B+D→C+H2O(4)E+BaCl2→F↓(白色,不溶于稀硝酸)+KCl根据上述变化关系,推断有关物质的化学式:A ;B ;C ;D ;E ;F 。
初三化学推断题专项练习(含答案)

初三化学——推断题专题复习一、考点、热点回顾1、固体物质的颜色A 白色固体:氧化钙 CaO 、氢氧化钙Ca(OH)2、碳酸钠Na2CO3、碳酸钙CaCO3、氢氧化钠NaOH、B 黄色固体:硫粉SC 红色固体:红磷P、氧化铁Fe2O3、铜CuD 蓝色固体:胆矾CuSO4.5H2OE黑色固体:木炭C、氧化铜CuO、二氧化锰MnO2、四氧化三铁Fe3O4、F 绿色固体:碱式碳酸铜Cu2(OH)2CO3G紫黑色固体:高锰酸钾KMnO4H 无色固体:冰,干冰,金刚石I 银白色固体:银,铁,镁,铝,汞等金属2、生成沉淀的颜色A 白色沉淀:不溶于水也不溶于稀硝酸:氯化银AgCl、硫酸钡BaSO4不溶于水但溶于稀硝酸或稀盐酸:氢氧化镁Mg(OH)2、碳酸钙CaCO3、碳酸钡BaCO3B 红褐色沉淀:氢氧化铁Fe(OH)3C 蓝色沉淀:氢氧化铜 Cu(OH)23、溶液的颜色A 蓝色溶液Cu2+:硫酸铜CuSO4、硝酸铜Cu(NO3)2 、氯化铜CuCl2等B 黄色溶液Fe3+:氯化铁FeCl3、硫酸铁Fe2(SO4)3、硝酸铁Fe(NO3)3等C 浅绿色溶液Fe2+:氯化亚铁FeCl2、硫酸亚铁FeSO4、硝酸亚铁Fe(NO3)2等D无色液体:水,双氧水E 紫红色溶液:高锰酸钾溶液F 紫色溶液:石蕊溶液4、气体的颜色A 红棕色气体:二氧化氮B 黄绿色气体:氯气C无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
解题技巧:抓住题目的题眼进行突破,常见的题眼就是上述物质的颜色与状态,还有就是某些物质的制备原理=二、典型例题1.A 、B 、C 、D 、E 、F 、G 为常见的物质,其中B 、E 、G 属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系。
请回答:(1)A 物质的化学式 。
(2)写出反应②的化学方程式 ,C 物质固态时的名称 ,该固体物质在实际生活中的一种用途是 。
中考化学推断题100题专题训练(含答案)

中考化学推断题100题专题训练(含答案)一、中考化学推断题1.现有一包不纯的K2CO3固体,可能含有Fe(NO3)3、CaCO3、KCl、BaCl2、Na2SO4、Na2CO3中的一种或几种。
现做如下实验:(1)取固体试样溶于足量水,得无色溶液A,则原固体一定不含______。
(2)向溶液A中加入足量Ba(NO3)2溶液,过滤得白色固体B和无色滤液C.加入Ba(NO3)2溶液时一定发生反应的化学方程式是______。
(3)向固体B中加入足量稀HNO3,固体完全溶解,则原固体一定不含______。
(4)取少量滤液C,先滴加过量稀HNO3,再滴加AgNO3溶液,出现白色沉淀,则原固体一定含有______。
(5)若所取固体试样为13.8g,实验(2)中得到白色固体B的质量为19.7g,则原固体中一定______(选填“不含”或“含”)Na2CO3。
【答案】Fe(NO3)3、CaCO3、BaCl2 K2CO3+Ba(NO3)2=BaCO3↓+2KNO3 Na2SO4 KCl 含【解析】【分析】硝酸铁溶于水,溶液显黄色,碳酸钙难溶于水,硝酸钡和碳酸钾反应会生成白色的碳酸钡沉淀,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀,碳酸根离子和钡离子也会生成溶于酸的碳酸钡沉淀。
【详解】(1)取固体试样溶于足量水,得无色溶液A,所以原固体一定不含Fe(NO3)3、CaCO3、BaCl2;(2)向溶液A中加入足量Ba(NO3)2溶液,过滤得白色固体B和无色滤液C,加入Ba(NO3)2溶液时一定发生的反应是碳酸钾和硝酸钡反应生成碳酸钡沉淀和硝酸钾,化学方程式是:K2CO3+Ba(NO3)2=BaCO3↓+2KNO3;(3)向固体B中加入足量稀HNO3,固体完全溶解,所以原固体一定不含Na2SO4;(4)取少量滤液C,先滴加过量稀HNO3,再滴加AgNO3溶液,出现白色沉淀,则原固体一定含有KCl;(5) K2CO3+Ba(NO3)2=BaCO3↓+2KNO3,138 19713.8g 19.7gNa2CO3+Ba(NO3)2=BaCO3↓+2NaNO3,106 19710.6g 19.7g13.8g的碳酸钾会生成19.7g的碳酸钡沉淀,10.6g的碳酸钠会生成19.7g的碳酸钡沉淀,原固体一定含有KCl,所以若所取固体试样为13.8g,实验(2)中得到白色固体B的质量为19.7g,所以原固体中一定含Na2CO3。
初中化学推断题(各种题型完整版)

初中化学物质推断题一、文字叙述型推断题:1、有一包固体粉末,可能由碳酸钙、硫酸钾、硝酸钠、氯化铁、氯化钡中的一种或几种组成,做实验得以下结论:(1)将此固体粉末加到水中,得到白色沉淀,上层溶液为无色。
(2)该白色沉淀部分溶于稀硝酸,且有气体放出。
从实验可判断出,该粉末中一定含有,一定不含有。
2、某固体混合物可能含有氯化钙、碳酸钠、硫酸铜、硫酸钾和硝酸钡。
现进行以下实验:(1)将该混合物放入足量水中,产生白色沉淀,得无色透明溶液;(2)再加入足量的稀硝酸,沉淀全部溶解,逸出无色气体,所得溶液澄清透明;(3)最后加入稀硫酸,又立刻出现白色沉淀。
据上可推断原混合物中肯定有,肯定没有,用化学方程式表示上述实验中肯定发生的反应二、方程式叙述型推断题:1、已知A、B、C、D、E、F,6种物质的转化关系如下:(1)A+B→C+H2O (2)C+KOH→D↓(蓝色)+E (3)B+D→C+H2O (4)E+BaCl2→F↓(白色,不溶于稀硝酸)+KCl根据上述变化关系,推断有关物质的化学式:A ;B ;C ;D ;E ;F 。
2、有属于酸、碱、盐的5种常见物质A、B、C、D、E,它们之间可以发生如下反应:(1)A+B→C+H2O (2)C+H2SO4→D↓+A (3)E+AgNO3→AgCl↓+C根据上述反应,推断下列各物质的化学式:A ;B ;C ;D ;E 。
3、A、B、C、D、E是初中化学中的五种常见物质。
C、D是单质,C为紫红色固体,D被认为是最清洁的能源。
B的浓溶液常用做干燥剂。
已知Fe和A、B的水溶液分别能发生反应:①Fe + A → C + E;②Fe + B → D + E 。
写出化学式:A ;B ;C ;D ;E 。
4、根据下述反应,判断未知物。
(1) A + HCl → B + H2O + CO2↑ (2) B + AgNO3 → AgCl↓+ C(3) C + CuSO4 → BaSO4↓+ D (4) D + NaOH → E↓+ NaNO3(5) (5) E + F → D + H2O已知A是一种盐,则A~F的化学式为:A、B、C、D、、E 、F 。
(完整)初中化学推断题专题附答案
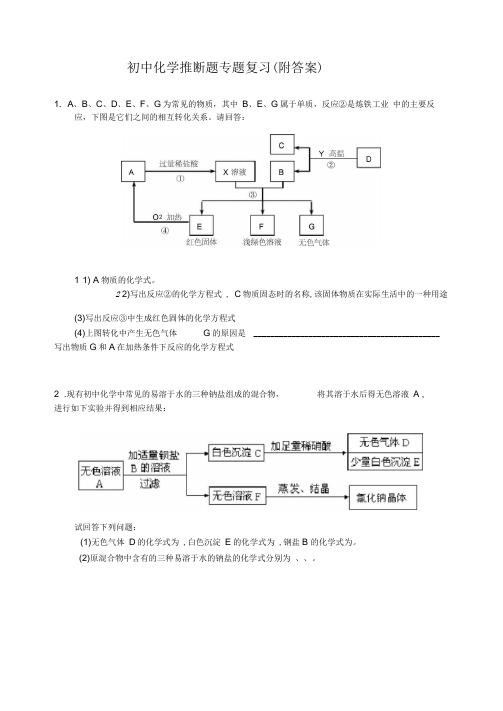
初中化学推断题专题复习(附答案)1. A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系。
请回答:1 1) A物质的化学式。
2 2)写出反应②的化学方程式 , C物质固态时的名称,该固体物质在实际生活中的一种用途(3)写出反应③中生成红色固体的化学方程式(4)上图转化中产生无色气体G的原因是 ____________________________________________ 写出物质G和A在加热条件下反应的化学方程式2 .现有初中化学中常见的易溶于水的三种钠盐组成的混合物,将其溶于水后得无色溶液A ,进行如下实验并得到相应结果:试回答下列问题:(1)无色气体D的化学式为 ,白色沉淀E的化学式为 ,钢盐B 的化学式为。
(2)原混合物中含有的三种易溶于水的钠盐的化学式分别为、、。
3 .为了除去食盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如下图所示的①至⑤步除杂方案:操作⑤中加入过量盐酸的作用是(2)假设整个操作过程中物质转化无损失,则固体丁中NaCl 的质量比原样品中 NaCl的质量 (填增大、不变或减小);若在操作②中改为加过量的 KOH 溶液,固 体丁中可能含有的杂质是 。
5.现有A 、B 、C 、D 、E 、F 、G 七种物质,C 、F 是最常见的金属,B 是气体单质,D 为 浅绿色溶液,G 为蓝色溶液,它们之间存在如下关系:6. A 、B 、C 、D 、E 是初中化学中常见的 5种无色气体,其中2种是单质,3种是化合 物。
它们之间的转化关系如下图所示。
甲沉淀溶解 过量 NaOH Wft 过滤一③过量 BaCl 2溶液丙沉淀过量 Na 2CO 3溶液请根据上述除杂方案,回答下列问题:(1)沉淀甲是;滤液C 中的溶质是过量 盐酸 加热蒸发(2)写出C-A 转化的化学方程式:(1)试推测下列物质的化学式: B, D, F请写出你的推断结果:A, B, C, D, E7 .有A、B、C、D四种无色溶液,分别是稀HCl、NaOH、MgSO4、NaCl溶液中的一种。
中考化学推断题50题专题训练(含答案)

5.A、B、C、D、E、F都是初中化学中常见的化合物,其中A、B是盐,且B中含有钠元素;D是酸,C为白色沉淀。它们相互之间在溶液中可发生如下反应:
(3)分别写出物质F和H的一种用途___________;____________________。
【答案】CaCl2Fe+2HCl=FeCl2+H2↑置换反应Ca(OH)2+CO2=CaCO3↓+H2O供给呼吸重要的建筑材料
【解析】
【分析】
A是人体胃液中帮助消化的物质,那么A是稀盐酸;B用于改良酸性土壤,故B是熟石灰氢氧化钙;稀盐酸与氢氧化钙发生中和反应生成氯化钙和水,根据反应条件可知C是水,D是氯化钙;水电解生成氢气和氧气,稀盐酸能转化为E,故E是氢气,那么F是氧气;氯化钙能与碳酸钠等物质反应生成碳酸钙,即白色沉淀物是碳酸钙。
考点:物质的推断
2.A、B、C、D是初中化学常见的物质,其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分,它们之间的转化关系如图所示(图中反应条件及部分反应物、生成物已省略)。
回答下列问题:
(1)写出下列物质的化学式:A_____;B_____;C_____。
(2)实验室常用_____鉴别B和C。
【解析】
【分析】
根据反应①C+D=A+2F,且D是酸,C为白色沉淀,A为盐,可知该反应为复分解反应,生成物中没有气体没有沉淀,则F是水,由于F的化学计量数是2,酸是二元酸硫酸,白色沉淀C为难溶性的二元碱氢氧化亚铁或氢氧化镁,则A可能为硫酸亚铁或硫酸镁;根据②2E+D=B+2F,E和酸反应生成盐和水,且E的化学计量数是2,那么E可能是一元碱氢氧化钠或氢氧化钾或氨水,则B可能为硫酸钠或硫酸钾或硫酸铵;将上述物质带入③A+2E=C↓+B检验,推断成立。
初三化学复习推断题专题

氧化铁
石灰水
A
B
⑴溶液B中的溶质有___________,溶液D中的溶质有 ___________,固体样品中一定含有的物质有________。 ⑵写出探究过程中发生反应的化学方程式____________ ____________________________________________
⑴E物质为___________; D物质为___________。 ⑵写出反应的化学方程式: A→B _____________________, B→C _____________________, F—B _____________________。
E
F
D
A
B
C
②
①
④
③
⑤
10. 如图所示, 已知A、B、C、D、E、F是初中化学常见的六种化合物。①、②、⑤基本反应类型相同,其中一个有沉淀生成,另一个有气体生成,还有一个没有明显现象 (图中 “→”表示物质间存在转化关系,图中已略去部分物质。)试回答以下问题。
⑴D物质为___________; A物质为___________。 ⑵写出反应的化学方程式: A→B _____________________, B→C _____________________, G→A _____________________。
B
A
C
E
D
F
A
9.在一次兴趣小组活动中,一小组利用物质间的转化,设计了一个平面“小别墅”,如图所示, 已知A、B、C、D、E、F是初中化学常见的六种化合物,A、F不含相同元素,E常用于改良土壤的酸性,其溶液还能检验二氧化碳的存在。它们之间的关系如下图所示。(图中“—”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质。 )试回答以下问题。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
子轩教育学科教师辅导教案3)能使 CuSO 4 粉末变蓝的气体是水蒸气。
4)在 O 2 中燃烧火星四射的物质是 Fe 。
5)在空气中燃烧生成 CO 2和 H 2O 的物质是有机物 如 CH 4 C 2H 5OH 等 6)不能溶于盐酸或稀 HNO 3 的白色沉淀有 AgCl 、BaSO 4。
4. 以元素或物质之最为突破口:5)相对分子质量最小 . 密度最小的气体是 H 2 6)相对分子质量最小的氧化物是 H 2O 。
7)自然界中硬度最大的物质是金刚石 8)最简单的有机物是 CH 4。
9)最常用的溶剂是 H 2O 。
10)人体中含量最多的物质是 H 2O 。
5. 抓唯一特性在空气中能自燃的固体是白磷;能使带火星的木条复燃的气体是O 2;溶于水显碱性、且能使湿润的红色石蕊试纸变蓝的气体是 NH 3;在氧气中剧烈燃烧 .火星四射 .生成黑色固体 的物质是铁;油状液体、且能使纸张、木材变黑的物质是浓硫酸。
6. 抓物质的性质① 具有刺激性气味的大气污染物: SO 2② 与黑色氧化铜反应生成红色物质 (铜)的物质(具有还原性的物质) :CO 、H 2、C③ 能使人发生煤气中毒的气体: CO1)地壳中含量最多的元素是 2)人体中含量最多的元素是 3)空气中含量最多的元素是4)形成化合物最多的元素是O.含量最多的金属元素是 Al O 。
N 。
C 。
④误作食盐. 用于烹饪. 使人食物中毒的盐:亚硝酸盐;⑤与碱反应. 产生有刺激性气味且使湿润的红色石蕊试纸变蓝的气体(NH3) 的盐是铵盐;⑥具有挥发性的酸:盐酸、硝酸;⑦在空气中质量增加且变质的是氢氧化钠、氧化钙;⑧放在空气中质量增加但不变质的酸:浓硫酸。
6. 抓常见物质的用途①用于人工降雨的物质:干冰;②调味用的食盐:氯化钠;③常用于金属除锈:稀硫酸、盐酸;④改良酸性土壤的物质:生石灰、熟石灰;⑤工业上常用做洗涤剂的盐:碳酸钠;⑥“钡餐”透视用的盐:硫酸钡;⑦人体中的胃酸:盐酸;7. 以化学反应的特殊现象为突破口特殊的反应现象常作推断题的突破口. 例如:氨气能使湿润的红色石蕊试纸变蓝;硫在空气中燃烧发出淡蓝色的火焰. 而在氧气中燃烧则发出蓝紫色火焰;白磷、红磷燃烧产生大量的白烟;铁在氧气中燃烧火星四射;能溶于盐酸或稀HNO3 的白色沉淀有CaCO3、BaCO3、Mg(OH2)、Al(OH) 3;不溶于稀HNO3的白色沉淀有AgCl、BaSO4 等等。
抓化学之最空气中体积分数、质量分数最大的物质是N2;地壳中含量最多的元素是氧. 含量最多的金属元素是铝;生物细胞中含量最多的元素是氧;形成化合物种类最多的元素是碳;动植物体内含量最多的物质是水;相对分子质量最小的氧化物是水;硬度最大的天然物质是金刚石;最软的矿物之一是石墨;金属活动性顺序中最活泼的金属是钾;最简单的有机物是甲烷;不含中子的原子是氢原子;最理想的燃料是氢气;最常用的溶剂是水;人类应用最早的金属是铜;当今世界上最重要的三大矿物燃料是煤、石油、天然气;检验水的最简便的方法是用无水硫酸铜。
8. 抓物质的热效应①溶于水吸热的物质:硝酸铵;②溶于水放热的物质:氢氧化钠、浓硫酸;③与水反应放热的物质:氧化钙。
9. 、以物质之间的转化关系为突破口1)三角形转化关系2)酸、碱、盐、金属氧化物之间的相互关系初中化学推断题常用“题眼”归纳题型实例讲解1. (2014? 南宁)某碳酸钾固体样品. 可能含有硫酸钾、碳酸钙、硫酸铜、氯化钾、氯化钙中的一种或几种杂质为了确定杂质的成分. 进行以下实验:①取少量样品溶于水得到无色溶液.然后滴加过量的氯化钡溶液. 出现白色沉淀 A.过滤.②沉淀 A 中加入过量的稀硝酸. 沉淀部分消失并放出气体.往步骤①所得的滤液中加入适量硝酸银溶液和稀硝酸生成白色沉淀 B. 过滤.回答下列问题:(1)白色沉淀B是. 步骤②中放出的气体是.(2)杂质中一定含有. 一定没有.(3)最终所得滤液中含有的阳离子是.2.有一包白色粉末. 可能由氯化银、碳酸钠、氢氧化镁、氯化钡、硫酸钠和硝酸钾中的某几种组成。
为了鉴定其成分. 实验如下:(1)将少量粉末放入足量水中. 搅拌、静置、过滤、得白色沉淀和无色滤液。
(2)向所得沉淀中加入足量稀硝酸. 沉淀全部溶解. 但无气体产生。
(3)向滤液中滴加硝酸银溶液.有白色沉淀生成. 加入足量稀硝酸.沉淀不溶解。
试根据以上现象推断该白色粉末中一定含有;一定没有;可能含有。
(填化学式)3.某化工厂排放的污水中.常溶有某些对人体有害的物质。
通过目测. 初步认为可能含有Fe3+、Ba2+、Na+、OH-、CI -、CO32-、SO42-;为了进一步确认.进行实验检测:(1)取污水仔细观察. 呈无色、透明、均一状态。
(2)向取样的污水中.滴入稀硫酸.有大量白色沉淀产生.再加稀硝酸. 白色沉淀不消失。
3)用pH试纸测定污水的pH值. 试纸显深蓝色。
由此可知. 该污水中. 肯定含有离子是。
肯定没有的离子是可能含有的离子是。
图11.(2015? 汕尾) A ~ E 是初中常见的物质:盐酸、氢氧化钠、氢氧化钙、碳酸钠、二氧化碳中的某一种.A 可用于金属表面除锈 .B 可用来改良酸性土壤.它们相互间发生反应或转化的关系如图所示(“﹣”表面两种物质间能发生反 应 .“→”表示两种物质间的转化关系). (1)A 、C 的化学式分别为 (2)E →D 反应的化学方程式为B 与 D 反应的化学方程式为. 其中部分反应物、生成物及反应条件已略去. . 则丙的化学式为 ;. 甲、乙、丙都为金属 . 则它们的金属活动性由强到弱的顺序是 . 丙溶液为蓝色 . 则丙生成乙的化学方程式为 写一个);②若甲为常见的碱 .且相对分子质量为 74. 甲、乙、丙含相同的金属元素 .丙溶液为无色 .则丙生成乙的化学方程式为 写一个).3. (2016 湖北省黄冈市) 12. A ~E 为初中化学常见的物质。
它们有下图所示的转化关系 .图中“—”表示相连的物质间能相互发生反应 . “→”表示物质间有相应的转化关系。
其中 .A 、B 都是黑色固体 .通常状况下 .C 是一种能使澄清石 灰水变浑浊的气体 .D 溶于水形成蓝色溶液 . 常用于配制一种具有杀菌作用的农药。
请回答下列问题: ⑴物质 C 的化学式是 ⑵写出下列反应的化学方程式: ① ;② ⑶物质 E 所属的类别可能是(写出一种物质的类别) 三、关系式型推断题1. (2016 绵阳) A ~F 是初中常见的化合物 . 有如下转化关系(部分生成物已省略).其中 可用于灭火 .F 俗名纯碱.题型二、框图型 ;D 在生活和生产中的一种用途是2. (2016 厦门)无机物甲、乙、丙经一步反应的转化关系如图所示 (1)若反应皆为化合反应 . 且均在点燃条件下发生 ( 2 )若反应皆为置换反应. 且均在溶液中举行(用“甲”、“乙”、“丙”表示); (3)若反应皆为复分解反应 . 乙为白色难溶物.①若甲为常见的酸 . 甲、乙、丙含相同的原子团图3A 是大理石的主要成分 .C图2(2)E与 F 反应的化学方程式为.(3)反应I 的化学方程式为. 该反应是反应(填基本反应类型).(4)A、E均能与盐酸反应. 反应的化学方程式分别为、.2. (2016河北)河北省)A~J表示初中化学常见的物质.其中.B 可用在铅酸蓄电池中、G是最清洁燃料、H是蓝色沉淀. 各物质间相互转化关系如图12 所示。
请回答下列问题:(1)G的化学式为。
(2)E 的一种用途是。
(3)反应④的基本反应类型为。
(4)反应③的化学方程式为。
3. (2016? 兰州)A﹣K为中学常见的物质.其中A为黑色粉末.H 是一种建筑材料的主要成分. 它们之间的转换关系如图所示.(1) D.F 的化学式: D .F ;(2)①的基本反应类型是;(3)反应②的化学方程式是;(4)气体 E 的用途是.四、表格型推断题1、有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。
将其任意编号:A、B、C、D、E. 进行两两混合其现象如下表:请回答下列问题:(1)E 的俗名. 写出物质 E 在农业上的一种用途(1)试推断并写出五种溶液中溶质的化学式。
A .B .C .D .E (2)写出有关反应的化学方程式。
A+E:B+E :2、现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠 4 瓶失去标签的溶液 . 分别编号为 A 、B 、C 、D 。
每次取少量溶液两两混合所观察到的现象记录在下表中(“—”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)。
由此推断 4 瓶溶液中的溶质的化学式分别为:课后作业( 2013 厦门 9 分)几种常见物质之间的相互转化关系如图 8 所示(各字母代表一种物质 . 部分反应物、生成物及 反应条件略去)。
己知: ① 五种物质均含铜元素 .且化合物中铜元素的化合价均为 + 2 ; ② A 为单质.在空气中 加热后生成黑色物质 B ; ③ X 溶液与铁反应可得到 A ; ④ X 溶液与氯化钡溶液反应可得到 D . 同时有白色沉淀生成; ⑤ D 溶液中加入少量的氢氧化钠溶液得到 E 。
结合信息推断: (1) B 的化学式是 。
(2)D →E 的反应基本类型是 ___________ ; E 与某种酸反应可实现 E →X 转化.该酸的名称是 _________ 。
(3)写出以下转化的化学方程式: X → A : ;X → D : _____________________ 。
2.(兰州 7 分)已知 A —H 均为初中化学常见的物质。
其中 A 、C 是组成元素相同的气体 . 且 C 能产生温室效应; B 为红棕色 . 是赤铁矿的主要成分; F 是紫红 色金属; H 是蓝色沉淀。
根据右图所示的转化关系 (图中 反应条件均已略去) . 请回答:( 1)写出下列物质的化学式: B 、 C; ( 2)写出下列反应的化学方程式:① ;② . 反应②的基本反应类型是 。
1.( 9 分)(1)CuO (2)复分解反应;硫酸。
( 3) CuSO 4+Fe=Cu+FeSO 4 ; CuSO 4+BaCl 2=CuCl 2+BaSO 4↓。
2. (1) Fe 2O 3 CO 2( 2)① Fe+CuSO 4 = FeSO 4+Cu (合理答案均可)② CuSO 4+2NaOH=Cu (OH )2↓+Na 2SO 4(合理答案均可) 复分解反应 (化学方程式 2分.其余每空 1分.共 7分)A .B .C.D1. ②的化学方程式分别为、;试剂 B 是(填化学式)溶液;反应③的发生需要氧气和水. 其化学方程式图17. (2013荆州 4 分)下图中 A ~ H 都是初中化学中常见的物质.已知A、B都是黑色固体.D、F为红色固体. 它们之间1)写出物质 A 的化学式;2)写出上述物之间转化时发生化合反应的化学方程式:;3)转化过程③可用化学方程式表示为:4)已知转化过程④在常温下就能进行. 该化学反应的基本类型为反应。
