某公司内部的CRISPR-Cas9操作流程
基因编辑技术CRISPRCas9的详细操作步骤

基因编辑技术CRISPRCas9的详细操作步骤基因编辑技术CRISPR-Cas9是一种革命性的工具,能够精确切割和修改DNA 序列。
它已被广泛应用于实验室研究、农业、医学和生物技术领域。
CRISPR-Cas9的操作步骤分为设计目标序列、构建修饰体、细胞转染、筛选、验证等几个阶段。
以下是基因编辑技术CRISPR-Cas9的详细操作步骤:1. 设计目标序列首先,确定要编辑的基因序列。
识别目标区域,通常选择高度保守的DNA 区域,以最大程度减少非特异性修饰。
目标序列的设计需要遵循一些规则,例如避免重复、剪切酶的PAM序列靠近目标区域等。
2. 构建修饰体根据设计的目标序列,构建CRISPR修饰体。
修饰体通常由CRISPR核酸(包括crRNA或sgRNA)和Cas9核酸组成。
crRNA(或sgRNA)负责定位到目标序列,Cas9则负责剪切目标序列。
合成修饰体的DNA或RNA序列后,可以使用PCR扩增或化学合成的方法得到修饰体。
3. 细胞转染将构建好的修饰体转染至目标细胞中。
转染可以选择不同的方法,例如化学法、电穿孔法、超声波法或病毒载体等。
转染后,修饰体会逐渐进入目标细胞,并开始作用于基因组。
4. 筛选在转染后,大部分细胞仍然具有未被编辑的基因组。
为了筛选出完成编辑的细胞,可以使用筛选方法。
最常用的方法是通过引入荧光蛋白标记的修饰体,利用流式细胞术或显微镜检查标记的细胞。
5. 验证对于筛选出来的细胞,需要进行进一步的验证。
最常用的方法是通过测序确认基因组是否发生了预期的编辑。
此外,也可以使用T7E1酶切或限制性内切酶消化等方法,进一步验证编辑效果的准确性。
总结起来,基因编辑技术CRISPR-Cas9的详细操作步骤包括设计目标序列、构建修饰体、细胞转染、筛选和验证等几个阶段。
通过遵循这些步骤,研究人员可以实现对目标基因组的精确编辑,进而揭示基因功能、治疗遗传疾病,并在农业和生物技术领域开拓新的应用前景。
基因编辑技术CRISPRCas9的使用教程与最佳实践分享

基因编辑技术CRISPRCas9的使用教程与最佳实践分享在现代生物学研究中,基因编辑技术的出现为研究人员提供了一种高效、精确、低成本的方式来研究基因功能和调控机制。
CRISPR-Cas9系统作为一种革命性的基因编辑工具被广泛应用于基因组编辑、疾病治疗和农业改良等领域。
本文将为您介绍CRISPR-Cas9基因编辑技术的使用教程,并分享一些最佳实践。
CRISPR-Cas9基因编辑技术概述CRISPR-Cas9是一种依靠细菌天然的免疫机制发展而来的基因编辑技术。
CRISPR是一种特殊的DNA序列,可与Cas9酶一起,通过识别和切割DNA序列来精确编辑基因组。
CRISPR-Cas9系统的主要组成部分包括CRISPR RNA (crRNA)、转录单元结构化RNA(tracrRNA)和Cas9酶。
crRNA负责识别目标DNA序列,而tracrRNA将crRNA与Cas9酶结合起来形成活跃的CRISPR-Cas9复合物。
CRISPR-Cas9基因编辑技术的使用教程1. 设计并合成RNA引导序列在使用CRISPR-Cas9进行基因编辑之前,首先需要设计并合成RNA引导序列。
该序列用于指导Cas9酶精确识别和切割目标基因组DNA。
合成的RNA引导序列通常由crRNA和tracrRNA合成而成,也可以合成一个融合的single-guide RNA (sgRNA)。
2. 构建CRISPR-Cas9载体CRISPR-Cas9基因编辑需要将Cas9酶和RNA引导序列导入目标细胞内。
可使用载体如质粒或病毒进行基因编辑构建。
选择合适的载体需考虑目标细胞类型、转染效率和所需编辑范围等因素。
将Cas9基因和RNA引导序列克隆至载体后,可通过转染或病毒介导转染等方法将其导入目标细胞。
3. 确定编辑效果在导入CRISPR-Cas9系统后,使用分子生物学方法来验证编辑效果。
例如,PCR、测序、Western blot或免疫组化等技术可以用于检测目标基因的突变、修复或敲除效果。
(仅供参考)某公司内部的CRISPR-Cas9操作流程
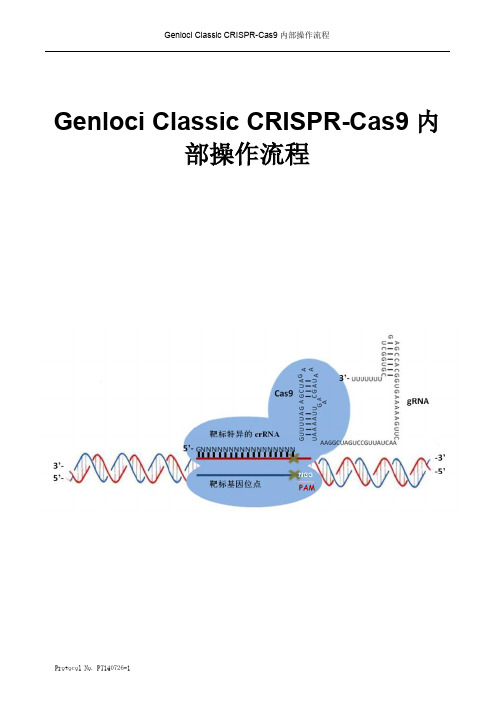
Genloci Classic CRISPR-Cas9内部操作流程Protocol No. PT140726-1Protocol No. PT140726-11,CRISPR-Cas9基因编辑实验流程图如下:pGK1.1U6 CACC G CAAA 4 55’ -5’3’-3’ -- ~20bp2,操作步骤实验前,请您务必做好以下验证实验:A.单细胞生长情况,确保单个细胞可以正常生长形成单克隆,即,低密度的细胞在培养皿中可以形成单克隆。
B.目的基因的表达情况分析,为防止因染色体缺失等情况导致靶基因缺失,首先需要PCR扩增靶基因,并对PCR结果进行测序,确保靶基因的完整存在;其次,您还可以用RT-PCR分析靶基因的活跃度。
1. 设计Oligo DNA序列首先,您需要在靶标DNA区域中设计一对20bp左右的oligo DNA,您可以通过以下在线工具设计:●麻省理工学院的CRISPR Design:/●德国癌症研究中心的E-Crisp:/E-CRISP/designcrispr下面我们选择麻省理工学院的CRISPR Design工具来做设计举例,以Fut8基因为例,一次只能输入大小为23~250bp的基因片段,最好一次只输入一个外显子,避免Guide序列跨内含子的。
点击“Download as genbank”按钮,出现以下界面:“Fut8”Array根据左边的score的高低选取合适的Guide序列,以Guide#1序列为例,2条单链oligo的序列如下(红色字体部分是要与Bbs I酶切后的载体相互补的部分):Fut8-F: cacc G AATGAGCATAATCCAACGCCFut8-R: aaac GGCGTTGGATTATGCTCATTC※注意:oligo DNA设计序列的第一个碱基必须是G,如果你选取的Guide序列的第一个碱基不是G,可自行加一个G上去。
另外,需在位点上下游各设计一条引物,用于后续PCR或测序检测阳性克隆,引物能扩增约300bp 的DNA片段,上游引物距突变位点约100bp,下游引物距突变位点约200bp。
CRISPRCas9基因编辑操作步骤及详细说明

CRISPRCas9基因编辑操作步骤及详细说明实验材料与方法一、细胞培养人宫颈癌细胞 HeLa,常规培养使用含 10% FBS 的 DMEM 培养基 ( 含 1.5 mg/L-Glutamine,100 U/mL Penicillin,100 μg/mL Streptomycin) 中,37ºC 5% CO2 饱和湿度培养箱中培养。
二、基因信息及双 gRNA 设计基因信息及分析1.hsa-mir-152 基因信息:pubmed2.hsa-mir-152 基因位于蛋白编码基因 COPZ2 内含子内,敲除hsa-mir-152 基因不会影响该蛋白编码3.hsa-mir-152 precursor 序列(87 bp):TGTCCCCCCCGGCCCAGGTTCTGTGATACACTCCGACTCGGGCTCTGGAGCAGTCAGTGCATGACAGAACTTGGGCCCGGAAGGACC双 gRNA 设计使用在线 gRNA 设计软件在 hsa-mir-152 precursor 基因组序列两侧设计双 gRNA注:dgRNA 即为双 gRNA.三、慢病毒侵染实验材料及试剂DMEM 培养基 + 10% FBSD-Hank’s SolutionTrypsin-EDTA Solution96 孔板24 孔板Lentivirus- 病毒液(GenePharma)步骤靶细胞侵染实验1.靶细胞铺板:24-well,加入2.5×105 cells/well(根据细胞种类调整),0.5 mL 完全培养基,37℃,5% CO2 过夜;2.稀释病毒:稀释液(靶细胞维持液培养基)400 μL + 终浓度 5 μg/mL Polybrene,将慢病毒原液按 1:9 加入到稀释液中;3.移去 Step1 中细胞培养液,加入 Step2 稀释后的病毒液,同时建立对照(blank、negative),37℃,5% CO2 过夜;4.12~24 小时移去细胞侵染后的病毒液,加入 0.5 mL 完全培养基,37℃,5% CO2 过夜;5.根据细胞状态和类型,如果必要分出 1/3~1/5,加入0.5 mL 完全培养基,继续培养 24~48 小时,荧光倒置显微镜下观察结果。
CRISPRCas9基因敲除细胞株详细构建流程

CRISPRCas9基因敲除细胞株详细构建流程Puro 抗性浓度摸索实验将细胞如下图1稀释。
给药7天后,弃培养液,用台盼蓝染色2 min,显微镜下观察细胞存活情况。
确定细胞多克隆细胞筛选和单克隆细胞筛选浓度。
图1 抗性浓度摸索单克隆形成验证实验细胞计数,将细胞悬液稀释混匀后加入96孔板,用封口胶将孔板封好,放于培养箱中培养。
静置培养48 h后每日观察并记录单克隆形成情况。
sgRNA 靶标设计根据基因序列信息,设计 sgRNA。
靶标位点序列信息确认PCR扩增(图2),测序验证基因序列,以确定sgRNA区域有无SNP。
图2 靶标序列扩增sgRNA克隆引物合成根据sgRNA设计sgRNA克隆引物。
lentiCRISPRv2-sgRNA载体构建退火,连接,转化,涂板(LB/Amp)培养。
lentiCRISPRv2-sgRNA载体验证每个实验组各挑取6个单克隆菌落,于LB/ Amp培养基中扩增,提取质粒,琼脂糖凝胶电泳检测质粒抽提效果(图3)。
图3 质粒抽提酶切验证:取3个单克隆进行酶切,琼脂糖凝胶电泳检测酶切效果(图4)。
选择2个样品送样测序。
图4 单克隆酶切验证病毒包装lentiCRISPRv2-sgRNA无内毒素质粒提取,病毒包装。
细胞转染配制梯度病毒稀释液,细胞于培养箱中静置培养48h。
阳性单克隆细胞株筛选细胞转染48h后,更换完全培养基,筛选至对照组大部分细胞死亡,实验组细胞扩大培养,进行单克隆筛选。
几天后挑选阳性单克隆进行扩增,并取样验证。
阳性单克隆细胞株验证测序验证阳性单克隆细胞株的基因序列,以确定是否敲除成功。
实验结果示例:该基因有两个单克隆细胞株,A1和A2。
单克隆细胞A1的目的基因在sgRNA2位置出现两种突变形式,分别缺失1个和19个碱基,在新序列的第337位和第355位碱基提前出现终止密码子。
单克隆细胞A2的目的基因在sgRNA2位置发生突变,插入1个碱基,在新序列的第340位碱基提前出现终止密码子。
CRISPR-Cas9体系实验流程(2)

CRISPR-Cas9体系实验流程(2)一、材料试剂准备1)质粒:pSpCa9(BB)(AddgeneplamidID:42230),若实验用gRNA为PCR扩增纯化产物,则需要该质粒做为U6的模版。
pUC19(Invitrogen,cat.no.15364-011)可用于构建gRNA,若用PCR 产物进行转染,则需要该质粒来进行共转染,做为DNAcarrier。
上述三种质粒,根据实验选择gRNA的表达方式(PCR产物/单载体系统/双载体系统)来确定具体使用哪种。
2)超纯水,DNae/RNae-free(LifeTechnologie,cat.no.10977-023) 3)高保真聚合酶,KapaHiFi(KapaBioytem),PfuUltra(Agilen),HerculaeIIfuionpolymerae均可,只需保真效果好,扩增过程不产生突变。
4)TaqDNApolymeraewithtandardTaqbuffer(NEB,cat.no.M0273S)用于一般检测。
5)QIAquickgele某tractionkit(Qiagen,cat.no.28704)6)QIApreppinminiprepkit(Qiagen,cat.no.27106)7)FatDigetBbI(BpiI)(Fermenta/ThermoScientific,cat.no.FD1014),如需要将gRNA构建到pSpCa9(BB)-2A-GFP质粒上,则需要该酶。
8)T7DNAligaewith2某rapidligationbuffer(Enzymatic,cat.no.L602L).或者T4DNAligae,二者无区别。
12)T4polynucleotidekinae(NewEnglandBioLab,cat.no.M0201S)13)PlamidSafeATP-dependentDNae(Epicentre,cat.no.E3101K)14)Adenoine5′-triphophate,10mM(NewEnglandBioLab,cat.no.P0756S)15)SOCmedium(NewEnglandBioLab,cat.no.B9020S)二、实验流程或者人工手动选择,在目的区域5′-NGG(即PAM)上游20bp片段均可做为targetite,一般targetite可选在正义链或者反义链,二者均可。
crispr-cas9复合体构建流程

crispr-cas9复合体构建流程1.为了构建CRISPR-Cas9复合体,首先需要设计和合成cas9核酸序列。
In order to construct the CRISPR-Cas9 complex, it is necessary to design and synthesize the Cas9 nucleic acid sequence.2.接着需要选择适当的crispr RNA或gRNA序列,与cas9相结合以指导靶向基因组的位置。
Then, an appropriate CRISPR RNA or gRNA sequence needs to be selected to guide the Cas9 to the targeted position in the genome.3.将设计好的cas9和crispr RNA或gRNA序列合并形成合成DNA 片段。
The designed Cas9 and CRISPR RNA or gRNA sequences are combined to form a synthetic DNA fragment.4.制备好的合成DNA片段需要进行定向克隆到适当的表达载体中。
The prepared synthetic DNA fragment needs to be directionally cloned into an appropriate expression vector.5.表达载体通常需要包含启动子、编码区和终止子,以确保目标基因能够被正确表达。
The expression vector usually needs to contain a promoter, coding region, and terminator to ensure proper expression of the target gene.6.将构建好的表达载体转化到大肠杆菌或酵母等宿主细胞中。
CRISPR实验流程

CRISPR实验流程CRISPR/Cas9 实验流程交流企鹅: 2621697472(大家做哪块?)一、利用Cas9质粒建立knock-out细胞系实验的详细过程1.1 确定待敲除基因的靶位点1.2 设计识别靶位点的识别的一对DNA Oligo(引物)1.3 构建表达sgRNA的质粒1.4 sgRNA活性检测1.5 利用Cas9质粒建立knock-out细胞系1.1、确定待敲除基因的靶位点根据提供的物种、基因名称或者基因ID在NCBI或ENSEMBLE中进行查找。
找到该基因CDS区,分析相应的基因组结构,明确CDS的外显子部分。
按照基因本身的性质,选择候选的待敲除位点,确定待敲除位点。
对于蛋白编码基因,如果该蛋白具重要结构功能域,可考虑将基因敲除位点设计在编码该结构域的外显子;如果不能确定基因产物性质,可选择将待敲除位点放在起始密码子ATG后的外显子上。
如果是microRNA,可以将待敲除位点设计在编码成熟microRNA的外显子或在编码成熟microRNA的外显子的5’和3’侧翼序列。
1.2、设计识别靶位点的一对DNA Oligos确定待敲除位点后,选择23-至250bp的外显子序列输入到在线免费设计sgRNA的软件Input框中(/),然后进行设计运算,软件会自动输出sgRNA序列(网站设计一般很慢或数据输出不完整,可使用我的内部软件,2天内输出全部结果,无物种限制)。
一般地,基因特异的sgRNA模板序列为位于PAM序列(Protospacer Adjacent Motif)前间区序列邻近基序,这是一种见于crRNA分子的短核苷酸基序,可以被Cas9蛋白特异性识别并切割)的20个nt。
而PAM序列的特征为NGG(其中N为任意核苷酸)。
因此,sgRNA模板序列选择非常方便,即使没有软件,研究者也可手工进行选择。
不过,在线软件可以给出该序列在基因组中存在相似序列的情况,即可能的脱靶位点。
因此,利用在线软件可以选择脱靶机会小的序列作为sgRNA模板序列。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Genloci Classic CRISPR-Cas9内部操作流程Protocol No. PT140726-1Protocol No. PT140726-11,CRISPR-Cas9基因编辑实验流程图如下:pGK1.1U6 CACC G CAAA 4 55’ -5’3’-3’ -- ~20bp2,操作步骤实验前,请您务必做好以下验证实验:A.单细胞生长情况,确保单个细胞可以正常生长形成单克隆,即,低密度的细胞在培养皿中可以形成单克隆。
B.目的基因的表达情况分析,为防止因染色体缺失等情况导致靶基因缺失,首先需要PCR扩增靶基因,并对PCR结果进行测序,确保靶基因的完整存在;其次,您还可以用RT-PCR分析靶基因的活跃度。
1. 设计Oligo DNA序列首先,您需要在靶标DNA区域中设计一对20bp左右的oligo DNA,您可以通过以下在线工具设计:●麻省理工学院的CRISPR Design:/●德国癌症研究中心的E-Crisp:/E-CRISP/designcrispr下面我们选择麻省理工学院的CRISPR Design工具来做设计举例,以Fut8基因为例,一次只能输入大小为23~250bp的基因片段,最好一次只输入一个外显子,避免Guide序列跨内含子的。
点击“Download as genbank”按钮,出现以下界面:“Fut8”Array根据左边的score的高低选取合适的Guide序列,以Guide#1序列为例,2条单链oligo的序列如下(红色字体部分是要与Bbs I酶切后的载体相互补的部分):Fut8-F: cacc G AATGAGCATAATCCAACGCCFut8-R: aaac GGCGTTGGATTATGCTCATTC※注意:oligo DNA设计序列的第一个碱基必须是G,如果你选取的Guide序列的第一个碱基不是G,可自行加一个G上去。
另外,需在位点上下游各设计一条引物,用于后续PCR或测序检测阳性克隆,引物能扩增约300bp 的DNA片段,上游引物距突变位点约100bp,下游引物距突变位点约200bp。
将设计后的序列送到值得信赖的公司合成,纯化级别为PAGE。
2. T4 DNA Ligase连接将合成后的2条单链oligo DNA退火形成双链DNA,再与载体连接,pGK1.1 linear vector是线性化载体,无需酶切处理,可直接用于T4 DNA Ligase连接反应,pGK1.1载体已经优化过,其转染和敲除的效率比一般CRISPR载体更高。
Protocol No. PT140726-1Protocol No. PT140726-1退火反应体系如下:将以上体系瞬时离心后,置于PCR 仪中95℃孵育3min ,孵育后自然冷却20min 。
取1.75μl 的杂交后的双链DNA 进行T4 DNA Ligase 连接反应,反应体系如下:pGK1.1 linear vector 2μl双链DNA1.75μl T4 DNA Ligase 1μl 10xT4 DNA Ligase Buffer 1μl ddH 2O 4.25μl 10μl※注意:请您根据步骤1自行设计正链Oligo 序列和负链Oligo 序列,合成后的2条单链 oligo DNA 退火复性成双链DNA ,再进行T4 DNA Ligase 连接反应。
连接产物可以直接转化DH5a 高效感受态细胞,转化和筛选阳性克隆的实验步骤请您参考《分子克隆实验指南》,pGK1.1的抗性为卡那霉素抗性,筛选后的阳性克隆,需测序验证序列的正确性。
3. 电转染靶细胞(推荐)转染前进行质粒大提,确保质粒浓度≥2μg /μl 浓度,再取4~7μg 进行电转染靶细胞,推荐使用Celetrix 细胞电转仪(型号:CTX-1500A),贴壁细胞的数量需1x106~3x106,悬浮细胞的数量需3x106~5x106。
另外,您也可以使用转染试剂转染靶细胞。
4. 混合克隆pool 检测48-72小时后做有限稀释,一般5块板足够,并取电转后细胞的pool 1000个细胞以上离心,去上清,PBS 洗一遍,细胞沉淀溶于适量的PBS 中,煮5min 后模板就制备好了,剩余的pool 细胞冻存。
PCR 检测(以Fut8基因为例):11步骤所制备的模板 5ulFut8-seq-F(10mM): 1ul Fut8-seq-R(10mM): 1ul dNTP Mixture(10mM each): 1ul Taq 酶: 0.5ul 10XTaq 酶buffer : 5ul Mgcl 2 3ulH2O: 33.5ul Total 50ul 程序: 95℃ 2min cycles 1x 95℃ 20SX ℃ 20S72℃ 30S72℃ 5min cycles 1x 95℃ 变性 5minPCR 产物使用Cruiser TM 酶切15-20分钟,酶切产物1%-1.5%凝胶电泳。
正链Oligo(100μM) 0.5μl负链Oligo(100μM)0.5μl ddH 2O18μl Annealing Buffer(20x)1μl 20μl}cycles 35x上图为混合克隆pool酶切检测,由此图可知此混合克隆pool中有敲除成功的细胞,则进行下一步并计算突变率。
5. Cruiser TM筛选阳性克隆将剩余的pool的靶细胞有限稀释后,分到96孔板中进行单克隆培养,如果靶细胞是悬浮细胞,推荐使用Cell Plaza™(Cat.No.: GP08250)培养细胞,待细胞长好后,取1000个左右的细胞,提基因组,推荐使用Genloci TNA抽提试剂盒(Cat.No.: GL10851S)。
然后使用核酸内切酶初步筛选阳性克隆,推荐使用Genloci Cruiser TM突变检测试剂盒(Cat.Nos.: GCMD025, GCMD100),对Cruiser TM筛选后的阳性克隆进行测序分析,并对碱基缺失结果进行比对分析。
Protocol No. PT140726-1IV.FAQQ-1:靶位点设计有哪些注意事项A-1:目前有几个在线设计软件,我们推荐使用Zhang Feng lab:/,该软件会对每一个潜在的靶位点打分,并告知是否存在脱靶现象。
在设计Guide序列时,需要特别注意第一个碱基必须是G,如果您选取的Guide序列的第一个碱基不是G,需要自行加上一个G,因为这个G对于起始转录非常重要。
Q-2:转染效率低,怎么办?A-2:因为Cas9蛋白比较大,就导致整个敲除质粒较大(8kb左右),如此大的质粒很容易导致转化效率低下,尤其是使用脂质体等化学试剂转染时,转染效率会比较低些。
所以,我们推荐使用电转的方法进行转染。
Bio-Rad的电转仪器需要根据不同的细胞单独配制转染buffer,所以不推荐使用;Life的Neon系统不错,但是因为耗材是镀金的,所以非常贵;而Genloci的CTX-1500A电转仪,转化效率高,不需要单独配制buffer,只需使用无血清的培养基就行,而且该电转仪的耗材也是相对比较便宜的。
Q-3:单个细胞不生长,怎么办?A-3:对于单细胞不长的细胞进行敲除,首先建议采用共培养的方法看看能否促进单个细胞的生长。
共培养可以采用培养过同种细胞的培养基培养单细胞;也可以使用Cell Plaza TM(单细胞培养板),可以把细胞的存活率提高三倍以上。
如果以上方法都不行,建议对细胞进行改造,加快其分裂速度,让单细胞可以很容易生长后,再对目的基因进行敲除。
具体方法可以联系Genloci的客服做进一步的了解。
Q-4:在做高通量样本时,如何才能快速筛选得到阳性克隆?A-4:建议使用错配酶进行筛选,可加快筛选的流程。
目前市面上主要有三种错配酶:Cruiser TM酶、T7E I 和Surveyor酶。
其中,Cruiser TM酶和Surveyor酶属于Cel I家族,这两种酶的筛选特异性比T7E I高。
在酶切筛选过程中,T7E1的特异性较差,容易出现假阳性的结果,这在一定程度上阻碍了阳性克隆的筛选进度;Surveyor酶较贵,并且货期较长,所以我们推荐Cruiser TM酶,它特异性高且价格合理。
Protocol No. PT140726-1Protocol No. PT140726-1VI .附录附录A pGK1.1 linear Vector以下为pGK1.1的插入位点示意图和质粒图谱,线性化pGK1.1所用的酶为Bbs I 。
Figure 3. pGK1.1插入位点图示Figure 4. pGK1.1质粒图谱pGK1.1:Protocol No. PT140726-1 Genloci Biotechnologies Inc.VII Cruiser TM 操作说明1,操作步骤1) 基因组 D NA 的准备提取细胞的基因组 DNA ,推荐使用 Genloci 公司专为阳性克隆筛选设计的 TNA 抽提试剂盒(Cat. No.: GL10851S ),只需 500 个左右的细胞即可提取全基因组 D NA ,详细实验步骤请参看 G enloci TNA 抽提试 剂盒(Cat. No.: GL10851S )说明书。
2) 杂交 D NA 的准备a) 第一轮和第二轮(巢式)PCR 引物设计分别设计 F irst Primers 和 N ested Primers 。
其中 F irst Primers 要求具有较高的特异性,其扩增产物推 荐为 500~1000 bp ,Nested Primers 推荐扩增产物长度为 300~600bp 。
First Primers 和 N ested Primers 引物对应目的序列的位置如下:模板 DNA第一轮 PCR 产物第二轮(巢式)b) 第一轮P CR:获得目的片段将已经提取的基因组作为模板,使用F irst Primers,以高保真D NA 聚合酶扩增获得目的片段,要求目的片段明亮(允许少量杂条带,以及少量弥散)。
同时获得野生型模板扩增产物和突变型模板扩增产物。
推荐扩增循环数35~40 cycles,反应体系25 μl,100 ng≤模板量≤300 ng。
PCR 完成后,取7~8 μl 进行电泳检测。
c) 第二轮(巢式)PCR:获得杂交D NA根据第一轮P CR 电泳检测中目的条带的亮度,用无菌去离子水稀释扩增产物(可参照M arker 的亮度估算产物中DNA 的浓度,稀释至总核酸浓度为10~20 ng/μl,一般需要稀释10~50 倍)。
其中野生型模板扩增产物标记为:WT DNA;待检测的突变型模板扩增产物标记为:MT DNA;根据您的检测样本量的大小取合适量的稀释产物作为第二轮P CR 的模板。
