表面张力 的测定
表面张力的测试方法

表面张力的测试方法
有几种常见的表面张力测试方法,包括:
1、渗透压法。
将浸渍液滴放在物质表面上,观察滴的形状以确定表面张力的大小。
一般来说,表面张力越大,液体滴的形状越接近球形;表面张力越小,滴的形状越平坦。
2、玻璃板法。
将一块均匀涂有液体样品的玻璃板悬挂在某一支架上,然后测量板的下沉深度,通过比较不同样品的下沉深度来确定表面张力的大小。
3、悬垂法。
将一块正方形或长方形的物体悬挂在液体上,并测量物体浸入液体的深度。
通过比较不同物体在相同液体中的浸入深度来确定表面张力的大小。
4、粘度法。
通过测量液体在毛细管中的上升高度或滴下时间来确定表面张力的大小。
一般来说,表面张力越大,液体的粘度越高,上升高度越小或滴下时间越长。
- 1 -。
表面张力的测定
1、表面张力的测定:
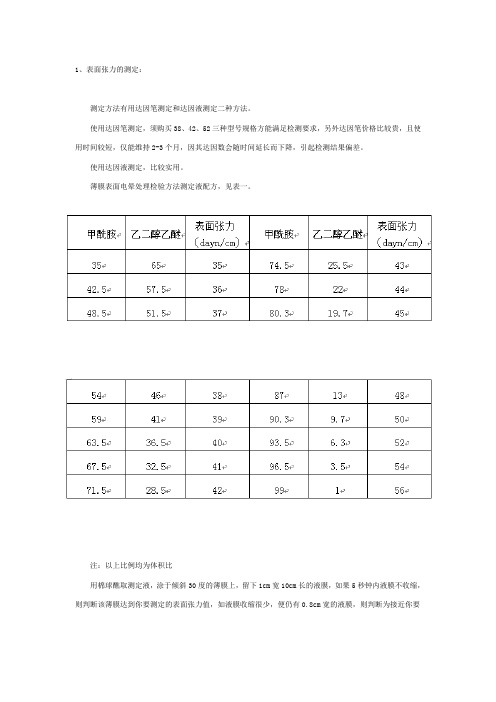
测定方法有用达因笔测定和达因液测定二种方法。
使用达因笔测定,须购买38、42、52三种型号规格方能满足检测要求,另外达因笔价格比较贵,且使用时间较短,仅能维持2-3个月,因其达因数会随时间延长而下降,引起检测结果偏差。
使用达因液测定,比较实用。
薄膜表面电晕处理检验方法测定液配方,见表一。
注:以上比例均为体积比
用棉球醮取测定液,涂于倾斜30度的薄膜上,留下1cm宽10cm长的液膜,如果5秒钟内液膜不收缩,则判断该薄膜达到你要测定的表面张力值,如液膜收缩很少,便仍有0.8cm宽的液膜,则判断为接近你要
测定的表面张力值,如液膜完全破裂,收缩成颗粒状或条状小于0.5cm宽度,则判断为该薄膜未达到你要测定的表面张力值。
(如下图)。
实验一表面张力的测定详解

2
3
平均
表面张力
(达因/ 厘米)
表面张力 降低
%
自来水
2.5%高效 氯氰菊酯 乳油500溶 液
10%吡虫 啉可湿性 粉剂1000
溶液
σ1/σ2 = N1/N2 或σ1×N1 =σ2×N2 σ1,σ2——两种液体的表面张力。 N1,N2——两种液体的滴数。 如果已知道两种液体中的一种液体的表
面张力(如:蒸馏水20℃时表面张力为 72.75达因/厘米),即可根据以上公式求 出另一种液体表面张力的相对值。
三.实验材料
3.1 药品与试剂 1%洗衣粉液、蒸馏水、自来水、10%吡
二.实验原理
在液滴脱离管口的那一刹那,该液滴的 重力等于该液滴的表面张力,可见液体 表面张力和一定容量液体自滴重器内流 出的滴数成反比,即流出液体表面张力 越大,液滴的体积也愈大,而流出的液 滴数就愈少,两种液体的表面张力之比, 等于同体积分别从同一根滴重器流出时 滴数的反比,得出以下公式:
二.实验原理
一.实验目的
表面张力小,例如减低到50达因/厘米时(蒸馏 水20℃时表面张力为72.75达因/厘米)药剂的 湿润展布能力增长,药效提高。乳油加水稀释 后,由于乳化剂的作用使原油分散成细小的油 珠,油珠直径小5微米以下,乳液稳定,洒布 均匀,覆盖面积大,药效高,并且对作物不易 发生药害,油珠直径大(10微米以上),乳液 不稳定,不仅药效低,而且容易发生药害。因 此,检查乳液中的油珠大小,可以作为鉴定乳 油质量的一项指标。
五.实验作业
根据实验,将测定结果填入各表中,求 出洗衣粉、2.5%高效氯氰菊酯乳油500溶 液、10%吡虫啉可湿性粉剂1000溶液对 水表面张力下降低的程度。(实验报告 应包括实验目的及意义、实验材料、实 验步骤和实验结果与分析):
溶液表面张力的测定实验报告

溶液表面张力的测定实验报告一、实验目的1、掌握最大气泡压力法测定溶液表面张力的原理和方法。
2、测定不同浓度正丁醇水溶液的表面张力,计算表面吸附量和表面活性剂分子的横截面积。
3、了解表面张力与溶液浓度之间的关系,加深对表面化学基本概念的理解。
二、实验原理1、表面张力在液体内部,每个分子都受到周围分子的吸引力,合力为零。
但在液体表面,分子受到指向液体内部的合力,使得液体表面有自动收缩的趋势。
要增大液体的表面积,就需要克服这种内聚力而做功。
在温度、压力和组成恒定时,增加单位表面积所做的功即为表面张力,用γ表示,单位为 N·m⁻¹或 mN·m⁻¹。
2、最大气泡压力法将毛细管插入待测液体中,缓慢打开滴液漏斗的活塞,让体系缓慢减压。
当压力差在毛细管端产生的作用力稍大于毛细管口液体的表面张力时,气泡就会从毛细管口逸出。
此时,气泡内外的压力差最大,这个最大压力差可以通过 U 型压力计测量得到。
根据拉普拉斯方程:\(\Delta p =\frac{2\gamma}{r}\)其中,\(\Delta p\)为最大压力差,\(r\)为毛细管半径,\(\gamma\)为液体的表面张力。
对于同一根毛细管,\(r\)是定值。
只要测出\(\Delta p\),就可以算出液体的表面张力\(\gamma\)。
3、表面吸附与吉布斯吸附等温式在一定温度下,溶液的表面张力随溶液浓度的变化而变化。
当溶质能降低溶剂的表面张力时,溶质在表面层中的浓度比溶液内部大,称为正吸附;反之,当溶质能升高溶剂的表面张力时,溶质在表面层中的浓度比溶液内部小,称为负吸附。
吉布斯吸附等温式为:\(\Gamma =\frac{1}{RT}\frac{d\gamma}{dC}\)其中,\(\Gamma\)为表面吸附量(单位:mol·m⁻²),\(R\)为气体常数(\(8314 J·mol⁻¹·K⁻¹\)),\(T\)为绝对温度,\(C\)为溶液浓度,\(\frac{d\gamma}{dC}\)为表面张力随浓度的变化率。
测定表面张力的实验操作指南

测定表面张力的实验操作指南实验目的:测定液体的表面张力。
实验原理:表面张力是指液体表面上的分子间相互作用力。
在液体表面,由于表面分子的自由度受到限制,分子受到的内力为向内收缩的趋势。
这种现象可以用表面张力来描述。
表面张力的测定可以通过测量液体在一定温度下液体表面凹陷或凸起的高度来进行。
根据杨氏方程,可以通过测量液体的凹陷或凸起高度来计算表面张力的数值。
实验器材:1. 试管:用于盛放液体的容器。
2. 量筒:用于测量液体的体积。
3. 针管:用于形成液体在试管内的凹陷或凸起。
4. 温度计:用于测量液体的温度。
5. 数码显微镜:用于测量凹陷或凸起的高度。
实验步骤:1. 准备工作:a. 所有器材清洗:将试管、量筒、针管等器材用去离子水进行清洗,确保无杂质干净。
b. 温度调整:将待测液体放置在恒温水浴中,使得液体温度稳定在实验所需温度。
2. 实验操作:a. 预备操作:用量筒准确地量取一定量的待测液体,并注入试管中。
b. 形成凹陷或凸起:将针管浸入试管中,先将其中的空气排出,然后再将针管插入待测液体,形成凹陷或凸起。
c. 测量凹陷或凸起的高度:使用数码显微镜,对凹陷或凸起的液面进行测量,并记录读数。
d. 温度控制:在每次测量前后,使用温度计对待测液体的温度进行测量,确保温度稳定。
3. 数据处理与计算:a. 计算表面张力:根据液体的凹陷或凸起高度数据,利用杨氏方程以及已知数据(液体密度、重力加速度等)计算表面张力。
b. 数据统计:对多次实验测得的数据进行平均,并计算测量误差。
实验注意事项:1. 液体选择:为了减小实验误差,最好选择具有较大的表面张力的液体进行实验。
2. 温度控制:确保待测液体在实验过程中温度保持稳定。
3. 器材清洗:要保证使用的器材干净,以避免干扰实验结果。
4. 液面读数:使用数码显微镜时,注意对液面的读数精度和准确性。
实验结果分析:根据实验测得的表面张力数值,可以得到不同液体表面分子间相互作用力的大小。
测定表面张力有几种方法?

测定表面张力有几种方法?测定表面张力有以下几种方法。
(1)表面张力法表面张力测定法适合于离子表面活性剂和非离子表面活性剂临界胶束浓度的测定,无机离子的存在也不影响测定结果。
在表面活性剂浓度较低时,随着浓度的加添,溶液的表面张力急剧下降,当到达临界胶束浓度时,表面张力的下降则很缓慢或停止。
以表面张力对表面活性剂浓度的对数作图,曲线转变点相对应的浓度即为CMC。
假如在表面活性剂中或溶液中含有少量长链醇、高级胺、脂肪酸等高表面活性的极性有机物时,溶液的表面张力—浓度对数曲线上的转变可能变得不明显,但显现一个低值(图2——15)。
这也是用以辨别表面活性剂纯度的方法之一。
(2)电导法本法仅适合于表面活性较强的离子表面活性剂CMC的测定,以表面活性剂溶液电导率或摩尔电导率对浓度或浓度的平方根作图,曲线的转变点即CMC。
溶液中若含有无机离子时,方法的灵敏度大大下降。
(3)光散射法光线通过表面活性剂溶液时,假如溶液中有胶束粒子存在,则一部分光线将被胶束粒子所散射,因此测定散射光强度即浊度可反映溶液中表面活性剂胶束形成。
以溶液浊度对表面活性剂浓度作图,在到达CMC时,浊度将急剧上升,因此曲线转变点即为CMC。
利用光散射法还可测定胶束大小(水合直径),推想其缔合数等。
但测定时应注意环境的干净,避开灰尘的污染。
(4)染料法一些有机染料在被胶团增溶时。
其汲取光谱与未增溶时发生明显更改,例如频那氰醇溶液为紫红色,被表面活性剂增溶后成为蓝色。
所以只要在大于CMC的表面活性剂溶液中加入少量染料,然后定量加水稀释至颜色更改即可判定CMC值。
采纳滴定尽头察看法或分光光度法均可完成测定。
对于阴离子表面活性剂,常用的染料有频那氰醇、碱性蕊香红G;阳离子表面活性剂可用曙红或荧光黄;非离子表面活性剂可用频那氰醇、四碘荧光素、碘、苯并紫红4B等。
采纳染料法测定CMC可因染料的加入影响测定的精准明确性,尤其对CMC较小的表面活性剂的影响更大,另外,当表面活性剂中含有无机盐及醇时,测定结果也不甚精准。
表面张力的测定

05 数据记录与处理
数据记录
实验前准备
记录实验日期、实验环境温度和湿度、实验人员等信 息。
实验过程
详细记录实验步骤,包括使用的仪器、试剂、溶液的 浓度和体积等。
实验后处理
记录实验后样品的状态、处理方式以及废弃物处理方 式等信息。
数据处理
数据清洗
表面张力的大小反映了液体分子间的相互吸引力。
03
表面张力单位
01 表面张力通常用牛顿(N)或达因(dynes)作 为单位。
02 1牛顿等于100达因,是国际单位制中的标准单位。 03 在实际应用中,测量表面张力时通常使用达因单
位,因为它更小,更适合表示较小的数值。
表面张力影响因素
温度
温度对表面张力有显著影响, 一般来说,温度升高会使表面
3
未来研究方向
提出进一步研究的方向和重点,如改进实验方法、 研究其他因素对表面张力的影响等。
THANKS
步骤五
记录表面张力计的读数,并重 复实验以获得多次测量结果。
实验操作
操作一
确保实验环境干净整 洁,避免灰尘和杂质 的干扰。
操作二
使用恒温水槽控制温 度,确保实验温度稳 定且符合要求。
操作三
使用天平称量试样时, 要保证精度和准确性。
操作四
在倒入表面张力计的 样品池时,要缓慢且 平稳,避免产生气泡。
操作五
表面张力的测定
目录
Contents
• 表面张力定义 • 表面张力测定方法 • 实验材料与设备 • 实验步骤与操作 • 数据记录与处理 • 结果分析与结论
01 表面张力定义
表面张力定义
01
表面张力的测定

(2-88)
最大附加压力由数字微压差计或 U 型管压差计读出。 用数字压力 计可以直接读出压差的值, Pa, 体系的导气管接数字微差计的负压口, 正压口与大气相通。若用数字微差计,压差则以Δ������������ 表示。 1 σ = ������Δ������ ������ 2
������ ������������ ������������
( ) ������ (2-87)
������������ ������������
������������
式中,Γ为表面吸附量,mol/������2 ;σ为表面张力,J m2 ;( ) ������ 为 在一定温度下表面张力随浓度的改变率,即 ( ) ������ < 0,Γ > 0,溶质能降低溶剂的表面张力,溶液表面层的浓度
B Linear Fit of Sheet1 B
0.07
Pearson's r Adj. R-Square
B
0.06
B
0.05
0.04
0.03
0.02 200
300
400
500
600
700
800
A
折射率-浓度曲线:
W2 n������ 0.05 0.1 1.3359 1.3385 0.15 1.34 0.2 1.3455 0.25 1.349 0.3 1.35 0.4 1.356 0.5 1.3599
Residual Sum of Squares Pearson's r Adj. R-Square
0.07
0.06
B
0.05
0.04
0.03
0.02 0.0 0.1 0.2 0.3 0.4 0.5 0.6 0.7
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
6.2溶液表面的吸附——最大气泡压力法测溶液表面张力6.2.1 实验目的:1、掌握气泡最大压力法测定液体表面张力的原理与方法,并测定不同浓度正丁醇水溶液的表面张力;2、了解溶液表面的吸附作用,应用Gibbs 吸附等温式和Langmuir 吸附等温式求出正丁醇的饱和吸附量,并计算正丁醇分子的截面积。
6.2.2 实验原理:当液体中加入溶质时,其表面张力就会升高或降低。
若升高,则溶质在表面层的浓度比溶液内部浓度小;若降低,则溶质在表面层的浓度比溶液内部浓度大。
这种溶质在溶液表面层的浓度与溶液内部浓度不一致的现象被称为溶液表面的吸附作用。
单位溶液表面积上溶质的过剩量称为表面吸附量Γ。
在一定温度下,溶液的表面吸附量Γ与表面张力γ及溶液本体浓度c 之间的关系符合吉布斯吸附等温式: dcd RT c γ⋅-=Γ (6-2-1) 式中:Γ为表面吸附量(mol ·m -2);T 为热力学温度(K );c 为稀溶液浓度(单位:mol ·L -1);γ为表面张力(单位:N ·m -1);R 为气体常数。
当溶液的表面张力随浓度的变化0d dcγ<时,0Γ>,称为正吸附,表明增加浓度时,能使溶液表面张力降低的溶质,在表面层的浓度大于溶液内部的浓度;反之,当0d dcγ>时,0Γ<,称为负吸附,也就是增加浓度,使溶液的表面张力增加的溶质,在表面层的浓度小于溶液内部的浓度。
用吉布斯吸附等温式计算某溶质的吸附量时,可通过实验测定不同浓度的溶液的表面张力γ,并以γ对c 作图,如图6-2-1所示。
在cγ-曲线上任取一点a ,通过a 点作曲线的切线和平行于横坐标的直线,分别与纵坐标交于',b b 。
令'b b Z =,则d Z cdcγ=-,代入式(6-2-1),得:ZRTΓ=;从c γ-曲线上取不同的点,就可求 图6-2-1 表面张力与浓度关系图b ’bγ得不同浓度时溶质在表面层的吸附量Γ。
(以上数据处理过程也可由计算机作图处理:由实验测出不同浓度c 对应的表面张力γ,利用计算机作c γ-图,拟合曲线方程()f c γ=;求导得到/d dc γ代入吉布斯方程可计算溶液表面吸附量Γ。
)对可形成单分子层吸附的表面活性物质,溶液的表面吸附量Γ与溶液内部浓度c 之间的关系符合Langmuir 吸附等温式:1kckc∞Γ=Γ⋅+ (6-2-2) 式中:∞Γ为 饱和吸附量;k 为常数。
将式(6-1-2)两边取倒数,并同乘以c ,可得11c c k∞∞=+ΓΓΓ (6-2-3) 根据式(6-1-3),以cΓ对c 作图应为一直线,直线的斜率的倒数即为∞Γ。
如果以N 代表饱和吸附时单位面积表面层中的分子数,则N=Γ∞L ,L 为阿伏加德罗常数。
而在饱和吸附时,每个被吸附的溶质分子在表面上所占的面积,即溶质分子的截面积m a 为: 1m a L∞=Γ⋅ (6-2-4) 本实验选用气泡最大压力法测定溶液的表面张力,其原理如下:处于溶液表面的分子,由于受到不平衡的分子间力的作用而具有表面张力γ,定义是在表面上垂直作用于单位长度上使表面积收缩的力,单位是牛顿每米(N·m-1)。
图6-2-2为气泡最大压力法测定溶液表面张力的装置。
其中4是管端为毛细管的玻璃管,当毛细管端面与待测液体表面相切时,液面即沿毛细管上升。
打开分液漏斗的活塞,使水缓慢滴下从而增加系统压力,这样毛细管内液面上受到一个比表面张力管中液面上大的压力,形成压力差,逐渐把管中液面压至管口,形成气泡。
由Laplace 方程可知,此压力差p ∆与溶液的表面张力γ成正比,与气泡的曲率半径r 成反比:rp γ2=∆ (6-2-5)图6-2-2 表面张力测定装置在形成气泡的过程中,气泡曲率半径经历了:大→小→大的过程。
气泡刚形成时,表面几乎是平的,此时曲率半径最大,随着气泡的形成,曲率半径逐渐减小,直到形成半球形时,曲率半径达到最小,并等于毛细管的半径r min =r 毛,由式(6-2-5)可知此时压力差达极大值。
即:图6-2-3 气泡的曲率半径毛r r p γγ22min max ==∆ (6-2-6) max max /2r p k p γ=∆=⋅∆毛 (6-2-7)式中:k 为仪器常数,通常用已知表面张力的物质确定,本实验用蒸馏水确定k 。
若用同一根毛细管,对表面张力分别为1γ和2γ的液体而言,则有下列关系: 11max k p γ=⋅∆, 2max k p γ=⋅∆2,1max12maxp p γγ∆=∆,2, (6-2-8) 由此可见,只要测出最大压力差,即可由已知表面张力的标准物质求出待测物质的表面张力。
6.2.3 仪器与药品:表面张力测定装置1套;恒温槽1套;电子天平1台;100ml容量瓶8个;正丁醇(AR)。
6.2.4 实验步骤:1、配制系列正丁醇溶液各100mL:2、将恒温槽调至25±0.05℃。
3、仪器准备与检漏将表面张力测定管与毛细管洗净并干燥好,按图6-2-2连接装置。
插上电源插头,打开电源开关,LED显示即亮,初显示忽略(过量程时显示±1999),2秒后正常显示。
预热五分钟后按下置零按钮显示为0000,表示此时系统大气压差为零。
(LED显示值即为压力腔体的压力值,如果压力腔体的压力成下降趋势,则出现的极大值保留显示约一秒钟。
)在洗净的表面张力测定管中装入适量的蒸馏水,打开放水阀6使毛细管管端与液面恰好相切,关闭放水阀6。
在滴液漏斗中装入适量水,打开滴液漏斗的活塞,滴液漏斗的水流到磨口烧杯中,使系统的压力增加,压力计上即显示一压力差。
关闭滴液漏斗的活塞,若2-3分钟内压力计的读数不变,则表明系统不漏气,可进行实验。
否则,需检查漏气原因,直至系统不漏气,方可进行实验。
4、以水作为待测液测定仪器常数打开滴液漏斗,控制滴液速度,使气泡由毛细管管口成单泡逸出,且每个气泡的形成时间约为5~10秒,记录最大的压差△p max,连续读数三次,取其平均值(在毛细管气泡逸出的瞬间最大压差在450Pa~900Pa左右,否则须调换毛细管)。
将△p max的平均值代入式(6-2-7)即可求得仪器常数k。
5、待测正丁醇溶液表面张力的测定用同样方法测定不同浓度的正丁醇水溶液,注意由稀至浓依次测定,每次更换溶液时,应用待测液洗涤毛细管内壁及表面张力管2~3次。
测定已知浓度的待测样品的最大压力差△p max,连续读数三次,取其平均值。
代入公式计算其表面张力。
6.2.5 数据记录与处理:1、实验数据记录:t/ ℃=2、实验数据处理:(1)查所测温度下水的表面张力γ ( H 2O )数据填入上表,并由()()2max 2H O H O k p γ=∆计算仪器常数k ;(2)计算同温度下各溶液的表面张力:()()()()()2max max max 2H O H O c k p c p c p γγ=⋅∆=⋅∆∆;(3)绘制γ-c的等温曲线;(4)在γ-c的等温曲线上取六、七个点用镜象法作切线,求出Z 值; (5)由/Z RT Γ=计算不同浓度溶液的Γ,并计算出/c Γ值;(6)作cc -Γ图,由直线斜率求出∞Γ(单位mol ·m -2),并根据式(6-2-4)计算正丁醇分子的截面积(单位nm 2)。
6.2.6 注意事项:1、测定用毛细管一定要清洗干净,测定时毛细管要保持垂直,管端与液面相切;2、实验用毛细管的管端一定要光滑、平整、力求程圆形。
6.2.7 思考题:1、做好本实验的关键是什么?2、毛细管不干净,对实验数据有何影响?3、为什么毛细管端口必须和液面相切?4、若气泡不成单泡逸出,或逸出速度太快,将会给实验带来什么影响?为什么?5、温度变化对表面张力有何影响?6.2.8 附录:1、镜象法作切线:在曲线上取某点作切线,其切线的任意性较大,为此介绍一种用玻璃镜作切线的方法。
在曲线上取任意一点a ,先将有一直边的镜子放在a 点,并以a 点为中心转移,直至曲线在镜中的图像与图上的曲线呈光滑连接为至,然后沿镜面作一直线,此线可被认为是曲线在该点的法线,再通过a 点作法线的垂线,即为曲线在a 点的切线。
2、本试验可利用Excel 或origin 处理实验数据:(1)在Excel 的工作表中输入数据并作计算; (2)作γ-c 图:①选取γ-c 数据,点击 菜单,选择 ; ②按图表向导选择图表类型──不带线的x , y 散点图; ③选取作图数据源; ④对图表选项作相应选择; ⑤选择图表位置── 嵌入工作表。
(3)添加趋势线并显示其公式: ①在图中的数据点上点击快捷菜单; ②选择添加趋势线;③由对话框上的 标签,选择相应的趋势线类型:a 、 对γ~ c 数据,可选择“多项式”型趋势线;b 、 对c ~ c 数据,选择“线性”趋势线。
④由对话框上的 标签,选择显示公式及显示R 2值;R ──相关系数. R →1时表示所添加的趋势线与实验数据的相关程度高。
插入 图表 类型 选项 γ3、不同温度下水的表面张力:表6-2-1 不同温度下水的表面张力参考资料:1、王正烈等编.物理化学第四版.北京:高等教育出版社,20012、北京大学化学学院物理化学实验教学组.物理化学实验(第4版).北京:北京大学出版社,20023、孙尔康,徐维清,邱金恒编.物理化学实验.南京:南京大学出版社,20024、贡雪东,张常山等.最大气泡法测溶液表面张力的改进.大学化学2004,19(5):37-38.。
