睾酮(T)测定试剂盒(化学发光法)产品技术要求科美
睾丸酮定量检测试剂盒(酶联免疫法)说明书

睾丸酮定量检测试剂盒(酶联免疫法)说明书目录●产品名称●包装规格●预期用途●检验原理●主要组成成分●储存条件及有效期●适用仪器●样本要求●检验方法●参考值(参考范围)●检验结果的解释●检验方法的局限性●产品性能指标●注意事项●参考文献●生产企业●医疗器械生产企业许可证编号●医疗器械注册证书编号●产品标准编号●说明书批准及修改日期产品名称通用名:睾丸酮定量检测试剂盒(酶联免疫法)英文名称:Testosterone ELISA包装规格96人份/盒预期用途定量检测样品血清或血浆中睾丸酮激素(T)的浓度。
睾丸激素(17β-hydroxy-4-androstene-3-one)是C19类固醇,C-4和C-5不饱和结合,C-3酮和C-17羟基在β的位置。
分子量为288.47。
睾丸激素是血液中非常重要的男性激素,由睾丸莱迪希细胞分泌;女性睾丸激素大约50%来自外围雄烯二酮的交换,约25%来自卵巢,约25%来自肾上腺。
睾丸激素维系男性第二性特征,测量这个激素对检查性腺机能非常重要。
对于女性来说,男性型多毛症、男性化、肾上腺肥大、多囊卵巢等都可以导致睾丸激素水平增高;对于男性来说,下丘脑垂体病变,睾丸瘤,先天性肾上腺增生和前列腺疾病等都可导致睾丸激素升高。
睾丸激素水平低则由于垂体机能减退,Klinefelter综合症,睾丸切除术和隐睾病,酶缺陷及自体免疫疾病等引起。
检验原理特异的T抗体包被在每个微孔表面。
样本中的T在微孔中与特异的单克隆抗体、酶结合物(抗-T抗血清结合辣根过氧化物)一起孵育,形成“三明治”夹心。
孵育过后洗脱未结合的物质。
结合的辣根过氧化与样本中睾丸激素的浓度成反比。
添加底物溶液,血清T浓度与显色强度成反比。
主要组成成分1.单克隆抗体包被的可拆卸的96(12×8)孔微孔板1块2.T标准品(0、0.2、0.5、1、2、6、16ng/ml)1ml/瓶7瓶3.酶结合物25ml1瓶4.底物溶液25ml1瓶5.终止液14ml1瓶6.洗液(40X浓缩)30ml1瓶7.说明书1份注:a)不同批号的试剂盒各组份不可以互换使用。
睾酮(Tes)测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求北京北方生物技术研究所

睾酮(Tes)测定试剂盒(磁微粒化学发光免疫分析法)适用范围:本产品用于体外定量测定人血清中的睾酮(Tes)的含量。
1.1包装规格100测试/盒,200测试/盒1.2主要组成成分注:1.不同批号试剂盒中各组分不可以互换使用。
2. 校准品和质控品具有批特异性,具体浓度见瓶签。
2.1外观试剂盒各组分应齐全、完整、液体无渗漏;磁微粒试剂摇匀后为棕色含固体微粒的均匀悬浊液,无明显凝集;其他液体组分应澄清,无沉淀或絮状物;包装标签应清晰,易识别。
2.2 装量各组分装量应不得低于标示体积。
2.3溯源性根据GB/T21415-2008及有关规定,提供试剂盒内校准品的来源、赋值过程以及测量不确定度等内容,溯源至企业一级校准品,一级校准品用纯品质量赋值,与已上市产品比对验证。
2.4线性在[0.2,20.0 ]ng/mL范围内,相关系数r应不低于0.9900。
2.5空白限应不高于0.1 ng/mL。
2.6准确度回收率应在85.0%~115.0%范围内。
2.7重复性变异系数(CV)应不大于8.0%。
2.8质控品的测定值质控品的测定结果均应在规定的质控范围内。
2.9特异性2.9.1 与孕酮(Prog)浓度不低于100 ng/mL的Prog在本试剂盒上的测定结果应不高于0.25 ng/mL。
2.9.2 双氢睾酮浓度不低于10 ng/mL的双氢睾酮在本试剂盒上的测定结果应不高于0.25 ng/mL。
)2.9.3 与雌二醇(E2浓度不低于10 ng/mL的E在本试剂盒上的测定结果应不高于0.25 ng/mL。
22.10批间差在三个不同批次产品之间,质控品测定结果的变异系数(CV)应不大于15.0%。
2.11稳定性试剂盒在2~8℃保存,有效期为12个月,在有效期结束的前后两个月内,检测试剂盒的线性、空白限、准确度、重复性、质控品的测定值,应符合相应的规定。
体外诊断试剂睾酮试剂盒检测方法

(5) Laurence-Moon-Biedl(性幼稚、多指(趾)、色素 性视网膜炎)综合征:为常染色体隐性遗传疾病,多 有阳性家族史、近亲结婚者发病率明显增加。本病的 血睾酮降低系继发性,因促性腺激素低所致。 (6) 男性更年期综合征:本病的血睾酮降低系睾丸制造分 泌睾酮的功能逐渐自然衰竭所致,但也有在正常低值 者,本病的促性腺激素也逐渐升高。 (7) 其它:如睾丸验证、肿瘤、外伤、放射性照射、高催 乳素血症、17α-羟化酶缺乏症、隐睾症、青春期延迟、 垂体功能低下、男性性功能低下、阳痿、系统性红斑 狼疮、骨质疏松、垂体性矮小症、甲低、男性乳房发 育、神经性厌食等,均可见血睾酮降低。
【产品特点】
灵敏度高,最低检测限小于0.25ng/ml;线性范围 宽;重复性好;操作简便。
【产品性能指标】
各实验室应根据自己实际条件及接触人群建立自己的参考范 围,下列参考值范围仅供参考: 成年男性 (2.6~12)ng/ml 成年女性 (0~2.0)ng/ml 1. 线性范围:(0.25~20)ng/ml。 2. 最低检测限:小于0.25ng/ml。 3. 精密度:批内变异小于15%,批间变异小于15%。
• 河南美凯生物科技有限公司
睾酮降低的常见疾病:
(1) Klinefelter’s 综合征:也称曲细精管发育不全症、先天性睾 丸发育不全症、原发性小睾丸症、先天性生精不能症等。 除血T值降低外,病人身材细长,体毛及胡须稀少,皮肤细 腻,染色体异常。 (2) 睾丸消失综合征:也称睾丸不发育症,本病睾酮极低,重 者只相当于女性睾酮水平,同时伴有促性腺激素升高。 (3) Kallmann综合征:也称溴神经-性发育不全综合征,系家族 性遗传性促性腺激素缺乏所致,除睾酮低以外,尚有LH、 FSH、E2和皮质醇降低。 (4) 男性假性Turner综合征:为性染色体畸变的遗传病之一, 除睾酮降低外,尚有血和尿中的促性腺激素增高。
睾酮(T)测定试剂盒(光激化学发光法)产品技术要求kemei
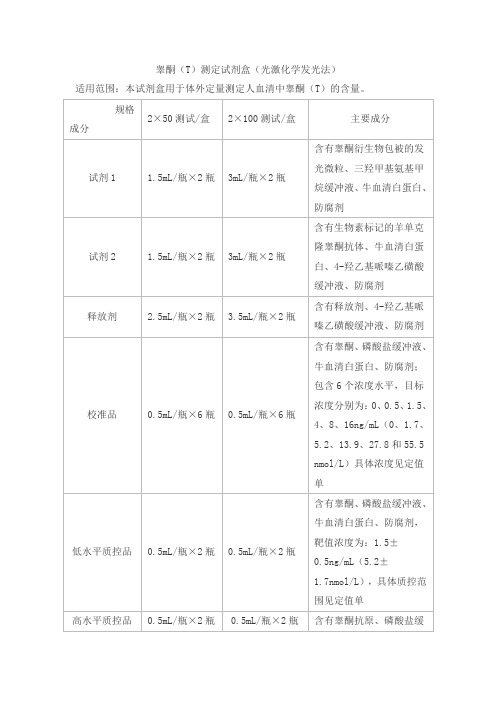
睾酮(T)测定试剂盒(光激化学发光法)
适用范围:本试剂盒用于体外定量测定人血清中睾酮(T)的含量。
说明:
1. 校准品靶值批特异,详见定值单。
2. 质控品质控范围批特异,详见定值单。
2.1 外观
试剂盒组分齐全,内外包装均完整,标签清晰,液体试剂无渗漏。
2.2 检出限
试剂盒的检出限不高于0.10ng/mL(0.35nmol/L)。
2.3 准确度
用国家参考物质GBW09197、GBW09198、GBW09199作为样本进行检测,其测量结果的相对偏差应该在±15%内。
2.4 线性
在[0.1,16]ng/mL([0.35,55.5]nmol/L)区间内,试剂盒的相关系数r应≥0.9900。
2.5 重复性
质控品测定结果的变异系数(CV)应不大于10.0%。
2.6 批间差
在三个不同批次产品之间,质控品测定结果的变异系数(CV)应不大于15.0%。
2.7 质控品测定值
同一套质控品的测定结果应在本试剂盒规定的范围之内。
2.8 特异性
浓度为10ng/mL二氢睾酮、100ng/mL的孕酮、10ng/mL的雌二醇本试剂盒上测定的浓度均应≤0.25ng/mL(0.87nmol/L)。
2.9 稳定性
取2℃~8℃保存至效期末后3个月内的试剂盒,检测2.1、2.2、2.3、2.4、2.5、2.7、2.8项,结果应符合相应规定。
2.10 溯源性
依据GB/T 21415-2008及有关规定提供所用校准品的来源、赋值过程以及测量不确定度等内容,校准品溯源至国家标准物质GBW09199。
睾酮(Tes)化学发光试剂盒使用说明书 - 济南杏恩生物公司

睾酮(Tes)化学发光试剂盒使 用 说 明 书济南杏恩生物科技有限公司睾酮(Tes)化学发光试剂盒说明书【检测目的】定量分析人的血清或血浆中睾酮(Testosterone, Tes)的浓度。
孕酮增高见于诊断女性患男性化肿瘤、女性两性畸形、睾丸间质细胞癌、先天性肾上腺皮质增生、肾上腺肿瘤,也可见于部分多囊卵巢综合症、肥胖及注射睾酮和促性腺激素。
降低见于先天性睾丸不发育或发育不全、xlinefelter综合症、睾丸炎或X 照射后、垂体前叶体能减退、性腺功能及甲亢肝硬化肾功能损伤。
评价多囊卵巢综合症的疗效,治疗后睾酮水平下降。
【产品原理】本公司睾酮(Testosterone, Tes)化学发光试剂盒的原理为: 将Tes单抗体包被于96孔微孔板,病人的血清或血浆加入微孔中,再加入睾酮(Tes)抗体和标记的睾酮(Tes)与病人血清或血浆中睾酮(Tes)含量做竞争反应,属于抗原-抗体竞争法。
15分钟后,洗板,去除多余未反应的结合物。
再由机器自动加注发光底物1与结合物氧化反应,5分钟,机器自动加注发光底物2的增敏触酶后,即时于1秒内发出光的讯号 (闪烁发光)。
藉由机器自动控制每加注一孔后立即测读,检测光的强度,并由相对应的标准曲线计算出病人的浓度。
【产品适用范围】本产品适用于检测人体的血清或血浆中睾酮(Testosterone, Tes)的含量浓度【试剂盒组成】1. 睾酮 (Tes) 包被板:可拆板,8×12孔。
2. 睾酮 (Tes) 标准品:6小管,0.2ml/管,各个标准品浓度分别为 0,0.1, 0.5,2.0,6.0和 18.0 ng /ml。
1%BSA, PBS PH7.4-7.53. 睾酮 (Tes) 抗体: 5 ml, 1瓶。
含Anti-Tes 1%BSA, PBS PH7.4-7.54. 睾酮 (Tes) 标记偶合液:1瓶,10ml/瓶。
含Anti-Tes hrpo 1%BSA, PBS PH7.4-7.55. 睾酮 (Tes) 低质控对照品: 0.15ml/管。
大鼠睾酮(T)说明书

10 nmol/L
1 号标准品
150µl 的 2 号标准品加入 150µl 标准品稀释液
2. 加样:分别设空白孔(空白对照孔不加样品及酶标试剂,其余各步操作相同)、标准孔、 待测样品孔。在酶标包被板上标准品准确加样 50µl,待测样品孔中先加样品稀释液 40µl,
然后再加待测样品 10µl(样品最终稀释度为 5 倍)。加样将样品加于酶标板孔底部,尽 量不触及孔壁,轻轻晃动混匀。 3. 温育:用封板膜封板后置 37℃温育 30 分钟。 4. 配液:将 30 倍浓缩洗涤液用蒸馏水 30 倍稀释后备用 5. 洗涤:小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置 30 秒后弃去,如此 重复 5 次,拍干。 6. 加酶:每孔加入酶标试剂 50µl,空白孔除外。 7. 温育:操作同 3。 8. 洗涤:操作同 5。 9. 显色:每孔先加入显色剂 A50µl,再加入显色剂 B50µl,轻轻震荡混匀,37℃避光显色 10 分钟. 10. 终止:每孔加终止液 50µl,终止反应(此时蓝色立转黄色)。 11. 测定:以空白空调零,450nm 波长依序测量各孔的吸光度(OD 值)。 测定应在加终止 液后 15 分钟以内进行。 操作程序总结:
用完,板条应装入密封袋中保存。 2.浓洗涤液可能会有结晶析出,稀释时可在水浴中加温助溶,洗涤时不影响结果。 3.各步加样均应使用加样器,并经常校对其准确性,以避免试验误差。一次加样时间最好
控制在 5 分钟内,如标本数量多,推荐使用排枪加样。 4. 请每次测定的同时做标准曲线,最好做复孔。如标本中待测物质含量过高(样本 OD 值
1 30 倍浓缩洗涤液
20ml×1 瓶
7 终止液
6ml×1 瓶
2 酶标试剂
6ml×1 瓶
8 标准品(320 nmol/L) 0.5ml×1 瓶
睾酮测定试剂盒(化学发光免疫分析法)产品技术要求frrk
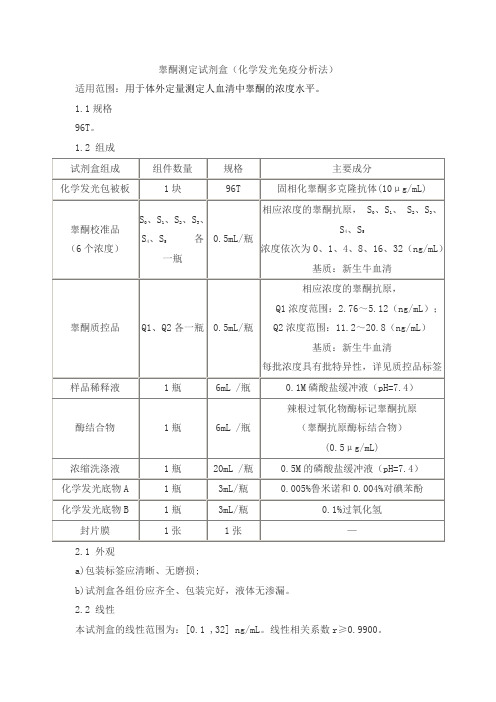
睾酮测定试剂盒(化学发光免疫分析法)
适用范围:用于体外定量测定人血清中睾酮的浓度水平。
1.1规格
96T。
1.2 组成
2.1 外观
a)包装标签应清晰、无磨损;
b)试剂盒各组份应齐全、包装完好,液体无渗漏。
2.2 线性
本试剂盒的线性范围为:[0.1 ,32] ng/mL。
线性相关系数r≥0.9900。
2.3空白限
不大于0.1ng/mL。
2.4准确度
回收率应在(85%~115%)范围内。
2.5重复性
重复检测质控品Q1和 Q2各10次,其批内变异系数(CV)应不大于10%。
2.6批间差
用三个批号的试剂盒检测质控品Q1和 Q2,三批号试剂盒之间的批间变异系数(CV)应不大于15%。
2.7质控品赋值有效性
质控品测量值应在质控范围内。
2.8特异性
2.8.1与雌三醇的交叉反应
检测浓度为32ng/mL的雌三醇,交叉反应率应小于1%。
2.8.2与雌二醇的交叉反应
检测浓度为32ng/mL的雌二醇, 交叉反应率应小于1%。
2.9稳定性
规定产品2℃~8℃储存,有效期6个月。
取到效期后的样品检测准确度、空白限、线性、重复性,应符合2.2~2.5的要求。
2.10溯源性
根据《GB/T 21415—2008 体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》及有关规定提供校准品的来源,赋值过程以及不确定度等内容,校准品溯源至企业工作校准品。
睾酮(T)测定试剂盒(化学发光免疫分析法)产品技术要求dacheng
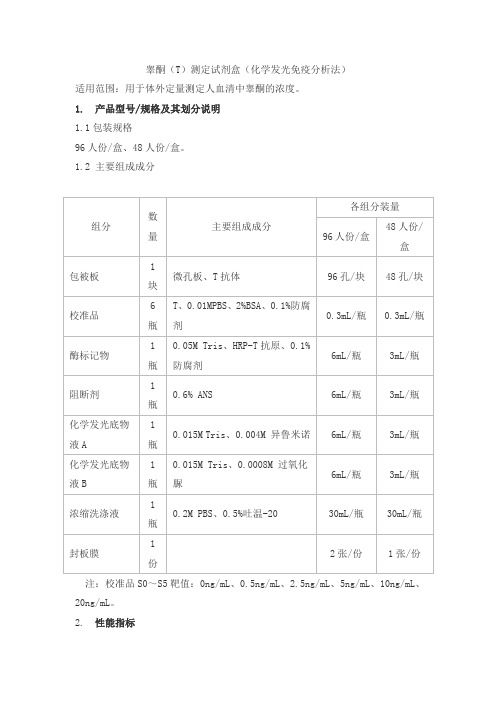
睾酮(T)测定试剂盒(化学发光免疫分析法)适用范围:用于体外定量测定人血清中睾酮的浓度。
1. 产品型号/规格及其划分说明1.1包装规格96人份/盒、48人份/盒。
1.2 主要组成成分注:校准品S0~S5靶值:0ng/mL、0.5ng/mL、2.5ng/mL、5ng/mL、10ng/mL、20ng/mL。
2. 性能指标2.1 外观所有液体组分应齐全、澄清,无沉淀或絮状物;包被抗体微孔板的真空袋,应无破损漏气现象;包装完好,液体无渗漏;中文包装标签清晰,无磨损。
2.2 准确度将已知浓度的睾酮加入到正常血清中,其回收率应在85%~115%之间。
2.3 最低检测限最低检测限应不大于0.2ng/mL。
2.4 线性在[0.5,20]ng/mL浓度范围内,相关系数(r)绝对值应不小于0.990。
2.5 重复性用高低两个浓度的样本,各重复检测10次,变异系数(CV)应不大于12.0%。
2.6 批间差用三个批号试剂盒检测同一样本,则三个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.7 特异性特异性符合如下要求:a)含浓度不低于50ng/mL的孕酮的零浓度T样本,检测结果不高于0.4ng/mL;b)含浓度不低于10000pg/mL的雌二醇的零浓度T样本,检测结果不高于0.4ng/mL。
2.8 稳定性2℃~8℃放置8个月后,测定结果应符合2.1~2.5各项要求。
2.9 校准品溯源性本产品校准品依照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求进行溯源,本产品校准品溯源至企业校准品,该校准品通过雅培检测系统比对赋值。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
睾酮(T)测定试剂盒(化学发光法)
适用范围:本试剂盒用于定量测定人血清中睾酮(T)的含量。
1.1 产品型号
2.1外观
T试剂盒组分齐全、完整;溶液无混浊,无沉淀或絮状物;微孔板包装袋无破损、漏气现象。
2.2 准确性
平均回收率应在90~110%范围内。
2.3 剂量反应曲线的线性
在(0.5~20.0ng/mL)浓度范围内,剂量反应曲线的相关系数r应不小于0.9900。
2.4 空白检测限
应不大于0.35ng/mL。
2.5精密度
2.5.1分析内精密度
测定QC血清,变异系数(CV)应小于15.0%。
2.5.2分析间精密度
测定QC血清,变异系数(CV)应小于20.0%。
2.6批间差
用三个批号的试剂盒,分别测量同一质控血清,变异系数(CV)应小于20.0%。
2.7 质控血清测定值
应在允许的质控范围内。
2.8 特异性
2.8.1与孕酮(P)的交叉反应
检测浓度为5μg/mL的P,测定值应不大于1.0 ng/mL。
2.8.2与雌二醇(E2)的交叉反应
检测浓度为10 ng/mL的E2,测定值应不大于0.40 ng/mL。
2.8.3与雌三醇(E3)的交叉反应
检测浓度为10μg/mL的E3,测定值应不大于0.40 ng/mL 。
2.9 稳定性
T试剂盒在2~8℃避光保存,有效期6个月。
在T试剂盒有效期满后2个月内,分别检测2.1、2.2、2.3、2.4、2.5.1、2.7项,结果应符合各项目的要求。
