电化学原理与应用-第3章 电极 溶液界面的基本性质
电化学基本原理与应用-第3章

净电荷
α
偶极层
3.2.1 “孤立相”的几种电位
(1)外电位(Ψα)
将试验电荷自无穷远处移至距球面约 10-4~10-5厘米处。在这一过程中可以认为 球体与试验电荷之间的短程力尚未开始作 用。根据电位的定义,此时所做的功为:
W1 = Zie0ψ α
ψ α = W1
Z ie0
球体α的外部电位
试验电荷电量
当试验电荷从相内逸出到相外时,这一过 程所涉及的能量变化(-Wiα)相当于试验电荷从 该相逸出而必须摆脱与该相物质之间的短程 相互作用及越过表面时对表面电势所做的功。 这部分功称为试验电荷在α相的“逸出功”, 显然应满足下列关系式:
−Wiα = μiα + Zi Fχ α
3.2.1 “孤立相”的几种电位
(b)内电位差,又称“伽伐尼(Galvani) 电位差”,定义为φα-φβ。直接接触的两相 间的内电位差,用 αΔβφ 表示。由于表面电 位无法测量,所以该值不能测量。也无法理 论计算。
3.2.2 相间电位差
φα −φ β = (χ α +ψ α ) − (χ β +ψ β ) = (ψ α − ψ β ) + ( χ α − χ β )
(1)相间电位差的种类 两相之间出现“相间电位差”的原因只可
能是界面层中带电粒子或偶极子的非均匀分 布,并形成了界面荷电层。
根据以上关于孤立相电位的讨论不难推 想,所谓α、β两相之间的电位差也因此可 能有各种不同的定义,其中较常用的有下面 三种:
3.2.2 相间电位差
(a) 外电位差,又称“伏打(Volta)电位 差”,定义为ψα-ψβ。直接接触的两相间的 外电位差,用 αΔβψ 表示。两相均为金属 时,为金属接触电位差,可直接测量。
电极过程动力学第2章电极-溶液界面的基本性质

电极表面吸附现象
物理吸附
物理吸附是指物质通过范德华力等物理作用在电极表面吸附的现象。 物理吸附对电极反应的影响较小。
化学吸附
化学吸附是指物质通过化学键合作用在电极表面吸附的现象。化学 吸附对电极反应的影响较大,可以改变电极表面的性质。
电极过程动力学第2章电极-溶 液界面的基本性质
目
CONTENCT
录
• 电极-溶液界面概述 • 电极表面特性 • 溶液性质对界面影响 • 界面电势差与双电层结构 • 界面电荷转移过程 • 界面传质过程与扩散层结构
01
电极-溶液界面概述
界面定义与分类
界面定义
电极与溶液之间的接触区域,发生电 化学反应的场所。
竞争吸附
当多种物质在电极表面发生吸附时,它们之间可能存在竞争关系。竞 争吸附的结果取决于各种物质的吸附能力和电极表面的性质。
03
溶液性质对界面影响
溶液组成与性质
溶质种类与浓度
不同溶质及其浓度会对电极-溶液界面的性质产生显著影响。例如 ,某些溶质可能在界面处发生吸附或反应,从而改变界面的结构 和性质。
电极表面的能量状态与晶体内部 不同,表面能的高低影响了电极 反应的进行。
电极表面粗糙度
表面形貌
电极表面的粗糙度是指表面形貌的不规则程度,它 对电极反应速率和电流分布有重要影响。
真实面积与表观面积
电极表面的真实面积通常比表观面积大,这是由于 表面粗糙度引起的。真实面积对电极反应速率有直 接影响。
粗糙度因子
扩散层结构特点
01
扩散层定义
在电极表面附近,由于浓度梯度引 起的物质扩散区域。
电化学原理-吴金平-2012第三章304-1-wu

OHP
水化程度高, 冲出水化膜、 钻进水偶极 层难! 水偶极层 水化阳离子层
外紧密层结构示意图
b.内紧密层结构(q>0)
特性吸附:内紧密层的离 子吸附称为特性吸附 紧密层厚度:仅为一个 阴离子半径,d=r-
IHP
0 r
x1
1 1 1 = C紧 C水 C 0 r
x2
x1 x2 1 = C紧 0 H2O 0
H2O
x1 1 C紧 0 H 2O
实验结果证明:在荷负电的电极上, 紧密层的
电容与组成双电层的水化阳离子的种类基本无关.
x1 1 C紧 0 H2O
紧密层是带有剩余电荷的两相之间的界面层,厚度不 超过几个埃;而分散层是液相中具有剩余离子电荷及 电位梯度的表面层,稀溶液中及表面电荷密度很小时 分散层厚度可达几百埃。 浓溶液中及表面电荷密度不太小时几乎可以忽视分散 层的存在,即可近似认为分散层中的剩余电荷均集中 在界面层的外表面上。
§3.5 零电荷电位
例:已知某电极的 求此时对应的零标电位
思考:零标电位能否用于热力学计算中的电位标度?
p162
课堂练习:
某电极的微分电容曲线如图2所示,试画出图中1和 2 电位下的双电层结构示意图及电位分布图。
四、
的作用
判断电极表面剩余电荷q的符号和数量
1、可以通过
规律:
例:已知汞在稀的KCl溶液中
2 . 通过零电荷电位可研究电极/溶液界面的许 多重要性质:
双电层电位分布、界面电容、界面张力、 离子的 界面吸附行为、气体在金属表面的附着、溶液对金属 电极的润湿性、电动现象和光电现象等 . 零电荷电位下的极值现象: 界面张力
第三章2电极溶液界面
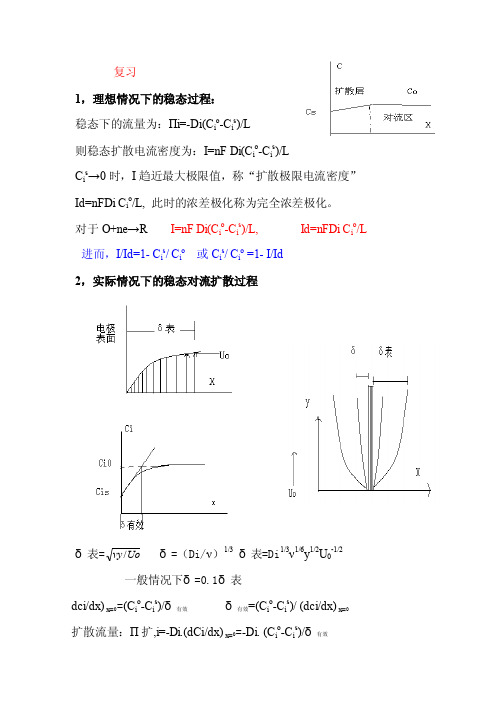
复习1,理想情况下的稳态过程:稳态下的流量为:Πi=-Di(C i o-C i s)/L则稳态扩散电流密度为:I=nF Di(C i o-C i s)/LC i s→0时,I趋近最大极限值,称“扩散极限电流密度”Id=nFDi C i o/L, 此时的浓差极化称为完全浓差极化。
对于O+ne→R I=nF Di(C i o-C i s)/L, Id=nFDi C i o/L 进而,I/Id=1- C i s/ C i o或C i s/ C i o =1- I/Id2,实际情况下的稳态对流扩散过程δ表=Uovy/δ=(Di/ν)1/3δ表=Di1/3ν1/6y1/2U0-1/2一般情况下δ=0.1δ表dci/dx) x=0=(C i o-C i s)/δ有效δ有效=(C i o-C i s)/ (dci/dx) x=0扩散流量:Π扩,i=-Di.(dCi/dx) x=0=-Di. (C i o-C i s)/δ有效I=-nF Π扩,i=nF Di. (C i o -C i s )/δ有效将δ=(Di/ν)1/3 δ表=Di 1/3ν1/6y 1/2U 0-1/2代入上两式得电极表面上各处的电流密度和极限电流密度:I=nF Di 2/3ν-1/6-y -1/2U 01/2 (C i o -C i s ) Id= nF Di 2/3ν-1/6-y -1/2U 01/2 C i o 同样:I/Id=1- C i s / C i o 或C i s / C i o =1- I/Id 旋转圆盘电极上的扩散过程δ=(C i o -C i s )/ (dci/dy) y=0=1.62 Di 1/3ν1/6y 1/2U 0-1/2=1.62 Di 1/3ν1/6ω-1/2 所以稳态对流扩散的电流密度为: I= nF Di. (C i o -C i s )/δ有效=0.62nF Di 2/3ν-1/6ω1/2(C i o -C i s )Id=0.62nF Di 2/3ν-1/6ω1/2C i o同样:I/Id=1- C i s / C i o 或C i s / C i o =1- I/Id§3.6 当电极反应速度由液相传质步骤控制时极化曲线的形成及其应用因为具体实验中,通常最容易得到的是I-Φ曲线,所以我们有必要对液相传质步骤的极化曲线的形状有所了解。
电化学原理与应用-第3章 电极 溶液界面的基本性质

的电极体系来说,可以把电子看成是一种能自由移动
并在界面发生吸附的粒子。
若电极表面剩余电荷密度为q(C/cm2),则电子 q 的表面吸附量为: e F
其化学位变化为: de Fd
G zFE
因此: e de qd
dσ i d i 0 d
3.1.3 电极/溶液界面性质的研究方法
界面结构—在这一过渡区域中剩余电荷和电势的分 布以及它们与电极电势的关系。
界面性质—界面层的物理化学特性,特别是电性质。
研究方法:
反映界面性质的参数: 界面张力σ、微分电容Cd、电极表面剩余电荷密度q 用实验方法测定界面参数,把这些实验测定结果与根据理论 模型推算出来的数值相比较,如果理论值与实验结果比较一
相对
在0.1M各种 电解质溶液中
zF
3.3 双电层微分电容
电极/溶液界面的双电层 平行板电容器 微分电容Cd
dq Cd d
σ q i
Cd 2
2σ
从电毛细曲线 可求得微分电 容值(F/cm2)
dq Cd d
dq Cd d
2. 电毛细曲线的微分方程
一般体系,Gibbs-Duham方程:
SdT Vdp ni di 0
其中:ni — 组分 i 的摩尔数, i — 组分 i 的化学势。 存在相界面的体系,Gibbs-Duham方程:
SdT Vdp Ad σ ni d i 0
Hg
其中:A — 界面面积 σ — 界面张力
致,那么该结构模型就有一定的正确性。
电毛细曲线法
双电层微分电容法
3.2 电毛细曲线
1. 电毛细曲线及其测定 对电极体系,界面张力(σ)不仅与压力、温度和界 面层的物质组成有关,而且与电极电势()有关。这 种界面张力随电极电势变化的现象叫做电毛细现象。
电极溶液界面课件

contents
目录
• 电极溶液界面基础 • 电极溶液界面的电化学性质 • 电极溶液界面的物理化学性质 • 电极溶液界面的应用 • 电极溶液界面的研究方法与技术
01
电极溶液界面基础
电极溶液界面的定义
总结词
电极溶液界面是指电极和与之接触的溶液之间的界面,是电化学反应的重要场 所。
燃料电池
燃料电池利用电极溶液界面将化学能转化为电能。电极溶液界面的性质决定了燃料电池的效率和耐久 性。优化电极溶液界面的结构和组成可以提高燃料电池的性能。
传感器与生物电分析
电化学传感器
电极溶液界面在电化学传感器中发挥着关键作用。通过监测电极溶液界面上的电化学反应,可以实现对气体、离 子、有机物等的快速、灵敏检测。例如,电化学气体传感器利用电极溶液界面检测环境中的有害气体。
形貌
电极表面形貌对溶液在电极表面的润湿和电化学反应过程产 生影响,不同形貌的电极具有不同的电化学性能。
04
电极溶液界面的应用
电化学能源存储与转换
电池技术
电极溶液界面在电池中起着至关重要的作用。它可以影响电池的能量密度、充放电速度和循环寿命。 例如,锂离子电池利用电极溶液界面进行电荷转移和离子传输,从而实现高效的能量存储和释放。
电极反应的步骤和涉及的中间产物。
电极反应动力学方程
描述电极反应速率与反应物浓度、温度等因素关系的方程。
离子传输与迁移
01
02
下的迁移 速率。
离子淌度
离子迁移速率与电场强度 的比值。
离子扩散系数
描述离子在溶液中扩散速 率的参数。
双电层结构与电动现象
双电层结构
电极表面与溶液之间的电荷分布, 包括紧密层和扩散层。
电化学原理第三章

2021/12/31
微分电容曲线可求给定电极电位下的电极表面剩余电荷q Cd=dq/dQ 积分后可得
qCdd积分常数
无电荷排斥作用,界面张力最大; 此时的电极电位称为零电荷电位,常用符号Φ0表示。
q( )i
3.6
无论电极表面存在剩余电荷符号如何,界面张力均随剩余电 荷数量的增加而降低。 由上式
可直接由电毛细曲线斜率求某一电位密度下电极电位 表面剩余电荷密度q判断表面剩余电荷密度符号 及零电荷电位。
2021/12/31
由微分电容定义和李普曼方程,由电毛细曲线很易求得微分电容 值
因
q
所以 Cd2
2
(3.25)
2021/12/31
可根据电毛细曲线确定零电荷电位φO,从而可利用式(3.24)求得 任-电极电位下的电极表面剩余电荷密度q,即
q
qodq
oCdd
(3.3)6
故可计算从零电荷电位φO到某一电位φ之间的平均电容值Ci
即由3.21和3.22求得该浓度下的离子表面剩余量。
2021/12/31
§ 双电层的微分电容
一、 双电层的电容
界面剩余电荷的变化将引起界面双电层电位差改变,因而电极/溶 液界面具有贮存电荷的能力,即具有电容的特性。
理想极化电极可作为平板电容器处理,即把电极/溶液界面的两个 剩余电荷层比拟成电容器的两个平行板,由物理学知,该电容器 的电容值为一常数,即
d为紧贴电极表面排列的水化离子的电荷中心与电极表面的 距离,也为离子电荷能接近表面的最小距离。紧密层厚度为d, 若假定d内介电常数为恒定值。则该层内电位分布是线性变化的。 从x=d到溶液中远处剩余电荷为零的双电层部分即为分散层。其 电位分布是非线性变化的。
电化学原理简答题

电化学原理简答题第三章电极/溶液界面的结构与性质1.为什么电毛细曲线是具有极大值的抛物线形状?溶液界面存在双电层,剩余电荷无论带正电还是负电,同性电荷间相互排斥,使界面扩大,而界面张力力图使界面缩小,两者作用效果相反,因此带电界面的张力比不带电时小,且电荷密度越大,界面张力越小,因此电毛细曲线是具有极大值的抛物线形状。
2.标准氢电极的表面剩余电荷是否为零?不一定,标准氢电极电位为0指的是氢标电位,是人为规定的,电极表面剩余电荷密度为0时的电位指的是零电荷电位,其数值并不一定为0;因为形成相间电位差的原因除了离子双电层外,还有吸附双电层\偶极子双电层\金属表面电位。
3.影响双电层结构的主要因素是什么?为什么?静电作用和热运动。
静电作用使符号相反的剩余电荷相互靠近,贴于电极表面排列,热运动使荷电粒子外散,在这两种作用下界面层由紧密层和分散层组成。
4.什么叫Ψ1电位?能否说Ψ1电位的大小只取决于电解质总浓度而与电解质本性无关? Ψ1电位的符号是否总是与双电层总电位的符号一致?为什么?距离电极表面d处的电位叫Ψ1电位。
不能,因为不同的紧密层d的大小不同,而紧密层的厚度显然与电解质本性有关,所以不能说Ψ1电位的大小只取决于电解质总浓度而与电解质本性无关。
当发生超载吸附时Ψ1电位的符号与双电层总电位的符号不一致。
5.简要概括电极/溶液界面发展的四个阶段、优缺点及其主要内容。
①亥姆赫兹紧密双电层模型:主要内容:将双电层比作是平行板电容器优点:a能够解释界面张力随电极电位变化b能够解释微分电容曲线上所出现的平台区域缺点:a解释不了界面电容随电极电位和溶液总浓度的变化规律b解释不了在稀溶液中,零电荷电位下微分电容最小等实验事实②Gouy和Chapman分散层模型:主要内容:溶液中的离子在静电作用和热运动作用下,按位能场中粒子的波尔兹曼分配律分布,完全忽略紧密层,只考虑分散层。
优点:a能较好解释微分电容最小值的出现b能较好解释电容随电极电位的变化规律缺点:a理论计算微分电容值与实验事实相差太大b解释不了微分电容曲线上的“平台区”的出现③Stern模型(双电层静电模型):主要内容:双电层由紧密层和分散层两部分组成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
从理论上解释微分电容的变化规律,说明界面结构及影响因素对 微分电容的影响,正是建立双电层模型时要考虑的一个重要内容, 根据微分电容曲线所提供的信息来研究界面结构与性质的实验方法 叫微分电容法。
汞电极上的电毛细曲线
表面剩余电荷密度~电势曲线
σ
cm-1) σ×105/(N· cm-2) C· q/(µ
面张力都将随剩余电荷数量的增加而降低。溶液一侧剩余电荷密度:
电极溶液
+ + + + + +
qs q zi Fi
式中:zi--离子i的价数 i—溶液一侧离子i的表面剩余量
+
+ + + +
q
+ + +
qs
d i d i qd
分布,因此可以认为金属中全部剩余电荷都是紧密分布
的,金属内部各点的电势均相等。 在溶液相中,当溶液总浓度较高,电极表面电荷密度较 大时,由于离子热运动较困难,对剩余电荷分布的影响
较小,而电极与溶液间的静电作用较强,对剩余电荷的
分布起主导作用,溶液中的剩余电荷也倾向于紧密分布,
形成紧密双电层。
• 如果溶液总浓度较低,或电极表面电荷密度较小,那么离子热 运动的作用增强,而静电作用减弱,形成紧密与分散层共存的 结构。
若参比电极对负离子可逆,则: 若参比电极对正离子可逆,则:
参比电极对负离子可逆:
相对
参比电极对正离子可逆:
相对
具体求解离子表面剩余量的步骤: (1)测量不同浓度电解质溶液的电毛细曲线 (2)从各条电毛细曲线上取同一相对电势下的σ值,作出 σ σ -lna关系曲线 (3)根据σ -lna关系曲线,求出某一浓度下的斜率 ln a
若保持 和除 i 组分外的其他各组分j不变
d 0, d j i 0
一定电极电势时 σ i 的i离子表面剩余 i , ji 量(mol/cm2)
(电中性) (等电量)
(化学势加和性) 当溶液成分发生变化时,由于参比电极电势变化而 引起的电极电势变化为: 其中相对为相对于浸在组成经历了同样变化的溶液 中的参比电极测得的研究电极电势的变化。 若所用参比电极对于溶液中的正 离子是可逆的(如氢电圾),则: 若参比电极对于溶液中的负离 子是可逆的(如甘汞电极),则:
= -1.6V
-1.2V < < 0.1V
理想极化电极:在一定的电势范围内,可以借
助外电源任意改变双电层的带电状况 ( 因而改
变界面区的电势差 ) ,而不致引起任何电化学
反应的电极。如KCl溶液中的汞电极。 不极化电极:指有电流通过时,电极与溶液界 面间电势差不发生任何变化的电极。
3.1.2 研究电极/溶液界面性质的意义
相对
在0.1M各种 电解质溶液中
zF
3.3 双电层微分电容
电极/溶液界面的双电层 平行板电容器 微分电容Cd
dq Cd d
σ q i
Cd 2
2σ
从电毛细曲线 可求得微分电 容值(F/cm2)
dq Cd d
dq Cd d
电极表面剩余电荷较少时,即零电荷电位附近,微分电容随电极 电位变化较明显。电荷密度增大时,电容值也趋于稳定值,进而出 现电容值不随电位变化的所谓“平台”区。在q>0的左半部曲线对 应的平台区 Cd值约为32~40μF/cm2, 右半部(q<0),平台区对应 的Cd值约为16~20μF/cm2, 表明由阴离子和阳离子组成的双电层在结 构上的差别。
的电极体系来说,可以把电子看成是一种能自由移动
并在界面发生吸附的粒子。
若电极表面剩余电荷密度为q(C/cm2),则电子 q 的表面吸附量为: e F
其化学位变化为: de Fd
G zFE
因此: e de qd
dσ i d i 0 d
非法拉第过程:在电极-溶液界面间没有电荷转移,但是随
着电势变化,由于吸附和脱附过程发生以及双电层的充放电, 导致电极-溶液界面结构发生变化,并引起电流流动,这种电 流流动过程称为非法拉第过程。不遵循法拉第定律。
界面电荷层
当性质不同的相接触时,在相界面上形成了不
同性质的电势差。 出现电势差的原因是带电粒子或偶极子在界面 层中的非均匀分布。 双电层(double layer):由于电极和溶液界面带 有的电荷符号相反,故电极/溶液界面上的荷电物 质能部分地定向排列在界面两侧。
Gibbs吸附等温式
把电子这一组分单独列出来,则有:
dσ i d i e d e i d i qd d
理想极化电极的界面上没有化学反应发生,溶液中物
质组成不变,即对于溶液中每一组分来说:di =0。
d qd d σ
σ q 电毛细曲线的微分方程—Lippman公式 i
φ/V(相对于标准氢电极)
微分电容曲线
1-0.1mM 2-1mM 3-10mM 4-100mM
滴汞电极在不同浓度KCl溶 液中的微分电容曲线
零电荷电势
求q 值时,微分电容法比毛细曲线法相比更为精确和 灵敏。电毛细曲线的直接测量只能在液态金属电极 上进行,而微分电容法测量还可以在固体电极上直 接进行。
3.1 非法拉第过程及电极/溶液界面的性能
法拉第过程:电极上发生氧化还原反应(电极反应)并
伴随电子在金属-溶液界面间转移(跃迁)的过程。这一过
程遵守法拉第定律,即:因电流通过而引起的化学反应的量 与所通过的电量成正比。 电极反应导致的电流 —法拉第电流
O ne R
Q It n zF zF
(1)当电极表面存在正的剩余电荷时,
σ 0, q 0
随电极电势变正,界面张力不断减小—带正电。 (2)当电极表面存在负的剩余电荷时,
σ 0, q 0
随电极电势变负,界面张力也不断减小—带负电
不论电极表面存在正剩余电荷还是负剩余电荷,界
σ
cm-1) σ×105/(N· cm-2) C· q/(µ
φ/V(相对于标准氢电极)
+ + + +
+ +
呈抛物线状, why?
+ +
+ +
+ +
汞/溶液界面存在着双电层,即界面的同一侧带有相 同符号的剩余电荷。无论是带正电荷还是带负电荷, 由于同性电荷之间的排斥作用,都力图使界面扩大, 而界面张力力图使界面缩小,二者作用恰好相反。因 此,带电界面的界面张力比不带电时要小,并且表面 电荷密度越大,界面张力就越小。最高点处是电极表 面剩余电荷密度为零时,其它点处表面带过剩电荷。
σ/ 0
表面电荷密度q=0时的 电极电势,也就是与界 面张力最大值相对应的 σ1
电极电势称为零电荷电
势,常用符号0表示。
零电荷电势0
根据Lippman公式,可以直接通过电毛细曲线的斜率 求出 某一电极电势下的电极表面剩余电荷密度q,做 图就得到 q-曲线(II)。
根据Lippman公式,可以判断表面剩余电荷密度的符号
溶液
在恒温、恒压下:
Ad ni d i 0 Ad σ
ni dσ d i 0 d A ni i — i 物种的界面吸附量(mol/cm2) A
dσ i d i 0 — Gibbs吸附等温式
一般情况下,不带电的固相中没有可以自由移动 而在界面吸附的粒子,因而对固/液界面,化学势一 项只需要考虑液相中的吸附粒子。但对电极电势可变
已知:q = 0时, = 0, 以此为边界条件进行积分, 可得:
q 0 Cd d
电极电势为时的q值相当 于图中的阴影部分。 求q 值时,微分电容法比毛细曲 线法相比更为精确和灵敏。电毛 细曲线的直接测量只能在液态金 属电极上进行,而微分电容法测 量还可以在固体电极上直接进行。
q
致,那么该结构模型就有一定的正确性。
电毛细曲线法
双电层微分电容法
3.2 电毛细曲线
1. 电毛细曲线及其测定 对电极体系,界面张力(σ)不仅与压力、温度和界 面层的物质组成有关,而且与电极电势()有关。这 种界面张力随电极电势变化的现象叫做电毛细现象。
界面张力与电极电势的关系曲线叫做电毛细曲线。
通常用毛细管静电计测取液态金属电极的电毛细曲线.
3.1.3 电极/溶液界面性质的研究方法
界面结构—在这一过渡区域中剩余电荷和电势的分 布以及它们与电极电势的关系。
界面性质—界面层的物理化学特性,特别是电性质。
研究方法:
反映界面性质的参数: 界面张力σ、微分电容Cd、电极表面剩余电荷密度q 用实验方法测定界面参数,把这些实验测定结果与根据理论 模型推算出来的数值相比较,如果理论值与实验结果比较一
• 热运动处使荷电粒子倾向于均匀分布,从而使剩余电荷不可 能完全紧贴着电极表面分布,而具有一定的分散性,形成分 散层。
电极溶液界面的紧密 双电层结构
考虑了热运动干扰时的电极溶 液界面双电层结构
在金属相中,自由电子的浓度很大,可达1025 mol/dm3 ,少量 剩余电荷在界面的集中并不会明显破坏自由电子的均匀
3.4 双电层的结构
在电极/溶液界面存在着两种相间相互作用:
(1)电极与溶液两相中的剩余电荷所引起的静电长程作用;
(2)电极和溶液中各种粒子(离子、溶质分子、溶剂分子等等)
之间的短程作用,如特性吸附、偶极子定向排列等,它只
在几个Å的距离内发生。
电极溶液界面的基本结构
• 静电作用使得符号相反的剩余电荷力图相互靠近,形成紧密 的双电层结构,简称紧密层。
