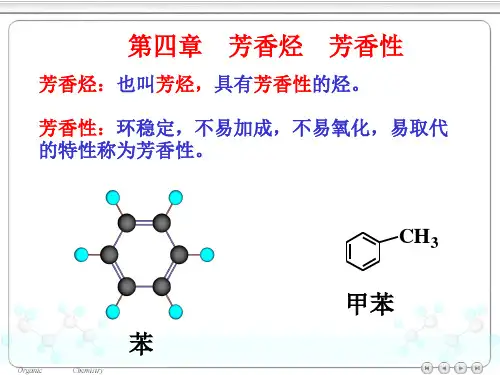
芳香烃
芳香烃

1.Birch还原反应 碱金属(钠、钾或锂)在液氨与醇(乙醇、异丙醇或二级丁醇)的混合液中,与芳香化合物反应,苯环可被还原成1,4-环己二烯类化合物,这种反应叫做Birch(伯奇)还原。例如,苯可被还原成1,4-环己二烯。 Birch还原反应与苯环的催化氢化不同,它可使芳环部分还原生成环己二烯类化合物,因此Birch还原有它的独到之处,在合成上十分有用。 萘同样可以进行Birch还原。萘发生Birch还原时,可以得到1,4二氢化萘和1,4,5,8-四氢化萘。 2.催化氢化反应 苯在催化氢化( catalytic hydrogenation)反应中一步生成环己烷体系。萘在发生催化加氢反应时,使用不同的催化剂和不同的反应条件,可分别得到不同的加氢产物。蒽和菲的9、10位化学活性较高,与氢气加成反应优先在9、10位发生。 3.用金属还原 用醇和钠也可以还原萘,温度稍低时得1,4-二氢化萘,温度高时得1,2,3,4-四氢化萘。[1]
萘、蒽和菲的亲电取代反应
在正常情况下,萘比苯更易发生典型的芳香亲电取代反应,硝化和卤化反应主要发生在α位上。 由于萘十分活泼,溴化反应不用催化剂就可进行,氯化反应也只需在弱催化剂作用下就能发生。 为什么取代反应主要发生在α位上?共振理论认为:取代基进攻α位形成的碳正离子中间体有两个稳定的含有完整苯环结构的极限式,而进攻卢位形成的碳正离子中间体只有一个稳定的含有完整苯环结构的极限式,所以前者比后者稳定。显然,稳定碳正离子相对应的过渡态势能也相对较低,所以进攻α位,反应活化能较小,反应速率快。 在发生可逆的磺化反应时,进入的位置和外界的条件很有关系。低温时,口氢先被取代,当温度升高后,再转移到较稳定的p位上,这结果表明α-萘磺酸的生成是受动力学控制的,而β-萘磺酸的生成是受热力学控制的。 上述现象表明,与萘的硝化、卤化反应一样,生成α-萘磺酸比生成β-萘磺酸活化能低,低温条件下提供能量较少,所以主要生成α-萘磺酸。但磺化反应是可逆的,由于,α-磺基与异环的α-H处于平行位置,空阻较大,不稳定,随着反应温度升高,α-萘磺酸的增多,α-磺化反应的逆向速率将逐渐增加;另外,温度升高也有利于提供β-磺化反应所需的活化能,使其反应速率也加大,β-磺基与邻近的氢距离较大,稳定性好,其逆向反应速率很慢,所以α-萘磺酸逐渐转变成β-萘磺酸。 萘的酰化反应既可以在α位发生,也可以在β位发生,反应产物与温度和溶剂很有关系。 一取代萘进行亲电反应时,第一取代基(G)也有定位效应,卤素以外的邻对位取代基使环活化,因此取代反应主要在同环发生。 如果第一取代基(G)在β位时,有时6位也能发生取代反应,因为6位也可以被认为是G的对位。 间位取代基使环钝化,因此取代反应主要发生在异环的α位。 但是,磺化和傅一克反应常在6,7位发生,生成热力学稳定产物。 蒽比苯、萘更易发生亲电取代反应,除磺化反应在1位发生外,硝化、卤化、酰化时均得9-取代蒽,取代产物中常伴随有加成产物。 菲的9,10的化学活性很高,取代首先在9,10位发生。 此外菲的1,2,3,4,10和5,6,7,8,9是对应的,所以应有五种一元取代产物
芳香烃名词解释

芳香烃名词解释
嘿,你知道啥是芳香烃不?芳香烃啊,就像是化学世界里的神秘宝藏!打个比方吧,就好比是一个充满奇妙味道和独特结构的宝藏箱子。
芳香烃,简单来说,就是具有芳香性的烃类化合物。
啥是芳香性呢?哎呀,这可不好简单解释清楚。
它就好像是一种独特的气质,让这些
化合物与众不同。
比如说苯,那就是芳香烃里特别有名的一个家伙!
它的结构稳定得很嘞,就像一座坚固的城堡。
想象一下,在那个奇妙的化学世界里,芳香烃们就像是一群有着特
殊魅力的小精灵。
它们有着各种各样的特点和性质,有的可能味道香
香的,有的可能在某些反应中表现得超级厉害。
咱再说说甲苯,这也是一种常见的芳香烃呀。
它在工业上可有大用
处呢!就像一个能干的小助手,在各种领域发挥着重要作用。
你看,芳香烃无处不在,从我们日常用的东西,到一些高科技的产品,都可能有它们的身影。
它们是不是很神奇呢?
芳香烃,真的是化学领域里非常重要的一部分啊!它们就像是隐藏
在幕后的英雄,默默地为我们的生活和科技发展贡献着力量。
所以啊,可别小看了这些小小的芳香烃哦!它们的价值和意义可大着呢!。
芳香烃ppt课件

+ HNO3
+ 2HNO3
浓硫酸 60℃
—NO2 + H2O
硝基苯
浓硫酸
100~110℃
间二硝基苯
NO +2H2O N2 O2
玻璃 管
实验步骤:①先将1.5mL浓硝酸注入 大试管中,再慢慢注入2mL浓硫酸,并 及时摇匀和冷却. ②向冷却后的酸中逐滴加入1mL苯, 充分振荡,混和均匀. ③将混合物控制在50-60℃的条件下 约10min,实验装置如左图.
CH3
C. CH3 CH2 CH CH3
D.
CH3
—CH2—CH3
练习2
CH3
COOH
KMnO4(H+)
COOH CH3
C| H3
CH3 |
CH3—CH2—
—C—CH3 | CH3
KMnO4/H+
HOOC |
HOOC—
CH3 | —C—CH3 | CH3
2、加成反应
+ H2
催化剂 △
3、取代反应
制鞋、皮革、箱包、家具、喷漆、油漆等工作
引起急性中毒或慢性中毒,诱发白血病
致癌物质
稠环 萘——过去卫生球的主要成分 芳烃 秸秆、树叶等不完全燃烧形成的烟雾中
香烟的烟雾中
()
B
A.C6H5Br和C6H6 B.C6H5NO2和H2O
C.C6H6和CCl4
D.C6H14和C6H6
第二单元 芳香烃
芳香烃的来源与应用
练习
1.下列有机物属于芳香族化合物的是__①_②__③__④_⑥______
2.下列有机物属于芳香烃的是___②__③__④__⑥____
①
—OH
有机化学第六章芳香烃

Y
可见,凯库勒式并不能确切地反映苯的真实情况
现代物理方法(射线法、光谱法、偶极距的测定)表明,苯分子是 一个平面正六边形构型,键角都是120°,碳碳键长都是0.1397nm。图 示如下:
杂化轨道理论解释
苯分子中的碳原子都是以sp2杂化轨道互相沿对称轴方向重叠形成6个C-Cσ键组成一个 正六边形,每个C各以一个sp2杂化轨道分别与H的1s轨道沿对称的方向重叠,形成六 个C-Hσ键,由于是sp2杂化,所以键角都是120。所有原子均在同一平面上。 每个C还有一个未参与杂化的垂直于与碳环平面σ键的P轨道,彼此侧面重叠,形成一 个封闭的共轭体系,每个P轨道上有一个P电子,组成了π66大π键。由于共轭效应使π 电子高度离域,电子云完全平均化,故无单双键之分。 因此,苯的电子云是一个整体,分布在环的上、下方,并且是完全平均的,所以苯分 子中每个C-C键都有π键的性质,并且是完全相同的,故邻位二元取代物也应当只有一 种。 应当注意且要牢记,苯环中并没有一般的C-C单键和C=C双键。
( 2 )体系能量降低,氢化热(208.5 kJ·mol-1)比环己烯氢 化热的三倍低得多( 3×119.3-208.5 = 149.4 kj·mol-1 ),这 149.4 kj·mol-1即为苯的共轭能。
苯现在的表达方式
价键式
分子轨道离域式
共振式
自旋偶合价键理论 (1986年Copper等提出)
+ Cl2 + Br2
Fe 或 FeCl3 55~60℃
Fe 或 FeBr3 55~60℃
+ 2Cl2 Fe 或 FeCl3
反应历程:
Cl
+ HCl
Br
+ HBr
Cl
+
有机化学-芳香烃
CH3
HNO3
HOAc
CH3
CH3 CH3
NO2 +
+
NO2
NO2
63% 34% 3%
Cl
Cl
Cl
Cl
HNO3
H2SO4
NO2 +
+ NO2
30%
NO2
69% 1%
(2) 第二类定位基─间位定位基
使新进入苯环的取代基主要进入它的 间位,并使苯环致钝。
例如: −CF3, −N(CH3)3+, −NO2, −CN, −SO3H, −CHO, −COCH3, −COOH, −COOCH3, −CONH2, −NH3+。
NO2
NO2
CH3 C CH3 CH3 无 α-H
KMnO4 H+
COOH
氧化剂: KMnO4 铬酸等
4.2.4 苯环上亲电取代反应的定位规则
Y
一取代苯:
芳环上的取代基既影响亲电 取代反应的速率又决定着亲电试 剂进入芳环的位置。
1. 两类定位基
芳环上的取代基分为两类:
(1)第一类定位基 ─ 邻、对位定位基 使得新进入苯环的取代基主要进入它的
均化,闭合共轭
苯
苯的分子结构 体系(环状大π键)
6 个C–C σ键: sp2–sp2相互交盖,6 个C –H σ键: sp2–1s 相互交盖。 6 个2p 轨道的对称轴垂直于环所在平面, 彼此相互平行,两侧进行侧面交盖,形成闭合的π轨道。 6个π电子离域在六个C原子上。由此形成一个闭合的
共轭体系。
2. 苯的构性相关分析
CH3
CH3
CH3
CH3
1,2-二甲苯 邻二甲苯 o-二甲苯
芳香烃

2-甲基-3-苯基戊烷 2-methyl-3phenylpentane
二烃基取代苯:有三种异构体,取代基的位臵可以用阿 拉伯数字标出,或用邻、间、对(o-,m-,p-)表示。
CH3 CH3
CH 3 CH3
CH3
CH3
1,2-二甲苯 邻二甲苯 1,3-二甲苯 间二甲苯 1,4-二甲苯 对二甲苯
1,2-dimethylbenzene 1,3-dimethylbenzene 1,4-dimethylbenzene
CH3
CH3 CH3
CH3 CH3 CH3
CH(CH3)2
CH
CH2
toluene
o-xylene
mesityene
cumene
styrene
2 芳基
芳基:芳烃去掉一个氢剩下的原子团,用Ar表示。 常见的有苯基用Ph表示,苄基用Bz表示。
CH2
苯基 phenyl 苄基 benzyl
3 多取代苯衍生物的命名 环上取代基顺序:
均-三甲苯 1,3,5-三甲苯
从最简单的取代基开始编号,使取代位次最小为原则。
CH3 H3 C CH CH3
H3C CH3
CH3 CH CH3
1-甲基-4-异丙基苯
2,4-二甲基-1-异丙基苯
在外文名称中,IUPAC允许甲苯、(邻、间、对)二甲苯、
1,3,5-三甲苯、异丙苯、苯乙烯的俗名继续使用,并可作 为母体名称来命名其衍生物。
OH
α位: 1,4,5,8 β位: 2,3,6,7 2-萘酚;β-萘酚;乙萘酚
α位: 1,4,5,8
β位: 2,3,6,7
γ位(中位): 9,10
3 2 1 10
α位: 1,4,5,8 β位: 2,3,6,7 γ位(中位): 9,10
芳香烃
H || —C—C— || H
C
| —C—C
× |
C
思考:产物是什么?
CH3 | CH3—CH—
C| H3
CH3 |
—C—CH3 |
KMnO4/H+
| CH3
CH2—R
思考:产物是什么?
CH3 | CH3—CH—
C| H3
CH3 |
—C—CH3 |
HOOC
KMnO4/H+
|
| CH3 CH2—R
稠环芳烃:苯环之间通过共用苯环的若干环边
而形成
萘(C10H8)
蒽(C14H10)
三、芳香烃的来源及其应用 1、芳香烃主要来源:
煤高温干馏后得到焦炭、煤焦油、粗氨水、粗苯和焦炉气。将煤焦油 分馏,便可获得芳香烃。现代工业生产,芳香烃主要来源于石油化学工业 中的催化重整和裂化
2、芳香烃的应用:
在芳香烃中,作为基本有机原料应用最多的是苯、乙苯和对二甲苯等 苯是生产本分、硝基苯、苯胺、环己烷、二氯苯、氯苯、苯乙烯等重 要有机化合物的原料。通过这些有机化合物又可生产多种合成树脂、合成 纤维、染料、医药、洗涤剂、合成橡胶、炸药等
❖ 2、通式:CnH2n-6(n≥6)
❖ 3、特点:
❖ (1):苯环上的取代基必须是烷基(CnH2n+1 )。(2):分子中只含 有一个苯环,
❖ (3):分子组成相差n个CH2
二、苯的同系物
苯的几种同系物的结构简式
C| H3
甲苯(C7H8)
C| H2CH3
C| H3
H3C C| H3 CH3
乙苯( C8H10)
第二课时
❖苯的同系物
芳香族化合物
历史含义:具有香味的物质
有机化学 第六章 芳香烃
(一) 芳烃的构造异构和命名 (二) 苯的结构 (三) 单环芳烃的来源 (四) 单环芳烃的物理性质 (五) 单环芳烃的化学性质 (六) 苯环上取代反应的定位规则 (七) 稠环芳烃 (八) 芳香性 (九) 富勒烯
第六章 芳烃 芳香性
• 芳烃——芳香族碳氢化合物。含有苯环的一 大类C、H化合物。 “芳香”二字的含义:
1,2,4,5-四甲苯
(2) 命名
命名时,一般以芳环为取代基,也可以芳环为母体。具
体情况,具体对待:
CH=CH2
CH=CH2
苯乙烯
对二乙烯基苯 CH=CH2
CH2Cl
CH2OH
苯氯甲烷 氯苄
苯甲醇 苄醇
• C6H5- 苯基(Ph-) ;
C6H5CH2- 苄基 ;
Ar- 芳基(芳环上去掉一个氢后,所剩下的原子团);
O
慢
H
SO3-
快 HSO4-
+
σ-络合物
SO3- 快
H3O+
SO3H + H2O
(丁) 烷基化反应机理
苯环烷基化反应中,AlCl3的作用是与卤烷起反应, 加速R+的生成:
RCl + AlCl3
R+ + AlCl4-
亲电试剂
+ R+
R
+H
σ-络合物
AlCl4-
R + HCl + AlCl3
苯环烷基化反应时,产生异构化的原因:
Br
p-二溴苯
注意:第二个卤素原子进入第一个卤素原子的邻、对位。
(乙) 硝化
+ HNO3
浓H2SO。4
50-60 C
芳香烃
CH3 CH3 CH3 连三甲苯
CH3 CH3 CH3
CH3
CH3
CH3
偏三甲苯
均三甲苯
3、苯环上连有多个烷基时,应使最小的基团有最 、苯环上连有多个烷基时, 小的编号。其余规则与脂环烃相似。 小的编号。其余规则与脂环烃相似。如:
CH3 CH2CH3
1-甲基-4-乙基苯 -甲基- -
4、 较复杂的(-NH2、-OH、-CHO、-COOH及C4以 、 较复杂的( 、 、 、 及 以 上R)把苯作为取代基,相应基团做母体。例如: )把苯作为取代基,相应基团做母体。例如:
CH2CH3
CH2CH2CH2CH3
甲苯
CH3 CH3
乙苯
NO2
正丁苯
Br
对二甲苯
硝基苯
溴苯
2、 苯环上连有三个相同基团时,用连、偏、均 苯环上连有三个相同基团时,用连、 来表示相对位置。 来表示相对位置。 注意必须是三个相同基团才能用连、 注意必须是三个相同基团才能用连、偏、 均来表示此三基团的相对位置。 均来表示此三基团的相对位置。
• 注意:当引入的烷基为三个碳以上时,引入的烷基 注意:当引入的烷基为三个碳以上时, 会发生碳链异构现象。 会发生碳链异构现象。
AlCl3
CH3 CH3
+ CH3CH2CH2Cl
CH
+
CH2CH2CH3
) 正丙苯(35~31% 异丙苯(65~69% )
原因:反应中的活性中间体碳正离子发生重排, 原因:反应中的活性中间体碳正离子发生重排,产生更稳定的碳正 离子后,再进攻苯环形成产物。? 离子后,再进攻苯环形成产物。?
亲电取代反应历程( 亲电取代反应历程(以溴代 反应为例) 反应为例)
芳香烃
H = –120kJ/mol
+ 3 H2
H = –208kJ/mol
苯的结构
苯分子是正六边形结构,六个碳原子和六个氢原子 在同一平面上,相邻的碳碳键之间的夹角是120, 碳碳键的键长都是0.139nm。 六个碳原子都是s p2杂化,所有的 键都在同一平 面上。每个碳原子都有一个未参加杂化的P轨道, 并且都垂直于键所构成的平面,六个p轨道侧面 相互重叠形成一个闭合的大 键共轭体系。大 键的电子云就象两个救生圈分布在分子平面的上下 方。 由于 电子的充分离域,离域能大,体系的势能就 低,因此,苯环就特别稳定。由于苯分子中所有的 碳碳键完全相同,为此,常常用正六边形内加一个 圆圈来表示苯的结构。
甲苯
乙苯
丙苯
异丙苯
单环芳香烃的异构和命名
苯的二元取代物有三种异构体。 例如:
C H3 C H3 C H3 C H3 C H3 C H3
1,2-二甲苯 1,3-二甲苯 1,4-二甲苯 (邻二甲苯或o-二甲苯) ( 间二甲苯或m-二甲苯) (对二甲苯或p-二甲苯)
单环芳香烃的异构和命名
取代基相同的三元取代物有三种异构体。 例如:
C H3 H3 C C H3 C H3 C H3 H3 C C H3 C H3 C H3
1,2,3-三甲苯 (连三甲苯)
1,2,4-三甲苯 (偏三甲苯)
1,3,5-三甲苯 (均三甲苯)
苯基
苯分子上去掉一个氢原子剩下的基团 C6H5—叫做苯基。可简写作Ph-。
甲苯基和苯甲基
甲苯分子中苯环上去掉一个氢原子, 得到甲苯基,
苯的共振能
+ 3 H2
150.0(共振能)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
芳香烃
第二单元芳香烃第一课时要点:1芳香族化合物及芳香烃的概念
2苯的分子结构特点及物理性质:(1)分子式、结构简式(2)分
子空间构型(3)苯分子中C原子成键特点3苯的化学性质:(1)
苯的溴代实验(2)苯的硝化实验(3)苯的加氢加成反应【问】根
据有机物的分类,我们知道有机物中有一类物质称为芳香族化合物,最初发现的这类物质绝大部分都是具有香味的,它们是从各种天然
的香树脂、香精油中提取出来的。
目前,已知的很多芳香族化合物
其实并不具有芳香气味,所以,“芳香族化合物”这一名称已经失去
了原先的意义,只是一直沿用至今,那么现在我们所定义的芳香族
化合物是一类怎样的物质呢?它们在结构上有什么共同的特点呢?
芳香族化合物——分子结构中含有苯环的有机物。
【问】什么是烃
类物质?只含有C、H元素的一类有机物。
把这两类物质合并起来,取个交集,就是我们今天要研究的一类有机物——芳香烃。
芳香烃——芳香族碳氢化合物,简称芳香烃或芳烃。
一苯的结构与性质1
苯的结构(1)分子式:C6H6(2)结构式:【交流与讨论】那么苯
分子的结构是怎样的呢?①苯的1H核磁共振谱图(教材P48)苯分
子中6个H所处的化学环境完全相同苯分子结构的确定经历了漫长
的历史过程,1866年,德国化学家凯库勒提出苯环结构,称为凯库
勒式:那么凯库勒式能完全真实的反应苯分子的结构吗?根据以下
信息,谈谈你对苯分子结构的认识?②苯的一取代物只有一种,邻
位二取代物只有一种和是同一种物质③苯不能使溴水腿色,不能使
酸性高锰酸钾溶液腿色④碳碳双键加氢时总要放出热量,并且放出
的热量与碳碳双键的数目大致成正比。
苯在镍等催化下可与氢气发
生加成反应生成环己烷,所放出的热量比环己二烯与氢气加成生成
环己烷的还要少。
说明苯环中并不存在单双键交替的结构,因此凯
库勒式不能全面的反应苯的结构,只是习惯上沿用至今。
【过渡】
那么苯分子的结构到底是怎样的?拓展视野:苯环中的碳原子都是
采用的sp2杂化,碳原子之间形成σ(sp2-sp2)键,六个C原子的
p轨道重叠形成一个大π键。
苯分子中碳碳键的键长都是一样长的
(1.4×10-10m),这说明碳原子之间形成的一种介于单键和双键之
间的特殊共价建,所以苯的结构可以表示为:或(3)分子空间构型
平面正六边形,12个原子共平面。
2苯的性质(1)物理性质苯是一
种没有颜色,有特殊气味的液体,有毒。
密度比水小,与水不互溶。
3苯的化学性质1苯的溴代反应原理:+Br2+HBr
装置:现象:1向三颈烧瓶中加入苯和液溴后,反应迅速进行,溶液几乎“沸腾”,一段时间后反应停止2反应结束后,三颈烧瓶底
部出现红褐色油状液体(溴苯)3锥形瓶内有白雾,向锥形瓶中加
入AgNO3溶液,出现浅黄色沉淀4向三颈烧瓶中加入NaOH溶液,产生红褐色沉淀(Fe(OH)3)注意:1直型冷凝管的作用——使苯和
溴苯冷凝回流,导气(HBr和少量溴蒸气能通过)。
2锥形瓶的作用——吸收HBr,所以加入AgNO3溶液,出现浅黄色沉淀(AgBr)3
锥形瓶内导管为什么不伸入水面以下——防止倒吸4碱石灰的作用——吸收HBr、溴蒸气、水蒸汽。
5纯净的溴苯应为无色,为什么
反应制得的溴苯为褐色——溴苯中溶解的溴单质6NaOH溶液的作用——除去溴苯中的溴,然后过滤、再用分液漏斗分离,可制得较为
纯净的溴苯7最后产生的红褐色沉淀是什么——Fe(OH)3沉淀,反
应中真正起催化作用的是FeBr32苯的硝化反应:原理:+HO-
NO2+H2O装置:现象:加热一段时间后,反应完毕,将混合物倒
入盛有水的烧杯中,在烧杯底部出现淡黄色油状液体(硝基苯)注意:1硝基苯难溶于水,密度比水大,有苦杏仁味2长导管的作用——冷凝回流3为什么要水浴加热——(1)让反应体系受热均匀;(2)便于控制温度,防止生成副产物(因为加热到100~110℃时
就会有间二硝基苯生成;4温度计如何放置——温度计水银球应伸
入水浴中,以测定水浴的温度。
3苯的加成反应在催化剂镍的作用下,苯与H2能在180~250℃、压强为18MPa的条件下发生加成反
应+3H24总结苯的化学性质:由于苯分子中的碳碳键是一种介于单
键和双键之间的特殊共价键,所以苯的化学性质,几乎也是介于饱
和烃和不饱和烃之间。
总的来说化学性质比较稳定、是易取代、难
加成。
第二课时二芳香烃的来源与应用1来源:(1)煤煤焦油芳香
烃(2)石油化工催化重整、裂化在芳香烃中,作为基本有机原料应
用的最多的是苯、乙苯和对二甲苯2苯的同系物(1)概念苯的同系
物只有一个苯环,它们可以看成是由苯环上的H被烷烃基代替而得
到的。
例如:甲苯乙苯对二甲苯(2)性质A氧化反应实验:甲苯中加入酸性KMnO4溶液→KMnO4溶液腿色乙苯中加入酸性KMnO4溶液→KMnO4溶液腿色结论:苯的同系物能被酸性KMnO4溶液氧化解释:苯的同系物中,如果与苯环直接连接的碳原子上连有H原子,该苯的同系物就能使酸性KMnO4溶液腿色,与苯环相连的烷烃基通常回被氧化为羧基
B取代反应+3HNO3+3H2O
TNT(三硝基甲苯)TNT是一种不溶于水的淡黄色针状晶体,烈性炸药。
(3)乙苯的制备
+CH2=CH2以前采用无水AlCl3+浓盐酸做催化剂,污染较大而且成本较高。
现在采用分子筛固体酸作催化剂,这种催化剂无毒无腐蚀且可完全再生。
3多环芳烃
总结:各类型烃的结构特点与化学性质对比碳碳键结构特点化学性质烷烃烯烃炔烃芳香烃。
