金属钝化实验中电流密度图像
《金属钝化》课件

深入研究金属钝化的微观机制与动力学过程
微观结构研究
深入研究金属钝化膜的微观结构、组成和性质,揭示其形成机制和 稳定性机理。
动力学过程分析
分析金属钝化过程中的动力学过程,包括反应速率、反应机理等, 为优化金属钝化技术提供理论支持。
跨学科研究方法
综合运用物理、化学、材料科学等多学科的理论和方法,深入探究金 属钝化的本质和规律,推动金属钝化技术的发展和应用。
金属钝化是一个热力学上有利的反应,意味着在一定条件下,金属 表面会自发形成钝化膜。
03
金属钝化的影响因素
金属的种类与合金元素
总结词
金属种类和合金元素对钝化效果有显著影响。
详细描述
不同金属的电子结构和表面特性不同,导致钝化行为差异。合金元素可以改变 金属的电子结构,从而影响钝化过程。例如,某些合金元素可以促进或抑制钝 化。
《金属钝化》PPT课件
contents
目录
• 金属钝化概述 • 金属钝化的原理 • 金属钝化的影响因素 • 金属钝化的应用 • 金属钝化的研究方法与技术 • 金属钝化的挑战与未来发展方向
01
金属钝化概述
定义与特点
定义
金属钝化是指金属在某些特定的介质中,由于表面生成了一 层非常薄的、致密的、覆盖性良好的固态物质,使金属的活 性大大降低,从而使其腐蚀速率明显减缓的现象。
提高安全性
对于一些重要的工程结构和设备,如桥梁、建筑、管道等 ,金属的耐腐蚀性直接关系到其安全性能。通过金属钝化 处理,可以提高这些结构的安全性。
金属钝化的历史与发展
历史回顾
金属钝化现象早在古代就已被人们发现和应用。例如,古代的兵器表面处理、铜器表面 的氧化膜等。随着科技的发展,人们对金属钝化的研究越来越深入,对其应用也越来越
物理化学-试验二十一:碳钢在碳酸铵溶液中的钝化行为与极化曲线的测定
实验二十一碳钢在碳酸铵溶液中的钝化行为与极化曲线的测定一、实验目的1.测定碳钢在碳酸铵溶液中的阳极极化曲线2.掌握线性电位扫描法测试阳极极化曲线的基本原理和方法。
二、实验原理线性电位扫描法是指控制电极电位在一定电位范围内、以一定的速度均匀连续变化,同时记录下各电位下反应的电流密度,从而得到电位-电流密度曲线,即稳态极化曲线。
在这种情况下,电位是自变量,电流是因变量,极化曲线表示稳态电流密度与电位之间的函数关系:i=f(Φ)。
金属作阳极的电解池中通过电流时,通常将发生阳极的电化学溶解过程。
如阳极极化不大,阳极溶解过程的速度随电势变正而逐渐增大,这是金属的正常阳极溶解。
在某些化学介质中,当电极电势正移到某一数值时,阳极溶解速度随电势变正反而大幅度降低,这种现象称做金属的钝化。
处在钝化状态的金属的溶解速度是很小的,在金属防腐及作为电镀的不溶性阳极时,这正是人们所需要的。
而在另外的情况如化学电源、电冶金和电镀中的可溶性阳极,金属的钝化就非常有害。
利用阳极钝化,使金属表面生成一层耐腐蚀的钝化膜来防止金属腐蚀的方法,叫做阳极保护。
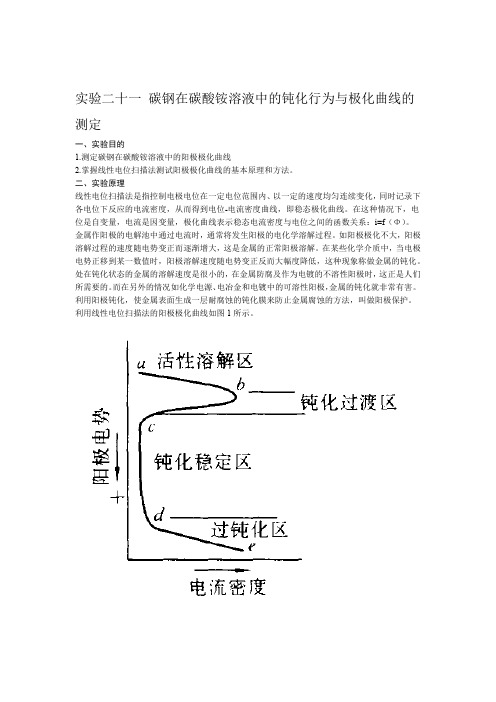
利用线性电位扫描法的阳极极化曲线如图1所示。
图1 阳极极化曲线曲线表明,电势从a点开始上升(即电势向正方向移动),电流也随之增大,电势超过b点以后,电流迅速减至很小,这是因为在碳钢表面上生成了一层电阻高、耐腐蚀的钝化膜。
到达c点以后,电势再继续上升,电流仍保持在一个基本不变的、很小的数值上。
电势升至d点时,电流又随电势的上升而增大。
从a点到b点的范围称为活性溶解区;b点到c点称为钝化过渡区;c点到d 点称为稳定区;d点以后称为过钝化区。
对应于b点的电流密度称为致钝电流密度;对应于c-d 段的电流密度称为维钝电流密度。
如果对金属通以致钝电流(致钝电流密度与表面积的乘积)使表面生成一层钝化膜(电势进入钝化区),再用维钝电流(维钝电流密度与表面积的乘积)保持其表面的钝化膜不消失,金属的腐蚀速度将大大降低,这就是阳极保护的基本原理。
第4章金属腐蚀极化曲线与测试方法课件

问题:腐蚀极化图(伊文思(Evans)图)原理与用途?
• 将腐蚀状态金属进行极化,电位从腐蚀电位偏离 • 阴极极化时极化电流
阴 极 极 化
lgiK
注意:均匀腐蚀用电流密度,局部腐蚀用电流强度
• 如果阴极极化使两极均远离平衡,则阴极极化电流ik:
•1
即表观总电流:
是相对于平衡电极的过电位么?
每个反应均有其真实极化曲线Ii=fi(E)
• 总的I-E曲线称为实验或表观极化曲线 特点:
(主要参考书:曹楚南,《腐蚀电化学》)
2、实测(表观)极化曲线(I-E曲线)与真实极化曲线的关系
• 腐蚀体系表观极化曲线(I-E曲线)的合成、分解
表观极化曲线
阳极电流
平衡电位
真实极化曲线
阴极电流
腐蚀电位
平衡电位
问题:已知真实阴极极化曲线,如何获得真实阳极极化曲线?
作业(WORD或PPT文件皆可)
1、简要回答: 实测与真实哪种极化曲线体现了阳、阴极反应的真实性?如何获得 真实极化曲线?
2、简要比较: 电位-pH图、波尔贝图、腐蚀极化图、Evans图、极化曲线的区别? 写出从腐蚀极化图推导的腐蚀电流计算公式,表明其与极化率、电 阻有何关系?
表观腐蚀电流腐蚀电位阳极平衡电位阴极平衡电位相似此后两线接近相似即可获得ei真实极化曲线3阳极钝化金属腐蚀的极化曲线?金属阳极钝化曲线平衡电位钝化电位过钝化电位钝化电流维钝电流活化电位flade电位活化溶解区钝化区过钝化区活化钝化过渡区钝化膜局部破坏的阳极曲线小孔腐蚀电位击穿电位临界孔蚀电位不到过钝化电位即发生破坏阳极钝化金属的腐蚀极化曲线具有完整阳极钝化曲线金属的腐蚀极化曲线可分多种情况
问题:
钝化曲线的测量

点蚀研究方法--钝化曲线的测量1.金属的钝化原理在以金属作阳极的电解池中,通过电流时,通常会发生阳极的电化学溶解过程:M →M n++ne 。
当阳极的极化不太大时,溶解速度随着阳极电极电位(电极电位)的增大而增大,这是金属正常的阳极溶解。
但是在某些化学介质中,当阳极电极电位超过某一正值后,阳极的溶解速度随着阳极电极电位的增大反而大幅度地降低,这种现象称为金属的钝化。
研究金属的钝化过程,需要测定钝化曲线,通常用恒电位法。
将被研究金属例如铁、镍、铬等或其合金置于硫酸或硫酸盐溶液中即为研究电极,它与辅助电极(铂电极)组成一个电解池,同时它又与参比电极(硫酸亚汞电极)组成原电池。
以镍作阳极为例,其基本测量线路如图,这个测量回路实际上分为两部分,一是研究电极和辅助电极形成的极化回路,由mA 表测量极化电流的大小;二是参比电极与研究电极形成的电位测量回路。
图中WE 表示研究电极,CE 表示辅助电极,RE 表示参比电极。
参比电极与研究电极组成原电池,可确定研究电极的电位;辅助电极与研究电极组成电解池,使研究电极处于极化状态。
通过恒电位仪研究电极给定一个恒定电位后,测量与之对应准稳态电流值I 。
以通过研究电极的电流密度i 的对数lgi 对超电位作图,即得到金属的钝化曲线。
超电位η即为电速密度为i 时的阳极电极电位E(i)与i=0时的阳极电极电位之差:()(0)i ηϕϕ=-图是Fe 在1.0mol/L H 2SO 4溶液中的阴极极化和阳极极化曲线图。
AR 为阴极极化曲线,当对电极进行阴极极化时,阳极反应被抑制,阴极反应加速,电化学过程以H 2析出为主。
AB 为阳极极化曲线,当对电极进行阳极极化时,阴极反应被抑制,阳极反应加速,电化学图1.恒电位法测定金属钝化曲线 图2.阴极极化和阳极极化曲线图过程以Fe溶解为主。
在一定的极化电位范围内,阳极极化和阴极极化过程以活化极化为主,因此,电极的超电位与电流之间的关系均符合Tafel方程。
6金属的钝化

电流密度i(mA/cm2) 800
600
B
400
钝化体系的阳极极化曲线
(Fe在10% H2SO4中)
A~D,电位增加 腐蚀速度减小
E
200
A
-250
0 +250
| 1|
+500 2
C
+750 |3|
D
+1000 +1250 +1500 +1750 +2000 电位(mv)
4
|
5
|
钝化体系的极化曲线
(4)交点在过钝化区
当去极化剂是特别强的氧化剂时,在自然腐
蚀状态金属发生过钝化。
返回
6.2实现自钝化的途径
自钝化条件:
E+>Ep;
≥ (ic)Ep ip
影响阳极极化曲线
E
ia
●
Ep
|ic|
lgi
ip (ic)Ep
使真实阳极极化曲线向左、向下移动。
(1)提高金属材料的钝化性能。
(2)加入阳极性缓蚀剂,抑制阳极反应,使ip降低。
B
i致 i
阳极保护
用阳极钝化方法达到减小金属腐蚀的目的,这
种防护技术叫做阳极保护。 阳极保护的适用条件是:
(1)具有活态—钝态转变。 (2)阳极极化时必须使金属的电位正移到稳定
钝化区内。
★阳极保护是危险性保护
钝化体系的类型
腐蚀体系的稳定状态取决于真实阴极 极化曲线和真实阳极极化曲线的交点。根 据交点位置不同,体系可有四种类型。
第六章 金属的钝化
钝化现象
• 研究钝化现象的意义 • 钝化现象的实验规律 • 金属钝化的定义
钝化体系的极化曲线
金属腐蚀电化学理论基础钝化详解PPT课件

lgi
➢ 单电极的极化方程和金属腐蚀速率方程:
A
E
E
e A
2.303 RT
F
lg
i0
2.303 RT
F
lg
iA
C
ECe
E
2.303 RT
F
第lg1i20 页/共2.4300页3FRT
lg iC
E EeC
氧扩散
阴极浓差极化(吸氧腐蚀)动力学
id
Ecorr
M →Mn+ + ne-
EeA
➢ 单电极的极化方程
2H++2e- → H2 M → Mn+ + 2e-
O lgiH,o lgiM,o lgicorr lgi
E EeC
氧扩散
E
EeO2
ηO
P
B
C
F EeH2
S
Q G
Ecorr EeA O
id M →Mn+ + ne-
lgi
lgiM,0
lgicorr
N
O
id
ic
完整的阴极极化曲线
第14页/共40页
二、金属钝化的电极过程
若金属原先处于B点的活化态, 则在该介质中不会钝化;
若金属原先处于D点的钝化态, 则在该介质中不会活化;
金属的钝化ppt

阴离子。常用的是由卤素离子及OH一、
SCN一等,特别是Cl—对钝化膜的破坏作用
最为突出。
钝化膜穿 孔发生溶 解所需要 的最低电 位值—临 界击穿电 位,随 Cl—浓度 增加,而 减少 。
阴离子浓度和电位对金属表面状态的影响
实验中采用的是100g/L的NaOH溶液对Al的 氧化膜进行的破坏,没有经过处理的铝棒以急快 的速度进行了溶解,而经过阳极氧化和着色处理 后的铝棒在将近十分钟的时间后才开始慢慢地被 腐蚀掉,对比图如下
4.钝化膜的性质
无定形绒毛状氧化物,含水较多,成分结 构多变;类似凝胶,具有强的吸附性。钝 化膜的种类很多,常见有氧化膜,还有磷 酸盐膜、硫酸盐膜、硫化物膜、氯化物膜、 氟化物膜等。钝化膜的组成以及性质与溶 液的pH值、阴离子性质、浓度和电极电位 有关。
氧化膜的多孔结构决定了其具有很强的吸 附性。 实验中,我们将经过阳极氧化处理的铝棒 进行了着色处理,得到了颜色较均匀的铝 棒
钝化膜的性质 钝化膜的性质与溶液的pH值、阴离子的性 质、浓度和电极电位有关系。
钝化膜的组成 (1)钝化膜组成与金属本身、溶液组成有关 (2)钝化膜的性质决定了钝化膜的钝性的大 小 (3)金属钝化膜稳定的条件是:在溶液中化 学溶解度小,附着力强、结构致密、环境 中没有让钝化膜还原或氧化溶解的因素。
成相膜理论与吸附膜理论比较
共同点 :是都认为由于在金属表面生成一 层极薄的膜阻碍了金属的溶解; 不同点 :在于对成膜的解释。吸附膜理论 认为形成单分子层的二维膜导致钝化;成 相膜理论认为至少要形成几个分子层厚的 三维膜才能保护金属,最初形成的吸附膜 只轻微的降低了金属的溶解速度,而完全 钝化要靠增厚的成相膜。
氢氧化钠对铝棒造成了碱蚀, 但其比未经过阳极氧化前时间要 就很多,主要是由于实验中我们 对样品进行了封闭处理,使腐蚀 介质不能很容易的浸入孔内进行 腐蚀,所以腐蚀时间会相应延长。
第06章 金属的钝化

stop 6.1 金属的钝化现象Phenomenon of Metallic Passivation6.2 阳极钝化Anode Passivation6.3 Flade电位与金属钝态的稳定性E F and Stability of Metallic Passivation6.4 金属的自钝化Metallic Self-Passivation6.6 金属的电化学保护Electrochemistry Protection of Metal 6.5钝化理论Theories of Passivation第六章金属的钝化一定时间内电位基本恒定不变,这个电位称活F 。
值越正,金属丧失钝态的倾向越大;负,金属越易保持钝态。
之间存在线性关系。
如0.059pH -2×0.059pH图6-36-1+E t0E F+EEF 越正,易保持钝态。
是衡量金属钝态稳定性的特征参数。
6-3图6-4若阴极过程为活化极化控制,极化曲线为Tafel不同的交换电密,阴极极化的影响有三种情况:阴极极化曲线与阳极极化曲线交于a点,该点处于活化区。
阴极极化曲线与阳极极化曲线有3个交点b阴极极化曲线与阳极极化曲线交于e点。
处于稳定钝化区。
条件易达到,但同时要满足在E pp下,点,才能实现金属自钝化。
图6-7图6-8Fig.6-9参比电极的作用是测量被保护金属设备的电位并向控制系统传送信号,以便调节保护电流和保护电位。
直流电源是提供保护电流的装置。
stop_+(辅助阳极)6-5stop6-6被保护金属图6-9 辅助阳极作用示意6-86-10。
