高等有机化学课后习题
高等有机化学各章习题及答案-(8)
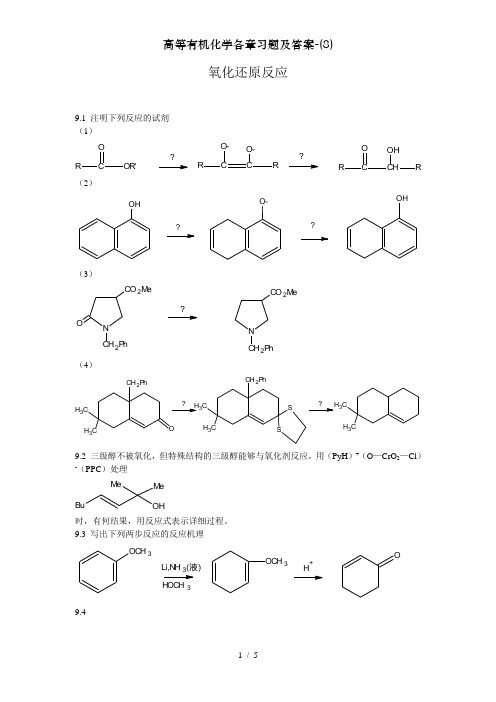
氧化还原反应9.1 注明下列反应的试剂 (1)ROR'O RCCO-RO-RO ROH ??(2)OHO-OH??(3)N O2P hCO 2M eN 2P hCO 2M e(4)C H 3CH 3CH 2P hOC H 3CH 3CH 2P hSSC 3H 39.2 三级醇不被氧化,但特殊结构的三级醇能够与氧化剂反应,用(PyH )+(O —CrO 2—Cl )-(PPC )处理BuOH M e M e时,有何结果,用反应式表示详细过程。
9.3 写出下列两步反应的反应机理OC H 3OC H 3OLi,N H (液)HOCH3H+9.4CO2HCH2COOHCO2HHO2用合成9.5 不饱和化合物A(C16H16)与OsO4反应,再用亚硫酸钠处理得B(C16H18O2),B与四乙酸铅反应生成C(C8H8O),C经黄鸣龙还原得D(C8H10),D只能生成一种单硝基化合物。
B用无机酸处理能重排为E(C16H16O),E用湿Ag2O氧化得酸F(C16H16O2),写出化合物A、B、C、D、E、F的结构式。
9.6 化合物A,分子式为C7H12,能使Br2—CCl4溶液褪色,A与稀冷KMnO4溶液反应得到一对旋光异构体B和C,若A与C6H5CO3H作用水解,则得到另一对旋光异构体D和E。
B、C、D、E互为同分异构体,将它们分别用HIO4处理后都得到同一化合物F,F能与2mol 苯肼反应,与Tollen试剂呈正反应,与NaOH+I2溶液作用生成黄色沉淀,试推测A、B、C、D、E、F的结构式。
9.7 提出下列反应机理(1)OC2H5O CO2C2H5O CO2OH1)LiAlH2)H3O+(2)C H2C OOE t O C C OOE t(C H3)2S(C H)SO+答案:9.1(1)Na,甲苯;CH3COOH(2)Li,液NH3;C2H5OH(3)B2H6(4)BF3,HSCH2CH2SH;Ni/H29.2BuOHM e M eCrOO OHOCH 3CH 3BuOCr OOHOH 3CH 3BuH CH 3OBuCH 3+Cr(Ⅴ)(P yH)+(O-Cr 2-C l)-9.3LiNH 3(液)Li +(NH 3)e-(NH 3)++OC H 3HHOC HCH3O-CH 3O +CH3OC H 3OC H 3O +H 2O +H CH 3OHOHOO+e-。
高等有机化学习题(1)

ProblemⅠWrite the IUPAC name for the following structures1.4-Ethyl-5-methyl octane2.5-(3-Pentenyl)-3,6,8-decatriene-1-yne3.Bicyclo[12,2,2]octadeca-14,16(1)diene4.5-methyl spiro[2,4]heptane5.4-Phenyl-2-naphthol6.1-methyl-1,2-ethanediol7.Magnesium di(1-propanolate)8.2-Hexen-4-ynedioic acid9.2,4,5-trioctanetriane10.Methyl 3-ethyl-5-phenyl heptanoate11.5,9,12,15,21-pentaoxaheptacosane-1,27-diol12.1,2-Cyclohexane dicarboxylic anhydride13.azocine14.6H-1,2,5-Thidiazine15.N-Methyl-N-propylpentylamine OR Methyl penthyl propyl ammonium16.1H-pyrazolo[4,3-d]oxazole17.4H-[1,3] oxathiolo[4,5-b]pyrroleWrite the systematic name for the following structures18.azine Hexahydrozine azole azolidone 1,2-Diazine 1,3-Diazine 1,3-Diazole1,2-oxazole oxin ThioleProblemⅡWrite the systematic name for the following structures1.3-bromo-2-(propenyl)-2,4-hexadienoic acid2.1-Ethoxy-6-octen-1-yne-3,5-dione3.4-chloro-2-methyl-2-cyclohexenol4.(2-methyl)butyl 3-bromo-2-hydroxy-2-methyl 3-butenate5.1,3,5-Naphthalene triacetic acid6.5-(4-Hydroxy-1-butynyl)-2-nonen-6-yne7.2-Amino-5-bromo diphenylamine8.4,5-Dichloro-2-(4-chloro-2-hydroxy methyl-5-oxo-3-hexenyl)-1-cyclohexane carboxylic acid9.N-(2,3-Dimethybutyl)-3,5-dihydroxy-3-ethyl pentanamide10.2-Ethyl-4-ethyl amino-2-methyl-3-oxobutanal11.2-hydroxy-1-(2-hydroxy-5methyl-1-phenylazo) Naphthalene-4-sulfonic acid12.Methyl 3-{4-[2-hydroxy-3-(1-methyl ethyl)amino propoxy]}benzenepropanoateProblem Ⅲ 1. Solution 1CH 3+Cl-F CH 3Cl +F △H =-105KJmol -1△H f146.5-51.1-88.178.5Solution 2Cl-FCl + FDH Cl-F =△H f (Cl )+△H f (F )-△H f (Cl-F)=250.9KJmol -1CH 3+Cl-F CH 3Cl +FDH250.9355.9△H =-105KJmol -12.C 6H 5C 6H 5(Liminting rate step)+(CN)2C=C(CN)2C 6H 56H 5(CN)2(CN)2C 6H 56H 5C 6H 56H 53.C 6H 5HN 6H 5C 6H 5N NH 2+ C 6H 5NNNC 6H 5NfastC 6H 5+ N 2C 6H 5+ C 6H 5N NH 2fast6H 6+ C 6H 5N=NH4.ClCH3NH-33- ClCH33NH2CH3+CH3 H2N5.(1) It is the first order isotopic effect K H/K D=6.76(2) It is a E2 reaction reaction6(1)A (2)A7.d[prod.]dt = k2[A-][HA],d[A-]dt= 0=k1[HA][B] - k2[A-][HA] - k-1[A-1][BH+][A-] =k1[HA][B]k2[HA] + k-1[BH+]Sod[prod.]dt=k1k2[HA]2[B]k2[HA] + k-1[BH+]for the general base catalysis, k2>>k-1d[prod.]dt =k1k2[HA]2[B]k2[HA]= k1[HA][B]for the specific base catalysis, k2<<k-1d[prod.]dt =k1k2[HA]2[B]k-1[BH+]but K b =[BH+][OH-][B]OH- is a specific base in the reactionSo d[prod.]dt =k1k2[HA]2[OH-]k-1k bProble mⅣ1.σm-IO2 = -3.50 + 4.2 = 0.70σp-IO2 = -3.44 + 4.2=0.76σp-xσm-x for m-NO2 ,for p-NO2 2.3.(1)ρ< 0(2)ρ> 0(3)ρ< 0(4)ρ< 0(5)ρ> 04.(1) pk a(p-Cl) = pk a–σp-Cl(2) pk a(p -Cl) = pk a -ρσp-Cl= pk a -ρσp-NO2(3) pk a(p -NO2)。
高等有机化学习题

高等有机化学习题第一章 化学键一、用共振轮说明下列问题1) 联本中的C 1-C 2键长为什么比乙烷中的键长短?联苯的硝化反应为什么主要发生在2-位和4-位?联苯的共振结构式可表是如下:(1) 由共振结构式可以看出C 1-C 2键有双键结构的贡献,故比乙烷的C 1-C 2键短。
(2) 由共振结构式可以看出邻对位负电荷相对集中,故有利于发生硝化反应。
2) 方酸为什么是强酸?(强于硫酸) 方酸的共振结构式可表是如下:对吗?由方酸的共振结构式可以看出方酸的电子离域效果更好。
二、试推测6,6-二苯基富烯的亲电取代发生于哪个环,哪个位置?亲核取代发生于哪个环,哪个位置?6,6-二苯基富烯的共振式如下:由6,6-二苯基富烯的共振式可以看出,亲电取代发生在五元环的2位上,而亲核取代发生在苯环的2位上。
三、计算烯丙基正离子和环丙烯正离子π分子轨道的总能量,并比较两者的稳定性。
烯丙基正离子有两个电子在成键轨道上其总能量为 E 烯丙基正离子=2E 1=2(α+1.414β)=2α+2.828β11'O HO O O O OH O O O OH O O OHO O O O S O O HO O S O O OH O S O O O S OOOH环丙烯正离子有两个电子在成键轨道上其总能量为 E 环丙烯正离子=2E 1=2(α+2β)=2α+2β 能量差值为E 烯丙基正离子- E 环丙烯正离子=(2α+2.828β)- (2α+2β)=0.828β 因此,环丙烯正离子比烯丙基正离子稳定。
四、用HMO 法分别说明烯丙基负离子和环丙烯负离子的电子排布和成键情况,并比较两者稳定性。
五、简要说明1)吡咯和吡啶分子的极性方向相反,为什么?吡咯分子中氮原子给出一对为共用电子参与了共轭分子的大π键,也就是电子从氮原子流向五员环,而吡啶分子中氮原子只拿出一个电子参与共轭,并且氮原子的电负性大于碳原子使电子流向氮原子的方向。
因此,两个分子的极性正好相反。
高等有机化学各章习题及答案 (7)

(Ⅰ)的水解存在分子内的亲核催化作用(邻基参与效应),故 (Ⅰ) 的水解速度比(Ⅱ)快。 6.2 按Cram规则,对羰基的加成产物可以由不对称碳上两个最小的取代基 (M,S)之间定位的基团所预测,试剂R从最小基团S—侧靠近,在上 例中苯基>乙基>甲基。
6.3(1)这是一个组合型的机理题,它涉及到亲核试剂对酮羰基的加成和 分子内的酯缩合。 (2) 6.4(1) (2) 6.5(1) (2) 6.6 (2) 6.7 这个机理的逆过程即为缩醛水解的机理。
ቤተ መጻሕፍቲ ባይዱ
羰基化合物的反应
6.1解释: (1)丙酮和H218O的混合物中,在中性条件下没有18O同位素交换,但 在微量酸性存在下,会存在下列平衡,说明理由。 (2)在二氧六环水溶液中,酯(Ⅰ)比酯(Ⅱ)的碱性水解速度快8300 倍。 6.2试解释为什么在反应(Ⅰ)和(Ⅲ)中会得到不同的结果。 由反应(Ⅰ)和(Ⅱ)得到的产物是非对映异构体。 6.3写出下列反应机理 (1) (2) 6.4完成下列反应 (1) (2) 6.5写出下列反应机理 (1) (2) 6.6试为下列反应提出合理的机理 (1) (2) 6.7对位取代的苯甲醛二甲基缩醛的形成和水解的速率与取代基有关。 预计随着对位取代基的吸电子能力增加k形成或k水解怎样变化?缩醛形成 的平衡常数K怎样变化?
由于第二步是速率决定步骤,不管是k形成还是k水解其大小都与中间体 Ⅰ和Ⅱ的稳定性有关,对缩醛形成来说,Ⅰ越不稳定,它的活性越高, k形成越大,对于缩醛水解来讲,Ⅰ越稳定,k水解越大,所以,随着取代 基X吸电子能力的增强,Ⅰ的稳定性减弱,k形成增加,k水解减弱。由于 苯环和醛基处于共轭体系,所以,对于吸电子基,增加了羰基碳的正电 性(亲电性),使它更易形成缩醛,K随之增大,相反,对于给电子基 团,K将减小。
高等有机化学各章习题及答案 (1)
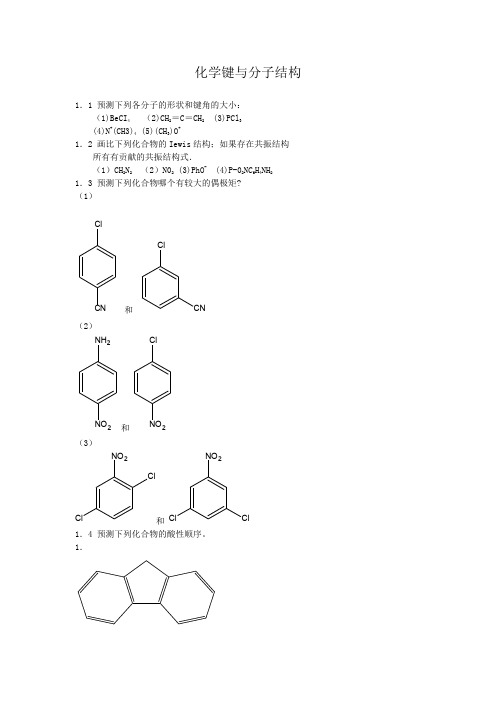
1.1 预测下列各分子的形状和键角的大小: (1)BeCI4 (2)CH2=C=CH2 (3)PCl3 (4)N+(CH3)4 (5)(CH3)O+
1.2 画比下列化合物的 Iewis 结构;如果存在共振结构 所有有贡献的共振结构式. (1)CH2N2 (2)N02 (3)PhO- (4)P-02NC6H4NH2
1.8 (2)和(7)不能形成分子间氢键 (1)HCN┈HCN (3)H2CO┈HOH
(6)H2NCH2CH2OH┈NH2CH2CH2OH
(4)Cl┈HOH
(5) (CH3)2CO┈HOOCC6H4OH
当第一个羧基上的 H+电离后,所形成的负离子是一个强的给电子基,它对第二个羧基所 发生的直接诱导,将使第二个羧基上好的电离趋于困难,这种影响也是顺式大于反式,所以 丁烯二酸的第二电离常数是顺式小于反式。这种诱导影响是通过空间或溶剂间的场效应传递 的。 1.6 (1)无芳香性
分子没有一个闭合的共轭体系,因而无芳香性,然后失去 H-以后生成的 A 为含有六个π 电子的离子,则具有芳香性。
1.8 下列各组化合物能否形成分子间氢键?若有的话,请画出分子间氢键。
(1)HCN 和 HCN (2)HCHO 和 HCHO
(3)HCHO 和 H2O
(4)Cl-和H
和丙酮
(6)HOCH2CH2NH2 和 HOCH2CH2NH2
答案: 1.1 (1)线性 (2)三个碳原子呈线型,氢位于相互垂直的平面上 (3)棱锥型,键角约
105~110°(4)正四面体 (5)棱锥型,键角约 105~110°。
1.2 (1) (2)
(3)
(4)
1.3 (1)Ⅰμ=2.5D Ⅱμ=3.4D (2)Ⅰμ=6.3D Ⅱμ=2.6D (3)Ⅰμ=3.48D Ⅱμ=2.68D
高等有机化学各章习题及答案 (4)

10.1 对于下列 A、B 反应途径,注明反应条件,并解释之。
O A H CH2 O H3CO CH2 H2C CH2 B
10.2 将化合物 A 加热时,可从反应混合物中分离出化合物 A。两个电环化反应相继发生: 第一个反应牵涉到一个 4π电子体系,而第二个反应则牵涉到一个 6π电子体系。略述第二 个电环化反应,并写出中间体的架构。 H
H
H
这个双键不参与第一个反应
三个双键全都参与第二个反应
10.3 (1)1,3—σ键迁移,异面迁移是对称性允许的,但由于分子的几何形形态,H 从一面转 移到平面的另一面所需能量较高,协同反应非加热所能活化。而 1,5—σ键迁移是对称性 允许的同面迁移,加热即可进行。 (2)最好用重氢标记的方法合成下列的分子,然后重排,反应物和产物的 1HNMR 不同。
D D D D △ CH2 CH2
10.4 (1) (Ⅰ)6π,△,对旋; (Ⅱ)△,C[1,3]σ同面迁移,构型翻转 (2) H3C CH3 1 H[1,7] Me[1,7] 2 7 C4H7对旋 (Ⅱ) (Ⅰ) (Ⅲ) 6 迁 移 环合 3 迁 移 H3C 4 5 10.5 (1)[3,3]σ迁移反应 (2)反应是通过椅式过渡态完成的 10.6
Cl 2 3 4 (甲) 5 1 6
7 Br 内向对旋 Cl 3;
7 5 6
Br
Br
2 3 4
Br Cl 1 7 6 5 外向对旋 Br-离去 H
+
H
Cl
假设离去基团的离去和 Cl—C6 键的打开(电开环)是协同的。 10.7 (1)
H3C C H C
+
H
H3C C S CH3 C H O Ph -CH C
大学《有机化学》课后习题答案
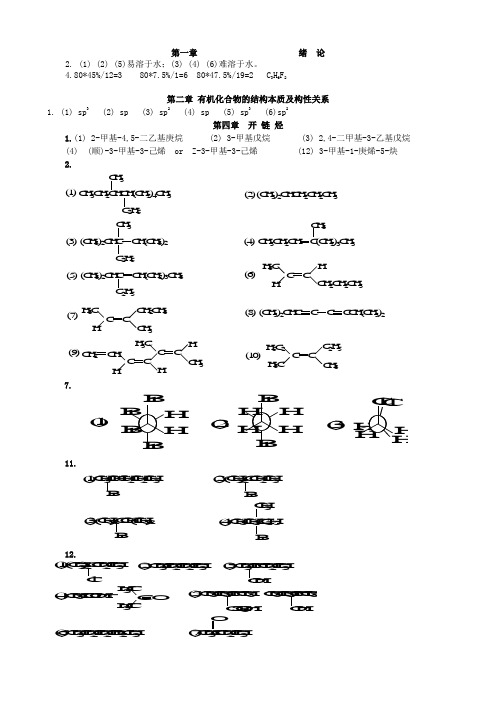
第一章绪论2. (1) (2) (5)易溶于水;(3) (4) (6)难溶于水。
4.80*45%/12=3 80*7.5%/1=6 80*47.5%/19=2 C3H6F2第二章有机化合物的结构本质及构性关系1.(1) sp3 (2) sp (3) sp2 (4) sp (5) sp3 (6)sp2第四章开链烃1.(1) 2-甲基-4,5-二乙基庚烷 (2) 3-甲基戊烷 (3) 2,4-二甲基-3-乙基戊烷(4) (顺)-3-甲基-3-己烯 or Z-3-甲基-3-己烯 (12) 3-甲基-1-庚烯-5-炔2.7.11.12.14. (5) > (3) > (2) > (1) > (4) 即: CH2=CHC +HCH 3 >(CH3)3C + >CH 3CH 2C +HCH 3 >CH 3CH 2CH 2C +H 2> (CH 3)2CHC +H 216. (1)(2)(3)17.21AB.10.(1)CH 3-CH=CH 2−−−−−→−+H /KMnO 4CH 3COOH(2)CH 3-C≡CH+HBr(2mol ) CH 3CBr 2CH 3(3)CH 3-3-C=CH 2−−→−2Br CH 3CBr 2CH 2Br 第四章 环 烃 2.1-戊烯 1-戊炔 戊 烷Br 2/CCl 4室温,避光√ 溴褪色√ 溴褪色× × √灰白色1-丁炔 2-丁炔 丁 烷Br 2/CCl 4 室温,避光√溴褪色 × Ag(NH 3)2+√灰白色↓ × ×1,3-丁二烯 1-己炔 2,3-二甲基丁烷Br 2/CCl 4√ 溴褪色 √ 溴褪色 × Ag(NH 3)2+×√ 灰白色↓C(CH 3)3CH 3(1)(2)(3)3.(1)反式CH 3Br(3)顺式4.C H 3B rC lC l +C l C lC O O HH 3CO 2N (C H 3)3C C O O H(1)(2)(3)(4)(5)(6)(7) B rC 2H 5C 2H 5B r +C H 3C O C H 3(C H 3)2C C H (C H 3)2B r(8) 1molCl 2 / h, 苯/无水AlCl 3N H C O C H 3N O 2C H 3C H 3S O 3H(9) (10)7. (2)有芳香性 10.第六章 旋光异构6-32. (1)× (2)× (3)× (4)√ (5)√ (6)√7.2.66120678.58.18][20+=⨯÷+=⨯=l c Dαα第七章 卤 代 烃2、C l C lC l (2)4、第八章 醇、酚、醚1. (1) 3-甲基-3-戊烯-1-醇 (2) 2-甲基苯酚 (3) 2,5-庚二醇 (4) 4-苯基-2-戊醇 (5) 2-溴-1-丙醇 (6) 1-苯基乙醇(7) 2-硝基-1-萘酚 (8) 3-甲氧基苯甲 (9) 1,2-二乙氧基乙烷(乙二醇二乙醚)(1)(2)3、4. (1) 甲醇 分子间氢键 (6) 邻硝基苯酚 分子内氢键、分子间氢键 5、(1)CH 2IH 3COOH(5)(6)HOOCH 3H(7)6、AgNO 3/乙醇,室温白↓× ×AgNO 3/乙醇,加热白↓×OH+OHBrBr(1)(2)10、OH O ClA B C D第九章醛、酮、醌一、命名下列化合物。
高等有机化学汪秋安课后习题答案

高等有机化学汪秋安课后习题答案1. 答案题目题目:将如下反应列出一次反应的化学平衡式,并指出每个反应物和生成物的类别。
反应: (a) 羰基化合物的还原 (b) 羧酸的酯化反应 (c) 核磁共振谱峰的解释 (d) 溴代烷的亲核取代反应 (e) 钯催化的Suzuki偶联反应1.1 答案解析(a)羰基化合物的还原还原的化学平衡式:R-C=O +2H2 → R-CH2OH 反应物:羰基化合物(R-C=O)生成物:醇(R-CH2OH)类别:有机化合物(b)羧酸的酯化反应酯化反应的化学平衡式:R-COOH+ R’-OH → R-COOR’ + H2O 反应物:羧酸(R-COOH)、醇(R’-OH)生成物:酯(R-COOR’)、水(H2O)类别:有机化合物(c)核磁共振谱峰的解释核磁共振谱峰的解释涉及到不同核磁共振峰对应的化学位移和峰积分的解释。
化学位移表示吸收峰在谱图中的位置,峰积分表示峰的强度或峰下面的面积。
每个峰的化学位移和峰积分可以提供有关分子结构和化学环境的信息,如化学官能团、取代基等。
(d)溴代烷的亲核取代反应亲核取代反应的化学平衡式:R-X + Nu^- → R-Nu + X- 反应物:溴代烷(R-X)、亲核试剂(Nu-)生成物:取代产物(R-Nu)、溴离子(X^-)类别:有机化合物(e)钯催化的Suzuki偶联反应 Suzuki偶联反应的化学平衡式:Ar(X)-B(OH)2 + R’-X → Ar(X)-R’ + B(OH)2-X 反应物:芳香化合物(Ar(X)-B(OH)2)、取代化合物(R’-X)生成物:偶联产物(Ar(X)-R’)、剩余反应底物(B(OH)2-X)类别:有机化合物2. 答案题目题目:简要描述一下以下有机化合物的结构和性质:(a)苯(b)乙酸乙酯(c)2-丙酮醛(d)正丁醇(e)反式-2-戊烯醇2.1 答案解析(a)苯:结构:苯是由6个碳原子(C)和6个氢原子(H)组成的环状芳香化合物,化学式为C6H6。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章习题1.用共振式说明苯甲醚分子中甲氧基的邻/对位效应。
2.比较下列各组化合物的酸性大小并予以解释。
(1)HOCH2CH2COOH 和CH3CH(OH)COOH (2)乙酸、丙二酸、乙二酸和甲酸(3)COOHNO 2和COOHHO(4)H 2C CH 2H 3C CH 3HC CH 、和3.比较碱性。
H 2N(1) CH 3CH 2NH 2 和(2)NH 2HO NH 2O 2N和(3)N HN和比较C-Br 键断裂的难易次序和CH 3CH 2CHCH 2CH 3CH 3OCHCH 2CH 3CH 3CH 2CHCF 2CF 3在极性条件下,、4.5.下列共振式哪一个贡献大,为什么?C C C C OAB6.在亲核加成反应中ArCH 2COR 和ArCOR 哪一个活性高,为什么?7.解释酸性大小。
COOH<COOH(1)COOH COOH(2)OH>8.为什么ArCOR 被HI 断裂时,得到的产物是RI 和ArOH ,而不是ROH 和ArI 。
9.下列反应中几乎不会生成PhCH 2CBr(CH 3)2,为什么?PhCH 2CH(CH 3)2 + Br 2 PhCHBrCH(CH 3)2 + HBr hv10.比较拗CH 3COCH 2COCH 3和CH 3COCH 2COOC 2H 5的酸性,并简要说明原因。
11.为什么胺的碱性大于酰胺?12.羧酸及其衍生物的亲核取代反应活性为什么是RCOCl>(RCO)2O>RC OOR’~RCOOH>RCONH 2。
13.为什么顺丁烯二酸的p K a1比反丁烯二酸小,p K a2却正相反?14.排列下列化合物与HCN反应的活性顺序。
NO2CHO(H3C)2N CHOCHO CHOCl(1)(2)(3)(4)15.五元杂环比苯更易进行亲电取代,为什么?第二章习题1.2-丁烯的顺反异构体,分别经稀、冷、碱性KMnO4水溶液氧化后,为什么生成的2,3-丁二醇都不能测出旋亮度?2.(R)-CH3CH2CH2CHDI在丙酮NaI溶液中共热,试解释下属现象,①化合物外消旋化;②有过量NaI128存在下,外消旋化速度是同位素交换的两倍;3.请根据下述现象,为反应H2C CH OC2H5 + H2O C2H5OH + CH3CHO提出反应机理:(1)该反应符合普通的酸催化反应.(2)水解反应速度在水中比在重水中快1.9倍.(3)如果用同位素标记的水进行水解,所得乙醇不含18O.(4)若在D2O中进行水解,只在乙醛中出现一个D.第4章习题1.完成下列反应。
(1)(CH3)2CHCH2CH2Cl2( )(2) (CH3)3N + CH3CHCH2CH3( )∆( )(3)NHC2H5过量CH3I( )( )(H3C)2N OC2H5OH-∆( )(4) 2CH3I + Na2S( )(5) ClCH=CHCH2Cl + CH3COONa( )(6) 2CH3I + NaOOCCOONa( )(7) CH3CSSNa + CH3( )2.卤代烷在甲醇水溶液中水解的历程为S N1,试推测溴甲烷、溴乙烷、2-溴丙烷和2-溴-2-甲基丙烷在甲醇吹溶液中水解的相对反应速度。
3.按S N1历程排列下列化合物的相对反应活性。
(1)苄溴、α-溴乙苯、β-溴乙苯(2)BrBrBr4.按S N2历程排列下列化合物的相对反应活性。
(1)溴甲烷、溴乙烷、2-溴丙烷、2-溴-2-甲基丙烷(2)PhBr、PhCH2Br、PhCHBrCH3(3)CH3CH2Br、CH3CH2Cl、CH3CH2I5.比较下列各组亲核试剂的亲核性大小。
(1)在质子性溶剂中:I-、Br-、Cl-、F-(2)在非质子性偶极溶剂如DMF和DMSO中:I-、Br-、Cl-、F- (3)CH3CH2-、(CH3)2N-、CH3O-、Cl-(4)CH3O-、C2H5O-、(CH3)2CHO-、(CH3)3CO-6.写出下列每组反应最可能发生的反应式并指明其历程。
(1) C2H5I + CH3O-CH3OH?(2) CH3Cl + KCN CH3OH?(3) CH2=CHCH2Br + CH3COONa?(4) PhCH2Br + OH-H2O?(5) CH3CCl2 + OH-H2O?7.解释下列反应结果。
(1) (CH3)2CHCHBrCH3 + Ag+252(CH3)2CHCHOC2H53+ (CH3)2C(OH)CH2CH3(2) (CH3)3CCH2Br + Ag+25H2O(CH3)2C(OH)C2H5+ (CH3)2C(OC2H5)CH2CH3+(CH3)2C=CHCH3CH2Br-2CH2OH+(3)8.二战期间德国法西斯使用的战场毒气ClCH2CH2SCH2CH2Cl是一种极活泼的烷基化试剂,与人体接触后使人体蛋白质迅速发生烷基化,从而中毒死亡。
用碱水对其处理消毒时,发现水解速度与OH-浓度无关,但随Cl-浓度增大而减慢。
试提出一个可能的历程解释这一现象。
9.S-3-甲基-3-溴己烷在丙酮水溶液中反应,得到外消旋体3-甲基-3-己醇,写出其反应历程。
10.写出新戊基碘在乙酸银和乙酸作用下得到乙酸叔戊酯的反应历程。
11.写出形成下列产物的历程。
CHClCH3Ag+2CH3OH+CH(OH)CH3+ CH3CH=CHCH2CH2OH12.以苯、甲苯以及四碳以内的有机原料合成下列化合物。
(1)(2)(3) CH 3CH=CHCH=CH 2(4) PhCH=CHCH 313.用化学方法区别CH 3CH 2CCl=CH 2、CH 3CHClCH=CH 2和ClCH 2CH 2CH=CH 2。
14.化合物A 与Br 2/CCl 4溶液作用可生成一种三溴化合物B ,A 容易与NaOH 水溶液作用,生成互为异构体的醇C 和D ,A 与KOH/C 2H 5OH 作用可生成一种共轭二烯E ,将E 臭氧化分解可得一分子乙二醛和4-氧代戊醛。
试推导A 、B 、C 、D 和E 的结构。
15.用丙二酸酯合成下列化合物,有机原料不超过四个碳,无机试剂任选。
CH 2OH(1)OH (2)HOOCCOOHCOOH NH 2CH 2OHCOOH COOH(3)(4)COOH(5)16.用乙酰乙酸乙酯合成下列化合物,有机原料不超过四个碳,无机试剂任选。
(1) CH 3COCH 2CH 2COPh(2)COCH 3(3)OO (4)CH 3O(5)第七章习题1.写出下列反应的主产物。
(1)CH 2+ NBS ?(2)H 2CCH COOH + HI?(3)C C HH 3CCH 3H(4)(CH 3)2C CH 2+ PhSCl??+ HOCl 2.完成下列反应。
RCH 2CH 2??2)Zn, H 2O?4.完成反应,写出第一步所生成的活性中间体。
CH 2CH COOH+ HCl?(2)CH 2CH CF 3+ HCl ?(3)CH 2CH 3)3+ HCl ?(CH 3)2C CH OEt + HCl ?(4)(5)CH 3COCl +CH 2CH 2?3(6)(CH 3)3CCl +CH 2CH 2?3(7)CH 3OCH 2Cl +CH 2CH 2?3CH 3CH 2CH CH (8)?AlCl (9)CH 3CH 2CH CH ?500~7000C CH 3CH 2CHCH ?(10)3.把下列各组烯烃按与HOCl 加成的活性大小排列成序。
(1)乙烯、丙烯、2-丁烯 (2)乙烯、溴乙烯、氯乙烯 (3)1-丁烯、2-丁烯、异丁烯(4)氯乙烯、溴乙烯、1,2-二氯乙烯(5)1-戊烯、2-甲基-1-丁烯、2-甲基-2-丁烯 (6)乙烯、丙烯、丙烯酸(7)丙烯、异丁烯、2-氯-1-丙烯、3-氯-1-丙烯 5.写出下列产物的立体结构。
C CH HC CH 2(1)+ Br CCl 4C CH 25CH 2+ Br 2hv(2)(3)C H 3C H C CHC CCH 33(4)Br CH 3CH 2+ HBr(5)+ CCl 2?????6.写出下列反应可能的历程。
(2)(5)CH 2CHCH(CH 3)2+ HBr 3CHBrCH(CH 3)2 + CH 3CH 2CBr(CH 3)2(1)CH 2CHC(CH 3)3+ HBr3CHBrC(CH 3)3 + CH 3CH(CH 3)CBr(CH 3)2(3)2(CH 3)2CCH 2+(CH 3)3CCH C(CH 3)2+(CH 3)3CCH 2CCH 2CH 3(4)CH 2=CH 2 + Br 2NaCl 2BrCH 2CH 2Br + BrCH 2CH 2OH + BrCH 2CH 2ClCH 2=CH-CH=CH 2 + Cl 23CH 3OCH 2CH=CHCH 2Cl + CH 2=CHCH(OCH 3)CH 2Cl(6)CH 3CH=CH 2H +2CH 3CH 3OH7.完成下列转变。
(1)CH 3CH=CH 22Ca(OH)( )( )(2)CH HBr过氧化物( )-4(3)CH 3CH=CH 2BrCH 2CHBrCH 2Cl( )(4)CH 2CH 3500CHBr 过氧化物( )(5)H 3C+ Br 2H O( )(构象式)(6)CH 3CH 2CH=CH 2Br 500CC 2H 5ONa ( )C 2H 5OH(7)CH 3(1) B 2H 622-CrO ( )( )CHCH 2RCOOOH2( )( )(8)(9)CH 3C CH + CH 3CH 2MgBr33( )( )( )(10)(1) O 3(2) Zn/H 2O第八章习题1.完成下列反应。
(1)O( )+ (C 6H 5)3P=C(CH 3)2( )(2)OHCH 2CHO+ (C 6H 5)3P=CHCH(CH 3)2CH 2(CO 2Et)2(1) C H ONa 25( )(1) C 2H 5ONa 3( )-+(3) ∆( )(3)(4) CH 3COCH 2CO 2Et(1) C H ONa (2) n-C 4H 9Br( )+(3) ∆( )(5) CH 3COOEt(1) PhMgBr 3( )(6) CH 3CH 2COOH + NH ∆25( )(7) (CH 3)2CO HCN -( )2HCl ( )∆(8)COOEtCOOEt25(1) C 2H 5ONa 3( )( )COCH 3COCH 3(9)2( )(10)CO 2Et CO 2Et(1) C H ONa +( )O+ CH 2(CO 2Et)225( )(1) C H ONa 22( )(11)2.将下列化合物按其亲核加成的活性顺序排列。
