有机合成化学
有机化学基础知识点整理有机合成反应的分类和机理

有机化学基础知识点整理有机合成反应的分类和机理有机化学是研究碳元素及其化合物的科学,是化学的重要分支之一。
在有机化学中,有机合成是一项关键的技术,用于合成复杂的有机分子。
有机合成反应是有机化学中最基本、最重要的内容之一,它通过不同的化学反应方式将简单的有机化合物转化为复杂、有用的有机分子。
一、有机合成反应的分类1. 加成反应:加成反应是指两个或多个分子的化学键被断裂,并形成新的键。
常见的加成反应有羰基化合物的加成反应、烯烃的加成反应等,这些反应能够构建碳碳键和碳氧键。
2. 消除反应:消除反应是指一个分子中的两个官能团结合并成为一个新的官能团,并且释放出一些小分子(如水或卤素)。
典型的消除反应有醇的脱水反应、酮或醇与酸脱水等。
3. 置换反应:置换反应是指原有分子中的一个官能团被另一个官能团所取代。
最常见的例子就是芳香族化合物的取代反应,通过氯代烷和芳香环之间的反应来实现。
4. 氧化还原反应:氧化还原反应是指反应中发生氧化和还原的过程,也是有机合成中最常用的反应之一。
在氧化还原反应中,电子转移导致了化学键的形成或断裂,它可以将一个官能团转化为另一个官能团。
例如,醛可以通过氧化反应转化为羧酸。
5. 缩合反应:缩合反应是指两个或多个分子之间的化合物反应,生成一个更大分子的过程。
例如,胺和酮缩合反应可以生成相应的醛。
二、有机合成反应的机理1. 加成反应机理:加成反应一般经历亲核试剂(nucleophile)攻击电子不足的位点,形成共价键,断裂旧键。
以酮和亲核试剂为例,亲核试剂攻击酮羰基碳上的δ+空穴,使酮羰基碳上的键断裂形成负离子中间体,之后再与亲核试剂发生亲核加成反应生成产物。
2. 消除反应机理:消除反应通常需要考虑酸碱性质和受限杂原子(如O、N等原子)对反应的影响。
脱水反应机理中,醇中的-OH基质子化生成强酸,然后酸催化下分子内的-ОН离子和酸质子反应,释放出水分子,从而形成双键。
3. 置换反应机理:典型的置换反应是芳香族化合物的取代反应。
什么是有机合成化学?

什么是有机合成化学?有机合成化学是研究有机化合物的制备方法和反应机理的学科。
有机合成化学的发展历史源远流长,它是现代有机化学的基础和核心。
本文将重点介绍有机合成化学的基本概念、方法和应用。
一、有机合成化学的基本概念有机合成化学是研究有机化合物的制备方法和反应机理的学科。
有机化合物是由碳、氢和其他元素构成的化合物,其分子中通常包含碳-碳键或碳-氢键。
有机合成化学的目的是通过特定的化学反应,将已知化合物转化为目标化合物,或从简单的原料中构筑出复杂的有机分子。
二、有机合成化学的基本方法1. 分子设计和合成路线规划有机合成化学的第一步是设计目标化合物的分子结构,确定反应的具体路径和步骤。
分子设计需要考虑合成的可行性、经济性和环境友好性。
合成路线规划需要考虑反应的选择性、高效性和产率。
2. 基本反应类型有机合成化学中常用的基本反应类型包括取代反应、加成反应、消除反应和重排反应等。
取代反应是指一个官能团被另一个官能团取代,加成反应是指两个或多个分子结合形成一个新的分子,消除反应是指分子中某些原子或基团被去除,重排反应是指分子结构的重组或转变。
3. 试剂的选择和反应条件的优化有机合成化学中,选择合适的试剂和优化反应条件是确保反应达到预期目标的关键。
试剂的选择取决于目标化合物的结构和反应的类型,反应条件的优化需要考虑温度、压力、溶剂、反应时间等因素。
三、有机合成化学的应用有机合成化学在药物合成、农药合成、材料合成等领域具有广泛的应用价值。
1. 药物合成有机合成化学在药物合成中起到重要作用。
药物的研发离不开大量有机合成的支持,通过有机合成可以合成出各种药物分子骨架和官能团,从而拓展药物的结构多样性和活性。
2. 农药合成有机合成化学在农药合成中也起着关键作用。
农药合成需要合成具有特定活性和安全性的化合物,通过有机合成可以合成出各种农药分子,提高农作物的产量和质量。
3. 材料合成有机合成化学还应用于材料合成领域。
通过有机合成可以制备出各种高分子材料、功能性材料和纳米材料,用于电子、光学、能源等领域。
有机化学有机合成ppt课件

合成路线:
浓 HNO3
浓H2SO4
Br
H2 Fe NO2
NH2 Br
Br2
NaNO2 H3PO2
Br
Br H2SO4 H2O
Br
Br
NH2
17
例四:用苯和二个或二个碳以下的有机原料和无机试剂合成:
OH + N Cl-
逆合成分析:
OH + N Cl-
O
N
OH N
O + HCHO + HN(CH3)2
H+
CH2OH
32
例十一 用苯,苯甲酸和五个碳以下的简单有机原料合成:
Ph O
O Ph
33
逆合成分析:
Ph O
O
Ph CHO
+ PhCH2CH2MgBr
OH Ph
CH2OH
PhCH2CH2Br
Br + CH2O
PhCH2CH2OH
O PhMgBr +
34
合成路线:
Br2
Mg Br anhydrous
7
(3) 碳架的重组;
碳架重组的反应是各种重排反应,包括: *1 Wegner-Meerwein 重排; *2 频哪醇 (Pinacol) 重排; *3 异丙苯氧化重排; *4 Bechmann 重排; *5 Favosky 重排; *6 Baeyer-Villiger 氧化重排; *7 Hofmann 重排; *8 联苯胺重排; *9 Benzilic acid重排;
H2O OH
Br Mg/I2
无水醚
H+
O CH3I O
O
OH
23
例七 用不超过二个碳的简单有机原料或苯合成下列化合物: O
大学化学实验:有机化学合成反应

大学化学实验:有机化学合成反应引言有机化学合成反应是大学化学实验中非常重要的一部分。
通过有机合成,我们可以合成各种有机化合物,探索不同反应条件对反应产物的影响,并理解有机化学原理和反应机制。
本文将介绍一些常见的有机化学合成反应及其实验操作方法。
1. 水杨酸合成1.1 实验目的水杨酸是一种重要的中间体,广泛用于制药、染料等领域。
本实验旨在通过苯酚和氧化剂制备水杨酸。
1.2 实验步骤1.将苯酚溶解在稀碱溶液中;2.加入适量的氧化剂,如过氧化氢;3.反应保持在室温下进行数小时;4.过滤沉淀并洗涤后得到水杨酸。
1.3 实验结果与讨论根据实验结果分析生成的水杨酸纯度和收率,并讨论可能影响产率的因素。
2. 醇与卤代烃之间的置换反应2.1 实验目的通过醇与卤代烃之间的置换反应,合成不同醇的卤代衍生物。
2.2 实验步骤1.将醇和卤代烃溶解在有机溶剂中;2.加入适量的碱催化剂;3.反应保持在适当温度下进行数小时;4.分离得到产物。
2.3 实验结果与讨论根据实验结果分析生成的卤代衍生物纯度和收率,并讨论可能影响反应速率和产率的因素。
3. 脱水反应:醇与酸催化剂反应3.1 实验目的通过脱水反应,将醇转化为烯烃或环状化合物。
3.2 实验步骤1.将含有醇的混合物与酸催化剂混合;2.加热反应混合物至适当温度;3.反应保持在一定时间后停止加热;4.分离得到产物。
3.3 实验结果与讨论根据实验结果分析生成的产物纯度和收率,并讨论不同条件对脱水反应产物选择性的影响。
结论有机化学合成反应是大学化学实验中的重要内容,通过实验操作可以深入理解有机化学原理和反应机制。
本文介绍了水杨酸合成、醇与卤代烃之间的置换反应以及脱水反应三个常见有机化学合成反应,并给出了实验步骤和结果讨论。
这些实验可以帮助学生掌握有机合成基础知识,并为将来的研究和工作打下坚实的基础。
有机合成化学试题及答案

有机合成化学试题及答案一、选择题(每题2分,共10分)1. 下列化合物中,哪一个不是芳香化合物?A. 苯B. 呋喃C. 环戊二烯D. 环己烷答案:D2. 在有机合成中,下列哪种反应不是还原反应?A. 氢化B. 还原胺化C. 氧化D. 硼氢化答案:C3. 以下哪个不是卤代烃的反应?A. 亲核取代B. 消除反应C. 还原反应D. 氧化反应答案:D4. 在有机合成中,下列哪种试剂不用于形成碳碳双键?A. 格氏试剂B. 羰基化合物C. 卤代烷D. 醇答案:D5. 以下哪个化合物不是烯烃?A. 乙烯B. 丙烯C. 环己烯D. 环己烷答案:D二、填空题(每题2分,共10分)1. 有机合成中,_________是一种常用的保护羟基的方法。
答案:甲硅烷基化2. 烷基化反应中,常用的烷基化试剂是_________。
答案:卤代烷3. 在有机合成中,_________反应可以用于合成环状化合物。
答案:Diels-Alder4. 有机合成中,_________是一种常用的氧化剂。
答案:铬酸5. 有机合成中,_________反应可以用来合成酯。
答案:酯化三、简答题(每题5分,共20分)1. 简述格氏试剂的制备过程。
答案:格氏试剂的制备通常涉及将卤代烷与金属镁在干燥的乙醚中反应,生成相应的格氏试剂。
2. 描述一下亲核取代反应的机理。
答案:亲核取代反应通常涉及一个亲核试剂攻击一个电性中心(如卤代烷),导致旧键的断裂和新键的形成。
3. 什么是E1和E2消除反应?它们的主要区别是什么?答案:E1和E2消除反应都是形成碳碳双键的反应。
E1是一个分步过程,涉及一个碳正离子中间体;而E2是一个协同过程,不涉及中间体。
4. 简述氧化还原反应在有机合成中的重要性。
答案:氧化还原反应在有机合成中非常重要,它们可以用来增加或减少分子中的氧化态,从而改变分子的化学性质和反应性。
四、计算题(每题10分,共20分)1. 给定一个反应:2-丁醇 + 铬酸→ 2-丁酮 + 水。
高中《化学》有机合成思路与方法
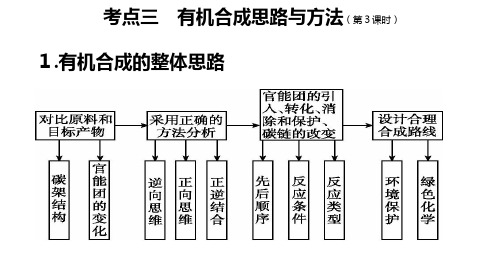
(2).官能团的消除 (1)消除双键:加成反应。 (2)消除羟基:消去、氧化、酯化反应。 (3)消除醛基:还原和氧化反应。 (3).官能团的保护 在引入一个新官能团或将某一官能团加以转换时,若反应会影响分子中原有的官能 团,则应对这一官能团进行保护。例如在含有碳碳双键的分子中,欲将羟基氧化时, 应先把碳碳双键保护起来,以防被破坏。为了保护其他官能团而人为引入的基团, 称为保护基。保护基的选择应满足以下条件:①易于引入且不影响分子中其他部位 结构;②形成的保护基在后续反应中保持稳定;③在保持分子其他部位结构不被破 坏的情况下易于除去。试题中出现的大多是对(酚)羟基、醛基、氨基、碳碳双键 等易于被氧化的官能团进行保护。
(3)成环的方法
①二元醇脱水成环醚; ②二元醇与二元羧酸成环酯; ③羟基酸分子间成环酯; ④氨基酸分子间成环等。 ⑤ 双烯合成[狄(弟)尔斯-阿尔德反应]
4. 有机合成路线的设计
能力要求:能利用不同类型有机化合物之间的转化关系及能
够从题给合成路线中选用必要的合成方法,设计合理路线
合成目标化合物。 综合能力要求高,是考查的难点! 一般是3分,也是拉开差距的部分!!!
和
为原料制备
的路线(无机试剂任选)。
(1)合成路线为:
(1)
(2)已知 :
。设计以
的路线(无机试剂任选)。
和
为原料制备
理解信息中给出的成环反应, 虚线左边来自于二烯烃,虚线右边来自于单烯烃,结合原
料中有含醛基物质,可推出
可由
与氢气加成反应得到,而
可
由 CH2=CHCH=CH2 和 CH2=CHCHO 加成得到。而 CH2=CHCH=CH2 可由 CH3CH=CHCH3 与溴发生加成反应,然后再发生卤代烃的消去反应得到,进而得到合成路线图。
有机合成化学10130149

吡咯烷类化合物的合成背景:吡咯烷即四氢吡咯,具有弱碱性,分子式为C4H9N,为无色至黄色液体,有刺鼻气味,避光密封保存,用作医药原料、有机合成、特殊有机溶剂。
其取代物具有很广泛的用途,例如l-Boc一3一氰基4-吡咯烷酮是一种药物的中间体,1一正丙基一2一吡咯烷酮是一种重要的与水互溶的有机溶剂,吡咯烷-2,3,5-三酮是合成稠杂环化合物的重要中间体等。
因此研究这类物质的合成方式,提高合成的产率对药物合成很有帮助。
摘要:吡咯烷酮的合成一般都需要依靠氮原子的孤对电子,由于孤对电子的存在,与氮原子连着的氢都比较活泼,容易发生加成反应或取代反应。
而环化反应使合成路线中最重要的一步,环化反应的类别多种多样,有通过周环反应环化,也有消去反应。
但由于合成路线较长,总体上讲收率都不太高。
本文将以3种吡咯烷类化合物为例讲述吡咯烷类化合物合成的几种思路。
(1)合成N-取代的吡咯烷酮①由γ -丁内酯与脂肪烃伯胺在高温、高压条件下,经过一步合成N一取代的吡咯烷酮衍生物是目前工业生产上应用最多、最广泛的合成方法。
反应第一阶段是γ -丁内酯与脂肪烃伯胺生成4一羟基一N一烷基丁酰胺;第二阶段是脱水生成N一烷基取代的吡咯烷酮,两阶段反应可在反应器中连续进行,中间体不需要分离。
以N-辛基吡咯烷酮为例,反应历程为两部,首先是胺化开环,胺化开环实际上是伯胺对γ -丁内酯进行的亲核加成反应,形成开环产物的一个过程。
γ -丁内酯分子内羰基O原子受氢离子影响带上部分负电荷,加上羰基本身的吸电子效应,使得羰基C原子带上部分正电荷而被活化,碱性较强的伯胺分子以N原子进攻被活化的羰基C原子发生亲核加成反应,生成链状酰胺,完成胺化开环过程,水可作为该开环过程的催化剂。
其次是缩合闭环,缩合闭环是由链状羟基丁酰胺脱水缩合成为五元环的过程。
理论上说是由非稳态转变为稳态的过程,应该是一个自发过程,但是本文中缩合闭环要比胺化开环困难得多,这可能是中间体羟基丁酰胺变为相应的吡咯烷酮时需要越过的能垒△E值较大。
有机合成化学ppt

7
8 O2N N
1 12 O2N N
9
6 N NO2
2 N NO2 5
10
11
O2N N
3
4 N NO2
图 1-1 HNIW的结构图
1.2 有机合成化学的任务
二、有机合 成化学要为 理论工作提 供具有多种 特殊性能的 分子,以验 证和发现新 的理论。
HH
HO
OH
H
H
O
N
H2C
N
N
H2NOC
Me H2NOC
六、光化学反应(光诱导反应)目前已达到了很高程度地化学、区域和立体控制 的水平。光化学机理研究和合成应用也是当前的研究热点。
1.3 有机合成反应和方法学
七、电有机合成近年来得到了进一步的重视和发展,在精细化工合成上可 能有发展前景,在基础研究方面正努力进一步改善电合成的选择性,并开拓其 应用范围。
OH
OH OH
OH
HO
OH
OH
OHOH
OH
HOΒιβλιοθήκη OHOOOH
OH
HO
N
N
O
OH
H
H OH
OH
OH
HO
O
OH
O OH
OH
OH O
OH
O
OH
OH
HO OH
O HO
OH
OH
OH
OH
OH
HO
OH
OH
海葵毒素
1.2 有机合成化学的任务
MeO
Me O
MeO
O
N
H OH
MeO
O
OH Me
O OH O H Me
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ON
1) 2SmI2 ,THF 2) H O+
3
O NH2
Possible Mechanism:
+ 2+
RX
Sm
RX-.
+ 2+
R
Sm
R + SH
(Solvent)
R + SH
. + RX-
3+
Sm
R +X
+ R
3+
Sm
. RH + S
RH + S
R
+ 2+
O
Sm
R
R. CO R
+
+
H
(or SH)
+ 1
RN3
2
RCN
1 . 2 SmI2/ THF 2. 10% K2CO3
H 1N
R2
R
NH
1
RN3
SmI2
.1
RN SmI2
2
RCN
SmI2
1
RN
R2
N2
N.
SmI2
SmI2
1
RN
R2
H2 O
1
HRN
R2
NSmI2
NH
Yield: 60-72%
J. Chem. Res.(s), 2001, 32
_
SmI2
ArX + PhZ THF-DMF
ArZPh + X
ArX=PhI, 1-BrPh, 1-BrAdm, 2-ClQuin
_
_
_
_
_
PhZ =PhSe , PhCH2Se , PhTe , PhS
Heteroatom Chem. 2001, 12, 539
O ArC Cl
1
SmI2
ArCO2
OSmI2
+
H
R
OH R
SmI2、SmI3促进的有机反应
SmI2 PhCOCH2Br THF
1. RCHO 2. H2O
O Ph
H
H R
SmI2 PhCOCH2Br -SmI2Br
_ Sm(III)/I PhCOCH2Br
O
.
Ph CH2
Sm(III) _
O
I
Br Ph
SmI2 -IBr
OSm(III) Ph
+ O
Ph
R1
2.2SmI2 Ph RCN THF, reflux R1
O
OH OH
R + Ph
Ph
OH
R1 R 1
O
Ph
R1
. SmI2
OSm2 R2CN
Ph R SmI2
Ph
OSmI2 R2
R1 NSmI2
H2O, HCl
Ph R1
H2O, HCl
O
R2 OH
I2SmO OSmI1
Ph
Ph
R1 R 1
R. + 2+ C OH Sm
R
R
C
OH
+
+
H
R
(or SH)
R. CO R
+ 3+
Sm
R. C OH R
R
+ C OH
3+
Sm
R
RH C
R OH
RX +
SmI2
R+
O
SmI2
SmI2
OSmI2
.
+
H
OH
R
OSmI2 R
RX + SmI2
R + SmI2
O
RSmI2 +
R + SmI2X
RSmI2
n-C12H25I n-C12H25OTs
2SmI2 2SmI2
+ n-C4H9I
n-C6H13COCH3
n-C12H26
n-C12H26
2SmI2
CH3 n-C6H13C n-C4H9
OH
PhCH2Br 2SmI2 PhCH2CH2Ph
PhCH2CH CH2 O
2SmI2 PhCH2CH CH2
CH3CN Ar
2
O2CAr Ar
Yield: 70-85% cis:/trans 90/10-95/5
O
SmI2
Ar C Cl
O
Ar C .
O
OO Ar C C Ar SmI2
2 SmI2 Ar C-
O
Ar CC........O_...
Ar
O
Ar
O
Sm I SmI2
C
2-
C
Ar
O
A
B
Ar O C Ar Sm I 2ArCOCl C
活泼金属参与的有机合成反应
Mediate Promote Catalyst
活泼金属参与的有机反应
1、还原反应
Metal
NO2
NH2
R
H+
R
M = Zn Fe Sn
R
Na
R
R
NH3(l)
R
Claimenson Reduction
O
R
R'
Zn-Hg H+
O
R
R'
R
R'
Zn
RBr
mechanism
ArNO2 2 SmI2
. . ArNO
SmI2
RCN ArN OSmI2
Ar
OSmI2
N
N
SmI2
I2SmOSmI2
R
Ar
OSmI2
N
N
SmI2 2 SmI2
Ar
SmI2 N
N SmI2 OH2
R
R
I2SmOSmI2
ArNH R NH
J. Chem. Soc. Perkin Trans. 1, 1998, 2899
H2O, HCl C
OH OH
Ph
Ph
R1 R 1
Tetrahedron Lett. 1998, 39, 8491
SRN1 Reaction of Haloarenes with Benzenethiolate, Benzeneselenolate, and
Benzenetellurolate ions Promoted by SmI2
-I2
_ I PhCOCH2Br
O Ph
_ Sm(III)/I
O
Sm(III)
_ I
I
I
Ph
Synth. Commun. 1988, 18, 2003
O
1
R
X + R3CHO SmI3
THF
R2
X=Br, COCH3, COOCH3
OH
1
R
R3
R2
Tetrahedron Lett. 1993, 24, 4547
O
+ Br
R
R'
Metal H2O
OH R'
R
M = Bi Al In Sm Sn
金属钐参与的有机反应
E0 aq Sm3+/Sm2+ = -1.55V
Kagan:
+ Ln ICH2CH2I THF
+ LnI2 H2C CH2
Ln=Sm, Yb
n-C7H15CHO
2SmI2
n-C7H15CH2OH
R'
R'
2、还原偶联反应
Mg or Sm
O
toluene
HO OH
3、Grinard 反应
Mg
RX
ether
R Mg X
O
R Mg X +
R''
R'
OH
R''
R'
R
4、Reformatsky 反应
X
OEt
Zn
R
ether
O
OH
R''
R'
OEt
R
O
ZnX OEt
R
O
O
R'' R'
5、Barbier 反应
C Ar O C Ar
O C
Chin. J. Chem. 2001, 19, 634
金属钐/辅助试剂促进的有机反应
Sm/I2 (cat)体系
RSSO3Na
Sm/Cat. I2 THF, r.t.
RSSR
Synth. Commun., 1997, 27 ,1043
RN3
Sm/Cat. I2 MeOH, N2, r.t. or reflux
O C6H5CCH2Br SmI2 or SmI3
RCOCl
OOO
OO
C6H5 H H
R OO
C6H5 COOH
Tetrahedron Lett., 1996, 37, 3885
+ R1NO2
R2CN 1.SmI2 (6 eq.), THF, r.t. 2. 10% K2CO3
H R1 N
R2
NH
