常见物质的相对原子质量分别是多少
相对原子质量

求NH4HCO3中N的质量分数 158克该物质中含有氮元素多少克? 某元素质量=整体的质量×该元素含量
1
2
练习:
4.求Fe2O3中Fe 元素的质量分数是多少? 50克氧化铁中含铁元素多少克?
15、已知相对原子质量:Cu-64 C-12 O-16 H-1, 在Cu2(OH)2CO3中 该物质由_4_种元素组成;一个该物质的分子中含有 _5_个氧原子;一个该物质的分子中含有_10_个原子; 该物质的分子中的原子个数比为:Cu:C:H:O= __2:1:2:5_; 该物质的式量为__222 该物质中各元素的质量比为:Cu:C:H:O= 该物质中所占质量分数最大的元素是_ _元素; 该物质中Cu元素的质量分数为_______; 22.2克该物质中含Cu元素____克。
79
碳酸氢铵由_____种元素组成。
10
1:3:5
4
已知下列元素的相对原子质量分别为: H:1 S:32 O:16 则H2SO4: (1)由_____种元素组成 (2)一个H2SO4分子中含有_____个原子 (3)各元素的原子个数比为_________ (4)各元素的质量比为_________ (5)式量为___________
3
2:1:4
7
1:16:32
98
相对原子质量和式量的相关计算
1、式量(相对分子质量)
已知相对原子质量为Ca-40 C-12 O-16 求 CaCO3 和 Ca (OH)2的式量
2、在上述两种化合物中各元素的原子个数比
3、求上述两种物质中各元素的质量比
4、在CaCO3 中O元素的质量百分含量(质量分数)
01
03
02
Байду номын сангаас
一些常见元素的名种.符号.相对原子质量
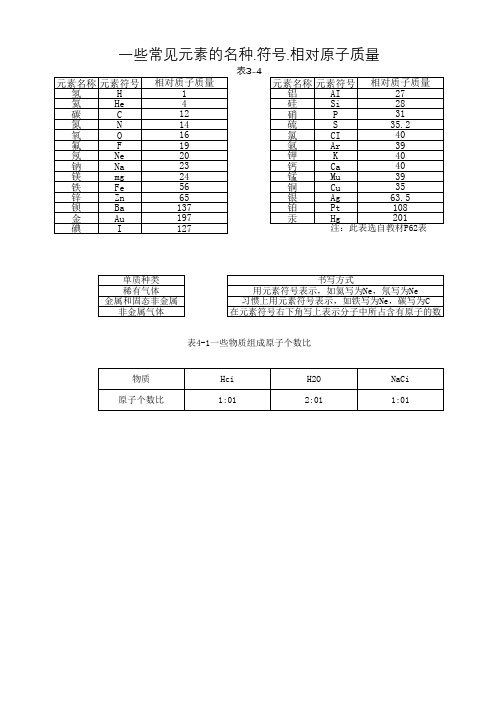
表3-4 元素名称 元素符号 氢 H 氦 He 碳 C 氮 N 氧 O 氟 F 氖 Ne 钠 Na 镁 mg 铁 Fe 锌 Zn 钡 Ba 金 Au 碘 I 相对质子质量 1 4 12 14 16 19 20 23 24 56 65 137 197 127 元素名称 元素符号 铝 AI 硅 Si 硝 P 硫 S 氯 CI 氩 Ar 钾 K 钙 Ca 锰 Mu 铜 Cu 银 Ag 铂 Pt 汞 Hg 相对质子质量 27 28 31 35.2 40 39 40 40 39 35 63.5 108 201
注:此表选自教材P62表
单质种类 稀有气体 金属和固态非金属 非金属气体
书写方式 用元素符号表示,如氦写为Ne,氖写为Ne 习惯上用元素符号表示,如铁写为Ne,碳写为C 在元素符号右下角写上表示分子中所占含有原子的数字
表4-1一些物质组成原子个数比
物质 原子个数比
Hci 1:01
H2O 2:01
Nபைடு நூலகம்Ci 1:01
常用相对分子质量

常用相对分子质量在化学的世界里,相对分子质量是一个非常重要的概念。
它就像是化学物质的“身份证号码”,能够帮助我们更好地了解和研究各种物质的性质和反应。
那么,什么是相对分子质量呢?简单来说,相对分子质量是指化学式中各个原子的相对原子质量的总和。
首先,让我们来了解一些常见的单质的相对分子质量。
氢气(H₂)的相对分子质量约为 2,因为氢原子的相对原子质量约为 1,所以两个氢原子组成的氢气分子的相对分子质量就是 2。
氧气(O₂)的相对分子质量约为 32,氧原子的相对原子质量约为 16,两个氧原子组成的氧气分子相对分子质量就是 32。
氮气(N₂)的相对分子质量约为 28,氮原子的相对原子质量约为 14,两个氮原子组成的氮气分子相对分子质量就是 28。
接下来看看一些常见的无机化合物。
水(H₂O)的相对分子质量约为18,氢原子的相对原子质量约为1,氧原子的相对原子质量约为16,一个水分子由两个氢原子和一个氧原子组成,所以相对分子质量就是2×1 + 16 = 18。
二氧化碳(CO₂)的相对分子质量约为 44,碳原子的相对原子质量约为 12,氧原子的相对原子质量约为 16,一个二氧化碳分子由一个碳原子和两个氧原子组成,所以相对分子质量就是 12 +2×16 = 44。
再来说说常见的酸。
盐酸(HCl)的相对分子质量约为 365,氢原子的相对原子质量约为 1,氯原子的相对原子质量约为 355,所以盐酸的相对分子质量就是 1 + 355 = 365。
硫酸(H₂SO₄)的相对分子质量约为 98,两个氢原子的相对原子质量约为 2,硫原子的相对原子质量约为 32,四个氧原子的相对原子质量约为 64,所以硫酸的相对分子质量就是 2 + 32 + 4×16 = 98。
常见的碱也有其特定的相对分子质量。
氢氧化钠(NaOH)的相对分子质量约为 40,钠原子的相对原子质量约为 23,氧原子的相对原子质量约为 16,氢原子的相对原子质量约为 1,所以氢氧化钠的相对分子质量就是 23 + 16 + 1 = 40。
相对原子质量用符号表示

相对原子质量用符号表示相对原子质量是描述化学元素质量的一个重要概念。
它是指一个元素相对于碳-12同位素的质量比值。
相对原子质量是一个无量纲的物理量,用符号Ar表示。
在化学中,相对原子质量的概念非常重要,它可以用来计算化学方程式中各个元素的质量比例,从而帮助我们理解化学反应的过程。
相对原子质量的计算方法是将元素的质量与碳-12同位素的质量进行比较。
碳-12同位素被定义为质量为12的标准,其相对原子质量被定义为12。
其他元素的相对原子质量则是相对于碳-12的质量比值。
例如,氧的相对原子质量为16,表示氧的质量是碳-12质量的16/12倍。
相对原子质量可以通过化学元素周期表上的相对原子质量数值来查找。
周期表上每个元素都标有一个数值,这个数值就是该元素的相对原子质量。
例如,氧在周期表上的相对原子质量为16。
需要注意的是,相对原子质量是一个平均值。
因为元素存在多种同位素,它们的质量不同,所以相对原子质量是这些同位素的质量加权平均值。
例如,氧有三种常见的同位素,分别是氧-16、氧-17和氧-18,它们的相对原子质量分别为16、17和18。
由于氧-16比例最高,所以氧的相对原子质量一般取为16。
相对原子质量在化学计算中有广泛的应用。
在计算化学方程式中各个元素的质量比例时,我们可以利用相对原子质量来确定各个元素所含有的摩尔数。
例如,当我们需要计算氧化铁中铁和氧的摩尔比例时,可以利用铁和氧的相对原子质量来计算出它们的摩尔数比例。
另外,相对原子质量还可以用来计算化学反应中物质的质量变化。
当我们知道一个物质在反应中消耗或生成了多少摩尔时,可以利用相对原子质量来计算出它们对应的质量变化。
这对于理解和预测化学反应的结果非常重要。
总之,相对原子质量是描述化学元素质量比例的重要概念。
它可以通过化学元素周期表上的数值来查找,用于计算化学方程式中各个元素的摩尔比例和物质的质量变化。
熟练掌握相对原子质量的概念和应用方法,有助于我们更好地理解和应用化学知识。
常见物质相对原子质量

常见物质相对原子质量1. 哎,你知道吗,我最近在研究一个特别无聊但又挺有趣的话题——相对原子质量。
听起来是不是有点高大上?其实,这东西就跟我们平时吃的盐一样,无处不在,但又经常被我们忽略。
2. 先说说这玩意儿是啥吧。
相对原子质量,简单来说,就是原子的重量。
不过,这重量不是我们平时称东西的那种重量,而是一种相对的重量,是相对于碳-12原子的1/12来计算的。
为啥选碳-12呢?因为它稳定,而且数量多,好测量。
3. 举个例子,比如说氢,这玩意儿轻得跟羽毛似的。
它的相对原子质量是1,也就是说,如果碳-12是12个单位重,那氢就只有1个单位重。
这就好比你拿一个乒乓球和一个篮球比重量,乒乓球肯定轻得多。
4. 再来说说氧,这家伙就重一些了。
氧的相对原子质量是16,比氢重,但比起铁来,还是轻了不少。
铁的相对原子质量是56,这就好比你拿一个篮球和一个铅球比,铅球明显重得多。
5. 说到这儿,你可能会觉得,这玩意儿有啥用啊?其实,相对原子质量在化学里可重要了。
比如,你知道水的分子式是H2O,这意味着一个水分子由两个氢原子和一个氧原子组成。
根据相对原子质量,你可以计算出水分子的重量。
6. 我还记得上化学课的时候,老师让我们计算水分子的重量。
我当时就想,这有啥难的,不就是1+1+16嘛。
结果,老师一脸严肃地说,不对,应该是2*1+16,因为有两个氢原子。
我当时就懵了,原来这玩意儿还有乘法啊。
7. 现在想想,那时候的自己真是傻得可爱。
不过,这也说明了相对原子质量的重要性。
它不仅仅是一个数字,更是我们理解物质世界的基础。
8. 其实,相对原子质量这东西,就跟我们生活中的很多东西一样,看似简单,实则深奥。
就像我们每天呼吸的空气,看似无形,实则包含了氮气、氧气、二氧化碳等等。
这些东西,都是由不同的原子组成的,而它们的相对原子质量,决定了它们的性质。
9. 说回相对原子质量,这玩意儿虽然听起来枯燥,但你要是仔细研究,就会发现它其实挺有意思的。
哪里有相对原子质量

相对原子质量是元素的一个物理常数,通常用于表示一个元素的相对质量。
相对原子质量的数值可以在元素周期表中找到。
每个元素都有一个相对原子质量的标准值,该值与碳-12的相对原子质量相对比。
在元素周期表中,每个元素的相对原子质量通常以小数的形式标记在元素符号的下方。
例如,氢的相对原子质量为约1.008,氧的相对原子质量为约16.00。
这些数值表示元素的平均相对原子质量,考虑到自然界中不同同位素的存在及其相对丰度。
需要注意的是,相对原子质量是一个无量纲的比值,以碳-12的相对原子质量为基准。
碳-12的相对原子质量被定义为12。
其他元素的相对原子质量是相对于碳-12的比值。
相对原子质量
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Cl—35.5 Ca—40一、选择题(本题共15小题,每小题只有一个选项符合题意。
每小题1分,共15分)1.下列各图所示变化属于化学变化的是()A.灯泡通电发光 B.铁丝在氧气中燃烧 C.湿衣晾干 D.食盐水的蒸发2.生活中常见的下列物质,属于溶液的是()A. 牛奶B. 泥水C. 蔗糖水D. 花生油3.某含铁盐溶液能够在高浓度的碱性环境下长期稳定存在,且具有较强的灭菌消毒功能,该盐是一种绿色、无污染的净水剂,其化学式为Na2FeO3。
则其中铁元素的化合价是()A.+2 B.+3 C.+4 D.+64.下图所示的实验操作中正确的是()5.据报道,科学家己经研制出世界上最薄的材料一碳膜片,其厚度只有一根头发的二十万分之一。
如右图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是()A. 碳膜片属于单质B.碳膜片与C60是同一种物质C. 碳膜片属于人工合成的有机高分子材料D.碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同6.学习化学的目的,不在于要成为化学家,重要的是要善于用化学知识去分析、解决生产、生活中的问题。
从化学角度看,下列说法中错误的是()A.发现燃气(天然气、煤气或液化石油气等)泄漏,点火检查出泄漏处B.进入小煤窑严禁吸烟C.炒菜时油锅着火,可用锅盖盖灭火焰D.面料厂、加油站严禁烟火7.在氧化铁(Fe2O3)、氧化亚铁(FeO)和四氧化三铁(Fe3O4)这三种铁的氧化物中,铁的质量分数按由大到小顺序排列的是A.Fe3O4、Fe2O3、FeO B.FeO、Fe2O3、Fe3O4C.FeO、Fe3O4、Fe2O3 D.Fe2O3、Fe3O4、FeO8.为了区别CO(可能混有氧气)与CO2两瓶无色气体,下列方法中可行的是A.分别通入少量澄清石灰水,振荡。
B.伸入燃着的木条。
常用的相对原子质量表
常用的相对原子质量表
相对原子质量是原子中最重要的物理性质之一,又称相对原子质量、平均原子
质量或多分子质量。
一般情况下,它可以显示出一种物质中所含原子的平均质量。
相对原子质量表是现代化学和物理学的重要组成部分,它提供了原子的基本信息,可以用来解释物质的行为、性质及性质的改变。
近年来,著名的相对原子质量表有官森-洛尔(Gosens-Rollet)表、古斯-洛
尔(Gosens-Rollet)表、盖尔(Gail)表和布雷尔(Brule)表。
官森-洛尔表是
由德国物理学家肯斯伯格(Konrad Gesens)和洛尔(Lorlet)在1902年以固定本征碳原子质量(12.0g/mol)为基础,根据质谱测定的原子质量而编制的。
盖尔表也是由著名的德国物理学家施瓦茨(Fritz Gail)在1914年编制的,
使用的基本船原子质量是12.04g/mol。
在古斯—洛尔表的基础上,施瓦茨进一步
将各种放射性元素的原子质量纳入其中,使其更加完善。
布雷尔(Brule)表是美国物理学家布雷尔(Harold Brule)在1935年编制的。
他将官森—洛尔表的原子质量作为主要参考,更新它,引入了古斯—洛尔表和盖尔表中提到的放射性元素,并对在官森—洛尔表中上调或下调的原子质量做出了调整。
在现代,相对原子质量表仍然是化学和物理的基础性研究工具和实用工具,它
可以直接适用于测定元素含量,可将化学行为映射到物理定义,估算不同气体的混合比例,计算组分量,等等。
无论是实验室实践还是理论研究,相对原子质量表都是不可或缺的工具和参考材料。
常用相对原子质量、化合价、金属活动顺序
00
如:O2、H2
-3
PO43-、
+1
NH4+
jiǎ ɡài nà měi lǚ xīn tiě xī qiān qīnɡ tónɡ ɡǒnɡ yín bó
钾 钙钠镁 铝 锌铁 锡 铅 氢 铜 汞 银铂
jīn
金 金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
Al、Si、 N
+2 +3 +2 +4
P、 Fe、Fe、C、C
化合价口诀二:
二四六价硫都全,铜汞二价最常见;
负一硝酸氢氧根,负二硫酸碳酸根;
Байду номын сангаас
+2 +4 +6
S、S、S、
+2 +2
Cu、Hg
单质零价永不变。
-1
-1
-2
-2
NO3-、 OH-、
、 SO4 2- CO3 2-
还有负三磷酸根,只有正一是铵根。
钾
K
39
金
Au
197
钠
Na
23
钙
Ca
40
汞
Hg
201
镁
Mg
24
锰
Mn
55
碘
I
127
常见物质(原子团)
物质名称 物质符号 相对原子 物质名称 物质符号 相对原子 物质名称 物质符号 相对原子
质量
质量
质量
二氧化碳
CO2
44
硫酸
H2SO4
98
氯化钠 NaCl
水
H2O
18
kmno4相对原子质量
kmno4相对原子质量
KMnO4是一种常见的日常物质,它的全称是高锰酸钾,英文可以写作Potassium Permanganate,简写为KMnO4。
它是一种氧化剂,通常用来消毒、漂白等。
KMnO4的主要成分是锰元素,因此它的相对原子质量也是非常重要的。
KMnO4的主要成分是锰元素,它的化学式为MnO4-,KMnO4的相对原子质量是158.0332。
因此,可以得出KMnO4中每个原子的质量为:氢原子的质量为1.00784,氧原子的质量为15.9994,锰原子的质量为54.938。
同时,KMnO4中键合在一起的锰元素两个原子的质量为109.876。
此外,KMnO4也含有其他元素,如钾元素,其相对原子质量为39.098,有机杂质,其相对原子质量为14.007。
同时,KMnO4的氧化物的相对原子质量也被认为是比较重要的,比如氧化物的质量为47.99,碳酸钾的质量为G分子重量计算的结果为136.14。
总而言之,KMnO4的相对原子质量取决于其主要成分的相对原子质量,这些主要成分包括氢、氧、锰、钾等元素,其相对原子质量分别为1.00784、15.9994、54.938、39.098,同时,KMnO4中还含有杂质,如有机杂质以及氧化物等,他们的相对原子质量分别为14.007和47.99。
因此,KMnO4的总的相对原子质量是158.0332。
上述介绍了KMnO4的相对原子质量,可以用来把握KMnO4的化学特性,这对研究KMnO4的化学成分和性质、开发新的应用也会有十分重要的作用。
当然,在实际应用过程中,还需要充分研究KMnO4的性
质,确定其最佳应用条件,以确保更好的应用效果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常见物质的相对原子质量分别是多少
由于原子的实际质量很小,如果人们用它们的实际质量来计算的话那就非常的麻烦,例如一个氢原子的实际质量为1.674×10⁻²⁷千克,一个氧原子的质量为2.657×10⁻²⁶千克。
一个碳-12原子的质量为1.993×10⁻²⁶千克。
元素的相对原子质量是其各种同位素相对原子质量的加权平均值。
元素周期表中最下面的数字为相对原子质量。
今天小编就来介绍一下我们初中阶段常见物质的相对原子质量分别是多少。
常见物质的相对原子质量:
相对原子质量的易错点:
1. 如果在元素符号前面添上系数,就只表示该元素原子个数,不能表示该元素。
如:H既表示氢元素,又表示一个氢原子;2H只能表示两个氢原子。
2. 相对原子质量只是一个比,不是原子的实际质量。
3. 在相对原子质量计算中,所选用的一种碳原子是碳12,是含6个质子和6个中子的碳原子,它的质量的1/12约等于1.66×10-27 kg。
常见物质的相对原子质量记忆方法:
1.相对原子质量等于质子数与中子数的和。
H没有中子,那么原子质量就是1.。
随着原子序数的增加,质量也增加。
2.第二周期记住C、N、O即可。
C为12,N为14,O为16。
3.接下来是第三周期,相对更重要一些Na为23,Mg为24, Al为27,Si为28,P为31, S为32,Cl为35.5。
这几个是常用的,所以在用的时候多看看书,或者拿一张纸专门记这几个原子质量,需要用的时候看看,看的多了自然就记住了。
还有K为39,Ca为40,Fe为56, Cu为6
4.这几个也是同样的道理。
4.至于其他的一些,通常都是在某一种专有的化合物中出现,如KMnO4等,这些就只要记住化合物的质量就行,不必专门记Mn了。
5.最后,最关键的一点是,在中考或者高考时都会有原子质量,不必为最后的大考担心,应付好平时的小考即可。
常见物质的相对原子质量就是本文表格中所介绍的这些了,记住这些常用的相对原子质量,才能进一步做好相关的题目。
