苏教版高中化学必修一《专题1》检测题.docx
2023版新教材高中化学专题1物质的分类及计量质量检测苏教版必修第一册

专题1质量检测物质的分类及计量考试时间:75分钟,满分:100分可能用到的相对原子质量:H—1 He—4 B—11 C—12 N—14 O—16 S—32 Cl—35.5 Ca—40一、选择题:本题包括9小题,每小题3分,共27分。
每小题只有一个选项符合题意。
1.中国文化中的“文房四宝”所用材料的主要成分为单质的是( )A.笔B.墨C.纸D.砚2.化学与生活、社会发展息息相关,下列说法不正确的是( )A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应C.“春蚕到死丝方尽,蜡炬成灰泪始干”诗句中涉及氧化还原反应D.屠呦呦提取的青蒿素属于混合物3.萤石(Fluorite),又称氟石,是一种矿物,其主要成分是氟化钙(CaF2),CaF2属于( )A.单质 B.盐 C.碱 D.酸4.下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量可忽略不计)。
其中能表示等质量的氢气与氦气的是( )5.已知X和Y能发生如下反应:X+Y―→H2O+盐。
下列有关X和Y所属种类的说法一定不正确的是( )选项A B C DX酸性氧化物碱性氧化物酸酸性氧化物Y碱酸碱碱性氧化物6.下列说法中正确的是( )A.标准状况下,18 g水的体积约为22.4 LB.293 K,1.01×105 Pa,64 g SO2中含有的氧原子数为3N AC.N A个一氧化碳分子和0.5 mol甲烷的质量比为 7∶4D.同温同压下,相同体积的气体单质含有的原子数目不一定相等7.某同学根据性质划分,把氢溴酸(HBr)与HCl划为一类,其理由是它们的化学性质十分相似。
据此判断下列反应不会发生的是( )A.2HBr+Na2CO3===2NaBr+CO2↑+H2OB.HBr+AgNO3===AgBr↓+HNO3C.HBr+NaOH===NaBr+H2OD.2HBr+2Ag===2AgBr+H2↑8.如果4 g NH3中含有x个NH3分子,那么8 g H2S中含有的电子数为( )A.x B.3.4x C.12x D.18x9.雾霾天气对环境造成了严重影响,部分城市开展PM2.5和臭氧的监测。
苏教版高一化学必修一练习题第一专题.doc

专题一《化学家眼中的物质世界》单元测试可能需要的原子量:H-l C-12 N-14 0-16 Ne-20 Na-23 S-32Cl-35.5 Cu-64第一卷(选择题共43分)一、选择题(本题包括5小题,每小题3分,共15分,每小题只有一个选项符合题意)1.我国的“神州五号”载人飞船已发射成功,“嫦娥”探月工程已正式启动。
据科学家预测,月球的土壤中吸附着数百万吨的^He,每觎「He核聚变所释放出的能量相当于目前人类一年消耗的能量。
在地球上,氮元素主要以42He的形式存在。
下列说法正确的是:()A.42He原子核内含有4个质子B. 32He和役氐互为同位素C.「He原子核内含有3个中子D.42He的最外层电子数为2,所以°2He具有较强的金属性2.气体的体积主要由以下什么因素决定的:①气体分子的直径②气体物质的量的多少③气体分子间的平均距离④气体分子的相对分子质量()A.①②B.①③C.②③ D .②④3.“纳米材料”是当今材料科学研究的前沿,1纳米(nm)=10-9m,其研究成果广泛应用于催化及军事科学中,“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中,所得混合物可能具有的性质是()A.有丁达尔效应B.能全部透过半透膜C.不能透过滤纸D.所得分散系不稳定4.每次实验焰色反应后都要用试剂清洗钳丝,这种清洗试剂是()A. NazCCh溶液B. NaOH溶液C.硫酸D.盐酸5.(2002上海高考题)1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。
他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。
下列说法正确的是()A.化学不再是纯实验科学B.化学不再需要实验C.化学不做实验,就什么都不知道D.未来化学的方向还是经验化二、选择题(本题包括7小题,每题4分,共28分,每小题有一个或两个选项符合题意。
苏教版高中化学必修一专题1 第一单元 丰富多彩的化学物质单元测试 .docx

高中化学学习材料唐玲出品专题1 第一单元丰富多彩的化学物质单元测试时间:60分钟满分:100分可能用到的相对原子质量:H-1,C-12,O-16,S-32,Cl-35.5,N-14,He-4,Na-23,Mg-24, Cu-64一、选择题(本题包括16小题,每小题3分,共48分,每小题只有一个正确答案)1、下列对物质的分类正确的是()A、盐酸酸B、纯碱碱C、二氧化硫酸性氧化物D、生石灰盐2、下列说法中正确的是()A、含有不同种元素的纯净物叫做化合物B、水溶液中能电离出H+的化合物一定是酸C、盐中一定含有金属元素D、含有氧元素的化合物一定是氧化物3、下列方程式书写正确的是()A、实验室制取H2:2Fe + 6HCl == 2FeCl3 + 3H2↑B、实验室制取CO2:CaCO3 + 2HCl == CaCl2 + H2O + CO2 ↑C、把铜丝伸入硫酸亚铁溶液:Cu + FeSO4 === Fe + CuSO4D、甲烷完全燃烧:CH4 + O2点燃CO + 2H2O4、下列反应类型判断错误的是()A、CaCO3 + 2HCl == CaCl2 + H2O + CO2 ↑中和反应B、H2 + CuO △2O 置换反应C、CaCO3高温CaO + CO2↑分解反应D、CuO + H2SO4 == CuSO4 + H2O 复分解反应5、下列反应中既是化合反应又是氧化还原反应的是()A、CaO + H2O == Ca(OH)2B、Ca + Cl2点燃CaCl2C、Fe + CuSO4 === FeSO4 + CuD、H2SO4 + BaCl2 == BaSO4↓+ 2HCl6、下列关于物质的量的叙述中,正确的是()A、物质的量就是物质的数量B、1mol任何物质都含有6.02×1023个原子C、1mol水中含有1mol氢分子和1mol氧原子D、1mol H2分子中含有2mol H7、下列叙述正确的是()A、1mol任何物质的质量都等于该物质的相对分子质量B、H的摩尔质量是1g·mol-1C、1 mol H2O的质量是18g·mol-1D、CO2的摩尔质量为44g8、下列说法中正确的是()A、标准状况下,1mol水的体积是22.4 LB、1mol任何气体,体积均为22.4LC、在标准状况下,0.3mol N2和0.7mol O2混合气体总体积约为22.4LD、通常状况下,1mol N2的体积约为22.4L9、下列物质中含分子数目最多的是()A、0.1mol Cl2B、0.4g H2C、4℃时9mLH2O(密度为1g/mL)D、标况下,6.72L CO210、标准状况下,相同物质的量的SO2和SO3,下列有关说法正确的是()A、具有相同数目的原子数B、具有相同的氧原子数C、具有相同的质量D、质量比为4∶511、标准状况下,具有下列量的物质,其体积最大的是()A、44g CO2B、11.2L H2C、2mol FeD、2mol H2O12、下列关于FeCl3溶液和F e(O H)3胶体的说法中正确的是( )A、都是无色透明、均一、稳定的分散系B、分散质颗粒直径都在10-9~10-7m之间C、F e(O H)3胶体具有丁达尔效应D、FeCl3溶液具有丁达尔效应13、下列物质属于电解质的是()A、铜B、AgNO3C、蔗糖D、盐酸14、下列电离方程式的书写正确的是()A、CuCl2= Cu + Cl2↑B、Na2CO3= 2Na+ + CO32-C、H2SO4=2H+ + S6+ + 4O2-D、Ba(OH)2 = Ba + 2OH15、某金属氯化物MCl2 40.5g,含有0.600mol Cl-,则金属MCl2的摩尔质量为()A、135B、135 g·mol-1C、64D、64 g·mol-116、下列关于阿伏加德罗常数的说法正确的是( )A.阿伏加德罗常数是一个纯数,没有单位B.阿伏加德罗常数就是6.02×1023C.n mol某种微粒集合体中所含微粒数约为n×6.02×1023D.阿伏加德罗常数的准确值为:6.02×1023mol-1第一单元丰富多彩的化学物质单元测试答题卡班级姓名座号一、选择题二、填空题(共43分)17、(11分)有下列物质:①Fe ②CO2③Na2O ④Cu(OH)2⑤MgCl2⑥NH4Cl ⑦H2SO4⑧C2H5OH(酒精)(用序号作答)。
苏教版高中化学必修一专题一测试卷

高中化学学习资料金戈铁骑整理制作专题一测试卷时间: 90 分钟满分: 100 分可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24S 32K39 Ca 40 Cu 64第Ⅰ卷 (选择题 共 48分)一、选择题 (此题包含 16 小题,每题 3 分,共 48 分。
每题只有一个选项切合题意 )1. ClO 2 是生产饮用水的新一代消毒剂,从物质的分类角度看, ClO 2 属于 ()A .氧化物B .酸C .碱D .盐 答案: A分析: ClO 2 由两种元素构成,此中一种为氧元素,A 项正确。
2.以下原子构造表示图所表示的元素与氩元素的化学性质相像的是( )A. B. C. D. 答案: D分析: D 项中表示的元素为 Ne 元素,属于惰性气体元素,性质与氩元素相像,D 项正确。
3.以下仪器: ①一般漏斗②容量瓶③长颈漏斗④洗气瓶⑤量筒 ⑥蒸馏烧瓶。
常用于物质分别的是 ( )A .①④⑥B .②⑤⑥C .①②③D .②③⑥ 答案: A分析: 一般漏斗用于过滤,洗气瓶用于气体分别,蒸馏烧瓶用于蒸馏分别, A 项切合题意。
4.将 4 g NaOH 固体溶解于10 mL 水中,再稀释至1 L ,从中拿出 10 mL ,则这 10 mL溶液的物质的量浓度是 ( )- 1- 1A . 1 mol L ·B . 0.1 mol L ·C .0.01 mol -1- 1L ·D . 10 mol L ·答案: B- 1 分析: 将 4 g NaOH 固体溶解于 10 mL 水中,再稀释至 1 L ,其浓度为0.1 mol ·L ,从中拿出 10 mL ,浓度不变, B 项正确。
5.某阳离子 M n +核外有 x 个电子,核内有 y 此中子,则 M 的质量数为 ( )A . x + yB . x - n + yC .x + n + yD . x + n - y 答案: C分析: M n +的质子数为 x +n ,质量数为 x + n +y , C 项正确。
苏教版高中化学必修一专题1 检测试题.doc
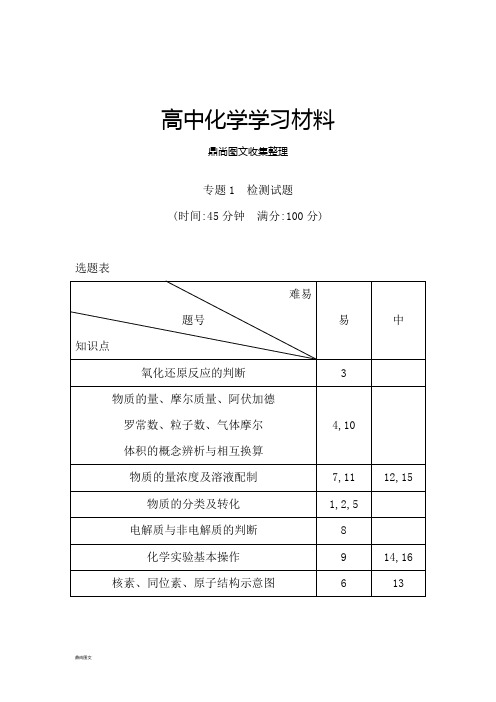
高中化学学习材料鼎尚图文收集整理专题1 检测试题(时间:45分钟满分:100分)选题表难易易中题号知识点氧化还原反应的判断 3物质的量、摩尔质量、阿伏加德4,10罗常数、粒子数、气体摩尔体积的概念辨析与相互换算物质的量浓度及溶液配制7,11 12,15 物质的分类及转化1,2,5电解质与非电解质的判断8化学实验基本操作9 14,16 核素、同位素、原子结构示意图 6 13一、选择题(共12小题,每小题5分,共60分)1.胶体区别于其他分散系的本质特征是( C )A.胶体的分散质通过滤纸空隙,而浊液的分散质不能B.产生丁达尔效应C.分散质粒子直径在1 nm~100 nm之间D.胶体在一定条件下能稳定存在解析:胶体区别于其他分散系的本质特征在于分散质粒子直径的大小。
2.(2012南京检测)下列说法中正确的是( A )A.红磷转化为白磷是化学变化B.原子是不能再分的最小微粒C.O3是由3个氧原子构成的化合物D.冰水混合物属于混合物解析:红磷→白磷,发生了键的断裂和形成,生成新物质,是化学变化,A正确;原子可以再分,B错;O3是单质,C错;冰水混合物是纯净物,D错。
3.厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中发生的变化不属于氧化还原反应的是( C )A.食物长时间放置后变质腐败B.燃烧液化石油气为炒菜提供热量C.用活性炭除去冰箱中的异味D.炒菜用过的铁锅出现红棕色斑迹解析:食物变质、燃料燃烧、铁锅生锈均是物质与空气中的氧气反应,均为氧化还原反应。
而活性炭除异味,是利用了活性炭多孔具有吸附性,属物理变化。
4.下列叙述中正确的是( D )A.NaOH的摩尔质量为40 gB.64 g SO2中含有1 mol O2C.1 mol N2的体积为22.4 LD.0.5 mol CO2约含有3.01×1023个CO2分子解析:摩尔质量的单位为g·mol-1,A错误;SO2中含氧元素,而不能说含氧气,B错误;不指明状况,不能确定1 mol N2的体积,C错误;D项正确。
苏教版高中化学必修第一册专题1物质的分类及计量物质的分散系练习含答案

第三单元物质的分散系基础过关练题组一分散系1.下列物质不属于分散系的是( )A.蒸馏水B.氯化钠溶液C.泥浆水D.淀粉溶液2.(2024江苏淮安期中调研)2023年的诺贝尔化学奖授予了三位在“量子点”发现和发展方面做出贡献的科学家。
所谓的“量子点”,属于半导体范畴,在1~10 nm之间。
下列哪种分散系的分散质尺寸更接近“量子点”的尺寸( )A.氯化钠溶液B.碳酸钙悬浊液C.蔗糖溶液D.氢氧化铁胶体3.(2024吉林长春第二实验中学月考)下列分散系中最不稳定的是( )A.向NaOH溶液中通入过量CO2得到的无色溶液B.向沸水中逐滴滴加FeCl3饱和溶液得到的红褐色液体C.向CuSO4溶液中加入NaOH溶液得到的分散系D.向Fe(OH)3固体中加入适量盐酸得到的棕黄色液体题组二胶体的性质和应用4.(易错题)(教材习题改编)(2024江苏盐城五校联考)当光束通过下列物质时,不会出现....丁达尔效应的分散系是( )①云、雾、烟②酒精溶液③FeCl3溶液④水⑤稀豆浆A.①③④B.③④C.②③④D.②③5.(2024江苏南京六校联合体联合调研)下列有关胶体的说法不正确...的是( )A.胶体的分散质粒子直径在1~100 nm之间B.可以用丁达尔效应鉴别胶体和溶液C.“纳米铜”是一种颗粒直径为纳米级的铜材料,属于胶体D.明矾可用于净水,因明矾中的Al3+可以和水反应生成Al(OH)3胶体,吸附水中悬浮物6.(2024河北石家庄第四十四中学月考)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向饱和氯化铁溶液中加入少量的NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
回答下列问题:(1)其中操作正确的同学是(填“甲”“乙”或“丙”)。
该同学想证明Fe(OH)3胶体已经制备成功,他可以利用进行检验。
苏教版高中化学必修第一册专题1物制质的分类及计量练习含答案
专题1物质的分类及计量一、选择题(本题共15小题,每小题3分,共45分。
在每小题给出的四个选项中,只有一项是符合题目要求的)1.化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是()A.《神农本草经》中记载的“石胆能化铁为铜”B.利用废弃的秸秆生产生物质燃料乙醇C.利用基本的化学原料生产化学合成药物D.北京冬奥会场馆使用CO2跨临界直冷制冰2.以下说法正确的是()A.向氢氧化钠溶液中滴加几滴石蕊溶液,溶液变红色B.酸具有相似的化学性质,是因为不同的酸溶液中都含有H+C.反应Fe2O3+3CO2Fe+3CO2属于置换反应D.碱性氧化物是指能与水反应生成相应的碱的氧化物3.下列叙述错误的是()A.CaCO3、(NH4)2CO3都属于碳酸盐B.HCl、醋酸钠和生石灰分别属于酸、盐和氧化物C.干冰属于化合物;铜矿石、水银均属于混合物D.通过化学反应,可由Ba(OH)2一步转化生成NaOH4.下列叙述正确的是()①摩尔是国际单位制中七个基本物理量之一②二氧化硫的摩尔质量是64g③质量相等、密度不等的CO和C2H4的分子数相等④一个钠原子的质量约等于236.02×1023g⑤标准状况下,11.2L H2O含有的分子数约为3.01×1023⑥常温常压下,11.2L CH4中含有的原子数约为1.505×1024⑦1mol H2和N2的混合气体在标准状况下的体积约为22.4L⑧常温常压下,22g CO2中含有的原子的物质的量为1.5mol A.①④⑥⑧ B.③④⑥⑦C.①②⑤⑦D.③④⑦⑧5.德国化学家维勒通过蒸发氰酸铵(NH4CNO,一种无机化合物,可由NH4Cl和AgCNO反应制得)水溶液得到尿素[CO(NH2)2,一种有机物]。
下列说法错误的是()A.NH4CNO的摩尔质量为60B.NH4CNO→CO(NH2)2实现了无机物到有机物的转化C.NH4Cl和AgCNO反应的化学方程式为NH4Cl+AgCNO AgCl↓+NH4CNOD.NH4Cl和AgCNO反应的反应类型属于复分解反应6.下列关于物质分类的正确组合是()碱酸盐碱性氧化物酸性氧化物A氨气硫酸小苏打氧化钙干冰B烧碱HNO3NaCl MgO COC纯碱冰醋酸(CH3COOH)胆矾(CuSO4·5H2O)氧化钾二氧化硫DNH3·H2OHNO3碳酸钙氧化铁SO37.物质的分类及部分转化关系如下图所示,下列有关说法不正确的是()A.转化b一定是化学变化B.转化a一定是化学变化C.转化b中一定有元素的化合价发生改变D.转化c可用于分离液态空气制取氧气8.如图分别为氯化钠在不同状态下的导电实验(X、Y均表示石墨电极,X与电源正极相连,Y 与电源负极相连)微观示意图。
高中化学必修一专题1-4测试题(苏教版4套,含答案)
高中化学必修一专题1-4测试题(苏教版4套,含答案)专题二从海水中获得的化学物质本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
可能用到的相对原子质量:O―16Na―23 第Ⅰ卷(选择题共48分) 一、选择题(本题包括16小题,每小题3分,共48分。
每小题只有一个选项符合题意)。
1.椰树牌天然矿泉水的成分:含钠46.31 g/L、含钙35.11 g/L、含碘0.051 g/L等,这里所标成分钠、钙、碘指的是( ) A.单质 B.元素 C.原子 D.纯净物【解析】钠、钙、碘指的是钠、钙、碘元素。
【答案】 B 2.氧化还原反应的实质是( ) A.氧元素的得失 B.氢元素的得失 C.电子的得失或偏移 D.元素化合价的升降【解析】氧化还原反应是有电子转移发生的化学反应。
【答案】 C 3.下列物质中,既含有氯气分子,又含有氯离子的是( ) A.氯化钠溶液 B.新制氯水C.漂白粉 D.液氯【解析】氯化钠溶液中只含有Cl-;新制氯水含有氯气分子、水分子和次氯酸分子,以及氢离子、氯离子,次氯酸根离子和少量的氢氧根离子;漂白粉中含有氯离子和次氯酸根离子,不含氯气分子;液氯中只含有氯气分子。
【答案】 B 4.“NaCl+CO2+NH3+H2O===NaHCO3↓+NH4Cl”是著名的“侯氏制碱法”的重要反应。
下面是4位同学对该反应涉及的有关知识发表的部分见解。
其中不正确的是( ) 【解析】相同温度下,NaHCO3的溶解度比NaCl的小,但仍属于可溶性物质,A对、C错;NaHCO3分解可得到Na2CO3,B对;NH4Cl属于氮肥,D正确。
【答案】 C 5.向饱和石灰水中不断通入二氧化碳(如图所示),其溶液导电性的变化是( ) A.由弱变强 B.由强变弱 C.由强变弱,再变强 D.由弱变强,再变强【解析】溶液中发生反应的离子方程式是Ca2++2OH -+CO2===CaCO3↓+H2O,CaCO3+CO2+H2O===Ca2++2HCO-3。
新教材 苏教版高中化学必修第一册 专题1 物质的分类及计量 课时练习题 含解析
专题1 物质的分类及计量第一单元物质及其反应的分类............................................................................................ - 1 -1、物质的分类................................................................................................................ - 1 -2、物质的转化化学反应的分类.................................................................................. - 6 -第二单元物质的化学计量.................................................................................................. - 13 -1、物质的量 ................................................................................................................. - 13 -2、气体摩尔体积.......................................................................................................... - 18 -第三单元物质的分散系...................................................................................................... - 23 - 第一单元物质及其反应的分类1、物质的分类[合格过关练]1.原油是一种没有固定沸点的液态物质,加热原油使不同沸点的组分分别汽化,然后冷凝,就能得到汽油、煤油、柴油等产品。
苏教版高中化学必修一化学专题测试.doc
高中化学学习材料鼎尚图文收集整理云霄城关中学2008级化学必修1专题测试专题一 化学家眼中的物质世界班级 姓名 座号 成绩可能用到的相对原子质量:H:1 C:12 N:14 O:16 S:32 Cl:35.5 Zn:65一、选择题(本题包括20小题,每小题2分,共20分,每小题只有一个正确答案)1.Na 2CO 3俗名纯碱,下面是对纯碱采用不同分类法进行分类,其中不正确的是A .Na 2CO 3是碱B .Na 2CO 3是盐C .Na 2CO 3是钠盐D .Na 2CO 3是碳酸盐2.某同学进行家庭小实验,将选项中的物质与水充分混合,所得分散系不是溶液的是A .食盐B .酒精C .蔗糖D .植物油 3.0.5mol Fe 2(SO 4)3中所含的Fe 3+离子数为A .3.01×1023B .0.5C .6.02×1023D .14.224mL 某气体在标准状况下的质量为0.32g ,该气体的摩尔质量约为A .32g·mol -1B .32C .64g·mol -1D .645.a molH 2SO 4 中含有b 个氧原子,则阿伏加德罗常数的值可表示为A .a/4b mol -1B .b/4a mol -1C .a/b mol -1D .b/a mol -16.下列实验设计方案中,可行的是A .除去CO 2中的少量HCl :通入NaOH 溶液B .除去KCl 溶液中的少量K 2CO 3:加入适量的盐酸C .向某无色未知溶液中仅加入BaCl 2溶液,以检验未知溶液中的SO 42-D .用BaCl 2溶液,可将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开7.放射性核素I 25153可用于治疗肿瘤。
该核素原子核内的中子数与核外的电子数之差是 A .19 B .53 C .72 D .125 8.、H 11、H 21、H 31H +、H 2,下列说法正确的是 A .具有相同的质子数 B .具有不同的电子数C .这些微粒互称同位素D .它们是氢元素不同的五种微粒9.30mL 1mol/L NaCl 溶液和40mL 0.5mol/L CaCl 2溶液混合后,混合液中Cl -浓度为(假设溶液体积混合前后不变)A.0.5mol/L B.0.6mol/L C.1.00mol/L D.2mol/L10.下列化学反应中,属于氧化还原反应的是A.NaOH + HCl == NaCl + H2O B.H2CO3 == H2O + CO2C.2FeCl2 + Cl2 == 2FeCl3D.NH3 + HCl == NH4Cl11.下列叙述正确的是A.同温同压下,相同体积的物质,其物质的量一定相等B.任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等C.1L一氧化碳气体一定比1L氧气的质量小D.一氧化碳气体和氮气,若体积相等,则质量一定相等12.下列属于电解质并能导电的物质是A.熔融的NaCl B.KNO3溶液C.Na D.酒精13.用N A表示阿伏加德罗常数的值,下列叙述正确的是A.标准状况下,11.2LH2O 含有的分子数为0.5N AB.在常温常压下,11.2L Cl2含有的分子数为0.5N AC.含有N A个氩原子的氩气在标准状况下的体积约为11.2LD.25℃,1.01×105 P a,64g SO2中含有的原子数为3N A14.某物质灼烧时,焰色反应为黄色,下列判断中错误..的是A.该物质可能是金属钠B.该物质一定含钠元素C.该物质一定是钠的化合物D.该物质中可能含钾元素15.向混浊的水中加入明矾〔K Al (SO4)2•12H2O 〕,水可得到净化,其中起到净化作用的是A.K+B.Al3+C.SO42-D.明矾溶于水后产生的氢氧化铝胶体16.下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是A.25ml 0.5mol/L HCl B.200mL 0.25mol/L AlCl3溶液C.50ml 1mol/L NaCl溶液D.100mL 0.5mol/L MgCl2溶液17.下列操作中正确的是A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学学习材料《专题1》检测题(时间:90分钟 满分:100分)可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Al 27 S32第Ⅰ卷(选择题,共48分)一、选择题(本题共16道小题,每小题只有一个正确选项,每小题3分,共48分)1.下列物质的分类合理的是( ) A .酸:HNO 3、H 2SO 4、NaHSO 4、NaHCO 3 B .碱性氧化物:K 2O 、Na 2O 、CaO 、MgO C .胶体:牛奶、豆浆、碘酒、石灰水 D .电解质:MgCl 2、Na 2CO 3、C 2H 5OH 、CO 2解析 A 项中NaHSO 4、NaHCO 3属于酸式盐;C 项中碘酒、石灰水属于溶液;D 项中C 2H 5OH 、CO 2是非电解质。
答案 B2.下列反应既是化合反应又是氧化还原反应的是( ) A .CuO +H 2=====△Cu +H 2O B .Na 2CO 3+CO 2+H 2O===2NaHCO 3C .3Fe +2O 2=====点燃Fe 3O 4 D .NH 4HS=====△NH 3↑+H 2S ↑解析 C 项中铁、氧元素的化合价发生了变化,又是化合反应。
答案 C3.同一状态下,20 mL A 2气体与30 mL B 2气体恰好完全反应生成20 mL 某气体X ,则X 的化学式为( )A .A 2B 3 B .AB 2C .AB 3D .A 3B 2解析 设反应的化学方程式为:a A 2+b B 2===x X ,则 a A 2 + b B 2===x X ,20 mL 30 mL 20 mL故a :b :x =20:30:20=2:3:2,即2A 2+3B 2===2X ,根据质量守恒定律可知X 的化学式为A 2B 3,A 项正确。
答案 A4.能表示阿伏加德罗常数数值的是( ) A .1 mol Na 含有的电子数B .标准状况下,22.4 L 水所含的分子数C .常温常压下,16 g 氧气所含的原子数D .1 L 1 mol ·L -1硫酸溶液所含的H +数解析 1 mol Na 含11N A 个电子;标准状况下水不是气态;16 g O 2物质的量为0.5 mol ,含N A 个O 原子;1 L 1 mol ·L -1硫酸溶液含2N A 个H +。
答案 C5.用CCl4萃取溴水中的溴,下列说法不正确的是( )A.实验使用的主要仪器是分液漏斗B.溴在CCl4中的溶解度比在水中的溶解度大C.溴的CCl4溶液呈橙红色D.分液时,水从分液漏斗下口流出,溴的CCl4溶液从漏斗上口倒出解析溴的CCl4溶液在下层,从下口流出。
答案 D6.美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数118,中子数为175的超重元素,该元素原子核内中子数与核外电子数之差是( )A.57 B.47C.61 D.293解析该元素原子的核外电子数=质子数=118,则中子数与核外电子数之差为175-118=57。
答案 A7.已知金属钠和水反应的化学方程式为:2Na+2H2O===2NaOH+H2↑。
将9.2 g金属钠投入到足量的重水D2O中,则产生的气体中含有( )A.0.2 mol中子B.0.4 mol电子C.0.2 mol质子D.0.4 mol分子解析钠和重水反应的化学方程式为:2Na+2D2O===2NaOD+D2↑,所以产生的气体全部是D2(21H2),1个分子中含有2个质子,2个电子和2个中子。
9.2 g金属钠的物质的量是0.4 mol,由反应方程式知,0.4 mol钠可生成0.2 mol D2,所以0.2 mol D2中含有的中子数、电子数、质子数均为0.4 mol 。
答案 B8.如果a g 某气体中所含的分子数为b ,那么c g 该气体在标准状况下的体积(N A 为阿伏加德罗常数)是( )A.22.4bcaN A LB.22.4acbN ALC.22.4ab cN AD.22.4bacN AL解析 c g 气体中分子数为:ba g ×c g =bca ,则c g 气体的体积为:bc a ·N A ×22.4L ·mol -1=22.4bc aN AL 。
答案 A9.下列叙述中不正确的是( ) A .利用丁达尔效应可以区别溶液与胶体B .在含有少量水的乙醇中加入氧化钙,然后蒸馏,可得到纯净的乙醇C .用结晶法提纯混有少量氯化钠的硝酸钾D .向某溶液中滴加盐酸无明显现象,再滴加氯化钡溶液产生白色沉淀,说明原溶液中含有CO 2-3解析 溶液无丁达尔效应,胶体有丁达尔效应,A 项正确;氧化钙和水反应使水完全转化为氢氧化钙,由于氢氧化钙和乙醇沸点差别很大,然后蒸馏出乙醇,B 项正确;氯化钠的溶解度随温度变化不大,硝酸钾的溶解度随温度变化大,故C 项正确;D 项中只说明原溶液中含有SO 2-4,不正确。
答案 D10.物质的量浓度相同的NaNO 3、Mg(NO 3)2、Al(NO 3)3三种溶液,取三种溶液的体积比为3:2:1时,三种溶液中c(NO-3) 之比为( ) A.1:1:1 B.1:2:3C.3:2:1 D.3:4:3解析所取三种溶液中的c(NO-3)与体积无关,只要算出原溶液中的硝酸根离子的浓度即可。
答案 B11.欲将CaCl2溶液中含有的盐酸除掉,应采用的最好方法是( )A.加生石灰,过滤B.加CaCO3粉末,过滤C.加过量的Na2CO3溶液D.加适量的AgNO3溶液解析CaCO3和盐酸反应生成CaCl2、CO2、H2O,过滤得到CaCl2溶液,故B项符合题意;A、C、D项均引入杂质。
答案 B12.甲、乙、丙、丁分别是氢氧化钙溶液、硝酸钾溶液、碳酸钠溶液、盐酸中的一种。
已知甲和丙可以反应,甲和丁也可以反应,则下列说法正确的是( )A.甲一定是氢氧化钙溶液B.乙一定是硝酸钾溶液C.丙不可能是碳酸钠溶液D.丁只能是盐酸解析由于氢氧化钙溶液、碳酸钠溶液和盐酸三者中任意两者都可以反应,所以甲、丙、丁无法确定;而硝酸钾溶液却不能和任何溶液反应,故乙是硝酸钾溶液。
答案 B13.设N A为阿伏加德罗常数,下列说法不正确的是( )A.常温下,22.4 L CO完全燃烧后生成CO2的分子数为N AB.18 g水中含有的电子数为10N AC.在1 L 2 mol·L-1的硝酸钙溶液中含有的NO-3离子数为4N AD.标准状况下,27 g金属铝与足量的稀硫酸反应,生成H2的体积约为33.6 L解析注意条件,常温下,22.4 L CO的物质的量要少于1 mol。
答案 A14.下列根据实验现象所得出的结论不正确的是( )A.无色溶液使紫色石蕊试液变蓝;结论:溶液一定呈碱性B.无色溶液焰色反应呈紫色(透过蓝色钴玻璃观察),结论:溶液中一定含有K+C.在无色溶液中加入Na2CO3溶液产生白色沉淀;结论:溶液中一定含有Ca2+D.在无色盐溶液中加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝;结论:溶液一定含有NH+4解析与Na2CO3溶液反应产生白色沉淀,可能含有Ca2+、Ba2+、Mg2+等。
答案 C15.下图是某学校实验室买回的硫酸试剂标签的部分内容。
判断下列说法正确的是( )A.该硫酸的浓度为9.2 mol·L-1B.配制200 mL 4.6 mol·L-1的稀H2SO4需该H2SO450 mL C.该硫酸与等体积水混合质量分数变为49%D.取该硫酸100 mL,则浓度变为原来的1 5解析由c=1 000ρwM可得c=1 000×1.84×98%98=18.4 mol·L-1,A项错;设配制200 mL 4.6 mol·L-1的稀H2SO4需该H2SO4V mL,则4.6 mol·L-1×0.2 L=18.4 mol·L-1·V,解得V=0.05 L=50 mL,B项正确;等体积水的质量小于硫酸的质量,C项错;硫酸是均一、稳定的分散系,100 mL与500 mL的浓度相同。
答案 B16.有BaCl2和NaCl混合溶液a L,将它平均分成两份,一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。
反应中消耗x mol H2SO4,y mol AgNO3。
据此得知原溶液的c(Na +)为( )A.(y-2x)/a mol·L-1B.(y-x)/a mol·L-1C.(2y-2x)/a mol·L-1D.(2y-4x)/a mol·L-1解析一份混合液中,n(BaCl2)=x mol,其中n(Cl-)=2x mol,又知n总(Cl-)=y mol,故n(NaCl)=n(Na+)=(y-2x)mol,则原溶液的c(Na+)=2(y-2x) mola L=(2y-4x)/a mol·L-1。
答案 D第Ⅱ卷(非选择题,共52分)二、非选择题(本题包括6道题,共52分)17.(10分)(1)3416S2-中的质子数是________,中子数是________,核外电子数是________,质量数是________。
(2)Fe、Fe2+、Fe3+是________元素的三种粒子,它们的________数相同,它们所带的________数不相同。
(3)由1H162O与2H172O所代表的物质中,共有________种元素,________种原子,互为同位素的原子有________________。
(4)已知元素X、Y的核电荷数分别为a和b,它们的离子X m+和Y n-核外电子排布相同,则a、b、m、n之间的关系是________。
解析(1)A Z R n±m中四个角标表示的意义各不相同,A表示R元素原子的质量数;Z表示R元素原子的质子数;n表示R n±所带电荷的数目,也就是R原子变成R n±时得到或失去电子的数目;m表示R m分子中所含R原子的数目。
(2)Fe、Fe2+、Fe3+是铁元素的三种粒子,其中Fe2+和Fe3+是Fe 原子分别失去2个和3个电子后形成的,三种微粒所含质子数相同,电子数不同。
(3)1H162O和2H172O中共含有氢、氧两种元素,1H、2H、16O和17O四种原子,其中1H和2H互为同位素,16O和17O互为同位素。
(4)X m+是由X原子失去m个电子形成的,Y n-是由Y原子得到n个电子形成的,若X m+和Y n-核外电子排布相同,则有a-m=b+n。
答案(1)16 18 18 34(2)铁质子电荷(3)2 4 1H与2H、16O与17O(4)a-m=b+n18.(6分)如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。
