化工分离工程例题 天大第一版 陈洪钫
天大分离工程试题库-(填写答案版)

118.吸附负荷曲线是分析( 119.透过曲线是以(时间 120. 121. 122. 透过曲线是分析(
透过曲线是以(流出物中吸附剂的浓度
透过曲线与吸附符合曲线是(镜面对称相似关系)相似关系。
6
第二部分 选择题
1. 计算溶液泡点时,若 K i X i 1 0 ,则说明 C a.温度偏低 b.正好泡点 c.温度偏高 2. 在一定温度和压力下,由物料组成计算出的 K i X i 1 0 ,且 Z i / K i 1 ,该 进料状态为 C a.过冷液体 b.过热气体 c.汽液混合物 3. 计算溶液露点时,若 yi / K i 1 0 ,则说明 22 A a.温度偏低 b. 正好泡点 c.温度偏高 4. 进行等温闪蒸时,对满足什么条件时系统处于两相区 22A a. K i Z i 1且 Z i / K i 1 b. K i Z i 1且 Z i / K i 1 c. K i Z i 1且 Z i / K i 1 d.
70. 低压下二元非理想农液的对挥发度 α12 等于( 71. 气液两相处于平衡时, ( 73. 逸度是(修正的 )压力
72. Lewis 提出了等价于化学位的物理量( 逸度) 。 74. 在多组分精馏中塔顶温度是由( 75. 露点方程的表达式为( ΣKixi=1 76. 泡点方程的表达式为( 露点议程)方程求定的。 ) )
3
)方程求 V j ,由( S )方程求 T j 。
41. 对窄沸程的精馏过程,其各板的温度变化由(组成的改变)决定,故可由(相
51. 为表示塔传质效率的大小,可用(级效率)表示。 52. 对多组分物系的分离,应将(分离要求高 )或(最困难)的组分最后分离。 )所消耗的净功之比。 53. 热力学效率定义为(系统)消耗的最小功与(过程 耗的功。 55. 在相同的组成下,分离成纯组分时所需的功(大于)分离成两个非纯组分时 所需的功。 56. 超临界流体具有类似液体的(溶解能力)和类似气体的(扩散能力) 。 57. 泡沫分离技术是根据(表面吸附)原理来实现的,而膜分离是根据(膜的选 择渗透作用)原理来实现的。 58. 新型的节能分离过程有(膜分离) 、 (吸附分离) 。 59. 常用吸附剂有(硅胶) , (活性氧化铝) , (活性炭 61. 离程分为( 机械分离 62. 传质分离过程分为( 63. 分离剂可以是(能量 64. 机械分离过程是( )和( 传质分离 ) 。 ) 。 ) 。 60. 54A 分子筛的孔径为( 5 埃 ) ,可允许吸附分子直径(小于 5 埃)的分子。 )两大类。 速率控制过程)两大类。 平衡分离过程 )和( )和(物质 吸收、萃取) 。 吸收、萃取) 。膜分离。渗透。
化工分离过程课件陈洪钫,刘家祺编第一章绪论

1.2.2 速率分离过程
膜分离 热扩散
速率分离:
在某种推动力(浓度差、压 力差、温度差、电位差等)的 作用下,有时在选择性膜的 配合下,利用各组分扩散速 率的差异实现组分的分离。
微孔过滤(MF):
目的:溶液脱离子,气体脱离子
进料
颗粒、纤维
(液体和气体)
溶剂、水、 气体
推动力:压力差(~100kPa) 传递机理:筛分 膜类型:多孔膜
超滤(UF):
目的:溶液脱大分子,大分子溶液脱小分子,大 分子分级。
进料
胶体大分子
溶剂、水
推动力:压力差(100~1000kPa) 传递机理:筛分 膜类型:非对称性膜
反渗透(RO):
目的:溶剂脱溶质,含小分子溶质溶液浓缩。
进料
溶质、盐 溶剂、水
推动力:压力差(1000~10000kPa) 传递机理:优先吸附毛细管流动溶解、扩散模型 膜类型:非对称性膜或复合膜
本课程的任务和内容
■地位:专业基础课 ■前期课程:
物理化学、化工原理、化工热力学 ■重点: 1.基本概念的理解
2.讨论各种分离方法的特征 3.对设计、分析能力的训练 4.提高解决问题能力
一般化工生产过程:
煤
石油
化
天然气
工 原
反应
分离
产 品
生物物质
料
第一章 绪论
第一节 分离过程在化工生产中的重要性
(蒸汽压)化装置主
(MSA);有较大差 蒸塔顶产
加入热量 别
物中回收
L
(ESA)
乙烷及较
轻的烃。
萃
取
MSA
或 L或V 共
沸
精
馏
化工分离工程试题库 -

分离工程试题库目录第一部分填空题 (1)第二部分选择题 (3)第三部分简答题 (7)第四部分计算题 (9)第一部分填空题1. 传质分离可分为和。
2 分离过程常见的开发方法有和。
3.相平衡关系的表示方法有、、。
4.精馏的数学模型有、、、。
5.产生恒沸物的原因是,二元恒沸物的判别式为。
6.在萃取精馏中,为使分离效果较好,所选溶剂与塔顶产品形成,与塔釜产品形成,常用的方法是。
7.常用的解吸方法有、、。
8.与物理吸收相比较,化学吸收平衡分压,推动力,溶解度,传质系数。
9.解吸操作中,解吸因数S 解吸分率β,解吸操作方能进行,当S增加时,β,理论板数。
10.在液流主体进行缓慢化学反应的吸收过程,传质速率由决定。
11. 衡量分离的程度用表示,处于相平衡状态的分离程度是。
12. 汽液相平衡是处理过程的基础,相平衡的条件是。
13. 当混合物在一定的温度、压力下,满足条件即处于两相区,可通过计算求出其平衡汽液相组成。
14.萃取精馏塔在萃取剂加入口以上需设。
15. 最低恒沸物,压力降低是恒沸组成中汽化潜热的组分增加。
16.吸收因子为,其值可反应吸收过程的。
17. 吸收剂的再生常采用的是,,。
18. 精馏塔计算中每块板由于改变而引起的温度变化,可用确定。
19. 用于吸收过程的相平衡关系可表示为。
20. 多组分精馏根据指定设计变量不同可分为型计算和型计算。
21. 在塔顶和塔釜同时出现的组分为。
22. 吸收的相平衡表达式为,在操作下有利于吸收,吸收操作的限度是。
23. 解吸收因子定义为,由于吸收过程的相平衡关系为。
24. 精馏有个关键组分,这是由于的缘故25. 采用液相进料的萃取精馏时,要使萃取剂的浓度在全塔内为一恒定值,所以在进料。
26.原溶液为非理想型较强的物系,则加入萃取剂起作用。
27.提高萃取剂的选择性,可萃取剂的浓度。
28.在多组分精馏计算中为了给严格计算提供初值,通常用或方法进行物料预分布。
29.通过精馏多级平衡过程的计算,可以决定完成一定分离任务所需的,为表示塔实际传质效率的大小,则用加以考虑。
“化工分离过程”考资料资料精

“化工分离过程”考资料1. 陈洪钫. 基本有机化工分离工程. 北京: 化学工业出版社, 1981.2. 陈洪钫, 刘家祺. 化工分离过程. 北京: 化学工业出版社, 1995.3. 刘家祺, 姜忠义, 王春艳. 分离过程与技术. 天津: 天津大学出版社, 2001.4. 刘家祺. 分离过程. 北京: 化学工业出版社, 2002.5. 李淑芬, 姜忠义. 高等制药分离工程. 北京: 化学工业出版社,2004.6. 刘家祺. 传质分离过程. 北京: 高等教育出版社, 2005.7. 刘家祺. 分离过程与模拟. 北京: 清华大学出版社, 2007.8. 史季芬. 多级分离过程——蒸馏、吸收、萃取、吸附. 北京: 化学工业出版社, 1991.9. 吴俊生, 邓修等. 分离工程. 上海: 华东化工学院出版社, 1992.10. 郁浩然. 化工分离工程. 北京: 中国石油出版社, 1992.11. 蒋维钧. 新型传质分离技术. 北京: 化学工业出版社, 1992.12. (日)大矢晴彦著,张瑾译. 分离的科学与技术. 北京: 中国轻工业出版社 1999.13. 邓修,吴俊生. 化工分离工程. 北京: 科学出版社, 2000.14. 耿信笃. 现代分离科学理论导引. 北京: 高等教育出版社, 2001.15. (美)塞德等,分离过程原理. 北京: 化学工业出版社,2002.16. 袁惠新. 分离工程. 北京: 中国石化出版社, 2002.17. 伍钦. 传质与分离工程. 广州: 华南理工大学出版社, 2005.18. 陈欢林. 新型分离技术. 北京: 化学工业出版社, 2005.19. 宋海华. 多级分离理论(一)精馏模拟. 天津: 天津大学出版社, 2005.20. 丁玉明. 现代分离方法与技术. 北京: 化学工业出版社, 2006.21. 郁浩然. 化工分离工程,北京: 中国石化总公司情报研究所出版社, 2006.22. 胡小玲, 管萍. 化学分离原理与技术. 北京: 化学工业出版社, 2006.23. 蒋维均, 余立新. 新型传质分离技术(第二版). 北京: 化学工业出版社, 2006.24. 西德尔, 亨利著; 朱开宏, 吴俊生译. 分离过程原理. 上海: 华东理工大学出版社, 2007.25. 袁惠新. 分离过程与设备. 北京: 化学工业出版社, 2008.26. 小岛和夫著; 傅良译. 化工过程设计的相平衡. 北京: 化学工业出版社, 1985.27. 张建侯, 许锡恩. 化工过程分析与计算机模拟. 北京: 化学工业出版社, 1989.28. 时钧, 汪家鼎, 余国琮, 陈敏恒. 化学工程手册. 第二版. 北京: 化学工业出版社, 1996.29. 倪进方. 化工过程设计, 北京: 化学工业出版社, 2001.30. 杨志才. 化工生产中的间歇过程-原料、工艺及设备. 北京: 化学工艺出版社, 2001.31. 武汉大学编写组. 化学工程基础, 北京: 高等教育出版社, 2002.32. 顾觉奋. 分离纯化工艺原理. 北京: 中国医药科技出版社, 2002.33. (美)吉科利斯著,齐鸣斋译. 传递过程与分离过程原理. 上海: 华东理工大学出版社, 2007.34. 刘茉娥. 膜分离技术. 北京: 化学工业出版社, 1998.35. 王湛. 膜分离技术基础. 北京: 化学工业出版社, 2000.36. 时钧, 袁权, 高从堦. 膜技术手册. 北京: 化学工业出版社, 2001.37. 徐南平, 邢卫红, 赵宜江. 无机膜分离技术与应用. 北京: 化学工业出版社, 2003.38. 任建新. 膜分离技术及其应用. 北京: 化学工业出版社,2003.39. 于丁一,宋澄章,李航宇. 膜分离工程及典型设计实例. 北京: 化学工业出版社, 2005.40. 许振良, 马炳荣. 微滤技术与应用. 北京: 化学工业出版社, 2005.41. 王湛, 周翀. 膜分离技术基础(第二版) . 北京: 化学工业出版社, 2006.42. 陈观文. 分离膜应用与工程案例. 北京: 国防工业出版社, 2007.43. 高自立, 孙思修, 沈静兰. 溶剂萃取化学. 北京: 科学出版社, 1991.44. 陈维枢. 超临界流体萃取的原理和应用. 北京: 化学工业出版社, 1998.45. 张镜 . 超临界流体萃取. 北京: 北京化学工业出版社, 2000.46. 朱自强. 超临界流体技术—原理和应用. 北京: 北京化学工业出版社, 2000.47. 汪家鼎, 陈家镛. 溶剂萃取手册. 北京: 北京化学工业出版社, 2001.48. 戴猷元. 新型萃取分离技术的发展及应用. 北京: 化学工业出版社, 2007.49. 孙彦. 生物分离工程. 北京: 化学工业出版社, 1998.50. 毛忠贵. 生物工业下游技术. 北京: 中国轻工业出版社, 1999.51. 欧阳平凯. 生物分离技术. 北京: 化学工业出版社, 1999.52. 严希康. 生化分离工程 . 北京: 化学工业出版社, 2000.53. 严希康. 生化分离工程. 北京: 化学工业出版社, 2001.54. 孙彦. 生物分离工程(第二版. 北京: 化学工业出版社, 2005.55. 卢鲜花. 中药有效成分提取分离技术. 北京: 化学工业出版社, 2005.56. 刘小平, 李湘南,徐海星. 中药分离工程. 北京: 化学工业出版社, 2005.57. 曹学君. 现代生物分离工程. 上海: 华东理工大学出版社, 2007.58. 谭天伟. 生物分离技术. 北京: 化学工业出版社, 2007.59. 辛秀兰. 生物分离与纯化技术. 北京: 科学出版社, 2008.60. 田瑞华. 生物分离工程. 北京: 科学出版社, 2008.61. 丁绪淮, 谈遒. 工业结晶. 北京: 化学工业出版社, 1985.62. 冯霄, 李勤凌. 化工节能原理与技术. 北京: 化学工业出版社, 1998.63. 褚良银等. 旋转流分离理论. 北京: 冶金工业出版社, 2002.65. 陈翠仙, 韩宾兵, 朗宁威 . 渗透蒸发和蒸气渗透. 北京: 化学工业出版社, 2004.66. (英])什顿,沃德, 霍尔迪奇著; 朱企新译. 固液两相过滤及分离技术(第2版) . 北京: 化学工业出版社, 2005.67. 蒋培华. 反应与分离工程基础. 北京: 中国石化出版社, 2008 .68. King C J. Separation Processes, 2nd. New York : McGraw Hill, 1980.69. Henley E J, Seader J D. Equilibrium Stage Separation in Chemical Engineering. New York : John Wiley&Sons, 1981.70. Rousseau R W. Handbook of Separation Process Technology. New York: John Wiley & Sons, 1987.71. Wankat P C. Equilibrium-Stage Separations in Chemical Engineering. New York : Elsevier, 1988.72. Wankat P C. Rate-Controlled Separations. New York : Elsevier Applied Science, 1990.73. Schweitzer P. Handbook of Separation Technique for Chemical Engineers, 3rd ed. New York : McGraw Hill, 1997.74. Seader J D, Henley E J. Separation Process Principles. New York : John Wiley & Sons, 1998.75. Clifton E. Meloan. Chemical Separations: Principles, Techniques and Experiments (Techniques in Analytical Chemistry) . Wiley-Interscience, 1999.76. Christie John Geankoplis. Transport Processes and Separation Process Principles (Includes Unit Operations) (4th Edition) . New Jersey, 2003.77. Phillip C. Wankat,Separation Process Engineering (2nd Edition). Prentice Hall PTR,2006.78. Michael E. Prudich, Huanlin Chen, Tingyue Gu, Ram B. Gupta, Keith P. Johnston, Herb Lutz, Guanghui Ma, Zhiguo Su . Perry's Chemical Engineers' Handbook 8/E Section 20:Alternative Separation Processes . McGraw-Hill Professional, 2007.79. Robinson C S, Gilliland E R. Elements of Fractional Distillation, 4th ed. New York : McGraW-Hi11, 1950.80. Smith B D. Design of Equilibrium Stage Processes. New York : McGraw-Hill, 1963.81. McCade W L, Smith J C. Unit Operation of Chemical Engineering. New York : McGram Hill, 1976.82. Broul M, Nyvlt K, Sohnel O. Solubilities in Binary Aqueous Solution. Prague : Academia, 1981.83. Lo T C, Baird M I, Hanson C. Handbook of Solvent Extraction. New York : John Wiley&Sons, 1983.84. Walas S M. Phase Equilibria in Chemical Engineering. Boston : Butterworths, 1985.85. Yang R T. Gas Separation by Adsorption Processes. Boston : Butterworths, 1987.86. Duong D D. Adsorption Analysis: Equilibria and Kineties. New York : Lmperial College Press, 1988.87. Myerson A S. Handbook of Industrial Crystallization. Boston : Butterworth-Heinemann, 1992.88. Thornton J D. The Science and Practice of Liquid-Liquid Extraction. Oxford : Oxford Press, 1992.89. Garside J. Separation Technology: The Next Ten Years. London : Institution of Chemical Engineers, 1994.90. Ruthven D M, Farooq S, Kanebel K S. Pressure Swing Adsorption. New York : VCH, 1994.91. Diwekar M U. Batch Distillation. US: Taylor&Francis, 1995.92. Michael C. Flickinger. Encyclopedia of bioprocess technology: fermentation, biocatalysis and bioseparation. New York : John Wiley&Sons, 1999.93. Antonio A. Garcia, Mathew R. Bonen. Bioseparation Process Science. Blackwell Science Inc, 1999.94. Seider W D, Seader J D, Lewin D R. Process design principles:synthesis, analysis,and evaluation. 北京: 化学工业出版社, 2002.95. Jones A G. Crystallization Process Systems. Boston : Butterworth-Heinemann, 2002.96. David Baldacci ,Split Second,艺州出版社, 2004.97. J.M. Smith, Hendrick C Van Ness, Michael Abbott. Introduction to Chemical Engineering Thermodynamics. McGraw-Hill, 2004.98. Richard M. Felder, Ronald W. Rousseau. Elementary Principles of Chemical Processes. Wiley, 2004.99. F. B. Petlyuk. Distillation Theory and its Application to Optimal Design of Separation Units . Cambridge University Press, 2004.100. J. D. Seader , Ernest J. Henley. Separation Process Principles,Wiley, 2005.101. Wallace,Woon-Fong Leung. Centrifugal Separations in Biotechnology. Academic Press, 2007.102. Henry Z. Kister, Paul Mathias, D. E. Steinmeyer, W. R. Penney, B. B. Crocker,James R. Fair. Equipment for Distillation, Gas Absorption, Phase Dispersion, and Phase Separation . McGraw-Hill Professional, 2007.网上资源:1. 泡露点及闪蒸过程计算Free Software about bubble point and dew point1.1 Flash Calculator/chemsim.htm#FTTech("FLSC") is a self-contained, easy-to-use product for getting single flash solutions and bubble or dew points. It contains Digital Analytics' vapor-liquid equilibrium database and modelling methodology which includes Peng-Robinson EOS, UNIFAC, and Wilson methods.1.2 ThermoSolver/education/Thermosolver/ThermoSolver is a software program which accompanies the textbook Engineering and Chemical Thermodynamics by Milo Koretsky. This software allows students to perform complex thermodynamics calculations, and explore thermodynamics for systems which would be impossible to solve without a significant investment in programming.•Thermodynamic properties for 350+ compounds are provided.•Saturation pressure calculator can be used with 338 species in the database. •Solver for the Peng-Robinson and Lee-Kesler equations of state is provided. •Fugacity coefficients can be solved for pure species or mixtures.•Models for Gibbs energy can be fit to isobaric or isothermal vapor-liquid equilibrium data. Sample data sets are provided. The results can be plotted.•Bubble-point and dew-point calculations can be made.•Equilibrium constant (KT) solver is provided.•General chemical reaction equilibria solver is provided.•Equations used in the calculation process can be viewed.1.3 BR AET Calculation Shareware/fractional-distillation/shareware.htmlThis program is a useful utility when estimating boiling points at reduced pressures. It allows the calculation of AET (Atmospheric Equivalent Temperature) by entering the actual temperature and pressure. The actual temperature can be calculated by entering the AET and the actual pressure.2.精馏过程计算2. Free Software about distillation2.1 /McCabe-Thiele.html2.2 Online Calculation of a Binary Distillation Column2.3 Pressure Swing Adsorption Calculator by James Ritter at the University of South CarolinaAdsorption and Chromatography Software at the University of Bath Basic programs and MS Excel spreadsheets employing the tanks in series modelNumerical Simulation of Nonlinear Multicomponent Chromatography Quattro Pro spreadsheet developed by D. D. Frey at UMBC. It's more sophisticated and accurate than the U. of Bath and UMCP software. Assorted online calculators for engineering problems3.膜分离过程计算3. Free Software about Membrane Separation3.1 Membrane Simulator Version 2.0/koros/index.php?do=resources3.2 Membrane Simulation 2.0/Default.asp?Category=Simulation4. 美国麻省理工学院“分离”开放课程网站(1) /OcwWeb/Chemical-Engineering/10-32Spring-2005/CourseHome/(2)/OcwWeb/Chemical-Engineering/10-445Summer-2005/CourseHome/。
《化工分离工程》试卷与答案
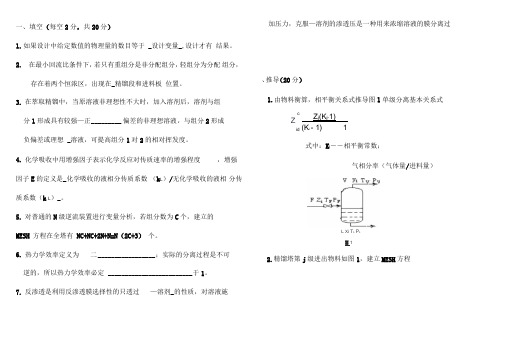
一、填空(每空2分,共20分)1.如果设计中给定数值的物理量的数目等于 _设计变量_,设计才有结果。
2.在最小回流比条件下,若只有重组分是非分配组分,轻组分为分配组分,存在着两个恒浓区,出现在_精镏段和进料板位置。
3.在萃取精镏中,当原溶液非理想性不大时,加入溶剂后,溶剂与组分1形成具有较强—正_________ 偏差的非理想溶液,与组分2形成负偏差或理想 _溶液,可提高组分1对2的相对挥发度。
4.化学吸收中用增强因子表示化学反应对传质速率的增强程度,增强因子E的定义是_化学吸收的液相分传质系数(k L)/无化学吸收的液相分传质系数(k°L)_。
5.对普通的N级逆流装置进行变量分析,若组分数为C个,建立的MESH 方程在全塔有NC+NC+2N+N=N(2C+3)个。
6.热力学效率定义为二_________________ ;实际的分离过程是不可逆的,所以热力学效率必定_________________________ 于1。
7.反渗透是利用反渗透膜选择性的只透过—溶剂_的性质,对溶液施加压力,克服—溶剂的渗透压是一种用来浓缩溶液的膜分离过、推导(20分)1.由物料衡算,相平衡关系式推导图1单级分离基本关系式cZidZ j(K j-1)(K i- 1) 1式中:K i――相平衡常数;气相分率(气体量/进料量)L Xi T L P L團12.精馏塔第j级进出物料如图1,建立MESH方程、简答(每题5分,共25分) 4.在精馏塔中设中间换热器为什么会提高热力学效率?1•什么叫相平衡?相平衡常数的定义是什么?由混合物或溶液形成若干相,这些相保持物理平衡而共存状态。
热力学上看物系的自由焓最小;动力学上看相间表观传递速率为零。
K i=y/X i。
2.关键组分的定义是什么;在精馏操作中,一般关键组分与非关键组分在顶、釜的分配情况如何?由设计者指定浓度或提出回收率的组分。
LK绝大多数在塔顶出现,在釜中量严格控制;HK绝大多数在塔釜出现,在顶中量严格控制;LNK全部或接近全部在塔顶出现;HNK全部或接近全部在塔釜出现。
化工分离工程考试题库

化工分离工程考试题库
1. 请解释传质系数和相对挥发度的概念,并说明它们在化工分离过程中的作用。
2. 请列举并简要描述至少五种常见的化工分离技术,包括其原理和应用领域。
3. 以乙醇和水的蒸馏分离为例,说明常压蒸馏和精馏的区别以及适用条件。
4. 请解释气液平衡和液液平衡的概念,以及它们在化工分离过程中的重要性。
5. 请说明萃取过程的基本原理,以及在化工生产中的应用和优缺点。
6. 请简要描述气相色谱和液相色谱的原理及其在化工分离工程中的应用。
7. 请解释膜分离技术的原理,以及其在化工领域中的优势和局
限性。
8. 以一个具体的工业应用为例,说明冷冻结晶过程的工艺流程和关键操作步骤。
以上题目涉及了化工分离工程中的基本理论和常见技术,希望能够帮助你更好地准备化工分离工程的考试。
如果你有其他问题,欢迎继续提问!。
天津大学化工学院 2003 级化工分离过程期末试卷答案.

天津大学化工学院2003级“化工分离过程”期末试卷答案一概念题(35分)1 填空题(19分)1) 分离过程可分为机械分离和传质分离两大类。
其中传质分离过程的特点是过程中有质量传递现象发生。
常见的传质分离过程有精馏、吸收、萃取。
2) 在泡点法严格计算过程中,除用修正的M-方程计算液相组成外,在内层循环中用S-方程计算级温度,而在外层循环中用H-方程计算汽相流率。
3) 效率常见的表示方法有全塔效率、默弗里板效率和点效率。
4)影响气液传质设备处理能力的主要因素有液泛、雾沫夹带、压力降和停留时间。
5) 常见的精馏节能技术有多效精馏、热泵精馏、采用中间冷凝器和中间再沸器的精馏和SRV精馏。
2选择题(6分)1)常压下a) 物系的相平衡常数更适合于用公式K i = p i s / P计算。
a) 苯-甲苯b) 甲醇-水2)假设相对挥发度与组成关系不大且不同组分的塔板效率相同,通过对若干不同组分系统的精馏计算结果分析研究发现,c) 下组分的分配比接近于实际操作回流比下的组分分配比。
a) 高回流比b) 低回流比c) 全回流d) 最小回流比3)多组分精馏与多组分吸收过程均不能对所有组分规定分离要求,而只能对分离操作中起关键作用的组分即关键组分规定分离要求,其中多组分精馏过程最多只能有 b) 个关键组分,多组分吸收过程最多只能有a) 个关键组分。
a) 1 b) 2 c) 3 d) 44)在二元精馏中,易挥发组分表面张力小于难挥发组分的物系宜采用a) ,反之宜采用b) 。
a) 泡沫接触状态b) 喷射接触状态3判断题(10分)1)分离因子相对于汽液平衡常数而言,随温度和压力的变化不敏感。
(√ )2)若轻、重关键组分是挥发度相邻的组分,则由Underwood公式可得出不止一个R m。
(×)3)由芬斯克公式可看出,最少理论板数与进料组成有关,且公式计算的精确度在很大程度上取决于相对挥发度数据的可靠性。
(×)三 计算题 (40分)1 (6分) 计算塔顶全凝器单元的固定设计变量数和可调设计变量数。
化工分离工程第2章 习 题

第2章 习 题2.11. 计算在0.1013MPa 和378.47K 下苯(1)-甲苯(2)-对二甲苯(3)三元系,当x 1 = 0.3125、x 2 =0.2978、x 3 =0.3897时的K 值。
汽相为理想气体,液相为非理想溶液。
并与完全理想系的 K 值比较。
已知三个二元系的wilson 方程参数(单位: J/mol ):λ12-λ11=-1035.33; λ12-λ22=977.83 λ23-λ22=442.15; λ23-λ33=-460.05 λ13-λ11=1510.14; λ13-λ33=-1642.81在T =378.4 K 时液相摩尔体积(m /kmol )为:=100.91×10 -3 ;=177.55×10 -3 ; =136.69×10 -3安托尼公式为(p :Pa ; T :K ):苯:1n =20.7936-2788.51/(T -52.36); 甲苯:1n=20.9065-3096.52/(T -53.67);对 -二甲苯:1n=20.989 1-3346.65/(T -57.84);2.11.答案解: 由Wilson 方程得:Λ12=l lV V 12exp[-(λ12-λ11)/RT]=331091.1001055.177⨯⨯×exp[-(1035.33)/(8.314×378.47)]=2.4450Λ21=0.4165Λ13=0.8382 Λ31=1.2443 Λ23=0.6689 Λ32=1.5034ln γ1=1-ln(Λ12X 2+Λ13X 3)-[323121221X X X Λ+ΛΛ+232131331X X X Λ+ΛΛ ]=0.0497γ1=1.0509同理,ln γ2=0.05148, γ2=1.6732 ln γ3=0.4190, γ3=1.5203lnP 1S =20.7936-2788.51/(378.47-52.36)=12.2428, P 1S =0.2075Mpa lnP 2S =20.9062-3096.52/(378.47-53.67)=11.3729, P 2S =0.0869Mpa lnP 3S =20.9891-3346.65/(378.47-57.84)=10.5514, P 3S =0.0382Mpa作为理想气体实际溶液,K 1=PP S11γ=2.134,K 2=1.4354, K 3=0.2733 若完全为理想系,K 1=PP S 1=2.0484K 2=0.8578 K 3=0.37712.在361K 和4136.8kPa 下,甲烷和正丁烷二元系呈汽液平衡,汽相含甲烷0.60387%( mol ),与其平衡的液相含甲烷0.1304%。
