第5章立体化学基础
立体化学基础培训课件

54
CHO HC OH
CH2OH D(+)-甘油醛
CHO HOC H
CH2OH L(-)-甘油醛
R
HC X R'
费歇尔投影式中,X在右边为D型,X在左边为L型。
55
这种人为规定的构型为相对构型,1951年 J.M.Bijvoet 测定了化合物的绝对构型,恰好与人为 规定的构型相一致,确定的相对构型就成为绝对构型 。 对于有一个以上的手性C原子化合物,就要看最 下边的手性C原子。
51
将手性碳上的四个基团中的任意两个对调,构型改变:
H
HOOC OH
CH3
(S)
H COOH COOH CH3 COOH CH3
H OH
构型改变
CH3
(R)
H OH
构型改变
COOH
(S)
52
53
(三)对映体的构型及其命名法 1.构型的D/L命名法
不对称碳原子连接的基团在空间真实排布的情 况称为该分子的绝对构型。
(C H 2)8
O
O
COOH
40
如一个碳原子连接四个不同的原子或基团时, 这个正四面体就不可能在任何地方被分成实物与镜 像的关系的两半,也就是没有对称面或对称因素。 成了不对称分子,就有了旋光性。这个碳原子所连 的四个不同的原子或原子团在空间就会有两种排列 方式,就成了两种异构体。
41
42
第二节 对映异构和非对映异构 一、含一个手性碳原子的化合物
COOH
COOH
COOH
COOH
H OH HO H H OH HO H H OH HO H HO H H OH
立体化学基础
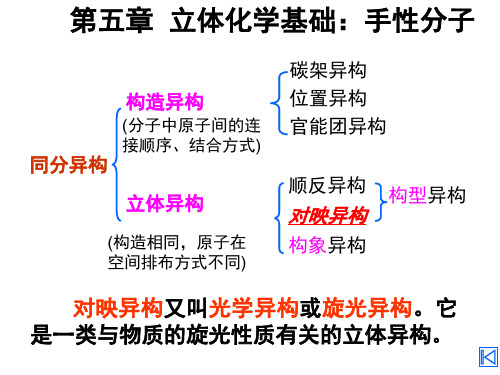
Cl大 HOCH2
Cl
键上,纸面 走向与实际
CH2Cl 走 向 相 同 ,
S-2,3-二氯丙醇
R-2,3-二氯丙醇
顺时针为R型, 逆时针为S型。
直接根据Fischer投影式命名的简便方法介绍
Problem 6: Give the names of the following compounds。(by R/S nomenclature)
有相等的距离。实物与镜像的关系叫对映关系。
镜面
实物与镜像
若实物与其镜像能够完全重合,则实物与镜像所 代表的两个分子为同一个分子。
OH
OH
CH H
CH3
HC H
CH3
OOHH
HH
CC HH 所有基团都重合 CCHH3 3
乙醇分子模型的重叠操作
对于某些分子,两个互为实物与镜像关系的分 子不能重合,如乳酸。
CO2H
CO2H
CO2H
NH2
NH2
H CH3
NH2 H
CH3 H
CO2H
CH3
H
NH2
CH3
即:固定*C上某个基团,其它三基团顺序轮换,不 改变其构型。
Problem 3: 下列Fischer式是否表示同一化合物?
COOH
CH2OH
H
OH
HO
H
--
CH2OH
COOH
镜 像
1
2
关
旋转180℃后可重叠
丙酸分子 的对称面
分子的对称面 具有对称面的分子为非手性分子
四、判断对映体的方法
1、看分子和它的镜像能不能重合。如果 不能重合,就具有对映异构现象。
2、寻找对称面和对称中心。如果分子没 有对称因素(对称面和对称中心),就 具有对映异构现象。
手性分子
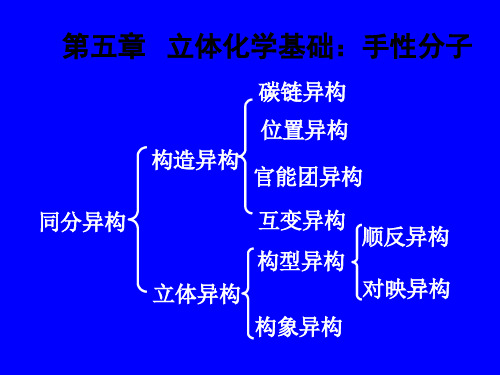
纸面上旋转180° 纸面上旋转180° 180
= HO
CH3 H
OH
COOH
COOH
H
纸面上旋转90° 纸面上旋转90° 90
H CH3 OH H3C OH COOH
投影式不能离开纸面进行翻转。 2、 Fischer 投影式不能离开纸面进行翻转。 3、如果使Fischer 投影式中的一个基团保持 如果使Fischer 固定, 固定,而把另外三个基团顺时针或逆时针调换 位置,不会改变原化合物的构型。 位置,不会改变原化合物的构型。
外消旋体:等量左旋体与右旋体的混合物。 外消旋体:等量左旋体与右旋体的混合物。无 混合物 旋光性。 用 (±) 、RS或 (dl)表示。 旋光性。 ± 或 表示。 表示 (±) –乳酸 ± 乳酸
原因:一对映体,旋光度相等,旋光方向相反。 原因:一对映体,旋光度相等,旋光方向相反。 性质: 性质:外消旋体的物理性质与纯的单一对映体 比较有所不同。 比较有所不同。
课堂练习:问题 - 课堂练习:问题5-2
第二节
一、投影方法
费歇尔投影式
COOH
HO
H
CH3
把主链竖 立,编号 最小碳放 在上端
划十字线, 划十字线, 交点代表手性 横键向前, 碳,横键向前,竖键向 。
含有两个手性碳的手性分子的投影
CH3 HO
HO C C OH CH3 H
H OH CH3
H
H H3 C
立体化学基础: 第五章 立体化学基础:手性分子
碳链异构 位置异构 构造异构 同分异构 立体异构 构象异构 官能团异构 互变异构 构型异构 对映异构 顺反异构
构造异构:分子组成相同而原子( 构造异构:分子组成相同而原子(团)相互连接方 异构 式和顺序不同 空间排列方式不同 立体异构:分子中原子( 立体异构:分子中原子(团)在空间排列方式不同
立体化学基础PPT课件

无手性碳原子的分子为非手性分子。
HN
CO OC
NH
OC
NH HN
CO
可见分子中有无手性碳原子不是判断分
子是否具有手性的依据。
第24页/共90页
不含手性中心的手性分子
CH3
CH3
A
H C CCH
A
B
NH2
B
H
NH2 H
分子中没有手性中心
H
端位上连接的基团 处于
垂直
平面
CH3
第25页/共90页
CH CH3
旋光方向
顺时针 右旋 用“+”表示 逆时针 左旋 用“-”表示
旋光度“”是一个变量,它受温度、光源、浓度、管长等许多因素的影响, 为了便于比较,就要使其成为一个常量,故用比旋光度[]来表示。
第9页/共90页
(三)比旋光度[α]
在一定温度和波长(钠光)条件下,样品浓 度为1 g.mL-1 时,在 1 dm 长的盛液管中测得的旋 光度。是一物理常数。
有手性碳原子的分子为手性分子。
Et Me
H
H
Me H
Et H
H
H Et Me
=
H Et
H Me
无手性碳原子的分子为非手性分子。
HN
CO OC
NH
OC
NH HN
CO
可见分子中有无手性碳原子不是判断分
子是否具有手性的依据。
第32页/共90页
不含手性中心的手性分子
CH3
CH3
A
H C CCH
A
B
NH2
B
H
OH
H
OH
CH2OH
L - 乳酸
D - 乳酸
立体化学基础演示文稿

CHO
H
OH
CH2OH
CHO H OH
CH2OH
D-甘油醛
CHO
HO
H
HO
CH2OH
L-甘油醛
H CH2OH
广东药学院
第二十四页,共78页。
主讲人: 申东升
凡是可以从D-甘油醛通过化学反应而得 到的化合物,或可以转变成D-甘油醛的化合 物,都具有与D-甘油醛相同的构型,即D型。与 L-甘油醛相同构型的化合物则是L型。
凡是具有对称中心或对称面的分子,都能与其镜像重叠,为非手性分子。
在绝大多数情况下,不具有对称中心或对称面的分子,与其镜像不能重叠,为手 性分子。
广东药学院第十六Leabharlann ,共78页。主讲人: 申东升
3.3. 对映异构体的表示方法与构型标记
3.3.1 对映异构体的表示方法
用透视式和投影式
表示对映异构体的最常用方法是由德国化学家费歇尔于
立体化学基础演示文稿
第一页,共78页。
(优选)立体化学基础
第二页,共78页。
3.1 同分异构现象
立体化学 以三维空间来研究物质结构与性质间关
系的科学
异 构 体 具有相同分子式的不同化合物
立体异构体 原子间的连接方式相同,但在空间 的排列方式不同的化合物
构象 通过单键旋转而能相互转变的不同的原 子排列方式
桂林风情
3.2.1 对映异构体和手性分子
1、非对映异构体-- 物体与镜像可以重合(为同一物质)
乙醇分子的实物和镜像可以重合
CH3
CH3
HC
H
OH
CH HO
H
两个分子完全能够重合,即代表同一化合物。 而且在分子中能找到对称面,即没有对映异构。
第五章 立体化学基础教学课件

碳架异构 位置异构 官能团异构
立体异构
顺反异构
对映异构 构型异构
(构造相同,原子在 构象异构
空间排布方式不同)
对映异构又叫光学异构或旋光异构。它 是一类与物质的旋光性质有关的立体异构。
上页 下页 首页 2
第五章 立体化学基础:手性分子 第一节 手性分子和对映体(一、手性)
第一节 手性分子和对映体
一、手 性
(二) 立体结构式
透视式是书写立体结构式常见的方法之一。 应注意它的书写方法,通常实线 “” 代表位 于纸平面上的键;虚线 “ ” (或“ ”) 代表 伸向纸平面后方的键,楔形线 “ ” 代表伸 向纸平面前方的键。
第五章 立体化学基础
第一节 手性分子和对映体 第二节 费歇尔投影式 第三节 旋光性 第四节 构型标记法 第五节 外消旋体 第六节 非对映体和内消旋化合物 第七节 无手性碳原子的对映体 第八节 外消旋体的拆分
1
第五章 立体化学基础:手性分子 第一节 手性分子和对映体(一、手性)
同分异构
构造异构
(分子中原子间的排 列顺序、结合方式)
5
6
CH3
CH3 Cl
7
CH3
Br
Br
CH3
上页 下页 首页 15
第五章 立体化学基础 第二节 费歇尔投影式
第二节 费歇尔投影式
对映异构体的结构可以用模型、透视式 (立体结构式) 或费歇尔(Fischer)投影式表示。
(一) 三维模型
上页 下页 首页 16
第五章 立体化学基础 第二节 费歇尔投影式
CH3 CH3
H 3C
8.
CH3 C H 3O
上页 下页 首页 11
第五章 立体化学基础 第一节 手性分子和对映体(三、对称面和非手性分子)
郑州大学远程教育有机化学(问答题)
各章练习题1.名词解释:(1)有机化学:研究有机化合物的结构、性能和合成方法的一门科学。
(2)有机化合物:碳的化合物。
(3)官能团:在有机化合物分子中能体现一类化合物性质的原子或基团。
(4)共价键的键长、键角、键能: 键长:成键两原子核间距离。
键角:两个共价键在空间的夹角。
键能:以共价键结合的双原子分子裂解成原子时所吸收的能量。
2.写出氯甲烷分子中碳氯键的异裂和均裂的化学反应式。
H 3CCH 3 + Cl CH 3 + ClClH 3CCl1.解释名词:(1)同系列:具有相同分子通式和结构特征的一系列化合物。
(2)构造异构:分子式相同,分子中原子间相互连接顺序和方式不同而产生的不同化合物。
(3)构象异构:由单键的旋转而产生的异构体。
2.写出含有7个碳烷烃的同分异构体的结构并用系统命名法命名。
CH 3CH 2CH 2CH 2CH 2CH 2CH 3CH 3CH 2CH 2CH 2CHCH 3CH 3CH 3CH 2CH 2CHCH 2CH 3CH 3庚烷 2-甲基己烷 3-甲基己烷CH 3CHCH 2CHCH 3CH 3CH 3CH 3CHCHCH 2CH 3CH 3CH 3CH 3CCH 2CH 2CH 3CH 3CH 32,4-二甲基戊烷 2,3-二甲基戊烷 2,2-二甲基戊烷CH 3CH 2CHCH 2CH 3CH 2CH 3CH 3CH 2CCH 2CH 3CH 3CH 3CH 3CHCCH 3CH 3CH 3CH 33,3-二甲基戊烷 2,2,3-三甲基丁烷 3-乙基戊烷第三章 烯烃和炔烃1.写出单烯烃C 5H 8的所有同分异构体,并用系统命名法命名。
CH 2=CHCH 2CH 2CH 3CH 3CH=CHCH 2CH 31-戊烯 2-戊烯CH 2=CCH 2CH 3CH 3CH 2=CHCHCH 3CH 3CH 3CH=CCH 3CH 32-甲基-1-丁烯 3-甲基-1-丁烯 2-甲基-2-丁烯2.完成下列反应(1)CH 3CH 2C=CH 2 + HBrCH 3CH 3CH 2CCH 3BrCH 3(2)CH 3CH=CCH 2CH 334,HCH 3COOH + O=CCH 2CH 33(3)CH 3CH=CHCH 3 + H 2PtCH 3CH 2CH 2CH 3(4)CH 3CH 2C CH + AgNO 3(NH 3)CH 3CH 2C CAg + NH 4NO 3 + NH 3(5)CH 3C CH + HCl CH 3C=CH 2ClClCH 3CCH 33、用简单的化学方法鉴别戊烷、1-戊烯、1-戊炔。
立体化学基础-药本课件
Cl 观察
C CH3
Cl CH2OH CH3 为逆时针方向
CH2OH
S-型
R/S标记法也可直接应用于Fischer投影式:
CO2H
H
OH 1#
3# CH3 R-(-)-乳酸
CH2Cl 2#
HOCH2
Cl
3# H 1#
S-2,3-二氯丙醇
CO2H
HO
H
CH3 S-(+)-乳酸
H
HOCH2
Cl
CH2Cl
D/L 和 R/S 两种标记方法,都不能通过其标记的构型来 判断旋光方向。因为旋光方向是化合物的固有性质。而对 化合物的构型标记只是人为的规定。
含有两个手性碳原子的化合物
(一) 含两个不同手性碳原子的化合物
2-羟基-3-氯丁二酸总共有四种旋光异构体:
COOH HO H Cl H
COOH
COOH H OH H Cl
D、L与 “+、-” 没有必然的联系
COOH H OH
CH2OH D£ ¸Ê ÓÍ Ëá
COOH H OH
CH3 D£ Èé Ëá
CHO H OH
CH2OH
D-(+)-甘油醛
COOH H2N H
CH3 L£ ± û ° ±Ëá
COOH H2N H
CH2OH L£ Ë¿ ° ±Ëá
-
CHO
HO H
(IV ) (I)与 (III)或(IV)、 (2S,3R()II)与(III)或
2R,3R (IV) 、 (III)与(I) 或(II) 、(IV)与(I) 或(II) 分别构成非 对映体;
对含有n个*C的化合物:
光学异构体数目=2n
高中化学——选修三全册教案
高中化学——选修三全册教案高中化学——选修三全册教案一、教学目的和要求通过学习选修三《有机化学基础》,希望学生能够掌握有机化学的基本概念、分类和命名,理解并掌握有机化学的反应机理和反应类型,为进一步学习和应用有机化学打下坚实的基础。
二、教学内容及学时分配本课程包括以下十章内容:第一章有机物的结构与性质第二章烷烃和环烷烃第三章不饱和烃第四章芳香烃第五章立体化学基础第六章醇、酚、醚第七章醛和酮第八章羧酸及其衍生物第九章胺及其衍生物第十章杂环化合物学时分配如下:第一章有机物的结构与性质 8学时第二章烷烃和环烷烃 6学时第三章不饱和烃 4学时第四章芳香烃 6学时第五章立体化学基础 4学时第六章醇、酚、醚 6学时第七章醛和酮 6学时第八章羧酸及其衍生物 6学时第九章胺及其衍生物 4学时第十章杂环化合物 4学时共计: 50学时三、教学方法和手段在教学过程中,可以采用讲解、演示、课堂讨论、案例分析等多种教学方法,使学生更好地理解和掌握知识。
同时,可以借助多媒体、实验设备等手段,增强学生的感性认识和实际操作能力。
四、实验设计为加深学生对有机化学的理解和应用,设计以下实验:实验一:有机化合物的基本性质和鉴别实验二:有机化合物的合成和转化实验三:有机化合物的结构和鉴定实验四:有机化合物的反应性和机理探究实验五:有机化合物的应用和性能评价五、考核方式采用平时作业、课堂表现、实验操作和期末考试等多种方式进行综合考核,以全面了解学生对有机化学的学习情况。
其中,平时作业和课堂表现占20%,实验操作占30%,期末考试占50%。
六、教学重点和难点教学重点包括有机化合物的结构、性质、合成和转化,以及有机化合物的反应性和机理探究。
教学难点是有机化合物的立体化学和复杂有机化合物的合成和转化。
七、教学反思与改进在教学过程中,要及时了解学生对知识的掌握情况,根据学生的反馈调整教学方法和手段。
要注重与实际生活的联系,让学生能够将所学知识应用到实际生活中,提高学生的学习兴趣和积极性。
《有机化学》练习题与参考答案
(4)苯酚分子中,羟基属于( )。 A.间位定位基 B.邻位定位基 C.对位定位基 D.邻、对位定位基
(5)苯分子中碳原子的杂化方式是( )。 A.sp 杂化 B.sp2 杂化 C.sp3 杂化 D.sp2d 杂化
6
(6)下列基团能活化苯环的是( )。 A.-NH2 B.-COCH3 C.-CHO D.-Cl
(7)
基团的名称是( )。
A.苄基 B.苯基 C.甲苯基 D.对甲苯基 (8)下列化合物中,在 Fe 催化下发生卤代反应最快的是( )。
A.乙苯 B.邻二硝基苯 C.苯酚 D.氯苯 (9)在苯分子中,所有的 C-C 键键长完全相同,是因为( )。
A.自由基加成反应 B.亲电取代反应 C.亲电加成反应 D.协同反应
2..判断题(对的打√,错的打×) (1)炔烃比烯烃的不饱和程度大,所以炔烃更容易发生加成反应。 (2)在卤化氢中,只有 HBr 与烯烃的加成才观察到过氧化物效应。 (3)凡是具有通式 CnH2n-2 的化合物一定是炔烃或环烯烃。 (4)顺-1,2-二氯-1-溴乙烯又可命名为(Z)-1,2-二氯-1-溴乙烯。
(7)
CC
H3CH2CH2C
CH3
4.写出下列化合物的结构式。
(2) CH3CH2CHCH2CH3 CH CH2
(4) H2C CH CH C(CH3)2
H
H
(6)
CC H
H3C
CC
H
CH2CH3
(1)3-甲基环戊烯
(2)3,3-二甲基-1-己炔
(3)2,4-二甲基-1,3-己二烯 (4)3-乙基-1-戊烯-4-炔
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CH3
CH3
H
OH
异丙醇
H
OH
H CH3
OH
2,32,3-丁二醇
CH3
H
CH3
H
CH3
CH3
H
1,11,1-二氯乙烷
H
顺-1,2-二甲基环丙烷 二甲基环丙烷
四、判断对映体的方法
1. 最直接的方法是建造一个分子及其镜像的模型。 最直接的方法是建造一个分子及其镜像的模型。 如果两者能重合,说明分子无手性, 如果两者能重合,说明分子无手性,没有对映异构现 象;如果两者不能重合,则为手性分子,有对映异构 如果两者不能重合,则为手性分子, 现象,存在对映体。 现象,存在对映体。 2. 考察分子有无对称面。如果分子有对称面, 考察分子有无对称面 如果分子有对称面, 对称面。 则该分子与其镜像就能重合,没有对映异构现象。 则该分子与其镜像就能重合,没有对映异构现象。 3. 大多数情况下,可根据分子中是否存在手性碳 大多数情况下,可根据分子中是否存在手性碳 原子(或手性中心 来判断分子是否有手性。 原子 或手性中心) 来判断分子是否有手性。 或手性中心
COOH COO H
CO OH H HO C CH 3
H OH CH 3 CH 3 OH H
COO H C H3 C H OH
-
二者的关系:互为镜象(实物与镜象关系, 二者的关系:互为镜象(实物与镜象关系,或 者说左、右手关系)。二者无论如何也不能完全重 者说左、右手关系)。二者无论如何也不能完全重 )。 叠。这种呈物体与镜像关系,彼此又不能重叠的性 这种呈物体与镜像关系, 呈物体与镜像关系 质称为手性。 质称为手性。
COOH COOH
H OH CH3 CH3 OH
H
对映异构体—— 对映异构体 互为镜像且不互 相重合
-
对映体的特点: 旋光度的大小相等, 对映体的特点 : 旋光度的大小相等 , 方向 相反(如乳酸[ 82° 相反 ( 如乳酸 [ α] 为 3 . 82 ° ) , 物理性质和化 学性质在一般条件下都相同 (除了对旋光性试剂 生物活性不同, 氯霉素、 外 ) 。 生物活性不同 , 如 ( - ) 氯霉素 、 ( - ) 多巴(治疗帕金森病) 多巴(治疗帕金森病)等。
三、对称面和非手性分子
对称面(planes of symmetry)是指能将分子 对称面 是指能将分子 结构剖成互为镜像的两半的面 结构剖成互为镜像的两半的面。如通过圆球心的 面;将长方形盒子分成各一半的面都是对称面。 将长方形盒子分成各一半的面都是对称面。
有对称面的分子 与它的镜像能重合, 与它的镜像能重合, 因此没有对映异构现 象,称为非手性分子 (achiral molecule)。 molecule)。 对称面 如下列化合物分子中都有1 个对称面, 如下列化合物分子中都有 1 个对称面 , 它们都 为非手性分子,无旋光性。 为非手性分子,无旋光性。
一、手性 手性碳原子——与4个完全不同的原子或原 与 手性碳原子 子团相连的碳原子 在结构式中常用星号*表示。 碳原子。 子团相连的碳原子。在结构式中常用星号*表示。 如:乳酸(2-羟基丙酸) 乳酸(2-羟基丙酸) (2
CH 3
* CH OH
COOH
乳酸 手性碳原子上所连的4个完全不同的原子或原 手性碳原子上所连的4 子团在空间可产生不同的排列形式( 立体结构) 子团在空间可产生不同的排列形式 ( 立体结构 ) 。
碳链异构 位置异构 构造异构
(分子中原 分子中原 子间的排列 顺序、 顺序、结合 方式) 方式
官能团异构 互变异构
同分异构
构象异构 立体异构
(构造相同,原子在 构造相同, 构造相同 空间排布方式不同) 空间排布方式不同
顺反异构 构型异构 对映异构
构造、 构造、构型和构象的关系
构造是分子中原子相互连接的顺序和方式。 构造 构造异构是指分子式相同,分子中原子相互连接的顺序和方式 构造异构 不同。 构型和构象是分子中各原子和基团在空间的相对位值,是分子 构型和构象 结构的一种外在表现,即分子的形象。 构型和构象异构统称为立体异构 立体异构。是分子的构型相同,而分子 构型和构象异构 立体异构 中各原子和基团在空间的相对位值不同。 一个分子由于单键的旋转而使分子呈现的立体形象称为构象 构象。 构象 一个分子,只要它有可自由旋转的单键,就有无数个不同的构 象存在。由于单键旋转需要的能量很低,构象异构体很难分离。 构型是指各原子在空间的排列次序。 构型 构型异构体包括顺反异构 光学异构 顺反异构和光学异构 构型异构体 顺反异构 光学异构。 单键旋转,使分子的构象改变了, 单键旋转,使分子的构象改变了,但是原子间的排列次序并没 有改变,所以构型没有改变。 有改变,所以构型没有改变。
当普通光通过一个由方解石制成的尼可尔( 当普通光通过一个由方解石制成的尼可尔(Nicol) 尼可尔 ) 振动方向和 的光才能通过, 棱镜时 只有振动方向 棱镜晶轴平行的光才能通过 棱镜时,只有振动方向和棱镜晶轴平行的光才能通过, 所得到的光就只在一个平面上振动。这种只在某一平 所得到的光就只在一个平面上振动。这种只在某一平 面上振动的光叫做平面偏振光,简称偏振光。 面上振动的光叫做平面偏振光,简称偏振光。偏振光 的振动平面称为偏振面。 的振动平面称为偏振面。
CO2H
CO2H H C HO
Cl I C H Br
Cl Br C H I
C
H3C OH
H
CH3
二、费歇尔(Fischer)投影式 费歇尔 投影式
1
CO2H
CO H 2
HO H
C2
CH3
3
HO H
CH3
费歇尔(Fischer)投影式书写规则: 投影式书写规则: 费歇尔 投影式书写规则 (1)将碳链竖直,把氧化态较高的碳原子或命 将碳链竖直, 名时编号最小的碳原子放在最上端。 名时编号最小的碳原子放在最上端。 (2)横前竖后:与手性碳原子相连的两个横键 横前竖后: 伸向前方,两个竖键伸向后方。 伸向前方,两个竖键伸向后方。 (3)横线与竖线的交点代表手性碳原子。 横线与竖线的交点代表手性碳原子。
COOH H H
C
COOH OH
HO
COOH HO
C H
COOH H CH3
OH CH3
CH3
ቤተ መጻሕፍቲ ባይዱ
CH3
书写费歇尔投影式时要注意: 书写费歇尔投影式时要注意: 费歇尔投影式是用平面式来表示分子的立体 结构。 结构。与手性碳原子相连的两个横键是伸向纸前 方的,两个竖键是伸向纸后方的。因此, 方的,两个竖键是伸向纸后方的。因此,表示某 一个化合物的费歇尔投影式只能在纸平面上平移, 一个化合物的费歇尔投影式只能在纸平面上平移, 也能在纸平面上旋转180°或其整数倍。但不能在 也能在纸平面上旋转180°或其整数倍。 纸平面上旋转180 纸平面上旋转90°或其整数倍, 纸平面上旋转90°或其整数倍,也不能离开纸平 90 面翻转, 面翻转,否则得到的费歇尔投影式就代表其对映 体的构型。 体的构型。
晶轴
普通光
偏振光 尼可尔棱镜
(二)旋光性 旋光性——能使偏振光的偏振平面发生旋转的 能使偏振光的偏振平面发生旋转的 旋光性 性质。 性质。
偏振光
旋光性物质 旋光性物质
旋转后的偏振光
如:乳酸、葡萄糖等 乳酸、 如:水、乙醇等
物质 非旋光性物质
二、旋光度与比旋光度
旋光度——偏振光的振动面被旋光性化合物所 偏振光的振动面被旋光性化合物所 旋光度 旋转的角度。 旋转的角度。用α表示。 表示。
立体化学基础: 第五章 立体化学基础:手性分子 (Basic of sterochemistry:Chiral Molecule)
学习要求: 学习要求: 掌握对映异构的基本概念及其命名方法、 掌握对映异构的基本概念及其命名方法、能 判断一个化合物是否有手性。 判断一个化合物是否有手性。 立体化学是研究化合物分子在三维空间的 立体化学是研究化合物分子在三维空间的 立体形象与其物理性质, 立体形象与其物理性质,反应性能以及生理活 性之间的关系的科学。 性之间的关系的科学。
对映异构现象——由于分子具有手性 , 而引 由于分子具有手性, 对映异构现象 由于分子具有手性 起旋光性不同的现象, 简称对映异构, 起旋光性不同的现象 , 简称对映异构 , 又称旋光 异构现象。属于立体异构。 异构现象。属于立体异构。
第一节 手性分子和对映体 (Chiral Molecule and enantiomers)
CHO H OH HO H CH2OH HO H H CH2OH OH CHO OHC CH2OH H HO H OH CHO HO H HO H CH2OH
第三节 旋光性
一、偏振光和旋光性
(一)偏振光 光是一种电磁波,光振动的方向 光是一种电磁波,
普通光的横截面
与它前进的方向垂直。普通光由不同波长的光组成, 与它前进的方向垂直。普通光由不同波长的光组成, 这些不同波长的光在无数个垂直于其传播路线的平 面内振动。 面内振动。
顺时 针 其旋 光方向 逆时 针 左 旋,以 “ l ” 或 “ ” 表 示。 右 旋,以 “ d ” 或 “ + ” 表 示。
旋光性物质的旋光度,除与化合物的结构有关外, 旋光性物质的旋光度,除与化合物的结构有关外, 还与测定时的条件有关。测定条件有: 还与测定时的条件有关。测定条件有:被测化合物 或密度g.cm-3;测定管的长度 测定管的长度 长度l(dm); 的浓度C(g.ml-1)或密度 浓度 或密度 ; 光源D(589nm);测定时的温度 ℃)有关。 ;测定时的温度t(℃ 有关 有关。 光源 温度
Fischer式的平移或纸平面内旋转180°, 其构型不变。 式的平移或纸平面内旋转 式的平移 ° 其构型不变。
CHO HO H CH2OH
CH2OH H OH CHO
