生物传感器法快速测定酒中的乙醇含量
酒精传感器的介绍
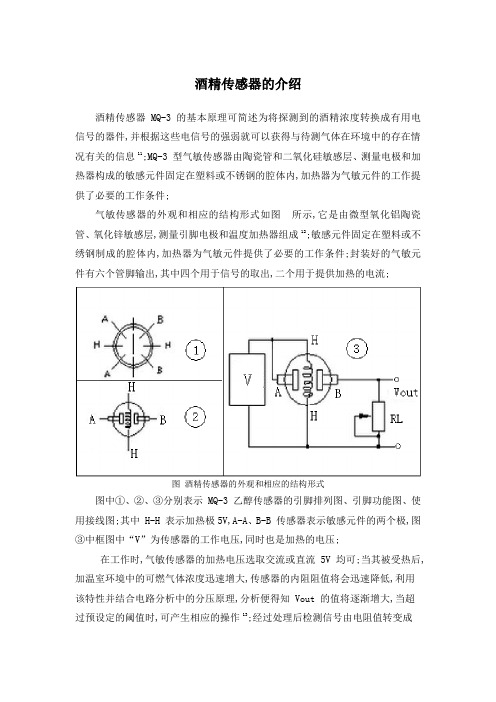
酒精传感器的介绍酒精传感器 MQ-3 的基本原理可简述为将探测到的酒精浓度转换成有用电信号的器件,并根据这些电信号的强弱就可以获得与待测气体在环境中的存在情况有关的信息11;MQ-3 型气敏传感器由陶瓷管和二氧化硅敏感层、测量电极和加热器构成的敏感元件固定在塑料或不锈钢的腔体内,加热器为气敏元件的工作提供了必要的工作条件;气敏传感器的外观和相应的结构形式如图所示,它是由微型氧化铝陶瓷管、氧化锌敏感层,测量引脚电极和温度加热器组成12;敏感元件固定在塑料或不绣钢制成的腔体内,加热器为气敏元件提供了必要的工作条件;封装好的气敏元件有六个管脚输出,其中四个用于信号的取出,二个用于提供加热的电流;图酒精传感器的外观和相应的结构形式图中①、②、③分别表示 MQ-3 乙醇传感器的引脚排列图、引脚功能图、使用接线图;其中 H-H 表示加热极5V,A-A、B-B 传感器表示敏感元件的两个极,图③中框图中“V”为传感器的工作电压,同时也是加热的电压;在工作时,气敏传感器的加热电压选取交流或直流 5V 均可;当其被受热后,加温室环境中的可燃气体浓度迅速增大,传感器的内阻阻值将会迅速降低,利用该特性并结合电路分析中的分压原理,分析便得知 Vout 的值将逐渐增大,当超过预设定的阈值时,可产生相应的操作13;经过处理后检测信号由电阻值转变成电压值,就可用于后续电路进行 A/D 转换和处理;传感器的标准回路有两部分组成;其一为加热回路,其二为信号输出回路,它可以准确反映传感器表面的电阻值变化;传感器表面电阻 Rs 的变化,是通过与其串联的负载电阻 RL上的有效电压信号 URL输出获得的;二者之间的关系表述为:R S /RL= V-URL/URL……………………………2-1其中,V 为回路电压,电压为 10V,负载电阻 RL 可调为—200KΩ;负载电阻RL可调,加热电压一般为 5V;传感器阻值变化率与酒精浓度、外界温度的关系慎密,为了使测量的酒精浓度最高误差最小,需要找到合适的温度,一般在测量前需将传感器预热 5 分钟;预热后半导体颗粒表面的吸附可导致材料载流子浓度发生相应变化,从而改变电导率,使传感器输出电压信号发生改变来相应反映浓度变化14;半导体方式的 MQ-3 酒精传感器具有灵敏度高、电路简单、使用方便、所需费用低、稳定性好以及寿命长等优点,可以把气体信号转换为电压信号输出,因此得到广泛应用;MQ-3 酒精传感器可用于机动车驾驶员呼气中酒精浓度的检测,以及其它严禁酒后操作的现场环境探测,也可用于其它场所的乙醇蒸气勘测工作等;MQ-3 酒精传感器的实物中包含有 6 只针状管脚,其中 4 个管脚两个 A 和两个 B用于信号读取,两个 H 脚用于提供加热电流;MQ-3 灵敏度市面上用的最广的酒精传感器是 MQ-3 乙醇传感器;MQ-3 乙醇气体传感器的突出技术特点为:★对乙醇蒸汽具有较高的灵敏度和优秀的选择性;★响应时间短并且恢复时间短的特性;★长期的使用寿命和可靠检测的稳定性;★驱动电路简单;MQ-3 型气敏传感器技术指标如下:★使用气体:酒精乙醇;★探测范围:10-100010-6 ;★灵敏度:air/Rin typical gas5;★特征气体:10010-6;★敏感体电阻:400-4000kΩ空气中;★响应时间:10s70% Response;★恢复时间:30s70% Response;★加热电阻:31Ω±3Ω;★加热电流:180mA;★加热电压:5V±;★加热功率:900mW;★工作条件:环境温度:-10~65 摄氏度湿度:95%RH;★贮存条件:温度-20~70 摄氏度,湿度:70%RH;图为 MQ-3 灵敏度曲线,具有气敏特性的电阻,其输出的电阻阻值会随着乙醇气体浓度的变化而相应变化;图 MQ-3传感器灵敏度曲线MQ-3 输出电压与酒精浓度关系通过实际测量,MQ-3 模拟端的输出信号与酒精浓度特性曲线近似为线性的关系15,如图所示;图输出电压与酒精浓度的关系。
酒精检测器原理

酒精检测器原理
酒精检测器的原理是通过测量人体呼出气体中的乙醇浓度来判断是否饮酒。
饮酒后,乙醇会进入人体的血液循环系统,并通过呼吸被排出体外。
酒精检测器通常采用电化学传感器或红外吸收传感器来测量呼出气体中的乙醇浓度。
电化学传感器是最常见的乙醇检测方法之一。
传感器内部包含一个电极,通常由铂或其他催化材料制成。
当呼出气体流经电极时,乙醇分子会与电极表面的氧发生反应,产生电流。
电流的大小与乙醇的浓度成正比,因此可以通过测量电流来确定呼出气体中的乙醇浓度。
红外吸收传感器则利用乙醇分子对红外光的吸收特性来进行检测。
传感器发射红外光束,通过呼出气体后,红外光束经过一个检测室,其室内装有对乙醇具有选择性吸收红外光的传感器。
通过测量透射光强度的变化,可以确定呼出气体中的乙醇浓度。
无论是电化学传感器还是红外吸收传感器,都需要在检测前进行校准,以确保测量结果的准确性。
此外,在使用酒精检测器时,也需要注意其他因素可能对检测结果产生干扰,例如使用口香糖、含有乙醇的口腔清洁产品等都可能导致误判。
为了确保准确性,最好在检测前不要摄入任何含有乙醇的物质。
食品安全快速检测技术汇总

食品安全快速检测技术汇总快速检测技术广泛用于食品安全快速检测,临床检验、检验检疫、毒品检验等公共领域。
食品安全快速检测是指对食品利用便携式分析仪器及配套试剂快速得到检测结果的一种检测方式。
食品安全问题主要有害污染物1.农药、化肥:有机磷,有机氯,硝酸盐2.兽药:兴奋剂,镇静剂,抗生素3.重金属离子:镉,铅,汞,铬,砷,钼4.生物毒素:黄曲霉毒素,呕吐毒素,肉毒素5.致病菌:大肠杆菌,沙门氏菌,葡萄球菌等快速检测含义包括样品制备在内,能够在短时间内出据检测结果的行为称之为快速检测。
三方面体现:(1)实验准备要简化(2)样品经简单前处理后即可测试,后采用先进快速的样品处理方式(3)分析方法简单,快速,准确食品安全快速检测分类按分析地点:现场快速检测,实验室快速检测按定性定量:定性快速筛选检验,半定量检验,全量检验农药残留检测方法(一)生物法1.生物化学测定法(酶抑制率法,速测卡法)2.分子生物学方法(如:ELISA)3.活体生物测定法(发光细菌,大型水藻,家蝇)4.生物传感器法生物传感器在食品分析中的应用:(1)食品成分分析(2)食品添加剂的分析(3)农药和抗生素残留量分析(4)微生物和生物毒素的检验(5)食品限度的检验(二)化学方法酶抑制法酶联免疫检测法蔬菜中硝酸盐含量的快速测定将NO3-还原N02-后,芳香胺与亚硝酸根离子发生重氮化反应,生成重氮盐,重氮盐再与芳香族化合物发生偶联反应,生成一种红颜色偶氮化合物(偶氮染料),其颜色强度与硝酸盐含量呈正比,通过试纸由无色变为红色,变色的试纸放入基于光学传感器原理的硝酸盐检测仪中比色测定硝酸盐含量。
仪器与材料:硝酸盐试纸. 快速测定仪硝酸盐速测管适用范围:乳品、饮用水、蔬菜等食物中硝酸盐的快速检测。
方法原理:按照国标GB/T5009. 33盐酸蔡乙二胺显色原理,在格林试剂中加入硝酸盐转化剂,并将其做成速测管,速测管中的试剂可将N03-还原为N02-后,再与芳香胺(氨基苯磺酸) 发生重氮反应,生成重氮盐,重氮盐再与芳香族化合物( A-祭胺)发生偶联反应,生成红色偶氮化合物(又叫偶氮染料),颜色深浅与硝酸盐含量成正比,与标准色卡比对,确定硝酸盐含量.兽药残留快速检测微生物法检测检测管中的培养基预先接种了嗜热脂肪芽孢杆菌,并含有细菌生长所需的营养以及pH指示剂。
白酒中乙醇含量测定

白酒中乙醇含量测定白酒中乙醇含量测定白酒中乙醇含量测定1.了解折光仪测定液体化合物的纯度的原理。
2.掌握折光率因素法和工作曲线法测定样品含量的方法原理。
3.学会阿贝折光仪的使用。
三、实验仪器与试剂仪器:阿贝折光仪一台、擦镜纸、滤纸。
试剂:无水乙醇、蒸馏水、白酒。
1、工作曲线法(1)配制乙醇—水体系的溶液:用酒精比重计配制含乙醇(V/V)10%,30%,40%,50%, 60%五个工作溶液。
仪器的清理,校正:将棱镜打开,用棉球蘸取丙酮擦洗棱镜上下两面,晾干。
用滴管在下面加2—3滴蒸馏水,注意:滴管不能碰到棱镜,润湿后关闭,测定蒸馏水的折光率,与表对照,得出校正值。
(2)工作液的测定:按折光仪的使用方法,测定工作液的折光率,以浓度为横坐标,折光率为纵坐标绘制工作曲线。
(3)样品的测定:按折光仪的使用方法,测定待测液的折光率,在工作曲线上找出其相应浓度。
2、折光率因素法:(1)乙醇—水体系折光率因素(F)的测定:根据工作曲线法所得结果,用已校正好阿贝折射计,按折光仪的使用方法测定与之浓度接近的工作液的折光率,并再次测定同温度蒸馏水的折光率,按下式分别计算折光率因素(F)值,并取平均值为结果。
(2)待测液的含量测定:用已校正好的阿贝折射计,按正常的使用方法测定折光率,并计算其含量:C末 = F(n末— n0)1、折光仪棱镜必须注意保护,不能在镜面上造成刻痕。
不能测定强酸、强碱及有腐蚀性的液体。
也不能测定对棱镜、保温套之间的粘合剂有溶解性的液体。
2、每次使用前后,应仔细认真地擦洗镜面,待晾干后再关上棱镜。
3、仪器在使用或储藏时均不得曝于日光中。
不用时应放入木箱内,木箱置于干燥的地方。
放入前应注意将金属夹套内的水倒干净,管口用东西封起来。
4、经常做彻底擦洗和检查。
六、附注:表2-15 不同温度下水和乙醇的折光率温度/℃ 水的折光率乙醇的折光率14 1.33348 1.3621016 1.33333 1.3612018 1.33317 1.3604820 1.33299 1.3588524 1.33262 1.3580326 1.33241 1.3572128 1.33219 1.35557 32 1.331641、简述测定折光率的原理及测定折光率的意义。
啤酒中乙醇和还原糖含量的测定
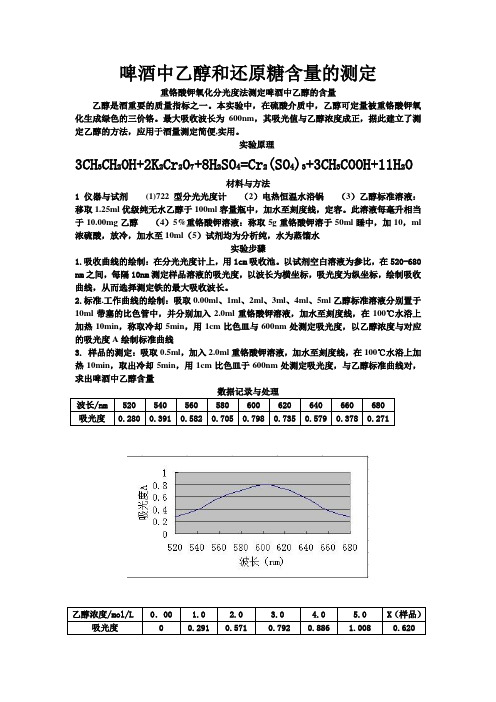
啤酒中乙醇和还原糖含量的测定重铬酸钾氧化分光度法测定啤酒中乙醇的含量乙醇是酒重要的质量指标之一。
本实验中,在硫酸介质中,乙醇可定量被重铬酸钾氧化生成绿色的三价铬。
最大吸收波长为600nm,其吸光值与乙醇浓度成正,据此建立了测定乙醇的方法,应用于酒量测定简便,实用。
实验原理3CH3CH2OH+2K2Cr2O7+8H2SO4=Cr2(SO4)3+3CH3COOH+11H2O材料与方法1 仪器与试剂(1)722型分光光度计(2)电热恒温水浴锅(3)乙醇标准溶液:移取1.25ml优级纯无水乙醇于100ml容量瓶中,加水至刻度线,定容。
此溶液每毫升相当于10.00mg乙醇(4)5%重铬酸钾溶液:称取5g重铬酸钾溶于50ml睡中,加10,ml 浓硫酸,放冷,加水至10ml(5)试剂均为分析纯,水为蒸馏水实验步骤1.吸收曲线的绘制:在分光光度计上,用1cm吸收池。
以试剂空白溶液为参比,在520-680 nm之间,每隔10nm测定样品溶液的吸光度,以波长为横坐标,吸光度为纵坐标,绘制吸收曲线,从而选择测定铁的最大吸收波长。
2.标准.工作曲线的绘制:吸取0.00ml、1ml、2ml、3ml、4ml、5ml乙醇标准溶液分别置于10ml带塞的比色管中,并分别加入2.0ml重铬酸钾溶液,加水至刻度线,在100℃水浴上加热10min,称取冷却5min,用1cm比色皿与600nm处测定吸光度,以乙醇浓度与对应的吸光度A绘制标准曲线3. 样品的测定:吸取0.5ml,加入2.0ml重铬酸钾溶液,加水至刻度线,在100℃水浴上加热10min,取出冷却5min,用1cm比色皿于600nm处测定吸光度,与乙醇标准曲线对,求出啤酒中乙醇含量数据记录与处理数据分析与总结由浓度与吸光度的图中可得:当A=0.620时 X=2.3mg/ml啤酒中乙醇的含量=(2.3X10)/0.5=46mg/ml参考文献1.与配制酒卫生标准的分析方法.GB/T5009.48-2003.[S].20032.生.彭榕妹.邓湘卫.等曙红内酯吸光度法测定酒中的乙醇含量J 李华检验-化学分册.1996.31啤酒中还原糖的测定(前言)实验原理将一定量的碱性酒石酸铜甲,乙液等量混合,立即生成蓝色的氢氧化铜沉淀,.这种沉淀很快与酒石酸甲钠反应,生成深蓝色的可溶性酒石酸钾钠铜络合物。
便携式酒醇(甲醇、乙醇)速测箱、速测盒

便携式酒醇(甲醇、乙醇)速测箱、速测盒酒醇速测仪适用于蒸馏酒中甲醇急性中毒剂量的现场快速测定。
甲醇速测盒适用于蒸馏酒中国家标准规定含量的现场快速测定,也适用于经过重新蒸馏的配制酒中甲醇含量的快速测定。
酒醇速测仪使用说明。
1方法原理在20℃时,水的折光率为,随着水中乙醇浓度的增加其折光率有规律地上升,当甲醇存在时,折光率会随着甲醇浓度的增加而降低,下降值与甲醇的含量成正比。
按照这一现象而设计制造出的酒醇含量速测仪,可快速显示出样品中酒醇的含量。
当这一含量与酒精度计测定出的酒醇含量出现差异时,其差值即为甲醇的含量。
在20℃时,可直接定量;在非20℃时,采用酒精度计温度—浓度换算表和选取与样品相当浓度的乙醇对照液进行对比定量。
2.在环境温度20℃时操作方法及结果计算掀开盖板(3),用擦镜纸小心拭净棱镜(2)表面,在棱镜上滴放5~7滴蒸馏水或纯净水,徐徐合上盖板,使试液遍布于棱镜表面。
手持镜筒(5)部位。
将盖板3对向光源或明亮处,将眼睛对准目镜(7),转动视度调节圈(6),使视场的分界线清晰可见。
用螺丝刀拧动仪器上的校准螺丝(4),调节仪器使视场中的明暗分界线对正刻线0%处,掀开盖板,用擦镜纸擦干棱镜。
取酒样5~7滴放在检测棱镜面上,徐徐合上盖板,以下操作与相同。
视场明暗分界线处所示读数,即为乙醇含量%。
重复操作几次,使读数稳定。
用酒精度计测定样品中的酒精度%。
即取1个洁净的100ml的量筒或透明的管筒,慢慢地倒进酒样到容器三分之二处,等液体无气泡时,慢慢放入酒精度计,用手轻按酒精度计上方,使酒精度计在所测刻线上下三个分度内移动,稳定后读取弯月面下酒精度示值。
结果计算甲醇含量=酒精度计测出的醇含量—酒醇速测仪测出的醇含量3.在环境温度非20℃时操作方法及结果计算对比法:首先用玻璃浮计测试样品的酒精度数,再选取一个与样品酒精度数相同或低于1度以内的乙醇对照溶液,然后用酒醇速测仪分别测试这两个溶液的醇含量,如果样品中不含甲醇,二者的酒醇速测仪读数应该一致,如果二者的读数相差1%以上时,或相差2%以上时,其差值即为甲醇的含量。
酒精化学品的安全检测与监测技术

酒精化学品的安全检测与监测技术引言:随着工业的发展和生活水平的提高,酒精化学品在我们的日常生活中扮演着重要的角色。
然而,由于其挥发性和易燃性的特点,酒精化学品的安全问题备受关注。
为确保人们的生命财产安全,酒精化学品的安全检测与监测技术迅速发展。
本文将重点介绍当前常用的酒精化学品的安全检测与监测技术。
一、传统的酒精化学品安全检测与监测技术1. 火焰离子化技术火焰离子化技术是一种传统的酒精化学品检测与监测方法。
该技术通过在火焰中产生离子,利用质谱仪或离子指示器进行检测。
然而,该技术存在着灵敏度不高、操作复杂和样品破坏性较大的缺点,限制了其在实际应用中的推广。
2. 气相色谱技术气相色谱技术是一种常用的酒精化学品检测与监测方法。
该技术通过样品蒸发和分离,利用色谱柱和检测器对样品中的化学成分进行分析。
虽然气相色谱技术具有高灵敏度、高分辨率和快速分析的优势,但仍然存在着设备昂贵、操作复杂和对操作者技术要求较高的问题。
二、新型的酒精化学品安全检测与监测技术1. 光纤传感技术光纤传感技术是一种新型的酒精化学品检测与监测技术。
该技术利用光纤传感器对酒精化学品的浓度进行监测。
光纤传感器具有高灵敏度、快速响应和无电磁干扰的优势,能够在远距离范围内实时监测酒精化学品的浓度变化。
2. 电化学传感技术电化学传感技术是另一种新型的酒精化学品检测与监测技术。
该技术通过电化学传感器对酒精化学品的电化学特性进行分析。
电化学传感器具有高选择性、高灵敏度和实时监测的特点,能够准确检测酒精化学品的浓度。
三、酒精化学品安全检测与监测技术的应用领域1. 工业领域酒精化学品在工业领域的应用广泛,如燃料、溶剂以及化学反应的催化剂等。
酒精化学品的安全检测与监测技术在工业领域起到了关键作用,能够及时发现潜在的安全隐患。
2. 医疗领域酒精是许多医疗用品的重要成分,如消毒酒精、外敷酒精等。
酒精化学品的安全检测与监测技术在医疗领域可以帮助医护人员准确调整酒精浓度,确保医疗过程的安全性和有效性。
近红外光谱法快速测定啤酒中乙醇的含量

每个样品的透射光谱检测 & 次, 以保证 & 次光谱检测中 的最大相对误差小于 ! 5 。 & 次光谱检测的平均值作为 最终光谱数据。 图 % 是某一品牌啤酒在近红外光谱仪上 采集的光谱图。
"一阶导数吸收光谱: 8;")":"0!=)1=19%<!!3)=1=9!<")#=%9&0%#=)#3!9$< %%$)!$=9#0&)=!"91
!"#$% &’(’)*$+"($,+ ,- ./0,1,/ 2,+(’+( $+ 3’’) 45 6789:!
;< =>?*@A,;&% 7?/B >/C DEF% GA/
(D?@@HBH ?I GA?@?BAJ>@ F/KAL?/0H/M>@ ?I NA>/BOP </AKHLOAMQ, RSH/TA>/B , NA>/BOP !"!#"$ , DSA/> )
近 红 外 光 是 波 长 范 围 ,-# .!-## /0 ( 波 数 范 围 之间的电磁波, 本谱区是于 ":## 年被 "$$$#.5### J0 ) \"] EHLOJSH@ 所发现的 。它包含基频振动大于 !### J0*" 基
*"
把握。 气相色谱法、 啤酒自动分析仪都是利用仪器法, 它 省去了传统方法的蒸馏与手工测定比重等烦琐操作, 且 分析方法准确, 但速度上仍然不够快。近红外光谱快速 检测也是一种仪器分析法, 只需要 ! 0A/ 左右就可以得 出结果, 而且可以同时测定几种成分。如果实现在线检 测, 则可以随时了解啤酒的发酵过程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
生物传感器法快速测定酒中的乙醇含量冯东;王丙莲;梁晓辉;李雪梅;李大海【摘要】Ethanol biosensor based on enzyme immobilization technology was used to determinate ethanol content in liquor.The results showed that the biosensor could measure ethanol content rapidly and accurately,with response time of 20 s,recovery ratio of 99.3 %~101.2 %,and repeatability relative standard deviation(RSD) 0.97 %~1.50 %.There was no significant difference(P〉0.05) in determination results between biosensor,gas chromatography(GC) and density bottlemethod.Besides,it had the advantages such as high sensitivity(detection limit was 1 mg/100 mL),easy operation,low cost and high specificity.It seemed that biosensor would become the novel method of ethanol detection in liquor.%利用酶固定化技术,制备乙醇生物传感器,并用其测定酒中乙醇含量。
结果表明,生物传感器法测定酒中乙醇含量快速而准确,检测时间为20 s,回收率为99.3%~101.2%,相对标准偏差为0.97%~1.50%;检测灵敏度高,检出限为1 mg/100 mL;与气相色谱法、密度瓶法相比较,差异不显著(P〉0.05);且具有操作简单、成本低廉、专一性强等优势,有望成为酒类乙醇含量测定的新方法、新手段。
【期刊名称】《酿酒科技》【年(卷),期】2012(000)002【总页数】4页(P83-86)【关键词】生物传感器;酒;乙醇;测定分析【作者】冯东;王丙莲;梁晓辉;李雪梅;李大海【作者单位】山东省科学院生物研究所,山东济南250014 山东省生物传感器重点实验室,山东济南250014;山东省科学院生物研究所,山东济南250014 山东省生物传感器重点实验室,山东济南250014;山东省科学院能源研究所,山东济南250014;山东省科学院生物研究所,山东济南250014 山东省生物传感器重点实验室,山东济南250014;山东省科学院生物研究所,山东济南250014 山东省生物传感器重点实验室,山东济南250014【正文语种】中文【中图分类】TS262.3;TS261.7对于酒精类饮品,譬如白酒、啤酒、果酒、米酒以及其他药酒、保健酒等酒类,乙醇含量是检测其质量的重要指标之一,国家对此有严格规定,故快速准确地检测酒中乙醇含量在食品工业质量控制中十分重要。
目前,酒中乙醇含量的测定方法包括密度瓶法[1]、酒精计法[2]、气相色谱法[3-4]、分光光度法[5]、比色法[6]、化学氧化法等[7]。
上述几种测定方法中,密度瓶法、酒精计法和化学氧化法均为国家标准规定方法,但是测定前需对样品进行蒸馏,且操作过程复杂,同时也会因为仪器和人为因素干扰而使测定结果与实际值存在一定误差。
分光光度法和比色法受样品颜色干扰较为严重。
相比较而言,气相色谱法结果准确,但是操作复杂、设备昂贵,大大提高了相关行业的生产成本,故在指导生产的实际应用中受到较大限制。
为此,有必要建立一种快速、准确且成本较低的乙醇含量分析方法,以适应当前食品、饮料、酿酒等相关行业对低成本、高效率的需求。
生物传感器法是采用酶固定化技术,将乙醇氧化酶固定于载体材料制成乙醇氧化酶酶膜,并结合生物传感器技术制备乙醇生物传感器。
利用酶催化反应特异性,从而实现对各种酒精类饮品中乙醇含量进行快速、灵敏、准确测定。
1 材料和方法1.1 试剂和材料乙醇氧化酶(AOX 5483 U/mL),美国 Sigma公司;缓冲溶液为0.1 mmol/L,pH7.2的磷酸缓冲液;市售中国劲酒(35%vol)、蒙山十足全蝎酒(35%vol)、张裕三鞭酒(30%vol)、特制二锅头(56%vol);其他试剂均为分析纯。
1.2 固定化乙醇氧化酶酶膜及酶电极制备乙醇氧化酶酶膜及乙醇酶电极结构见图1,乙醇氧化酶经戊二醛交联剂固定于核微孔基质膜。
固定化乙醇氧化酶酶层通过酶膜片及O型密封圈固定于过氧化氢电极顶端,制备酶电极[8]。
乙醇酶电极系统包括2个电极及其插头。
固定化乙醇氧化酶对溶液中乙醇进行催化反应,生成的H2O2由过氧化氢电极检测并进行结果显示,从而实现对乙醇的定量。
图1 酶电极(左)及固定化酶膜(右,放大)注:1.银电极;2.铂电极;3.酶膜片;4.酶膜圈;5.热敏电阻;6.电极杆;7.电极引线;8.O 型密封圈;9.核微孔基质膜;10.酶层;11.内膜层1.3 乙醇生物传感器制备本研究中,乙醇生物传感器是利用酶促反应来定量乙醇,其样品分析原理如下:该生物传感器系统通过H2O2的定量分析实现对乙醇含量的测定,故过氧化氢电极和固定化乙醇氧化酶均是乙醇生物传感器的核心器件。
乙醇生物传感器系统结构见图2,样品室侧面装有过氧化氢电极,电极表面覆盖固定化乙醇氧化酶酶膜。
含有乙醇的底物在样品室内与固定化乙醇氧化酶层接触并反应,产生的H2O2由过氧化氢电极检测并转变为电信号,该电流信号经放大处理显示测定结果,并自动记录和打印。
因为产生的H2O2的量与乙醇质量浓度成线性比例关系,故该乙醇生物传感器系统可测定样品中乙醇含量。
图2 乙醇生物传感器结构示意图注:1.进样帽;2.光传感器;3.反应池顶帽;4.过氧化氢电极;5.电磁搅拌子;6.样品室;7.乙醇氧化酶酶膜;8.缓冲液进口和废液排空管;9.电极旋钮;10.废液吸出管;11.进样口1.4 测定方法1.4.1 乙醇标准溶液配制无水乙醇溶于蒸馏水或传感器专用缓冲液,配制浓度依次 0 mg/100 mL、0.50 mg/100 mL、1.00 mg/100 mL、2.00mg/100mL、4.00mg/100mL、6.00mg/100mL、8.00mg/100 mL、10.00 mg/100 mL、20.00 mg/100 mL、40.00 mg/100 mL、60.00 mg/100 mL、80.00 mg/100 mL、100.00 mg/100 mL、120.0 mg/100 mL的乙醇标准溶液。
乙醇标准液现配现用,用于检验乙醇生物传感器的线性范围和检测限。
1.4.2 测定步骤1.4.2.1 乙醇生物传感器定标乙醇生物传感器使用前先定标,以100 mg/100 mL乙醇标准溶液作为仪器的定标溶液[9]。
传感器最终自动定标为100,然后即可进行线性范围、检测限的确定,以及待测样品乙醇含量的测定。
1.4.2.2 乙醇生物传感器标准曲线的制作乙醇生物传感器自动定标后,用特制微量进样器吸取浓度 0 mg/100 mL、0.50 mg/100 mL、1.00 mg/100 mL、2.00mg/100mL、4.00mg/100mL、6.00mg/100mL、8.00mg/100 mL、10.00 mg/100 mL、20.00 mg/100 mL、40.00 mg/100 mL、60.00 mg/100 mL、80.00 mg/100 mL、100.00 mg/100mL、120.0 mg/100 mL的乙醇标准溶液各25 μL,进行测定,每个浓度重复3次。
以乙醇标准溶液浓度为横坐标,测定结果为纵坐标,绘制标准曲线,测定乙醇生物传感器的检测灵敏度及线性响应规律。
1.4.2.3 酒样样品测定乙醇生物传感器线性范围及检测限确定之后,将酒样用蒸馏水或乙醇传感器专用缓冲液按相应比例稀释,调整pH值为6~8。
准确吸取25 μL稀释的酒样,根据仪器“进样”指示将酒样注入反应池。
20 s后乙醇生物传感器自行显示并打印测定结果,结合稀释倍数即可测得酒样中乙醇含量,整个测定周期控制在1 min左右。
1.5 数据处理方法采用t检验分析,比较酒精计法、气相色谱法与乙醇生物传感测定结果之间的显著性差异。
判断标准:p>0.05,差异不显著;p<0.05,差异显著;p<0.01,差异极显著。
2 结果与分析2.1 pH值对乙醇氧化酶酶膜活性的影响乙醇氧化酶在不同的pH值测定环境中,酶活性、稳定性及使用寿命不同,过酸或过碱的溶液环境均导致其活性下降,以致失活,从而严重影响乙醇生物传感器测定的准确度。
调整0.1 mmol/L磷酸缓冲液pH值为1~11。
乙醇氧化酶膜活性随pH值变化曲线及不同pH值环境中酶膜寿命曲线见图3。
图3 pH值对乙醇氧化酶酶膜活性(A)及酶膜寿命(B)的影响图3表明,在pH值6~8范围内,乙醇氧化酶均保持很高活性;pH7左右时酶活性达到最高。
此外,pH7的测定环境中乙醇氧化酶膜能长时间(35 d)保持较高的活性。
鉴于此,乙醇生物传感器选用pH7.2的磷酸缓冲液,待测酒样需调整pH 值6~8,强酸或强碱样品液均将导致传感器酶膜寿命短以及测定不准确。
2.2 线性范围及检出限图4为乙醇生物传感器的标准曲线。
由图4(A)可知,乙醇浓度为0~120.00mg/100mL范围时,传感器线性关系较差,回归方程为Y=1.38987X-5.10163,相关系数r=0.94012。
去掉0.50 mg/100 mL、120.00 mg/100 mL乙醇浓度,绘制传感器标准曲线,见图4(B)。
结果表明,乙醇浓度在1.00~100.00 mg/100 mL范围内时,传感器测定值与乙醇浓度呈良好线性关系,其回归方程为:Y=0.99696X+0.12329,相关系数r为0.99984。
由此可认为,乙醇生物传感器的线性范围为1.00~100.00mg/100mL,检出限为1.00 mg/100 mL。
2.3 共存物对乙醇生物传感器测定结果的影响按方法“1.4.1”配制浓度均为50 mg/100 mL的甲醇、丙醇、丁醇、乙酸、乙酸乙酯、乙醇+甲醇、乙醇+丙醇、乙醇+丁醇、乙醇+乙酸、乙醇+乙酸乙酯等溶液。
利用乙醇生物传感器对各溶液分别进行含量检测,并以50 mg/100 mL的乙醇标准溶液做对比。
每个测试重复3次,结果见表1。
图4 乙醇生物传感器的标准曲线?????? ?????? ???????? ? ? ????? ? ? ?!? ?????? ??? ????????"??? ??? ?????? ???? ??? "??? ??? ? ???? ???"??? ??? ? ???? ?? "? ? ? ? ?"? ?!???? ? ?!? ? ?由表1可以看出,乙醇生物传感器能够准确测定溶液中乙醇的含量,而对其他类似结构干扰物无明显响应;且对于乙醇与干扰物的混合溶液,传感器测定值亦与乙醇浓度相接近,由此可认为,乙醇溶液中其他醇类、酯类等物质对测定影响甚微。
