蛋白质和核酸的化学
简述核酸和蛋白质代谢的相互关系

简述核酸和蛋白质代谢的相互关系全文共四篇示例,供读者参考第一篇示例:核酸是细胞内的一种重要有机物质,它由核苷酸构成,是构成核酸的基本单元。
核酸分为DNA(脱氧核糖核酸)和RNA(核糖核酸)两种。
核酸在细胞内具有非常重要的功能,它们可以携带遗传信息,参与蛋白质的合成,调控细胞的生长和分化等过程。
蛋白质则是细胞内最重要的有机物质之一,是生命体内各种生物学功能和生命活动不可或缺的组成部分。
蛋白质合成是一个复杂的生物化学过程,需要核酸的介入才能完成。
在细胞内,RNA起着传递DNA信息的作用,RNA通过转录过程将DNA上的遗传信息转换成RNA信息,然后RNA将这些信息传递给细胞内的核蛋白合成机器,进而合成蛋白质。
核酸代谢和蛋白质代谢是密切相关的,两者之间存在着相互关系。
在细胞内,核酸和蛋白质代谢之间的相互关系主要体现在以下几个方面:核酸还可以调控蛋白质的合成。
在细胞内,存在着一些特殊类型的RNA,如miRNA和siRNA等,它们能够通过靶向特定基因的mRNA,抑制或促进这些基因的表达,从而影响蛋白质的合成。
这种核酸介导的蛋白质合成调控,使得核酸和蛋白质代谢之间形成了一种复杂的调控网络。
核酸代谢和蛋白质代谢还存在着其他相互关系。
核酸可以通过调节细胞内mRNA的降解速率,影响蛋白质的合成水平;而蛋白质也可以参与核酸的合成和修复过程。
这些相互关系构成了细胞内核酸和蛋白质代谢的相互调节机制,维持了细胞内生物学功能的正常运行。
第二篇示例:核酸和蛋白质是生物体内两种重要的生物大分子,它们在生物体内的代谢过程中密不可分。
核酸是生物体内的遗传物质,负责信息的传递和储存,而蛋白质则是生物体内的最重要的功能分子,承担着多种生物过程中的功能。
核酸和蛋白质之间通过一系列生物化学反应相互转化,相互影响,共同维持着生物体内的代谢平衡和生物功能的正常进行。
核酸的合成过程称为核酸代谢,蛋白质的合成过程称为蛋白质代谢。
核酸和蛋白质的代谢密切相关,二者之间的相互关系主要体现在以下几个方面:核酸和蛋白质的合成过程相互依赖。
第1单元 第3讲 蛋白质和核酸

第3讲蛋白质和核酸判断正误并找到课本原文1.细胞的各项生命活动都离不开蛋白质,蛋白质是生命活动的主要承担者。
(必修1P29)(√)2.氨基酸是组成蛋白质的基本单位。
(必修1P29)(√)3.每种氨基酸都含有一个氨基(—NH2)和一个羧基(—COOH),并连接在同一个碳原子上。
(必修1P29)(×)4.连接两个氨基酸分子的化学键叫作肽键。
由两个氨基酸缩合而成的化合物,叫作二肽。
(必修1P30)(√)5.氨基酸之间能够形成氢键等,从而使肽链能盘曲、折叠,形成具有一定空间结构的蛋白质分子。
(必修1P30)(√)6.氨基酸序列改变或蛋白质的空间结构改变,可能会影响其功能。
(必修1 P31)(√)7.经过加热、加酸、加酒精等引起细菌和病毒的蛋白质变性,可达到消毒、灭菌的目的。
(必修1P32)(√)8.真核细胞的DNA主要分布在细胞核中,线粒体、叶绿体内也含有少量的DNA。
(必修1P34)(√)9.一般情况下,DNA由两条脱氧核苷酸链构成,RNA由两条核糖核苷酸链构成。
(必修1P35)(×)10.DNA分子是储存、传递遗传信息的生物大分子,部分病毒的遗传信息储存在RNA中。
(必修1P35)(√)11.细胞中的各种化合物的含量和比例是保持不变的,以保证细胞生命活动的正常进行。
(必修1P36)(×)12.一切疾病都与基因受损有关。
(必修1P36)(×)(2018·浙江4月选考)蛋白质在生物体内具有重要作用。
下列叙述正确的是()A.蛋白质化学结构的差异只是R基团的不同B.某些化学物质可使蛋白质的空间结构发生改变C.蛋白质控制和决定着细胞及整个生物体的遗传特性D.“检测生物组织中的蛋白质”需同时加入双缩脲试剂A和B答案 B解析蛋白质化学结构的差异包括组成其氨基酸的种类、数量、排列顺序及肽链的盘曲、折叠方式及其形成的空间结构不同,A错误;某些化学物质可使蛋白质的空间结构发生改变,如酒精,B正确;控制和决定着细胞及整个生物体的遗传特性的是基因(或DNA),C错误;检测生物组织中的蛋白质时应先加入双缩脲试剂A液创造碱性环境,再加入双缩脲试剂B液发生显色反应,D错误。
【苏教版】高中化学选修五:5.2《氨基酸、蛋白质、核酸》教学案

1.羧酸中的官能团是什么?它能否与NaOH溶液发生反应?提示:羧酸中的官能团为-COOH,它能与NaOH溶液发生反应生成-COONa。
2.蛋白质是由哪些元素组成的?蛋白质能否发生水解反应?淀粉、油脂、蛋白质是否都是天然高分子化合物?提示:蛋白质的组成元素除C、H、O外,还含有N、S、P等;蛋白质能发生水解反应;淀粉、蛋白质是天然高分子化合物,油脂不属于高分子化合物。
3.如何鉴别蚕丝和人造丝?提示:蚕丝为蛋白质,人造丝属于纤维素,可以用灼烧的方法鉴别蚕丝和人造丝。
[新知探究]探究1什么是氨基?α氨基酸的结构通式是怎样的?提示:氨基是指氨分子(NH3)中去掉一个氢原子后剩余的部分(-NH2)。
α氨基酸的结构通式为。
探究2甘氨酸(α氨基乙酸)具有两性,你能写出甘氨酸与盐酸、NaOH溶液反应的化学方程式吗?探究3有两种氨基酸,分别是甘氨酸和丙氨酸,两分子氨基酸之间脱水能形成几种二肽?试写出它们的结构简式。
提示:甘氨酸两分子脱水形成二肽,;丙氨酸两分子脱水形成二肽:;甘氨酸与丙氨酸分子间脱水形成两种二肽:,共形成四种二肽。
[必记结论]1.组成和结构(1)组成:氨基酸可看作是羧酸分子中烃基上的H被氨基取代后的产物。
(2)结构:α氨基酸的结构简式可表示为,αC为手性碳原子。
其官能团为-COOH和-NH2。
(3)常见的氨基酸:2.氨基酸的化学性质(1)两性:氨基酸分子中既含有氨基(显碱性),又含有羧基(显酸性),因此,氨基酸是两性化合物,能与酸、碱反应生成盐。
(2)成肽反应:概念:两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与另一分子的羧基间脱去一分子水,缩合形成含有肽键()的化合物,称为成肽反应。
[成功体验]1.关于氨基酸的下列叙述中,不正确的是()A.氨基酸都是晶体,一般能溶于水B.氨基酸都不能发生水解反应C.氨基酸是两性化合物,能与酸、碱反应生成盐D.天然蛋白质水解最终可以得到α氨基酸、β氨基酸等多种氨基酸解析:选D氨基酸熔点较高,室温下均为晶体,一般能溶于水而难溶于乙醇、乙醚;氨基酸是两性化合物,能与酸、碱反应生成盐;氨基酸分子间能发生成肽反应,但氨基酸都不能发生水解反应;天然蛋白质水解的最终产物是多种α氨基酸。
《蛋白质和核酸》 知识清单

《蛋白质和核酸》知识清单一、蛋白质(一)蛋白质的组成蛋白质是由氨基酸组成的大分子化合物。
氨基酸是蛋白质的基本组成单位,它们通过肽键相连形成多肽链,进而折叠形成具有特定空间结构的蛋白质。
组成蛋白质的氨基酸有 20 种,其中 8 种为必需氨基酸,人体不能自身合成,必须从食物中获取。
(二)蛋白质的结构1、一级结构指多肽链中氨基酸的排列顺序。
这是蛋白质结构的基础,决定了蛋白质的性质和功能。
2、二级结构主要有α螺旋、β折叠等形式。
α螺旋是常见的结构,氨基酸链像螺旋一样卷曲。
β折叠则是多肽链呈折叠状。
3、三级结构是整条多肽链的空间构象,包括侧链基团的相互作用、二硫键的形成等。
4、四级结构对于由多条多肽链组成的蛋白质,这些多肽链之间的相互作用和空间排列称为四级结构。
(三)蛋白质的性质1、两性解离在不同的pH 条件下,蛋白质可以解离成带正电荷或负电荷的离子。
2、胶体性质蛋白质分子大小较大,在溶液中形成胶体溶液。
3、变性与复性变性是指蛋白质在某些物理或化学因素作用下,其空间结构被破坏,导致性质改变。
但在一定条件下,变性的蛋白质可能恢复其原有的结构和功能,即复性。
4、沉淀通过加入某些试剂,如盐析、重金属盐等,可以使蛋白质沉淀。
(四)蛋白质的功能1、催化作用许多酶都是蛋白质,能够加速生物体内的化学反应。
2、运输功能如血红蛋白运输氧气、脂蛋白运输脂质等。
3、调节作用例如胰岛素调节血糖水平。
4、免疫功能抗体是具有免疫功能的蛋白质。
5、构成生物体结构如胶原蛋白构成结缔组织、肌肉中的肌动蛋白和肌球蛋白等。
二、核酸(一)核酸的分类核酸分为脱氧核糖核酸(DNA)和核糖核酸(RNA)两大类。
(二)核酸的组成核酸是由核苷酸组成的。
核苷酸由含氮碱基、戊糖(核糖或脱氧核糖)和磷酸组成。
1、 DNA 的组成含氮碱基有腺嘌呤(A)、鸟嘌呤(G)、胸腺嘧啶(T)和胞嘧啶(C)。
2、 RNA 的组成含氮碱基有腺嘌呤(A)、鸟嘌呤(G)、尿嘧啶(U)和胞嘧啶(C)。
生命科学中的蛋白质与核酸相互作用机制研究

生命科学中的蛋白质与核酸相互作用机制研究生命科学是一门研究生物体及其生命现象的学科,其中的蛋白质与核酸相互作用机制研究属于其中的重要领域。
蛋白质与核酸是生命体系中最为基础和常见的大分子,两者之间的相互作用可谓是生命功能调控的基础。
本文将从以下几个方面进行介绍与探讨。
一、蛋白质与核酸的概念及其结构蛋白质和核酸都是生命体系中最为重要的分子。
蛋白质是由氨基酸组成的多肽,它们在体内担任着各种结构、传递、催化以及调控功能的重任。
而核酸是生命体系中的遗传物质,形成了DNA和RNA两种不同类型的核酸,DNA负责存储遗传信息,而RNA负责将遗传信息转化为具体的功能。
蛋白质与核酸的结构也是二者相互作用的基础。
蛋白质的结构分为四个层次:一级结构指蛋白质中氨基酸的化学序列,二级结构指蛋白质在局部呈现的空间结构,常见的包括a-螺旋和b-片层,三级结构指蛋白质整体的空间结构,包括局部折叠和全局折叠,四级结构指由多个蛋白质组成的复合物。
核酸的结构也具有大的类似性。
DNA分子大部分呈现出螺旋形状,通过镶嵌在螺旋内的氢键和VanderWaals力来保持稳定。
RNA的结构则有更多的变化,可以是线性或环形结构,提供了诸如催化反应和调控遗传信息等功能。
二、蛋白质与核酸的相互作用在生命系统中,蛋白质与核酸之间的相互作用可以体现出多种生物过程,如DNA复制、转录和翻译、RNA修饰、RNA剪切以及蛋白质的折叠和降解等。
其中,DNA复制是生命系统中最为基础和重要的过程之一,它需要依靠DNA聚合酶和其他辅助因子来实现。
在DNA复制过程中,DNA聚合酶能够在模板链上识别特定的配对碱基并合成新的链,一旦出现错配会被修复酶进行纠错。
复制完成后,两个完全相同的双链DNA分子得以产生。
RNA转录也是生命系统中非常重要的过程,它可以从DNA模板中复制一份RNA分子,并且有着诸多的调控机制。
转录过程中,RNA聚合酶沿着DNA模板链滑动,在核酸序列上拼接RNA,以此形成RNA多肽序列。
蛋白质与核酸的相互作用核酸结合蛋白模板
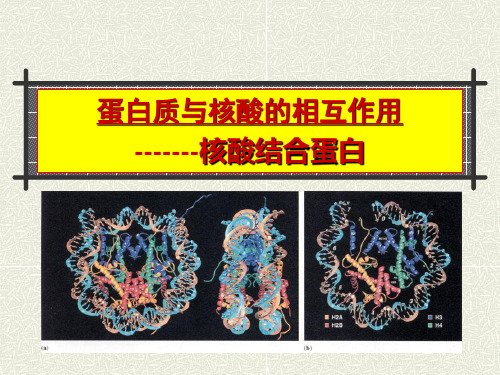
3.2.3 锌指结构的特点
Cys2His2锌 指蛋白与DNA 形成复合物的 X-射线晶体衍 射图谱。 三个锌指以 半环状排列于 DNA的大沟中。
3.2.3 锌指结构的特点
雌激素受体 (ER) DNA结 合结构域与 DNA识别因子 配位的同二聚 体。其中四个 圆代表二聚体 中的四个Zn 离子。
RNA结构的特点:胞内RNA一般呈单链结构,但往往 折叠成各种二级结构(突起、发夹、茎环等)。
RNA结合蛋白中的基本结构
结合结构 核糖核酸蛋白结 构域 dsRBD 结合部位 β-折叠 β-折叠 分布 真核生物 所有生物 举 例 U1A snRNP 果蝇的Staufen蛋白
K-同源蛋白
环区
真核生物
6.3 解读蛋白中的氨基酸
部分替换:用基因工程方法替换结构域中的某 些残基,研究其对与DNA结合的重要性。 结构分析:用X-射线、NMR方法研究发现,在 DNA和蛋白质结合过程中,蛋白质和DNA的构 象发生了适宜性的变化,水分子在蛋白和DNA 的相互作用中也发挥了特殊的作用。
6.4 假定的锌指蛋白DNA识别密码
目前还没有发现一套普遍的密码适用于所有的蛋白质 和氨基酸,但在锌指蛋白中发现了一个初步的规律。 锌指蛋白氨基酸残基与DNA碱基对应关系
3’
T A G
5’
与Zif268相关的锌指蛋白的部分DNA识别密码
三联体密码中碱基的位置
碱基
A C
5’
中部
3—Asn 3—Asn,Leu,Thr,Val
3’
-1—Gln+2--Ala
类固醇受体家 族 碱性结构域 带状-螺旋-螺旋 组蛋白-核心
α -螺旋
α -螺旋
真核生物
真核生物
生物化学核苷酸代谢与蛋白质的生物合成
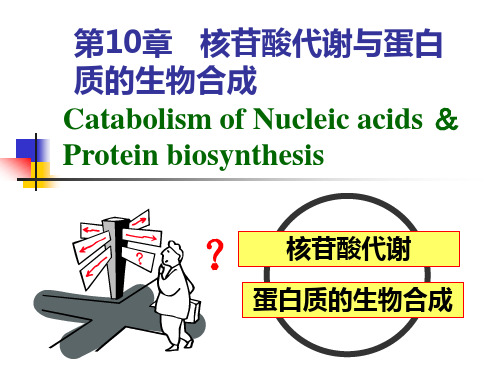
嘌呤碱或嘧啶碱+戊糖 磷酸 嘌呤碱或嘧啶碱+戊糖-1-磷酸
核苷+ 核苷+H2O
核苷水解酶
嘌呤碱或嘧啶碱+ 嘌呤碱或嘧啶碱+戊糖
一、核酸和核苷酸的分解代谢 (一)嘌呤核苷酸的分解代谢
Hale Waihona Puke 嘌呤碱的降解1、人的嘌呤碱的降解 、
共同中间产物
人和猿类等缺乏分解尿酸的能力,因此尿酸是人、 尿酸是人 人和猿类等缺乏分解尿酸的能力,因此尿酸是人、 等缺乏分解尿酸的能力 猿、鸟类及爬虫类体内嘌呤碱分解的最终产物。 鸟类及爬虫类体内嘌呤碱分解的最终产物。
二、核苷酸的生物合成 (一)嘌呤核糖核苷酸的合成 2、补救途径
——体内有些组织(脑、血细胞等)缺乏从 体内有些组织( 体内有些组织 血细胞等) 头合成的酶,只能利用游离的嘌呤碱或嘌呤核苷 嘌呤碱或嘌呤核苷为 头合成的酶,只能利用游离的嘌呤碱或嘌呤核苷为 原料合成嘌呤核苷酸的过程,称为补救合成。 原料合成嘌呤核苷酸的过程,称为补救合成。
二、核苷酸的生物合成 (二)嘧啶核糖核苷酸的合成 2、补救途径
第二节 核酸的生物合成
一、遗传信息传递的中心法则
DNA
replication reverse transcription
transcription
protein
translation
RNA
replication
分子生物学的中心法则( 分子生物学的中心法则(central dogma)
(白血病,恶性肿瘤) 白血病,恶性肿瘤)
0.27mmol/L, :0.21mmol/L 男: 0.27mmol/L, 女:0.21mmol/L
血中尿酸↑ 血中尿酸
>0.48mmol/L(8mg%), 0.48mmol/L(8mg%), 析出结晶
蛋白质和核酸

【讨论】若不小心误服了铅离子,在去医院前可 以采用什么急救措施?
盐析与变性的对比
盐析
变性
相同点
加入某种物质后有沉淀生成
不 同
盐 加入某些浓盐溶液,
不 如: Na2SO4 同 (NH4)2SO4等
重金属盐、醛、加 热或剧烈震动
点 复原 可逆,加水即可
不可逆
的缩反合应机理: 酸脱羟基,氨脱氢
+
肽键
+ H2O
多种氨基酸分子按不同的排列顺序以肽键相互结合,
可以形成千百万种具有不同的理化性质和生理活性 的多肽链。相对分子量在10 000以上的,并具有一 定空间结构的多肽,称为蛋白质。
知识拓展
H
NH HO O
CH2
C
Δ
O
C
CH2 OH HN
H
H NO ON H
3、具有酸性
4、分类: (1)脱氧核糖核酸(DNA):生物遗传信息的载体; 还指挥着蛋白质的合成、细胞的分裂和制造新的细胞。 (2)核糖核酸(RNA):根据DNA提供的信息控制 体内蛋白质的合成。
二、蛋白质的结构与性质
1、蛋白质的组成
组成元素主要包括: C、H、O、N、S等
组成基本结构单元: 氨基酸
相对分子质量:
几万----几千万
属于含氮生物高分子化合物
2、蛋白质的结构
一级结构:蛋白质中各种氨基酸的连接方式和排列顺序, 肽键是一级结构的主键。
二级结构:多肽链卷曲盘旋和折叠的空间结构
三级结构:二级结构 的肽链进一步盘曲折 叠形成亚基。
1、什么是酶
一类由细胞产生的,对生物体内的化学反 应具有催化作用的蛋白质。
