核-壳结构Fe2O3@SnO2负极材料的制备及性能
高性能锂离子电池负极材料的制备及其性能的研究PPT课件

2021
17
·
谢谢聆听
2021
18
2021
7
碳基负极材料
常见的碳基负极材料有:石墨、硬碳、软碳等。对碳基材料进 行改性的方法常有:机械研磨、表面包覆、表而氧化、掺杂等。碳 基材料首次充放电效率高、导电性好、不可逆容量低、电极电势较 低且价格低廉来源广。但碳基材料比容量低难以满足现在越来越高 的能量需求。
钛基负极材料
常见的钛基负极材料为:TiO2、Li4Ti5O12。钛基材料的常见合 成方法有:水热合成法、溶胶-凝胶法、模板法、电化学阳极氧化 法、液相沉淀法、超声合成法等。TiO2 较高的嵌锂离子电位(1.5~ 1.8 V),可以避免锂枝晶的生成,然而TiO2本身是半导体,导电性 差;Li4Ti5O12由于在嵌锂离子时具有零应变(体积变化约 0.2%)特性 ,具有较正的理论嵌锂离子电位(1.55 V,vs. Li/Li+),被认为是一 种理想的锂离子电池负极材料;然而, Li4Ti5O12导电性差,导致 其大电流倍率性能差为提高材料的电子导电性,目前的研究主要 集中在掺杂和表面修饰。
• 1980 年,Armand 率先提出锂蓄电池负极不再采用金属锂,而是正负极均采 用能让锂离子自由脱嵌的活性物质TiS2。从此以后,锂离子电池得到了迅猛 的发展。
• 1990 年日本的索尼(Sony)公司率先开发了首个商用锂离子电池,随后革新了 电子产品的新面貌,它是把锂离子嵌入碳中形成负极,取代传统锂原电池的 金属锂或锂合金作负极。
2021
10
研究内容以及方案
需要解决的问题
a)硅负极方面:
1(减缓体积膨胀)电化学储锂时,由于硅原子结合锂原 子得到合金相的过程对应的材料体积变化大(~400%)引起 的电极可逆容量的迅速衰减。
单双壳层SnO_2@C纳米空心球多级结构的设计制备及其高效二次锂离子电池负极的储能研究

单/双壳层SnO_2@C纳米空心球多级结构的设计制备及其高效二次锂离子电池负极的储能研究近年来,伴随科学技术的不断创新,便携式电子设备、电动运输等新兴领域得到了飞速发展。
因此,这些新产品对于电动能源的需求和依赖与日俱增。
锂离子电池作为一种新能源设备正是凭借其超高的容量密度、杰出的功率密度以及稳定的循环性能等诸多优势得以脱颖而出,获得世界范围内的广泛关注。
众所周知,锡基负极材料作为下一代锂离子电池的负极材料得到了广大科研工作者的一致认可。
那是因为其理论容量高达992 mA h g-1,这几乎是现如今使用的商业化石墨负极材料(372 mA h g-1)的两倍多。
所以,锡基负极材料的改性,尤其是对其形貌的调控得到了广泛的研究和报道。
目前,合成形貌多变、纯度高且结晶性良好的晶体材料的主要方法是水热合成法。
本论文中的双壳层SnO2@C纳米空心球、单壳层SnO2@C纳米空心球和双壳层SnO2纳米空心球都是采用多步水热合成的方法制得。
合成采用了模板法,其中核-壳结构的SiO2模板发挥重要的作用。
随后,我们将这些合成的锡基材料应用到锂离子电池上并测试了它们的电化学性能。
课题中得到的主要结论如下:(1)通过对核-壳结构SiO2的形貌表征,我们推测出了SiO2胶球向核-壳结构转变的可能原理。
从形貌的变化过程可以清楚的看到SiO2内部核的消融与外部壳层的生长这两个过程是单独且并发的。
在整个过程中,NaBH4起到了至关重要的作用。
反应开始,NaBH4会和H2O发生缓慢的反应,并产生出NaBO2和H2。
一方面,这一反应会使体系呈碱性,因此SiO2很容易在碱性溶液中发生溶解,比如SiO2在NaOH溶液中的溶解。
另一方面,单硅酸盐和聚硅酸盐类大量释放到体系中,最终会达到过饱和的程度。
同时,NaBO2的量也会伴随着NaBH4的反应而增加。
这些导致SiO2再次沉淀到正在溶解的内部核表面,形成壳层结构。
(2)双壳层SnO2@C纳米空心球具有诸多杰出性能。
SnO2的研究

二氧化锡膜气敏传感器核心研究深入探讨摘要:在论述二氧化锡气敏机理的基础上,介绍了通过掺杂金属、金属离子、金属氧化物等方法制备二氧化锡膜气敏传感器的研究成果以及二氧化锡传感器阵列电鼻子的研究现状,并对其发展趋势进行了展望。
一、引言随着纳米技术的发展,与该项技术相结合的气敏传感器的研究已经成为热门课题。
这类传感器以其较好的灵敏度和选择性、良好的响应和恢复时间以及较长的使用寿命,而被广泛应用于各种有毒有害气体、可燃气体、工业废气、环境污染气体的检测。
1931年,研究人员发现金属氧化物 Cu2O的电导率随H2O蒸汽的吸附而改变,从此拉开了材料气敏特性研究的序幕,并将这种特性与传感器技术相结合而制成气敏传感器。
气敏传感器的敏感材料主要是导电聚合物、金属氧化物和复合氧化物。
导电聚合物包括聚吡咯、聚噻吩、聚吲哚、聚呋喃等;金属氧化物则包括SnO2、ZnO、WO3、Fe2O3、 TiO2、CeO2、Nb2O5、Al2O3、In2O3、LnMO3(Ln=La、Gd ,M=Cr、Mn、Fe、Co)等,其中又以SnO2、 ZnO、Fe2O3 三大体系为主;复合氧化物主要为MxSnO3(M=Cr、Mn、Fe、Co)。
目前普遍采用的方法是以二氧化锡(SnO2)为基材,通过掺杂等方法制备出气敏传感器,用以检测某种气体的成分和浓度。
二、二氧化锡气敏机理的理论模型SnO2 属于N型半导体,含有氧空位或锡间隙离子,气敏效应明显。
关于其气敏机理的理论模型有多种[1],一般认为其气敏机理是表面吸附控制型机制[2],即在洁净的空气(氧化性气氛)中加热到一定的温度时对氧进行表面吸附,在材料的晶界处形成势垒,该势垒能束缚电子在电场作用下的漂移运动,使之不易穿过势垒,从而引起材料电导降低;而在还原性被测气氛中吸附被测气体并与吸附氧交换位置或发生反应,使晶界处的吸附氧脱附,致使表面势垒降低,从而引起材料电导的增加,通过材料电导的变化来检测气体。
纳米二氧化钛太阳能电池的制备及其性能测试实验报告

纳米二氧化钛太阳能电池的制备及其性能测试一、前言1.1实验目的(1)了解纳米二氧化钛染料敏化太阳能电池的组成、工作原理及性能特点。
(2)掌握合成纳米二氧化钛溶胶、组装成电池的方法与原理。
(3)学会评价电池性能的方法。
1.2实验意义随着世界各国的工业发展,煤、石油等传统能源的使用量急剧增长,寻找干净的新能源成为当务之急。
太阳能是唯一种永不枯竭的清洁能源,受到众多研究者的青睐。
目前市场上的太阳能电池种类较多,其中硅半导体太阳能电池占了绝对的优势,另外还有无机半导体太阳能电池、p-n结型太阳能电池等。
1991年Gratzel等制备了TiO2太阳能电池,把多吡啶钌配合物吸附在多孔膜上,制作成染料敏化纳米晶TiO2太阳能电池,简称DSSC。
该太阳能电池的光电转换效率大于10%,且具有永久性、清洁性和灵活性三大优点。
只要有太阳光,DSSC就可以一次投资而长期使用。
1.3文献综述与总结1991年瑞士学者Grätzel等在Nature上发表文章,提出了一种新型的以染料敏化二氧化钛纳米薄膜为光阳极的光伏电池,现称为Grätzel型电池。
这种电池的出现为光电化学电池的发展带来了革命性的创新。
目前,此种电池的效率已稳定在10%左右,成本比硅太阳能电池大为降低,且性能稳定。
纳米TiO2的粒径和膜的微结构对光电性能的影响很大,纳米TiO2的粒径小,比表面积越大,吸附能力越强,吸附染料分子越多,光生电流也就越强,所以人们采用不同方法使之纳米化、多孔化、薄膜化。
只有紧密吸附在半导体表面的单层染料分子才能产生有效的敏化效率。
[1](1)半导体电极的制备目前,合成纳米TiO2的方法有溶胶凝胶法、水热反应法、溅射法、醇盐水解法、溅射沉积法、等离子喷涂法和丝网印刷法等。
应用在DSSC中的TiO2多孔薄膜常用制备方法有胶体涂膜直接低温烧结法、水热法烧结、热液法烧结、微波烧结、紫外-化学气相沉积法等。
[1]溶胶凝胶法是用水解钛酸正丁酷(或无机钛盐,如TiCl4)制得TiO2胶体溶液,后经由浸渍、提拉、丝网印刷、旋涂等方法在导电基底上生长纳米高温锻烧制备出纳米TiO2电极,向溶胶中加入聚合物则有助于TiO2纳米晶粒径的大小的控制。
MnZn铁氧体材料的制备
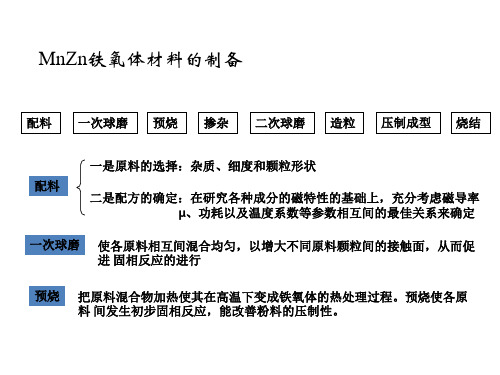
对低功耗铁氧体磁性材料系列检测所取得的大量数据,必需进行有效的 采集和分类,为此,根据材料的物理特性、实验规律、实验数据和相关结 果,建立了反映数千个样品的成分—制备工艺—物理性能之间关系的数据 库
低功耗MnZn铁氧体材料的组合合成和高通量 筛选
二次制备和筛选材料
对初选材料的成分、制备工艺、材料结构、物理和化学性能进行分析、研 究,进一步缩小材料库的可能范围,对成分—工艺—结构加以优化。第一 轮筛选实施后,找出频率在100-500kHz范围内、性能符合要求的初选材料 系列。在此基础上,实施第二轮筛选。 规模化试制
掺杂3与掺杂2相比较
Co2+和Cr3+离子进入晶格后,都将优先进入B位, 由于Co2+离子半径比Cr3+离子小,掺杂3中Co2+离 子的添加将使A-O-B离子间健角较掺杂2大,从而 增加了A-B间交换作用,导致其居里温度相对较高。
(1) 0.04 wt%CaCO3+0.03 wt%Nb2O5+0.03 wt%Ta2O5+0.02 wt%Cr2O3+0.15 wt%SnO2; (2) 0.04 wt%CaCO3+0.03 wt%Nb2O5+0.03 wt%Ta2O5+0.02 wt%Cr2O3+0.1 wt%SnO2; (3) 0.04 wt%CaCO3+0.03 wt%Nb2O5 +0.03 wt%Ta2O5+0.02 wt%CoO+0.1 wt%SnO2;
技术优势
1、可以极大地加速新材料的开发 2、能够大大减少材料研制中的浪费 3、可以显著增加材料研制过程中意外发现的机会
4、特别适用于三元或三元以上的无机材料的研制
几种常见碳包覆策略案例

柠檬酸包覆法:案例简介
制备流程 由C@SnS@C纳米片构建的3D多孔微球:在磁力搅拌下,将226mg SnCl2·2H2O(1mmol),228mg CH4N2S (3mmol)和226mg 柠檬酸溶解在30mL丙三醇溶液中。将所得溶液转移到Teflon衬里的不锈钢高压釜(40mL 容量)中,然后在190℃下进行水热处理18小时。过滤收集产物,依次用去离子水和无水乙醇洗涤数次,并在 60℃下干燥24小时。 SnO2@ATC复合物:将30mg葡萄糖溶解在30mL去离子水中,并在剧烈磁力搅拌下将30mg由C@SnS@C夹层纳 米片构成的3D多孔微球加入到溶液中。将所得悬浮液密封在40mL聚四氟乙烯衬里的高压釜中,然后在180℃下 水热处理12小时后,过滤收集产物,用去离子水和无水乙醇连续洗涤数次,并在60℃下干燥24小时。
ChemicalEngineeringJournal240(2014)379–386383
单宁酸包覆法
一、物性介绍 单宁酸又叫鞣酸,丹宁酸,是一种黄色或淡棕色轻质无晶性粉末或鳞片,有特异微臭,味极涩。是一种植物
多酚,在工业上,鞣酸被大量应用于鞣革与制造蓝墨水。它来源广泛,可以从诸如茶叶,橡树和漆树等植物中提 取,因此成本也较低。与聚多巴胺包覆类似,在中性的缓冲溶液下,它几乎能立即包覆在任何材料的表面。可为 收敛剂,能沉淀蛋白质,与生物碱、甙及重金属等均能形成不溶性复合物。溶于水及乙醇,易溶于甘油,极不溶 于乙醚、氯仿或苯,在空气中颜色逐渐变深,有强吸湿性;。其水溶液与铁盐溶液相遇变蓝黑色,加亚硫酸钠可延 缓变色。在210~215℃时熔融分解为焦性没食子酸和二氧化碳。 二、优劣对比 优势:对于不同的材料,单宁酸包覆的厚度不一样。 劣势:单宁酸包覆的特点是它包覆的环境是在中性条件下且几乎能 包覆在任何材料表面。它包覆的厚度可以精确的控制,从几纳米到 几十纳米不等,且可以通过layer-by-layer方式进行累计包覆。
纳米氧化铁的制备和表征

纳米氧化铁的制备和表征北京师范大学化学学院小灰(081015xxxx)指导教师司书峰摘要:通过控制pH值,缓慢水解FeCl3合成纳米Fe2O3,对其物相进行XRD和TEM表征,并作气敏性质的测试。
XRD和TEM显示制得的粒子为椭球形α-Fe2O3,粒径约为28nm,且分散性好。
粒子对乙醇、丙酮和90#汽油都有响应,且随气体浓度增加,气敏阻值线性降低。
关键词:纳米Fe2O3;XRD;SEM;气敏性质Preparation and characterization of Iron Oxide NanoparticlesAbstract:Iron oxide nanoparticles were prepared by a solution phase controlled hydrolysis method, and were characterized by XRD and SEM techniques. Its gas-sensitivity was also tested later.XRD and SEM results show that ellipsoidal alpha iron oxide particles with an average particle size of about 28nm were obtained through our method. And these particles show sensitivity to acetone, ethanol and gasoline with a linear dependence on the gas concentration.Key words:Fe2O3Nanoparticles; XRD; SEM; Gas-sensitivity1.介绍氧化铁系列化合物,按其价态、晶型和结构之不同可分为(α,β,γ)-Fe2O3、(α,β,γ,δ)- FeOOH、Fe3O4、FeO[1]。
热处理气氛对α-Fe_(2)O_(3)光阳极光电化学性能影响研究

第33卷第1期2021年1月化学研究与应用Chemical Research and ApplicationVol.33,No.1Jan.,2021文章编号:1004-1656(2021)01-0090-07热处理气氛对a-Fe203光阳极光电化学性能影响研究李龙珠*,吴浩宇,陈玉伟,杨蓉,唐惠东(常州工程职业技术学院化工与制药工程学院,江苏常州213164)摘要:分别在空气和氮气中对水热制备的薄膜进行热处理获得了纳米棒状a-Fe2()3光阳极。
对样品分别进行T X射线衍射(XRD)、扫描电镜(SEM)、X射线光电子能谱(XPS)、紫外-可见吸收光谱和光电化学性能测试。
与空气热处理获得的a-Fe2O3Air光阳极相比,氮气气氛热处理获得的a-Fe2O3N2光阳极正面光照电流密度显著提升达到0.42mA-cm'%正面光照下,a-Fe2O3N2光阳极的体内电荷分离效率弘强和表面电荷注入效率Nwfaee都有较大增加,说明%热处理明显增加了«-Fe203膜的载流子浓度,增强了体内载流子的传输和表面载流子注入效率。
关键词:光电化学电池;水分解;a-Fe203;水热法中图分类号:TK91文献标志码:AEffects of annealing atmosphere on the photoelectrochemicalperformance of a-Fe2O3photoanodesLI Long-zhu*,WU Hao-yu,CHEN Yu-wei,YANG Rong,TANG Hui-dong(School of Chemical and Pharmaceutical Engineering,Changzhou Vocational Institute of Engineering,Changzhou213164,China)Abstract:The hydrothermal prepared films were converted into nanorods-like a-Fe203photoanodes by annealing treatment in air and nitrogen,respectively・The samples were characterized by X-ray diffraction(XRD),scanning electron microscopy(SEM) ,X-ray photoelectron spectroscopy(XPS),UV-vis absorption spectroscopy and photoelectrochemical properties.Under front illumination,the photocurrent density of the a-Fe2O3photoanode annealed in nitrogen atmosphere increased significantly to0.42mA•cm'2compared with that of hematite photoanode annealed in air.The a-Fe203photoanode annealed in nitrogen atmosphere had gready increased ^buik i7surface under front illumination,which indicated that nitrogen heat treatment significantly increased the carrier concentration of the hematite film and enhanced the carrier transport in the bulk and surface carrier injection efficiency.Key words:photoelectrochemical;water splitting;a-Fe203;hydrothermal method收稿日期=2020-06-09;修回日期:2020-10-12基金项目:江苏省高等学校自然科学研究面上项目(19KJB510001)资助;江苏省青蓝工程项目资助;国家自然科学基金项目(51874050)资助联系人简介:李龙珠(1981-),女,副教授,主要从事新能源材料制备研究。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
核-壳结构Fe2O3@SnO2负极材料的制备及性能韦悦;陈丽辉;丁瑜;付争兵【摘要】用低熔点盐LiCl和LiNO3作为反应介质,以FeCl3和SnCl2为反应原料,通过低温熔盐法制备Fe2O3@SnO2颗粒.对材料进行XRD、SEM和透射电子显微镜(TEM)分析,以及恒流充放电、循环伏安和交流阻抗等测试.制备的Fe2O3@SnO2复合材料为球形核-壳结构,电化学性能好于纯Fe2O3和SnO2.SnO2包覆量为α-Fe2O3的4%时,Fe2O3/SnO2复合材料的充放电性能最好,以0. 1 A/g的电流在0. 8~2. 5 V循环100次,比容量仍有1 000. 7 mAh/g.【期刊名称】《电池》【年(卷),期】2018(048)005【总页数】4页(P322-325)【关键词】锂离子电池;熔盐法;核-壳结构;电化学性能;Fe2O3@SnO2材料【作者】韦悦;陈丽辉;丁瑜;付争兵【作者单位】湖北工程学院化学与材料科学学院,湖北孝感 432000;湖北工程学院化学与材料科学学院,湖北孝感 432000;湖北工程学院化学与材料科学学院,湖北孝感 432000;湖北工程学院化学与材料科学学院,湖北孝感 432000【正文语种】中文【中图分类】TM912.9负极材料是决定锂离子电池工作性能和价格的重要因素。
目前,商业化的负极材料主要是石墨类碳材料,但理论容量低(仅372 mAh/g)、安全性能有欠缺(大电流充放电时容易析锂)[1]。
二氧化锡(SnO2)和三氧化二铁(Fe2O3)具有资源丰富、对环境友好和比容量较高(分别为780 mAh/g和1 005 mAh/g)等优点,受到人们的广泛关注,有望用作锂离子电池负极材料[2-3]。
SnO2和Fe2O3单独作为电极材料时,有明显的不足,如SnO2在充放电时的体积膨胀超过300%,易粉化、团聚,形成的固体电解质界面(SEI)膜不稳定,导致容量快速衰减[2];Fe2O3的循环稳定性和导电性差等[3]。
本文作者拟结合SnO2和Fe2O3两者的优点,采用简单的熔盐法制备核-壳结构Fe2O3@SnO2纳米复合电极材料,重点考察Fe2O3@SnO2复合电极材料的电化学性能。
1 实验1.1 材料的制备将8.457 4 g LiCl(国药集团,AR)和4.137 0 g LiNO3(国药集团,AR)溶于30 ml 无水乙醇(国药集团,AR)中,再加入1.622 g FeCl3(国药集团,AR),充分搅拌后,将得到的溶液先在鼓风干燥箱中、60 ℃下干燥9 h,再在80 ℃下干燥至溶剂完全挥发。
将得到的固体在马弗炉中、300 ℃下热处理3 h(升温速度为2 ℃/min),冷却至室温后,将得到的粉体产物水洗,再在鼓风干燥箱中、105 ℃下干燥12 h。
将干燥后的粉末再溶于LiCl和LiNO3的无水乙醇溶液中,加入SnCl2(国药集团,AR),重复上述干燥和热处理步骤,得到Fe2O3@SnO2复合材料。
SnCl2的添加量为0.04 g、0.08 g和0.16 g的材料,分别记为Fe2O3@SnO2-1、Fe2O3@SnO2-2和Fe2O3@SnO2-3。
在同样实验条件下,向LiCl和LiNO3的无水乙醇溶液中分别只添加SnCl2和FeCl3,制备纯SnO2和Fe2O3。
1.2 电池的制备及电池组装分别将制备的电极材料、导电炭黑(上海产,AR)和聚偏氟乙烯(绍兴产,AR)按质量比8∶1∶1混合,添加适量的十二甲基吡咯烷酮(国药集团,AR)调成糊状,涂覆到10 μm厚的铜箔(深圳产,≥99.9%,)上。
将涂覆好的铜箔在80 ℃下真空(-0.1 MPa)干燥24 h,再在MRX-SG100W型对辊机(深圳产)上辊压至0.09 mm 厚,最后冲切成面积为1.13 cm2的圆片(活性物质质量为0.700~0.800 mg)。
以金属锂片(上海产,电池级)为电极,Celgard 2400膜(美国产)为隔膜,1 mol/L LiPF6/EC+DEC+EMC(体积比1∶1∶1,上海产,电池级)为电解液,在氩气保护的手套箱中组装CR2016型扣式电池。
1.3 性能测试用D8 ADVANCE 型X射线分析仪(德国产)测试材料的晶型,CuKα,波长为0.154 18 nm,管压40 kV、管流40 mA,扫描速度为10 (°)/min,步长为0.08 °。
用CJSM-6510F扫描电子显微镜(日本产)测试材料的形貌;用JEM-2100HR透射电子显微镜(TEM,日本产)测试材料的微观结构。
用T2001A型电池测试系统(武汉产)对电池进行充放电性能测试,电流分别为0.1 A/g、0.2 A/g、0.5 A/g、1.0 A/g和2.0 A/g,电压为0.8~2.5 V。
用CHI660E 电化学工作站(上海产)对电池进行循环伏安(CV)和交流阻抗谱测试。
CV测试的电压为0.01~3.00 V,扫描速率为0.1 mV/s;交流阻抗谱测试的频率为10-2~105 Hz,交流振幅是5 mV。
2 结果与讨论2.1 材料的XRD分析对制备的电极材料进行XRD测试,结果如图1。
图1中,Fe2O3、Fe2O3@SnO2-1、Fe2O3@SnO2-2以及Fe2O3@SnO2-3等4种材料均在33.82 °、35.40 °、49.01 °、54.80 °、58.24 °和65.99 °处出现尖锐的衍射峰。
与Fe2O3的标准卡(33-0664)对比,发现与体心立方结构Fe2O3的(111)、(311)、(400)、(333)、(331)和(440)晶面的衍射峰位置一致,表明所制备材料主体是α-Fe2O3,且结晶性较好、结晶度高。
对比制备的纯SnO2的衍射峰,Fe2O3@SnO2-1、Fe2O3@SnO2-2和Fe2O3@SnO2-3中没有出现SnO2的特征衍射峰。
一方面可能是混合物中SnO2的含量低;另一方面可能是偏聚于Fe2O3表面的SnO2受到Fe2O3的晶界势垒的影响,阻碍了SnO2晶粒的长大,使SnO2结晶不充分,即电极材料中的SnO2以非晶态存在。
SnO2包覆Fe2O3后,未改变Fe2O3的衍射峰位,说明没有改变Fe2O3的晶型结构,即包覆的SnO2未掺杂到α-Fe2O3晶格内部。
图1 制备材料的XRD图Fig.1 XRD patterns of prepared materials2.2 材料的SEM分析实验过程中,LiCl和LiNO3作为反应介质,在所用醇溶液中的溶解度较大,在一定程度上加快了离子在溶液中的扩散速率,使反应物在液相中实现原子尺度的混合,有利于形成微纳颗粒;Cl-和作为氧化剂,促进了Fe2O3和SnO2的形成。
在降温过程中,Fe2O3的表面被LiCl和LiNO3包裹,水洗后,LiCl和LiNO3溶解脱落,在Fe2O3表面形成凹坑,SnO2在凹坑处生长,形成包覆层即壳层。
这可从SEM图(图2)得到证实。
比较而言,图2(b)中颗粒分布较稀疏,SnO2颗粒周围的空隙有利于Fe2O3的分布,并缓解Fe2O3的团聚。
从制备的过程来看,SnO2包覆在Fe2O3的表面,改变了相邻界面的静电能和畸变能,宏观上SnO2起着钉扎Fe2O3晶界的作用,导致迁移困难,阻止了Fe2O3颗粒的进一步生长和团聚,并限制Fe2O3体积膨胀,可保持材料结构的稳定。
SnO2用SnO2包覆Fe2O3,可提高电极的电导率、减轻电极的极化,保持结构稳定,并尽量使Fe2O3不受周围环境的影响。
图2 制备材料的SEM图Fig.2 SEM photographs of prepared materials2.3 材料的TEM分析选取Fe2O3@SnO2-2样品进行TEM测试,结果见图3。
图3 Fe2O3@SnO2-2的TEM图Fig.3 Transmission electron microscope(TEM) photographs ofFe2O3@SnO2-2的禁带宽度较窄,电子容易跃迁,从图3(a)可知,样品呈球形,球的直径约为500 nm,外层有约15 nm厚的包覆层。
从图3(b)可知,在样品内部和边缘分别出现晶面间距为0.27 nm和0.34 nm的两组晶格条纹,依次对应于Fe2O3的(104)晶面和SnO2的(110)晶面。
这不但验证了XRD测试的结果,也证实了样品的核-壳结构。
这种球形核-壳结构有利于表面活性位点的分散,有利于增加与电解液的接触面积,球体堆积产生的孔道有利于Li+的扩散和迁移,使Li+在充放电过程中的嵌脱更容易。
2.4 材料的电化学性能测试对Fe2O3@SnO2、Fe2O3和SnO2电极材料在0.1 A/g电流下进行循环性能测试,结果见图4。
图4 制备材料在0.1 A/g时的循环性能Fig.4 Cycle performance of prepared materials at 0.1 A/g从图4可知,Fe2O3@SnO2-1、Fe2O3@SnO2-2、Fe2O3@SnO2-3、Fe2O3和SnO2在电流为0.1 A/g时的首次放电比容量分别为1 198.2 mAh/g、1 188.7 mAh/g、1 171.8 mAh/g、961.7 mAh/g和660.2 mAh/g。
Fe2O3@SnO2复合电极材料的首次放电比容量高于纯的Fe2O3和SnO2电极材料,说明在Fe2O3中掺入适量的SnO2,可提高充放电性能。
SnO2为n型半导体,导电性良好,与Fe2O3的晶体结构相似,原子间距和热膨胀系数相近,两者可形成n-n异质结,提高电子迁移率;材料的组成单元为纳米尺寸,具有较短的电子传输路径、Li+扩散距离,以及更大的电极/电解液接触面积;球形核-壳结构拥有低维和三维纳米结构,可提高嵌锂性能,球形结构间的空隙可缓冲Li+嵌脱导致的体积变化,为电子传输搭建高度连续的快速通道,并抑制纳米颗粒的团聚和溶解[4]。
随着充放电的进行,5种材料的比容量都是先降低、后增加。
比容量下降,一方面是因为SEI膜的形成,另一方面是因为Li+被束缚在Fe2O3和SnO2晶粒的内部。
随着充放电的深入,材料被活化,放电能力增强,比容量增大,且持续上升。
在第100次循环时,Fe2O3@SnO2-1、Fe2O3@SnO2-2、Fe2O3@SnO2-3、Fe2O3和SnO2的比容量分别为565.5 mAh/g、1 000.7 mAh/g、946.9mAh/g、596.8 mAh/g和175.7 mAh/g。
这种良好的循环性能,得益于材料独特的核-壳结构。
Fe2O3@SnO2-2复合材料(SnO2包覆量为4%)的比容量最高,循环稳定性好。
