高考一轮复习铝及其化合物的化学方程式和离子方程式
【快乐考生】2014届高考化学一轮复习 (理教材 析考点 悟规律) 第7讲 铝及其重要的化合物课件 新人教版

+
n[Ba(OH)2]=1:2,此时 n(Al3+):n(OH-)=1:4,故 B 正 确;D 选项,当 C 式恰好反应来自,再加 Ba(OH)2 溶液,
2 反 应 方 程 式 为 2Al(OH)3 + Ba2 + 2OH + SO 4
+ - -
===BaSO4↓+2AlO-+4H2O, 沉淀的物质的量将减少。 2
2 下列离子方程式表示:2Al3 +3SO4 +3Ba2 +6OH
+ - + -
===2Al(OH)3↓+3BaSO4↓ D.随加入的 Ba(OH)2 的物质的量不断增大,沉淀 的物质的量不断增大
[解析] 当 Al3 恰好反应时,离子方程式与 C 同,
2 故 A、C 正确。当 SO4 恰好反应时,n[KAl(SO4)2]:
[答案] C
+ +
盘点二
铝的重要化合物
1.氧化铝 (1)物理性质: 白 色固体, 难 溶于水,有很高的 熔点 。 (2)化学性质
2.氢氧化铝 (1)物理性质
白 色胶状不溶于水的固体,有较强的 吸附 性。
(2)化学性质(用化学方程式表示)
△ ②受热分解: 2Al(OH)3=====Al2O3+3H2O
[解析]
Al与Fe3O4配成的铝热剂恰好反应时有:
高温 8Al+3Fe3O4 ===== 4Al2O3+9Fe。第一份铝热反应的生 成物为Fe和Al2O3,只有Fe与HCl反应放出H2,由方程 式8Al~9Fe~9H2,即生成9mol H2;第二份Al和Fe3O4 直接与NaOH溶液反应,只有Al与之反应放出H2,由 电子得失守恒8Al~12H2,即生成12mol H2。故生成气 体在相同情况下的体积之比为9mol:12mol=3:4。此
《3年高考2年模拟》2022课标版高中化学一轮复习 第2讲 镁、铝及其化合物(1)

第2讲 镁、铝及其化合物考试要点核心素养1.掌握镁、铝及其化合物的主要性质及应用。
2.了解镁、铝及其化合物的制备方法。
1.宏观辨识与微观探析:认识镁、铝及其化合物的性质和应用,同时知道两性氧化物和两性氢氧化物的特征反应。
2.科学探究与创新意识:科学领悟镁、铝及其化合物的性质及探究方案。
3.科学精神与社会责任:利用铝土矿的开发利用理解可持续发展意识和绿色化学理念。
一、铝及其重要化合物的性质1.铝(1)原子结构与物理性质(2)化学性质2.氧化铝(1)物理性质:白色固体,难溶于水,有很高的熔点。
(2)化学性质3.氢氧化铝(1)物理性质:白色胶状不溶于水的固体。
(2)化学性质a.Al(OH)3的电离:H++AlO2-+H2O ⏟酸式电离Al(OH)3Al3++3OH-⏟碱式电离b.c.受热分解:2Al(OH)3Al2O3+3H2O(3)制备向铝盐中加入氨水,离子方程式为Al3++3NH3·H2O Al(OH)3↓+3N H4+。
NaAlO2溶液中通入足量CO2,离子方程式为Al O2-+CO2+2H2O Al(OH)3↓+HC O3-。
NaAlO2溶液与AlCl3溶液混合:3Al O2-+Al3++6H2O4Al(OH)3↓。
4.常见的铝盐——明矾明矾的化学式为KAl(SO4)2·12H2O ,它是无色晶体,可溶于水,水溶液的pH<7。
明矾可以净水,其净水的原理是Al3++3H2O Al(OH)3(胶体)+3H+,Al(OH)3胶体吸附水中杂质形成沉淀而净水。
二、镁及其化合物的性质和用途1.镁(1)物理性质:具有银白色金属光泽的固体。
(2)化学性质(写化学方程式)a.与O2反应:2Mg+O22MgO (产生耀眼白光)b.与N2反应:3Mg+N2Mg3N2c.与CO2反应:2Mg+CO22MgO+Cd.与沸水反应:Mg+2H2O Mg(OH)2+H2↑(3)用途:生产合金,冶金工业上用作还原剂和脱氧剂。
高考化学一轮复习:铝及其化合物知识点总结

高考化学一轮复习:铝及其化合物知识点总结(一)铝单质——Al(两性单质)1、物理性质:银白色金属,质较软,但比镁要硬,熔点比镁高,有良好的导电、导热性和延展性。
2、用途:铝有良好的导电、导热性和延展性,主要用于导线、炊具等,铝的最大用途是制合金。
3、铝合金特点:①密度小①强度高①塑性好①制造工艺简单①成本低①抗腐蚀力强4、化学性质:铝是较活泼的金属,自然界中没有铝单质(1)与非金属:4Al + 3O2 == 2Al2O3生成致密的氧化膜起保护作用。
(2)与酸的反应:2Al + 6HCl == 2AlCl3+ 3H2↑ 2Al + 6H+ == 2Al3+ + 3H2↑钝化:在常温下,铝与浓硝酸、浓硫酸反应,在表面生成致密的氧化膜,阻止进一步反应,保护铝。
(3)与碱的反应:2Al + 2NaOH + 6H2O == 2Na[Al(OH)4] + 3H2↑ 2Al + 2OH− + 6H2O == 2[Al(OH)4]− +3H2↑ (4)与某些盐溶液反应:如能置换出CuSO4、AgNO3等溶液中的金属。
(5)铝热反应:高温下铝与某些金属氧化物的反应(如Fe、Cr、Mn、V的氧化物)2Al + Fe2O3Al2O3 + 2Fe。
Al和Fe2O3的混合物叫做铝热剂(混合物)。
可用于焊接钢轨、冶炼金属。
(二)氧化铝——Al2O3(两性氧化物)白色固体,熔点高(2054①),常作为耐火材料和冶炼金属铝的原料。
两性氧化物:既能与强酸反应又能与强碱反应生成盐和水的氧化物。
1、与酸的反应:Al2O3 + 6HCl == 2AlCl3 + 3H2O Al2O3 + 6H+ == 2Al3+ + 3H2O2、与碱的反应:Al2O3 + 2NaOH + 3H2O == 2Na[Al(OH)4] Al2O3 + 2OH− + 3H2O == 2[Al(OH)4]−3、电解熔融的氧化铝制备金属铝:(三)氢氧化铝——Al(OH)3(两性氢氧化物)白色难溶于水的胶状沉淀,是两性氢氧化物,加热易分解。
高考化学一轮复习学案课件(人教版)第3章金属及其化合物第2节铝及其重要化合物

(2)用途:①氧化铝是冶炼铝的原料,化学方程式为______________________; ②氧化铝是较好的耐火材料,可用于制造__________、________和耐高温的________ 等。 2. 氢氧化铝 (1)两性氢氧化物:电离方程式为______________________。 ①与盐酸反应的离子方程式:______________________。 ②与氢氧化钠溶液反应的离子方程式: ________________________________________________________________________。 (2)受热分解:化学方程式为______________________。
常温下,铝发 生____,加热 时剧烈反应
3. 镁、铝的制备
工业制备均用电解法,化学方程式分别为__________________________、 __________________________。
答案:
一、1. 银白 金属 较软 较小 < < < 2. 2Mg+O2==2MgO 4Al+3O2==2Al2O3 Mg+Cl2==MgCl2 2Al+3Cl2==2AlCl3 Mg+S==MgS
(1)铝与盐酸反应时,铝过量而盐酸不足。 (2)铝与氢氧化钠反应时,铝不足而氢氧化钠过量。
1. 向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体 b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全, 得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则 下列关系不正确的是( )
铝分别与盐酸、氢氧化钠溶液反应的原理
2Al+6HCl===2AlCl3+3H2↑ 2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 1. 等量铝分别与足量盐酸和氢氧化钠溶液反应,产生氢气的体积比=1∶1 2. 足量的铝分别与等物质的量的盐酸和氢氧化钠反应,产生氢气的体积比为=1∶3 3. 一定量的铝分别和一定量的盐酸和氢氧化钠反应,若产生氢气的体积比为(1/3,1) 则必定是:
高三化学一轮复习【镁、铝及其化合物】

在空气中都能跟氧气反应,表面覆盖一层致密而坚硬的氧化物薄膜,都具有自我抗腐蚀能力铝合金汽车、船舶、飞机制造、防锈油漆、导线、电缆等易错点:(1)常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、浓硝酸不反应。
(2)铝不但能与酸(H +)反应,还能够与碱溶液反应,表现为特殊性。
2Al +2OH -+2H 2O===2AlO -2+3H 2↑。
其反应机理应为:铝先与强碱溶液中的水反应生成H 2和Al(OH)3,然后Al(OH)3再与NaOH 反应生成H 2O 和NaAlO 2,反应中铝作还原剂,水作氧化剂,NaOH 无电子得失。
(3)铝热反应是在高温干态下进行的置换反应,铝只能与排在金属活动性顺序其后的金属氧化物反应。
铝不能与MgO 反应,铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
(4)Mg 在CO 2中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。
同时镁与氮气反应生成Mg 3N 2。
二、铝的重要化合物1.氧化铝(1)物理性质 色态: ;硬度: ;熔点: 。
(2)化学性质①属于两性氧化物,写出有关反应的离子方程式:,②电解 化学方程式为 2Al 2O 3(熔融)=====电解4Al +3O 2↑。
(3)用途熔点很高,是一种较好的耐火材料,天然产刚玉的成分是Al 2O 3,还可制作各种宝石。
2.氢氧化铝 (1)物理性质Al(OH)3是一种难溶于水的白色胶状物质,具有较强的吸附能力。
(2)化学性质 ①两性Al(OH)3的电离方程式为Al(OH)3既能溶于强酸又能溶于强碱,且都生成盐和水。
与强酸反应: , 与强碱溶液反应: 。
②不稳定性Al(OH)3受热分解: 。
(3)制备①向铝盐中加入氨水,离子方程式为 。
②NaAlO 2溶液中通入足量CO 2,离子方程式为 。
③NaAlO 2溶液与AlCl 3溶液混合:离子方程式为 。
第四章玩转铝及其化合物(附带答案解析)-2023年高考化学一轮复习重难点突破讲义
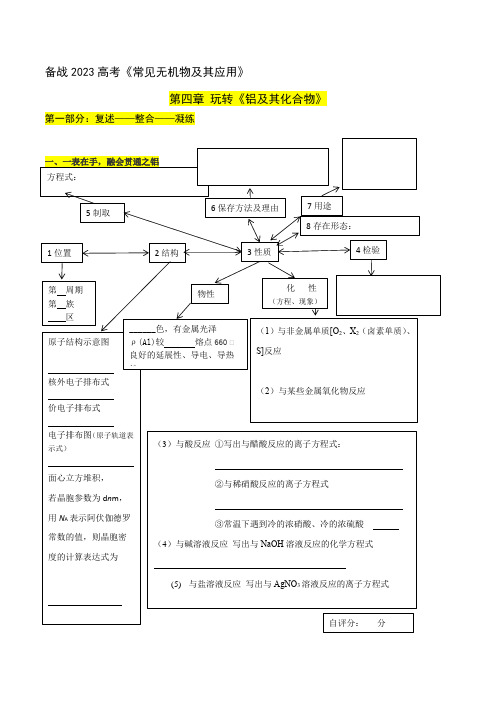
备战2023高考《常见无机物及其应用》第四章玩转《铝及其化合物》第一部分:复述——整合——凝练【核心补充1】【重要的实验】1、铝热反应①在下面方框中画出简易装置图并指出所用试剂的用途 ② 在下面方框中写出实验现象③铝热反应的用途:注:Al 和某些金属氧化物在高温下进行,反应迅速并放出大量的热,新生成的金属单质呈熔融态且易与Al 2O 3分离重要的实验】2、离子检验问题写出检验Al 3+写出检验AlO -2【核心补充2】【Al 的工业冶炼方法】从铝土矿(主要成分是Al 2O 3、含SiO 2、Fe 2O 3、MgO 等杂质)中冶炼铝的两种工艺:要求:1.补全主要微粒或添加的试剂的化学式 2.写出步骤1—5中含铝物质发生反应的离子方程式步骤1: 步骤2: 步骤3: 步骤4: 步骤5: 注:冶炼Al 时只能电解熔融Al 2O 3而不能电解熔融AlCl 3,原因是AlCl 3是共价化合物,熔融态不导电;加入冰晶石(Na 3AlF 6)的目的是降低Al 2O 3的熔化温度。
【核心补充3】【基本图像问题】1.可溶性铝盐溶液与NaOH溶液反应的图像:偏铝酸盐溶液与盐酸反应的图像:2.总结:Al3+、Al(OH)、AlO-2相互转化的比例关系二、一图在手融汇贯通之铝及其化合物连线。
用箭头表示出价类二维图中各物质之间可能存在的转化线,并标清楚反应条件。
+3 Al 2O 3 Al(OH)3 Al Cl 3NaAl O 20 Al单质氧化物氢氧化物盐三、Al 及其化合物易错点全掌控1、结合必要的化学用语解释明矾能净水的原因:2、注意反应的先后顺序当溶液中有多种离子H +、NH 4 +、Mg 2+、Al 3+存在时,向溶液中逐滴加入NaOH 溶液,与NaOH 反应的微粒的先后顺序是: 。
3、离子共存问题 画图连线,标记出微粒间不能大量共存的原因4、从分类观角度总结 既能与酸反应,又能与碱反应的物质 (1)无机物:①金属 如:Al 等 ②两性氧化物 如:Al 2O 3等 ③两性氢氧化物 如:Al(OH)3等④多元弱酸的酸式盐 如:NaHCO 3、KHS 、KHSO 3等⑤弱碱弱酸盐 如:CH 3COONH 4、(NH 4)2CO 3等。
2014高考化学一轮复习课件3-2铝及其化合物
基 础 知 识 梳 理
感 悟 考 点 透 析
实 验 典 例 探 究 高 考 真 题 重 组 课 时 规 范 训 练
基 础 知 识 梳 理
感 悟 考 点 透 析
实 验 典 例 探 究 高 考 真 题 重 组 课 时 规 范 训 练
基 础 知 识 梳 理
考点一
“铝三角”的转化关系及应用
基 础 知 识 梳 理
感 悟 考 点 透 析
实 验 典 例 探 究 高 考 真 题 重 组 课 时 规 范 训 练
制备方法
主要用途
2.常见铝盐——明矾
12H (1)明矾的化学式为: KAl(SO4)2· 2O ,它是白色晶体,易溶于
基 础 知 识 梳 理
水,水溶液 pH<7 (填“<”、“>”或“=”)。明矾可以净水,其 净水的原因是: Al3+水解生成的Al(OH)3胶体 水中的悬浮物使之沉淀下来。 (2)向明矾溶液中逐滴加入 Ba(OH)2 溶液, ①当 n[KAl(SO4)2]∶n[Ba(OH)2]=2∶3 时,铝元素的存在形式 是 Al(OH)3 ;②当 n[KAl(SO4)2]∶n[Ba(OH)2]=1∶2 时,铝元素的存 在形式是 AlO 2 。,
感 悟 考 点 透 析
实 验 典 例 探 究 高 考 真 题 重 组 课 时 规 范 训 练
化 学 性
质 (NaOH) 2NaOH===2NaAlO2 反应 +H2O
化学 性质
加热
△ 2Al(OH)3=====Al2O3+ 3H2O Al(OH)3 加热分解 ①作 耐火 材料 ②冶炼铝的原料 ①Al3+与氨水反应 ②AlO-溶液中通 CO2 2 ①制药 ② 净水 作用
基 础 知 识 梳 理
2014高考化学一轮复习高频考点通关练:3.2铝及其化合物
[练习点点清]
3.用含有少量Mg的Al片制取纯净的Al(OH)3,下列操作中 最恰当的组合是 ①加盐酸溶解 ②加NaOH溶液 ③过滤 ( ) ④通入过量
CO2生成Al(OH)3 ⑤加盐酸生成Al(OH)3 ⑥加过量氨
水生成Al(OH)3
A.①⑥③ C.②③④③ B.①③⑥③ D.②③⑤③
解析: 2Al+2OH - +2H2O===2AlO - +3H2↑,Mg 和 2 NaOH 溶液不反应,过滤后向 NaAlO2 溶液中通入过量 CO2 生成 Al(OH)3 沉淀,再过滤就可得到 Al(OH)3。
解析:(1)步骤①中加入盐酸,Al2O3、Fe2O3均与盐酸反 应,而SiO2与盐酸不反应。
(2)步骤①所得的滤液为AlCl3和FeCl3溶液,加入过量
NaOH溶液,使AlCl3转化为NaAlO2,而Fe3+转化为 Fe(OH)3;若加入氨水,则使AlCl3也转化为Al(OH)3沉淀,
而达不到分离Al3+和Fe3+的目的。
量 ) + 2H2O===Al(OH)3↓ + HCO
-
3
, ③Al3
+
+ 3AlO
-
2
+
6H2O===4Al(OH)3↓。 4.掌握6个化学方程式: + + ①2Al + 6H ===2Al3 + 3H2↑ , - 2H2O===2AlO2 +3H2↑, + + ③Al2O3 + 6H ===2Al3 + 3H2O, - ===2AlO2 +H2O, - - ⑤Al(OH)3 + OH ===AlO 2 + 2H2O, + ===Al3 +3H2O。
A.NH+、Ba2+、HCO-、Cl- B.K+、Al3+、S2-、ClO- 4 3 C.Na+、Fe3+、Cl-、SO2- 4 D.NH+、Mg2+、SO2-、NO- 4 4 3
铝的相关化学方程式
铝的相关化学方程式文件排版存档编号:[UYTR-OUPT28-KBNTL98-UYNN208]铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:4Al +3O 22Al 2O 32、铝在氯气中燃烧:2Al +3Cl 22AlCl 33、铝和硫共热:2Al +3S Al 2S 34、铝与稀硫酸反应:2Al +3H 2SO 4Al 2(SO 4)3 +3H 2 ↑ 2Al +6H +2Al 3++3H 2 ↑5、铝和氢氧化钠溶液反应:2Al +2NaOH +2H 2O 2NaAlO 2+3H 2 ↑2Al +2OH -+2H 2O 2AlO 2-+3H 2 ↑ 6、铝和浓硫酸共热:2Al +6H 2SO 4Al 2(SO 4)3 +3SO 2 ↑+6H 2O 7、铝和浓硝酸共热:Al +6HNO 3Al(NO 3)3 +3NO 2 ↑+3H 2OAl +6H ++3NO 3-Al 3++3NO 2 ↑+3H 2O 8、铝和稀硝酸反应:Al +4HNO 3Al(NO 3)3 +NO ↑+2H 2O Al +4H ++NO 3-Al 3++NO ↑+2H 2O 8、铝和硝酸银溶液反应:Al +3AgNO 3Al(NO 3)3 +3Ag Al +3Ag +Al 3++3Ag9、铝与硫酸铜溶液反应:2Al +3CuSO 4Al 2(SO 4)3 +3Cu 2Al +3Cu 2+2Al 3++3Cu 10、铝和氧化铁高温下反应:2Al +Fe 2O 3Al 2O 3+2Fe11、铝和四氧化三铁高温共热:8Al +3Fe 3O 44Al 2O 3+9Fe12、铝和氧化铜高温共热:2Al +3CuOAl 2O 3+3Cu13、铝和二氧化锰高温共热:4Al +3MnO 22Al 2O 3+3Mn 二、氧化铝1、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO 4Al 2(SO 4)3 +3H 2O Al 2O 3+6H +2Al 3++3H 2O2、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH 2NaAlO 2+H 2OAl 2O 3+2OH -2AlO 2-+H 2O3、电解氧化铝的熔融液:2Al 2O 34Al +3O 2 ↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4Al 2(SO 4)3 +6H 2OAl(OH)3 +3H +Al 3++3H 2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOH NaAlO 2+2H 2O Al(OH)3 +OH -AlO 2-+2H 2O冰晶电解3、加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O 四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:Al 2(SO 4)3 +3BaCl 22AlCl 3+3BaSO 4 ↓SO 42-+Ba 2+BaSO 4 ↓2、硫酸铝的水溶液呈酸性:Al 2(SO 4)3+6H 2O 2Al(OH)3 +3H 2SO 4 Al 3++3H 2O Al(OH)3 +3H +3、硫酸铝溶液中加入少量的氢氧化钠溶液:Al 2(SO 4)3 +6NaOH 3Na 2SO 4+2Al(OH)3 ↓ Al 3++3OH -Al(OH)3 ↓4、向硫酸铝溶液中加足量的氢氧化钠溶液: Al 2(SO 4)3 +8NaOH 2NaAlO 2+3Na 2SO 4+4H 2O Al 3++4OH -AlO 2-+2H 2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液: Al 2(SO 4)3 +3Ba(OH)2 2Al(OH)3 ↓+3BaSO 4 ↓ 2Al 3++3SO 42-+3Ba 2++6OH -2Al(OH)3 ↓+3BaSO 4 ↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液: Al 2(SO 4)3 +4Ba(OH)2 Ba(AlO 2)2 +3BaSO 4 ↓+4H 2O 2Al 3++3SO 42-+3Ba 2++8OH -2AlO 2-+3BaSO 4 ↓+4H 2O7、向明矾溶液中加入少量的氢氧化钡溶液: 3Ba(OH)2 +2KAl(SO 4)2 2Al(OH)3 ↓+3BaSO 4 ↓+K 2SO 4 3Ba 2++6OH -+2Al 3++3SO 42-3BaSO 4 ↓+2Al(OH)3 ↓8、向明矾溶液中加入足量的氢氧化钡溶液: KAl(SO 4)2 +2Ba(OH)2 KAlO 2+2BaSO 4 ↓+2H 2O Al 3++2SO 42-+2Ba 2++4OH -AlO 2-+2BaSO 4 ↓+2H 2O9、向硫酸铝溶液中加入氨水:Al 2(SO 4)3 +6NH 3·H 2O 2Al(OH)3 ↓+3(NH 4)2SO 4 Al 3++3NH 3·H 2O Al(OH)3 ↓+3NH 4+ 10、向硫酸铝溶液中加入碳酸钠溶液: Al 2(SO 4)3 +3Na 2CO 3+3H 2O 2Al(OH)3 ↓+3Na 2SO 4+3CO 2 ↑ 2Al 3++3CO 32-+3H 2O 2Al(OH)3 ↓+3CO 2 ↑ 11、向硫酸铝溶液中加入碳酸氢钠溶液: Al 2(SO 4)3 +6NaHCO 32Al(OH)3 ↓+3Na 2SO 4+6CO 2 ↑ Al 3++3HCO 3-Al(OH)3 ↓+3CO 2 ↑ 12、向硫酸铝溶液中加入硫化钠溶液: Al 2(SO 4)3 +3Na 2S +6H 2O 2Al(OH)3 ↓+3Na 2SO 4+3H 2S ↑ 2Al 3++3S 2-+6H 2O 2Al(OH)3 ↓+3H 2S ↑ 13、向硫酸铝溶液中加入硫氢化钠溶液: Al 2(SO 4)3 +6NaHS +6H 2O 2Al(OH)3 ↓+3Na 2SO 4+6H 2S ↑ Al 3++3HS -+3H 2O Al(OH)3 ↓+3H 2S ↑ 14、向硫酸铝溶液中加入硅酸钠溶液: Al 2(SO 4)3 +3Na 2SiO 3+6H 2O 2Al(OH)3 ↓+3Na 2SO 4+3H 2SiO 3 ↓ 2Al 3++3SiO 32-+6H 2O 2Al(OH)3 ↓+3H 2SiO 3 ↓15、向硫酸铝溶液中加入偏铝酸钠溶液: Al 2(SO 4)3 +6NaAlO 2+12H 2O 3Na 2SO 4+8Al(OH)3 ↓ Al 3++AlO 2-+6H 2O 4Al(OH)3 ↓ 五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO 2+2H 2O AI(OH)3 +NaOH AlO 2-+2H 2O Al(OH)3 +OH -2、偏铝酸钠溶液滴入少量盐酸:NaAlO 2+HCl +H 2O Al(OH)3 ↓+NaCl AlO 2-+H ++H 2O Al(OH)3 ↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO 2+4HCl NaCl +AlCl 3+2H 2O AlO 2-+4H +Al 3++2H 2O4、向偏铝酸钠溶液通入少量二氧化碳气体: 2NaAlO 2+CO 2+3H 2O 2Al(OH)3 ↓+Na 2CO 3 2AlO 2-+CO 2+3H 2O 2Al(OH)3 ↓+CO 32-5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO 2+CO 2+2H 2O Al(OH)3 +NaHCO 3AlO 2-+CO 2+2H 2O Al(OH)3 +HCO 3-6、向偏铝酸钠溶液中加入硫酸铝溶液: Al 2(SO 4)3 +6NaAlO 2+12H 2O 3Na 2SO 4+8Al(OH)3 ↓ Al 3++AlO 2-+6H 2O 4Al(OH)3 ↓7、向偏铝酸钠溶液中加入氯化铵溶液: NaAlO 2+NH 4Cl +H 2O Al(OH)3 ↓+NaCl +NH 3 ↑ AlO 2-+NH 4++H 2O Al(OH)3 ↓+NH 3 ↑ 8、向偏铝酸钠溶液中加入氯化铁溶液: 3NaAlO 2+FeCl 3+6H 2O 3Al(OH)3 ↓+Fe(OH)3 ↓+3NaCl 3AlO 2-+Fe 3++6H 2O 3Al(OH)3 ↓+Fe(OH)3 ↓。
高考化学总复习讲义:3.2铝及其化合物
第二节 铝及其化合物[考纲定位] 1.了解铝的主要性质及应用。
2.了解铝的重要化合物的主要性质及应用。
知识点一 铝的主要性质及其应用1.铝的结构和存在铝位于元素周期表第三周期ⅢA 族,原子结构示意图为○+13 2 8 3 。
铝元素在地壳中含量丰富,仅次于硅。
自然界中的铝全部以化合态存在。
2.金属铝的物理性质银白色有金属光泽的固体,有良好的延展性、导电性和传热性等,密度较小,质地柔软。
3.铝的化学性质写出图中有关反应的化学方程式或离子方程式:+④2Al +2OH -+2H 2O===2AlO -2+3H 2↑ ⑤2Al +Fe 2O 3=====高温2Fe +Al 2O 3(用于冶炼Fe) 【小提醒】铝与氢氧化钠溶液反应的实质铝先与强碱溶液中的水反应生成H 2和Al(OH)3然后Al(OH)3再与NaOH 反应生成H 2O 和NaAlO 2,反应中铝作还原剂,水作氧化剂,NaOH 无电子得失。
【巩固练习】1.同浓度同体积的盐酸和NaOH 溶液与足量的Al 充分反应,放出H 2的质量之比为________。
【答案】1∶32.(写一写)将含氧化膜的铝条放入足量的NaOH溶液中,依次发生的离子方程式为____________________________________________________________________________________________________。
【答案】Al2O3+2OH-===2AlO-2+H2O2Al+2OH-+2H2O===2AlO-2+3H2↑知识点二铝的重要化合物的性质1.氧化铝和氢氧化铝(是离子反应的写离子方程式)2.明矾(1)化学式为KAl(SO4)2·12H2O。
(2)电离方程式KAl(SO4)2===K++Al3++2SO2-4。
(3)应用:净水。
净水原理为明矾电离出的Al3+在水中水解生成Al(OH)3胶体,吸附水中悬浮物而沉淀,使水净化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学学习材料
金戈铁骑整理制作
铝及其化合物的化学方程式和离子方程式
一、铝
1、铝在氧气中燃烧:4Al+3O22Al2O3
2、铝在氯气中燃烧:2Al+3Cl22AlCl3
3、铝和硫共热:2Al+3SAl2S3
4、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3 +3H2 ↑
2Al+6H+2Al3++3H2 ↑
5、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2 ↑
2Al+2OH-+2H2O2AlO2-+3H2 ↑
6、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3 +3SO2 ↑+6H2O
7、铝和浓硝酸共热:Al+6HNO3Al(NO3)3 +3NO2 ↑+3H2O
Al+6H++3NO3-Al3++3NO2 ↑+3H2O
8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3 +NO ↑+2H2O
Al+4H++NO3-Al3++NO ↑+2H2O
8、铝和硝酸银溶液反应:Al+3AgNO3Al(NO3)3 +3Ag
Al+3Ag+Al3++3Ag
9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3 +3Cu
2Al+3Cu2+2Al3++3Cu
10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe
11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe
12、铝和氧化铜高温共热:2Al+3CuOAl2O3+3Cu
13、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn
二、氧化铝
1、氧化铝与稀硫酸反应:Al2O3+3H2SO4Al2(SO4)3 +3H2O
Al2O3+6H+2Al3++3H2O
2、氧化铝与氢氧化钠溶液反应:Al2O3+2NaOH2NaAlO2+H2O
Al2O3+2OH-2AlO2-+H2O
3、电解氧化铝的熔融液:2Al2O34Al+3O2 ↑
三、氢氧化铝
1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H2SO4Al2(SO4)3 +6H2O
Al(OH)3 +3H+Al3++3H2O
2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOHNaAlO2+2H2O
Al(OH)3 +OH-AlO2-+2H2O
3、加热氢氧化铝:2Al(OH)3 Al2O3+3H2O
四、硫酸铝
1、硫酸铝溶液与氯化钡溶液混合:Al2(SO4)3 +3BaCl22AlCl3+3BaSO4 ↓
SO42-+Ba2+BaSO4 ↓
2、硫酸铝的水溶液呈酸性:Al2(SO4)3+6H2O2Al(OH)3 +3H2SO4
Al3++3H2OAl(OH)3 +3H+
3、硫酸铝溶液中加入少量的氢氧化钠溶液:Al2(SO4)3 +6NaOH3Na2SO4+2Al(OH)3 ↓
Al3++3OH-Al(OH)3 ↓
4、向硫酸铝溶液中加足量的氢氧化钠溶液:
Al2(SO4)3 +8NaOH2NaAlO2+3Na2SO4+4H2O
冰晶石
电解
Al3++4OH-AlO2-+2H2O
5、向硫酸铝溶液中加入少量的氢氧化钡溶液:
Al2(SO4)3 +3Ba(OH)2 2Al(OH)3 ↓+3BaSO4 ↓
2Al3++3SO42-+3Ba2++6OH-2Al(OH)3 ↓+3BaSO4 ↓
6、向硫酸铝溶液中加入足量的氢氧化钡溶液:
Al2(SO4)3 +4Ba(OH)2 Ba(AlO2)2 +3BaSO4 ↓+4H2O
2Al3++3SO42-+3Ba2++8OH-2AlO2-+3BaSO4 ↓+4H2O
7、向明矾溶液中加入少量的氢氧化钡溶液:
3Ba(OH)2 +2KAl(SO4)2 2Al(OH)3 ↓+3BaSO4 ↓+K2SO4
3Ba2++6OH-+2Al3++3SO42-3BaSO4 ↓+2Al(OH)3 ↓
8、向明矾溶液中加入足量的氢氧化钡溶液:
KAl(SO4)2 +2Ba(OH)2 KAlO2+2BaSO4 ↓+2H2O
Al3++2SO42-+2Ba2++4OH-AlO2-+2BaSO4 ↓+2H2O
9、向硫酸铝溶液中加入氨水:Al2(SO4)3 +6NH3·H2O2Al(OH)3 ↓+3(NH4)2SO4
Al3++3NH3·H2OAl(OH)3 ↓+3NH4+
10、向硫酸铝溶液中加入碳酸钠溶液:
Al2(SO4)3 +3Na2CO3+3H2O2Al(OH)3 ↓+3Na2SO4+3CO2 ↑
2Al3++3CO32-+3H2O2Al(OH)3 ↓+3CO2 ↑
11、向硫酸铝溶液中加入碳酸氢钠溶液:
Al2(SO4)3 +6NaHCO32Al(OH)3 ↓+3Na2SO4+6CO2 ↑
Al3++3HCO3-Al(OH)3 ↓+3CO2 ↑
12、向硫酸铝溶液中加入硫化钠溶液:
Al2(SO4)3 +3Na2S+6H2O2Al(OH)3 ↓+3Na2SO4+3H2S ↑
2Al3++3S2-+6H2O2Al(OH)3 ↓+3H2S ↑
13、向硫酸铝溶液中加入硫氢化钠溶液:
Al2(SO4)3 +6NaHS+6H2O2Al(OH)3 ↓+3Na2SO4+6H2S ↑
Al3++3HS-+3H2OAl(OH)3 ↓+3H2S ↑
14、向硫酸铝溶液中加入硅酸钠溶液:
Al2(SO4)3 +3Na2SiO3+6H2O2Al(OH)3 ↓+3Na2SO4+3H2SiO3 ↓
2Al3++3SiO32-+6H2O2Al(OH)3 ↓+3H2SiO3 ↓
15、向硫酸铝溶液中加入偏铝酸钠溶液:
Al2(SO4)3 +6NaAlO2+12H2O3Na2SO4+8Al(OH)3 ↓
Al3++AlO2-+6H2O4Al(OH)3 ↓
五、偏铝酸钠
1、偏铝酸钠溶液呈碱性:NaAlO2+2H2OAI(OH)3 +NaOH
AlO2-+2H2OAl(OH)3 +OH-
2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2OAl(OH)3 ↓+NaCl
AlO2-+H++H2OAl(OH)3 ↓
3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HClNaCl+AlCl3+2H2O
AlO2-+4H+Al3++2H2O
4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3 ↓+Na2CO3
2AlO2-+CO2+3H2O2Al(OH)3 ↓+CO32-
5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2OAl(OH)3 +NaHCO3
AlO2-+CO2+2H2OAl(OH)3 +HCO3-
6、向偏铝酸钠溶液中加入硫酸铝溶液:
Al2(SO4)3 +6NaAlO2+12H2O3Na2SO4+8Al(OH)3 ↓
Al3++AlO2-+6H2O4Al(OH)3 ↓
7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2OAl(OH)3 ↓+NaCl+NH3 ↑
AlO2-+NH4++H2OAl(OH)3 ↓+NH3 ↑
8、向偏铝酸钠溶液中加入氯化铁溶液:
3NaAlO2+FeCl3+6H2O3Al(OH)3 ↓+Fe(OH)3 ↓+3NaCl
3AlO2-+Fe3++6H2O3Al(OH)3 ↓+Fe(OH)3 ↓
