《溶液》2022年中考化学真题分项详解(黑龙江专用)(打印版)
2022年中考化学专题复习 溶液专题练习卷

溶液专题练习卷 1.常温下,下列物质水溶液的pH<7的是 A.KOH B.草木灰 C.生石灰 D.醋酸 2.下列说法不正确...的是
A.硝酸铵固体溶于水是吸热过程 B.乙醇与水混合可形成溶液 C.饱和溶液的质量分数一定大于不饱和溶液 D.氯化钠溶液能够导电是因为溶液中存在自由动的离子 3.进行“一定溶质质量分数的氯化钠溶液的配制” 实验活动常出现以下错误操作,其中不影响所配溶液浓度的是
4.某实验小组将Ba(OH)2溶液逐滴滴入硫酸溶液中,溶质的质量与加人的Ba(OH)2溶液的质量关系如下图所示。下列说法错误的是
A.a点溶液为酸性 B.b点恰好完全反应 C.c点溶液的溶质为硫酸 D.b、c两点沉淀质量相等 5.下列四个图像能正确反映其对应实验操作的是 A.①用一氧化碳气体还原一定质量的氧化铁粉末 B.②用两份等质量、等浓度的过氧化氢溶液分别制取氧气 C.③向一定体积的稀盐酸中逐滴加入足量的氢氧化钠溶液 D.④某温度下,向一定量饱和硝酸钾溶液中加人硝酸钾晶体 6.用溶质质量分数为98%、密度为1.84克/厘米3的浓硫酸配制溶质质量分数为10%的稀硫酸100毫升,计算时必须查阅的数据是 。配制过程除使用量筒、玻璃棒和胶头滴管外,还需要的一种玻璃仪器是 。
7.在室温条件下,对100mL氯化钠饱和溶液进行如图所示操作: (1)最终甲、乙两烧杯中溶液一定是饱和溶液的是 。 (2)乙溶液在加50mL水的过程中,下列这些量逐渐减小的是 。 ①溶解度 ②溶质质量分数 ③溶剂的质量 ④溶液的密度
8.溶液在生产、生活中起着十分重要的作用。请回答下列问题: (1)可以作为溶质的是_________。 A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以 (2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为________,水的体积为________mL (水的密度近似看作1g/cm3)。 (3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右下图.t1℃时,甲物质的溶解度是________。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是________(填“甲”或“乙”)物质的饱和溶液。 选项 x y
2022年中考化学真题强化训练:溶液之坐标曲线图
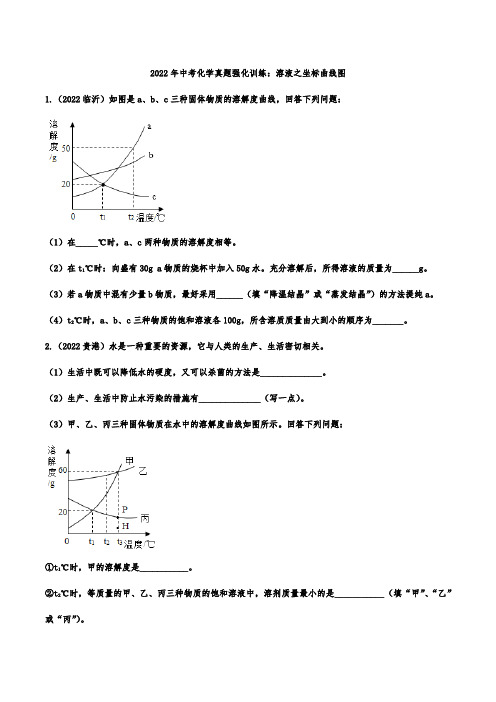
2022年中考化学真题强化训练:溶液之坐标曲线图1.(2022临沂)如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:(1)在_____℃时,a、c两种物质的溶解度相等。
(2)在t1℃时:向盛有30g a物质的烧杯中加入50g水。
充分溶解后,所得溶液的质量为______g。
(3)若a物质中混有少量b物质,最好采用______(填“降温结晶”或“蒸发结晶”)的方法提纯a。
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶质质量由大到小的顺序为_______。
2.(2022贵港)水是一种重要的资源,它与人类的生产、生活密切相关。
(1)生活中既可以降低水的硬度,又可以杀菌的方法是______________。
(2)生产、生活中防止水污染的措施有______________(写一点)。
(3)甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。
回答下列问题:①t1℃时,甲的溶解度是___________。
②t2℃时,等质量的甲、乙、丙三种物质的饱和溶液中,溶剂质量最小的是___________(填“甲”、“乙”或“丙”)。
③乙中混有少量的甲,可用___________的方法提纯乙。
④将丙溶液由P点转化到H点的方法是____________。
3.(2022黑龙江龙东地区)水和溶液与人类的生活息息相关。
(1)①生活中常用活性炭净化水,主要利用活性炭的_____性。
②日常生活中硬水软化的方法是____。
(2)甲、乙、丙三种物质的溶解度曲线如图。
回答下列问题:①在____℃时,乙和丙的溶解度相等。
②t3℃,将35g甲加入到50g水中,所得溶液中溶质与溶剂的质量比为_____。
③t1℃,将乙溶液的状态由M点变为N点,方法是_____。
④t3℃时,甲、乙、丙三种物质的饱和溶液同时降温至t2℃时,所得溶液中溶质质量分数由大到小的顺序为_____。
4.(2022铁岭葫芦岛)如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题。
2023年黑龙江牡丹江中考化学试卷试题及答案详解(精校打印版)

B.烘焙饼干
C.蒸馒头
(5)存放膨松剂时的注意事项是
(写一条)。
五、计算与应用(本题共 2 小题,30 题 3 分,31 题 7 分,共 10 分)
30.根据题意回答下列问题:
(1)农业生产上,常用溶质质量分数为 16%的氯化钠溶液选种,现要配制 100kg 这种溶
液,需要氯化钠
kg,需要水
kg。
(2)在 SO2 和 SO3 组成的混合物中,硫原子与氧原子的个数为 3:7,混合物中 SO2 和 SO3
,BC 段氧
气体积分数快速下降,BC 段对应的实验操作是
(写一种)。
(2)图 2 中,打开弹簧夹,向试管Ⅰ中加入一定量稀盐酸,关闭弹簧夹(保持导管口在液
面以下)。观察到试管Ⅰ中有大量气泡产生且有液体流入试管Ⅱ中,产生此现象的原因
是
。反应结束后,试管Ⅱ中的溶液由红色变为无色且无沉淀生成,试管Ⅱ中发生
反应的化学方程式为
D.侯德榜
2.如果空气成分按体积计算,含量最多的是
A.氮气
B.氧气
C.稀有气体
D.二氧化碳
3.加油站应张贴的消防安全图标是
A.
B.
C.
D.
4.下列物质由原子直接构成的是
A.氯化钠
B.过氧化氢
C.汞
5.下列关于“生命、健康”的说法正确的是
D.C60
A.A
B.B
C.C
6.下列生活中的物质属于纯净物的是
A.不锈钢
,试管Ⅱ的溶液中一定含有的溶质是
(除酚酞以外)。
29.实践活动课中,同学们对膨松剂能使油条膨胀这一现象产生浓厚的兴趣,于是围绕
膨松剂的成分和原理进行了如下项目式探究。
【查阅资料】①某膨松剂配料表成分:碳酸氢钠、磷酸二氢钙[Ca(H2PO4)2]、玉米淀粉。 ②玉米淀粉是一种填充剂,不参与反应。
《我们周围的空气》2022年中考化学真题分项详解(黑龙江专用)(附答案)

专题02 我们周围的空气1.(2020·黑龙江哈尔滨·中考真题)下列物质的用途错误的是A.充氮气以防腐B.氧气用于医疗急救C.洗涤剂用于洗碗D.用于改良碱性土壤【答案】D【解析】A、氮气常温下化学性质稳定,不和空气中气体成分反应,可以充氮气以防腐,故A正确;B、氧气能供给呼吸,氧气可以用于医疗急救,故B正确;C、洗涤剂具有乳化作用,洗涤剂可以用于洗碗,故C正确;D、熟石灰显碱性,不能用于改良碱性土壤,故D不正确。
故选D。
2.(2020·黑龙江齐齐哈尔·中考真题)下列有关实验现象的描述正确的是()A.红磷在空气中燃烧,产生大量白雾B.铁丝在空气中燃烧,火星四射,生成黑色固体C.向氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀D.氯化铵和熟石灰混合研磨生成氯化钙、氨气和水【答案】C【解析】A、红磷在空气中燃烧,产生大量白烟而不是白雾,错误,不符合题意。
B、铁丝在氧气中燃烧,火星四射,生成黑色固体,而不是空气,错误,不符合题意。
C、向氢氧化钠溶液中加入硫酸铜溶液,产生氢氧化铜蓝色沉淀,正确,符合题意。
D、氯化铵与熟石灰混合研磨可生成氯化钙、氨气和水属于实验结论,不属于实验现象,错误,不符合题意。
故选C。
3.(2020·黑龙江龙东·中考真题)下列有关实验现象描述正确的是A.硫在空气中燃烧,发出蓝紫色火焰,放出大量的热B.打开盛有浓盐酸试剂瓶的瓶盖,瓶口出现大量白烟C.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁D.将打磨后的铝丝浸入硫酸铜溶液中,铝丝表面有红色固体析出,溶液由蓝色变为无色【答案】D【解析】A、硫在空气中燃烧,发出淡蓝色火焰,放出热量,生成具有刺激性气味的气体,不符合题意;B、打开盛有浓盐酸试剂瓶的瓶盖,浓盐酸具有挥发性,挥发出的氯化氢气体与空气中的水蒸气结合成盐酸小液滴,瓶口出现大量白雾,不是白烟,不符合题意;C、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,生成四氧化三铁是实验结论,不是实验现象,不符合题意;D、将打磨后的铝丝浸入硫酸铜溶液中,铝与硫酸铜反应生成硫酸铝和铜,故铝丝表面有红色固体析出,溶液由蓝色变为无色,符合题意。
中考化学真题分项汇编 专题06 溶液(第01期)(全国通用)(原卷版+解析版)

专题06 溶液 考点1 溶液及组成 1.(2023年重庆市中考A卷)食堂里的下列饮品属于溶液的是 A.可乐 B.西瓜汁 C.冰水 D.绿豆汤 2.(2023年湖南省永州市中考)下列溶液中,溶剂不是水的是 A.稀硫酸 B.生理盐水 C.蔗糖溶液 D.碘的酒精溶液 3.(2023年云南省中考)下列溶液中,溶质不是固体的是 A.食盐溶液 B.硝酸钾溶液 C.酒精溶液 D.蔗糖溶液 4.(2023年湖南省邵阳市中考)推理是化学学习中常用的思维方式。下列推理正确的是 A.离子是带电的粒子,则带电的粒子一定是离子 B.溶液是均一、稳定的,则均一、稳定的液体一定是溶液 C.有机物都含碳元素,则含碳元素的物质一定是有机物 D.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物 考点2 乳化 溶解时的能量变化
5.(2023年湖南省邵阳市中考)化学老师带领学生在实验室开展“自制简易冰袋”的探究活动,下列用来制作冰袋最佳的固体物质是 A.氢氧化钠 B.硝酸铵 C.生石灰 D.氯化钠 6.(2023年四川省南充市中考)下列实验设计能达到预期目的或效果的是
A.证明CO2能与水反应
B.证明可燃物燃烧需要与氧气接触 C.证明NaOH固体溶于水放热 D.证明MnO2是H2O2分解的催化剂 7.(2023年山东省滨州市中考)下面是四位同学在小组学习群中的交流记录,其中错误的是 A.小云:硝酸铵溶于水后,溶液温度降低 B.小丁:饱和溶液的溶质质量分数不一定大于不饱和溶液的溶质质量分数 C.小丽:具有均一性、稳定性的液体一定是溶液 D.小凯:利用洗洁精的乳化作用,可洗去餐具上的油污 考点3 配制一定溶质质量分数的溶液
8.(2023年江苏省苏州市中考)在配制50 g溶质质量分数为2%的23NaCO溶液的实验中,一定不.需要用到的仪器是 A.漏斗 B.玻璃棒 C.50 mL量筒 D.烧杯 9.(2023年重庆市中考)某小组用NaCl固体配制50g质量分数为6%的NaC1溶液,下列说法正确的是 A.玻璃棒的作用只有引流 B.水倒入时洒出烧杯外,质量分数变大 C.实验中会用到蒸发皿 D.实验中选用25mL规格的量筒 10.(2023年安徽省中考)为制作叶脉书签,某同学在实验室配制10%的NaOH溶液,部分操作如下,其中正确的是
《实验设计与探究、气体的制取》2022年中考化学真题分项详解(黑龙江专用)(打印版)
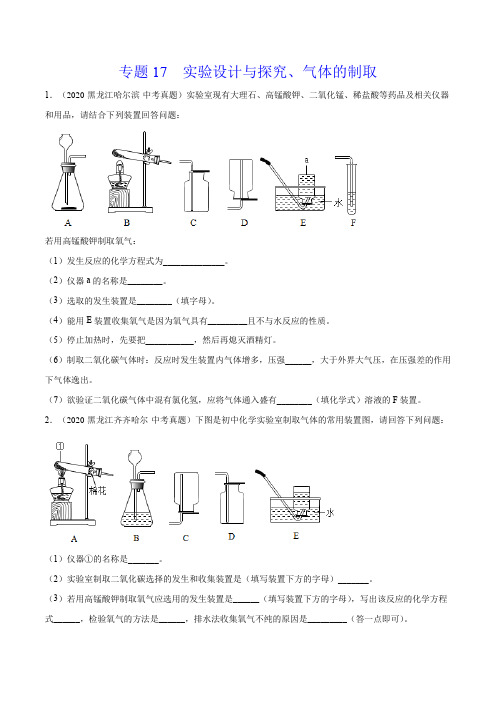
专题17 实验设计与探究、气体的制取1.(2020·黑龙江哈尔滨·中考真题)实验室现有大理石、高锰酸钾、二氧化锰、稀盐酸等药品及相关仪器和用品,请结合下列装置回答问题:若用高锰酸钾制取氧气:(1)发生反应的化学方程式为______________。
(2)仪器a的名称是________。
(3)选取的发生装置是________(填字母)。
(4)能用E装置收集氧气是因为氧气具有_________且不与水反应的性质。
(5)停止加热时,先要把___________,然后再熄灭酒精灯。
(6)制取二氧化碳气体时:反应时发生装置内气体增多,压强______,大于外界大气压,在压强差的作用下气体逸出。
(7)欲验证二氧化碳气体中混有氯化氢,应将气体通入盛有________(填化学式)溶液的F装置。
2.(2020·黑龙江齐齐哈尔·中考真题)下图是初中化学实验室制取气体的常用装置图,请回答下列问题:(1)仪器①的名称是_______。
(2)实验室制取二氧化碳选择的发生和收集装置是(填写装置下方的字母)_______。
(3)若用高锰酸钾制取氧气应选用的发生装置是______(填写装置下方的字母),写出该反应的化学方程式______,检验氧气的方法是______,排水法收集氧气不纯的原因是_________(答一点即可)。
3.(2020·黑龙江绥化·中考真题)气体制备、收集是初中化学的重要知识。
请结合下图回答有关问题。
(1)写出图中仪器a的名称:_____。
(2)实验室用氯酸钾和二氧化锰制取氧气,应选择的发生装置为___(填字母),写出该反应的化学方程式:_____。
(3)用装置C代替装置B制取二氧化碳的优点是:用D装置收集二氧化碳,则气体应从____(填“①”或“②”)端进入。
(4)用质软的塑料瓶收集满两瓶二氧化碳气体。
向其中一瓶加入约1/3体积的水(如图F所示),立即旋紧瓶盖,振荡。
《化学计算题》2022年中考化学试题分项详解(重庆专用)(打印版)

专题18 化学计算题1.(2020重庆市A)过氧化氢溶液俗称双氧水,是一种常见消毒剂。
实验员用以下方法制取了少量过氧化氢溶液,在低温下,向某浓度的稀硫酸中逐渐加入一定量的过氧化钡(BaO2),发生的化学反应为BaO2+H2SO4=BaSO4↓+H2O2,当恰好完全反应时生成沉淀。
计算:(1)加入BaO2的质量。
(2)反应后所得溶液中溶质质量分数。
(3)医用双氧水常为溶质质量分数为3%的过氧化氢溶液,如果将(2)中所得溶液稀释到医用双氧水浓度,计算需加入水的质量(结果精确到0.1g)。
2.(2020重庆市B)84消毒液的有效成分是次氯酸钠(NaClO),次氯酸钠工业制法的反应原理是: 22Cl+2NaOH=NaClO+NaCl+H O。
某同学将Cl2通入185.8 g NaOH溶液中(NaOH过量),充分反应后得到混合溶液200g。
计算:(计算结果精确到0.1%)(1)参加反应的氯气质量是多少g。
(2)混合溶液中次氯酸钠的质量分数。
(3)84消毒液中起消毒作用的是次氯酸钠中的氯元素。
已知某品牌84消毒液中起消毒作用的氯元素质量分数为6%,计算该84消毒液中次氯酸钠的质量分数。
3.(2019重庆市A)高铁酸钠( Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。
某工厂以22.35 kg NaClO固体和若干Fe2(SO4)3固体和质量分数为20%的NaOH溶液为原料生产Na2FeO4,反应原理为:3NaClO+Fe2(SO4)3+10NaOH = 2Na2FeO4+3NaCl+3Na2SO4+5H2O。
假设反应物均恰好完全反应。
试计算: [已知:相对分子质量为NaClO 74.5 Fe2(SO4)3 400 Na2FeO4166](1)Na2FeO4中质量分数最大的元素是_____(2)制备过程中需加入20%的NaOH溶液的质量是多少?_____(3)最后所得溶液中Na2FeO4的质量分数是多少?_____(计算结果精确到0.1%)4.(2019重庆市B)AgNO3可用于电影胶片制作。现取含有NaNO3的AgNO3样品100g,在一定条件下让样品充分反应,只有AgNO3发生反应,得到固体69g,该过程中发生反应的化学方程式为:2AgNO3一定条件2Ag+2NO2↑+O2↑。试计算:(1)AgNO3中N、O元素的质量比为_____。(2)分解产生的混合气体中O2的质量。_____(3)另取100g该样品和一定质量的NaCl固体全部溶解于水中得到含一种溶质的溶液,该溶液溶质的质量分数是多少?_____5.(2018重庆市A)化学反应在防治环境污染中扮演了重要角色。
黑龙江省哈尔滨市2022年中考化学真题试题(含答案)

哈尔滨市 2022 年初中升学考试综合试卷考生须知:1.本试卷满分为140分,考试时间为120分钟。
2.答题前,考生先将自己的“姓名”、“考号”、“考场”、“座位号”在答题卡上填写清楚,将“条形码”准确粘贴在条形码区域内。
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案无效,在草稿纸、试题纸上答题无效。
4.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹的签字笔书写,字迹工整、笔迹清楚。
5.保持卡面整洁,不要折叠、不要弄脏、不要弄皱,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:H-1 C-12 0-16 S-32 Cl-35.5 K-39 Ca-40 Cu-64 Zn-65一、选择题(1-27小题,每小题2分,共54分,每小题只有一个正确答案)1.哈尔滨市秋林食品深受广大市民的喜爱,下列秋林食品中含蛋白质相对较多的是()2.下列过程中不发生化学变化的是()3.下列叙述错误的是()A.餐具上的油污可用加入洗涤剂的水洗掉B.用大量的亚硝酸钠腌渍蔬菜、鱼、肉、蛋等C.为减少水体污染,可将生活污水集中处理达标后排放D.在火场的浓烟中逃生,可用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域4.下列实验操作正确的是()A.液体的倾倒 B.液体的加热 C.量取一定量的液体 D.用滴管取液体5.下列物质的用途错误的是()A.氧气用于炼钢B.聚氯乙烯用于食物包装C.干冰用于人工降雨D.稀有气体用于霓虹灯6.下列实验现象描述正确的是()A.硫在空气中燃烧:发出蓝紫色火焰,产生有刺激性气味的气体,放热B.加热通入足量二氧化碳后的石蕊溶液:溶液由红色变为紫色C.生石灰中加入一定量的水:白色固体变成白色浆液,吸收大量的热D.把铁钉放在硫酸铜溶液中:银白色固体表面有铜析出,溶液由蓝色变为浅绿色7.下列叙述、对应的化学方程式、所属基本反应类型都正确的是()A.服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl=AlCl3+3H2O 复分解反应 B.拉瓦锡研究空气成分 2Hg0△2Hg+02分解反应C.用天然气作燃料 CH4+O2点燃CO2+2H2O 氧化反应D.验证铜和铝的活动性 3Cu+A12(S04)3=3CuS04+2Al 置换反应8.关注健康,预防疾病。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题09 溶液1.(2020·黑龙江龙东·中考真题)下列说法不正确的是A.浓硫酸具有吸水性,因此在实验室中常用作干燥剂B.当喝了冰镇汽水后常常会打嗝,这种现象说明气体的溶解度与压强有关C.在测定空气中氧气的含量时,若红磷量不足,进入集气瓶中水的体积会少于瓶内气体体积的1/5 D.物质在溶解过程中常伴随热量变化,如硝酸铵溶解时会出现吸热现象2.(2020·黑龙江哈尔滨·中考真题)如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是A.t2℃时,甲的溶解度为70B.乙中含有少量的甲,可用蒸发溶剂的方法提纯乙C.t2℃时,甲、乙两种物质的溶液分别降温到t1℃,析出晶体的质量甲一定大于乙D.t2℃时,甲的溶液降温到t1℃,一定能得到甲的饱和溶液3.(2020·黑龙江大庆·中考真题)A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是()A.阴影区域中,A、C均处于不饱和状态B.除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯B C.将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>BD.t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7%A.70℃时,硝酸钾的溶解度为114B.70℃时,C点为硝酸钾的不饱和溶液C.70℃时,B点为硝酸钾的饱和溶液D.A、C两点对应溶液的溶质质量分数相同5.(2019·黑龙江哈尔滨市·中考真题)分析下图溶解度曲线,判断下列说法错误的是()A.t2℃时,硝酸钾的溶解度为110gB.硝酸钾中含有少量氯化钠时,可以用冷却热饱和溶液的方法提纯硝酸钾C.将t2℃时硝酸钾的饱和溶液降温到t1℃,一定会析出(110-a)g晶体D.t2℃时,等质量的两种物质的饱和溶液中,含硝酸钾的质量一定比含氯化钠的质量大6.(2019·黑龙江龙东·中考真题)实验室需配制50g 6%的NaCl溶液。
在配制溶液过程中,下列做法不正确的是()A.用药匙取用NaCl固体时,瓶塞倒放于桌面B.用玻璃棒搅拌,加速NaCl固体的溶解C.用量筒量取水时仰视读数D.称量时,天平指针向右偏转,应向左盘添加NaCl固体至天平平衡A.恒温蒸发溶剂的方法不可以使B得到饱和溶液析出晶体B.将t2℃时A、B的饱和溶液分别降温至t1℃,A成为不饱和溶液C.t2℃时,用等质量的A、B分别配制成饱和溶液,所得溶液的质量A>BD.t2℃时,将150g A的饱和溶液稀释成质量分数为20%的溶液,需水100g8.(2018·海林市朝鲜族中学中考真题)医院里的下列物质属于纯净物的是()A.生理盐水B.止咳糖浆C.冰水D.碘酒9.(2018·黑龙江绥化市·中考真题)化学就在我们身边,它与我们的生活息息相关。
下列应用中,错误的是()A.将硝酸铵溶于水制作热敷袋B.用汽油或加了洗涤剂的水都能除去衣服上的油污C.把水喷向空中,可以增加养鱼池水中氧气的溶解量D.进入久未开启的菜窖,要先做灯火实验10.(2018·黑龙江绥化市·中考真题)甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是()A.甲物质的溶解度大于乙物质的溶解度B.t1℃时甲、乙两物质形成的饱和溶液中溶质质量分数相等C.当甲中含有少量的乙时,可以采用降温结晶的方法提纯甲D.将M点的甲溶液变为饱和溶液可采取升高温度的方法11.(2018·黑龙江哈尔滨市·中考真题)下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是A.乙中含有少量甲,可用冷却热饱和溶液的方法提纯甲B.t3℃时,甲的溶液溶质质量分数一定大于乙的溶液溶质质量分数C.t3℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t2℃,析出晶体的质量甲一定大于乙D.t1℃时,乙的不饱和溶液只有通过蒸发溶剂的方法才能转变成饱和溶液12.(2018·黑龙江大庆·中考真题)许多化学反应都是在溶液中进行的,关于溶液理解正确的是()A.通过加热蒸发的方法提高75%酒精的浓度B.将氧化钙溶于水,可以形成氧化钙溶液C.5gCuSO4·5H2O溶于95g水中配制CuSO4溶液,此溶液溶质的质量分数小于5%D.将50℃下的饱和KNO3溶液冷却至室温,硝酸钾固体析出,过滤后可得纯水和硝酸钾固体13.(2018·黑龙江龙东·中考真题)如图所示,将液体X加入到集气瓶中与固体Y作用,观察到气球逐渐变大,如表中液体X和固体Y的组合,符合题意的是()A.①②⑤B.①③④C.①②④D.②③⑤14.(2020·黑龙江齐齐哈尔·中考真题)如图是a、b、c三种物质的溶解度曲线,回答下列问题:(1)P点的含义是______。
(2)t2℃时,将50克a物质加入到100克水中,充分溶解后,所得溶液的质量是______克。
(3)若a中含有少量b,可用_____的方法提纯a(选填“蒸发结晶”或“降温结晶”);(4)t2℃时,等质量a、b、c三种物质的饱和溶液中溶剂质量由大到小的顺序为_______。
15.(2020·黑龙江绥化·中考真题)如图是甲、乙、丙三种物质的溶解度曲线。
(1)t1℃时,三种物质的溶解度由大到小的关系为____。
(2)t2℃时,甲、乙、丙三种物质的饱和溶液降温至t1℃时为不饱和溶液的是__。
(3)现有含少量甲的乙固体,若要通过结晶法进行提纯乙(甲与乙不发生反应),现有下列实验步骤可供选择:①取一定量的水将固体溶解②充分冷却后过滤③趁热过滤④加热蒸发至大部分晶体析出⑤加热蒸发至溶液接近饱和⑥停止加热用余热将溶液蒸干⑦用少量水洗涤晶体并烘干。
合理的操作顺序为_______(按顺序填编号)。
(4)t3℃时,取等质量甲、乙、丙三种物质的饱和溶液,恒温蒸发一定质量的水(析出的晶体均不含结晶水),析出晶体的质量关系为甲=乙<丙,则剩余溶液的质量由大到小的关系为______。
(5)t2°C时,配制甲、乙、丙三种物质的饱和溶液,一定相等的是___(填字母)。
A 溶质质量B 溶剂质量C 溶质质量分数D 溶解度16.(2020·黑龙江龙东·中考真题)甲、乙、丙三种物质的溶解度曲线如图所示。
(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小顺序为____________。
(2)当甲中混有少量的乙时,可采用___________(填“降温结晶”或“蒸发结晶”)的方法提纯甲。
(3)将t2℃时180g甲的饱和溶液降温到t1℃,析出晶体的质量为_____________。
(4)取等质量的甲、乙、丙三种物质,分别配制成t2℃时的恰好饱和溶液,所得三种溶液的质量由大到小顺序为_________。
17.(2019·黑龙江绥化·中考真题)甲、乙、丙三种固体物质的溶解度曲线如图所示。
(1)_____℃时,甲、乙两种物质的溶解度相等。
(2)甲中含有少量的乙,可采用_____方法提纯甲。
(3)t1℃时,要配制100g质量分数为10%的甲溶液,需要甲物质的质量为_____g。
(4)t2℃时,甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序是_____。
(5)t1℃时,将15g甲物质加入到50g水中充分溶解后,所得溶液中溶质的质量分数为_____。
18.(2019·黑龙江齐齐哈尔市·中考真题)t1℃时,向盛有等体积水的①、②两支试管中分别加入等质量的甲、乙两种可溶性固体,充分溶解后,观察到如图1所示的现象。
请回答:(1)t1℃时,_____(选填“①”或“②”)试管中的溶液一定是饱和溶液;(2)图2中表示乙的溶解度曲线的是_____(选填“a”或“b”);(3)下列说法正确的是_____。
A 若甲中混有少量的乙,可以采用降温结晶的方法提纯甲。
B t1℃时,试管①中溶液的溶质质量分数小于试管②中溶液的溶质质量分数C 保持温度不变,向试管①中加入一定质量的水,溶液中溶质的质量分数一定变大19.(2019·黑龙江龙东·中考真题)甲、乙、丙三种物质的溶解度曲线,如图所示,回答下列问题:(1)P点的含义_____;(2)t2℃时,甲、乙、丙三种物质溶解度从大到小的顺序为_____;(3)当乙中混有少量甲时,可采用_____(填“降温结晶”或“蒸发结晶”)的方法提纯乙。
(4)t2℃时,将甲、乙、丙三种物质的饱和溶液同时降温t1℃,所得溶液中溶质质量分数由大到小的顺序为_____。
20.(2018·海林市朝鲜族中学中考真题)作图法是常用的数据处理方法,甲,乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:(1)甲,乙两种物质中溶解度受温度影响较大的是________(2)t2o C时,甲,乙两种物质各70g分别加入100g水中,能形成饱和溶液的是______物质(3)若甲物质中混有少量的乙物质,提纯甲物质可采取的方法是___________(填降温结晶或蒸发结晶)(4)将t1o C时甲,乙的饱和溶液升温到t2o C,所得溶液的溶质质量分数的关系是甲_________(填“﹥”“﹤”“=” )乙。
21.(2018·黑龙江大庆市·中考真题)已知A、B、C三种物质的溶解度曲线如图所示。
(1)在阴影区域部分,处于不饱和状态的是__________(选填“A、B盐酸反应生成、C”)。
(2)若饱和A溶液中含有少量的C,提纯A的方法为______结晶,过滤。
(3)P点表示的含义为_________。
(4)在t1℃下,B、C的饱和溶液升温至t2℃,所得溶液溶质的质量分数大小关系为_______。
(5)向试管中滴入2mL水后,若X中有固体析出,则X为______(选填“A、B、C”)。
22.(2018·黑龙江齐齐哈尔市·中考真题)请根据下图a、b、c三种固体物质的溶解度曲线,回答下列问题:(1)在_______℃时,a 、c 两种物质的溶解度相等。
(2)在t 2℃时,向盛有50ga 物质的烧杯中加入50g 水,充分溶解后,所得溶液的质量为______g 。
(3)若a 物质中混有少量b 物质,最好采用___的方法提纯。
(填“降温结晶”或“蒸发结晶”)。
(4)t 2℃时,a 、b 、c 三种物质的饱和溶液各100g ,所含溶剂的质量由大到小的顺序是_____。
(5)下列说法正确的是______。
A .将a 物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小B .将t 1℃时c 物质的饱和溶液升温到t 2℃,其溶液的质量一定减小C .配制一定溶质质量分数的b 物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b 溶液中溶质的质量分数将偏高23.(2018·黑龙江龙东·中考真题)甲、乙、丙三种物质的溶解度曲线如右图所示,回答下列问题:(1)三种物质中________的溶解度随温度变化趋势与气体溶解度的变化相似(填“甲”或“乙”或“丙”);(2)将2t ℃时甲、乙两物质饱和溶液分别蒸发等质量的水,析出固体的质量甲___乙 (填“>”或“<"或“=”);(3)当甲中混有少量乙时,可采用___的方法提纯甲;(4)将2t ℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至1t ℃,所得溶液中溶剂质量由大到小的顺序为_____。
