【医疗药品管理】国家医疗器械审评专家库审评专家推荐表-国家食品药品监督管理
国家食品药品监督管理局关于公布第四批国家药品GMP认证检查员名单的通知

国家食品药品监督管理局关于公布第四批国家药品GMP认证检查员名单的通知文章属性•【制定机关】国家食品药品监督管理局(已撤销)•【公布日期】2004.05.25•【文号】国食药监安[2004]185号•【施行日期】2004.05.25•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家食品药品监督管理局关于公布第四批国家药品GMP认证检查员名单的通知(国食药监安[2004]185号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为做好《药品生产质量管理规范》认证检查员库的建立工作,我局对各地推荐、参加过我局药品GMP认证检查员培训班人员重新进行了审核、登记,并根据药品GMP认证现场检查实践考察,决定聘任第四批国家药品GMP认证检查员77名,现予公布。
国家食品药品监督管理局二00四年五月二十五日国家药品GMP认证检查员名单北京市:周玉兰高媛姚胜林张亚冬天津市:刘京敏李明义王玉洁河北省:高纪辰许海鹰高华丽辽宁省:张秋实吉林省:战峰王云海江苏省:孙大权焦灵利李国亮浙江省:金标新杨国栋宗珏安徽省:刘斌周鹏程福建省:潘碧英史晓燕连斐宏谢永军江西省:杨国华刘江江张建民山东省:夏林谢金洲梁宏赵运江河南省:邢兰敏胡荣敏湖北省:孙佑元广东省:卢君强谭飞腾文灏广西壮族自治区:赖家范文东旭海南省:陈海峰重庆市:张节姜学美李克健张慧四川省:伍丕娥李洪培张向崇何畏贵州省:海市衣林云南省:李在浒业应楷魏有曙余彩仙陕西省:杨志信王斌卜绥云马恩哲甘肃省:崔强文惠玲新疆维吾尔自治区:李颖中国药品生物制品检定所:侯继峰程亚琴局药典会:张培培特邀:于淑渤(北京市)夏金友孙玉龙(天津市)张群(江西省)章力生(湖南省)王夏娜(广东省)孟慎怡(四川省)叶瑛瑛(局认证中心)周国安刘大英夏振民(中国药品生物制品检定所)刘玉珍(中国医药质量协会)。
新药审评专家库
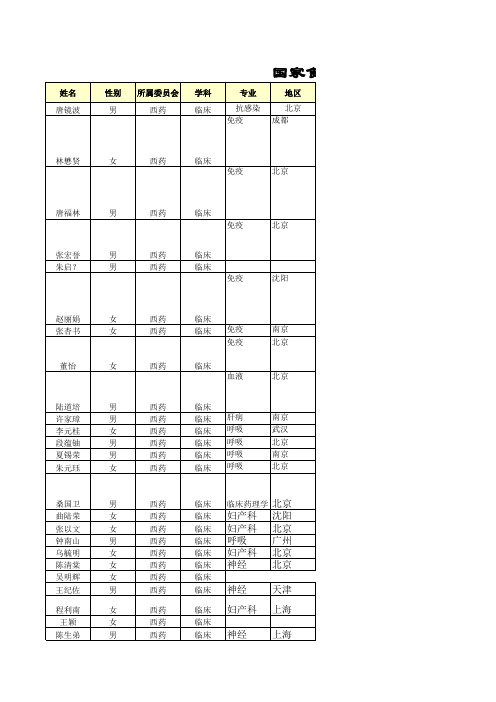
临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床 临床
武正炎
男
樊明文
男
孙芳娥
姓名 唐镜波
国家食品与药品监督管理局药品
性别 男
所属委员会 西药
学科 临床
专业
抗感染 免疫
地区
北京 成都
林懋贤
女
西药
临床 免疫
北京
唐福林
男
张宏誉
男
朱启?
男
西药
西药 西药
临床 免疫
临床 临床
免疫
北京 沈阳
赵丽娟
女
张杏书
女
董怡
女
陆道培
男
许家璋
男
李元桂
女
段蕴铀
男
夏锡荣
男
朱元珏
女
桑国卫
男
曲陆荣
女
张以文
女
钟南山
女
王惠吉
女
王海燕_1
女
陈香美
女
郑法雷
男
季大玺
男
吴平生
男
张旭明
男
苏诚坚
男
游凯
男
蒋宝琦
男
邓伟吾
男
段连山
男
西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药 西药
国家食品药品监督管理局关于公布第五批重新聘任的国家药品GMP检查

国家食品药品监督管理局关于公布第五批重新聘任的国家药
品GMP检查员名单的通知
【法规类别】药品管理
【发文字号】国食药监安[2011]64号
【发布部门】国家食品药品监督管理局(原国家药品监督管理局)(已撤销)
【发布日期】2011.02.09
【实施日期】2011.02.09
【时效性】现行有效
【效力级别】XE0303
国家食品药品监督管理局关于公布第五批重新聘任的国家药品GMP检查员名单的通知
(国食药监安[2011]64号)
各省、自治区、直辖市食品药品监督管理局(药品监督管理局):
为加强对药品GMP检查员的管理,规范检查员队伍建设,按照国家局开展药品GMP检查员重新聘任工作计划,经各省(区、市)食品药品监管部门推荐,国家局综合考评,刘明华等167人为第五批重新聘任的国家药品GMP检查员,现予公布并核发《国家药品GMP 检查员证》。
附件:第五批重新聘任的国家药品GMP检查员名单
国家食品药品监督管理局
二○一一年二月九日
附件:第五批重新聘任的国家药品GMP检查员名单。
国家药品监督管理局关于公布全国医疗器械标准化联络员名单的通知

国家药品监督管理局关于公布全国医疗器械标准化联络员名单的通知文章属性•【制定机关】国家药品监督管理局•【公布日期】2001.06.26•【文号】•【施行日期】2001.06.26•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家药品监督管理局关于公布全国医疗器械标准化联络员名单的通知各省、自治区、直辖市药品监督管理局及各医疗器械标准化归口单位:为加强医疗器械标准化工作队伍建设,便于全国医疗器械标准化工作的交流和沟通,保证医疗器械标准化工作的顺利进行,更好地为医疗器械监督管理提供技术保障,经研究决定,聘任黄荣健等42名同志为全国医疗器械标准化联络员。
现将全国医疗器械标准化联络员名单予以公布(见附件)。
请各单位注意保持联络员队伍的稳定,积极督促他们的工作,并为他们的工作提供必要的支持和保障。
各医疗器械标准化联络员要加强学习、交流和沟通,不断提高业务水平,努力做好工作,开创医疗器械标准化工作的新局面。
特此通知附件:全国医疗器械标准化联络员名单国家药品监督管理局二00一年六月二十六日附件:全国医疗器械标准化联络员名单┌────┬─┬─┬──────┬──────────┬────────────┬───────┬────────┬──────┐│姓名│性│年│ 职务/职称│工作单位│通讯地址│电话│传真│电子信箱│││别│龄│││││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│黄荣建│女│31│工程师│北京市药品监督管理局│北京市霄云路霄云里7号508│010-84551489 │010-│Huang.r.j@bj│││││││室││84551489│.on│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│XXX萍│男│48│高级工程师│天津市药品监督管理局│天津市和平区岳阳道79号│022-│022-│││││││││23322300-│23129559│││││││││2206│││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│林唯曾│男│54│副处调研员│上海市药品监督管理局│上海市普安路189号│021-│63870350│SMDA22@S││││││医疗器械注册处││63855666-128││H163.NET│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│马芳│男│46│助理调研员/│山东省药品监督管理局│济南市解放路11号│0531-8562071 │0531-││││││高工││││8541141││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│陈丽华│女│37│工程师│广东省药品监督管理局│广州市东山竹丝岗四马路2 │020-87773349 │020-│││││││医疗器械处│号│87778092-│87765366│││││││││8602│││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│边巴次仁│男│29│药师│西藏药品监督管理局│西藏拉萨市林廓北路27号│0891-6826671 │6837705││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│聂银初│男│50│助理调研员│湖南省药品监督管理局│长沙市戥子桥26号│0731-│0731-│││││││││2228108│4431012││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│蒋西佛│男││主任科员│贵州省药品监督管理局│贵阳市北京路八角饭店新楼│0851-│0851-│││││││医疗器械处│三楼│6839273│6832494││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│谭宪圣│男│60│主任/│黑龙江省医疗器械技术│哈尔滨市道里区河广街41号│0451-4627947 │0451-││││││高级工程师│标准化委员会│││4834189││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│纪志│男│35│经济师│内蒙古药品监督管理局│呼和浩特市迎宾南路1号│0471-6966658 │0471-│││││││医疗器械处│││6964537││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│ 暴荣华│男│38│工程师│云南省药品监督管理局│昆明市东风西路16号-││││││││││3640195││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│狄天云│男│25││宁夏回族自治区药品监│宁夏银川市文化东街50号│0951-6026348 │0951-│dtyl976@16 ││││││督管理局│││6042223││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│王鲜梅│女│35│主科/工程师│山西省药品监督管理局│山西太原上马街54号│0351-2024262 │0351-│││││││医疗器械处│030001││4031887││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│张弦│男│29│副科│安徽省药品监督管理局│合肥市屯溪路253号│0551-4655881 │0551-│HFZX@21cn││││││医疗器械处│││4658092│.com│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│陈连东│男│35│主任科员│河南省药品监督管理局│郑州市金水路96号│0371-6256040 │││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│李春│男││副处长│四川省药品监督管理局│成都市通惠门路1号│028-6638757││LiChun-││││││││││@│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│赫广安│男│50│高工│辽宁省药品监督管理局│沈阳市和平区十伟路16号│024-22716992 │024-││││││││││22823433││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│孟晓东│男│31│助工│甘肃省药品监督管理局│甘肃省药品监督管理局医疗│0931-8410167 ││││││││医疗器械处│器械处│(办)││││││││││0931-7673181 ││││││││││(家)│││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│李晓琼│女│37│科员│福建省药品监督管理局│福州市鼓屏路57号│0591-│0591-│││││││医疗器械处││7817394-303│7815150││││││││││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│杨建中│男│57│副处级调研│重庆市药品监督管理局│重庆市大坪长江支路2号│023-68812339 │023-││││││员/工程师│医疗器械处│││68813201││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│巴丹│女│44│工程师│吉林省药品监督管理局│长春市人民大街57号│0431-8905595 │0431-│││││││医疗器械处│││8905595││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│乐春林│男│41│科长/高工│江苏省药品监督管理局│南京市中山东路448号│4508384-205│025-│LCLCXM@s│││││││210002│4407585-205│6645698││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│刘东│男│43│副处长/高工│广西区药品监督管理局│广西南宁市园湖南路1号│0771-5854122 │0771-│││││││医疗器械处│││5854772││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│李彩霞│女│51│助理调研员/│河北省药品监督管理局│石家庄市合作路175 号│0311-7041217 │031l-││││││高工│医疗器械处│││7041217││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│张宇│男│33││陕西省药品监督管理局│西安市南二环西段东桃园B │029-4235819│029-│olddonbey@y ││││││医疗器械处│-18虹阴大厦││4260457││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│张娜萍│女│45│副处调/高工│湖北省药品监督管理局│武汉市武昌东湖路138号│027-87331702 │027-│││││││医疗器械处│││87331702││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│吴维│男│33│主任科员│江西省药品监督管理局│南昌市北京西路104号│0791-6270174 │0791-│Weiwu828@││││││医疗器械处│││6272516│hotmail.corn│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│俞洪亮│男│35│主任科员/│浙江省药品监督管理局│杭州市莫干山路文北巷27│0571-8077810 │8077514│Yjjyxc2@mail│││││工程师│医疗器械处│号││8077284││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│陈迅曙│男│39│主任科员│海南省药品监督管理局│海口市白龙南路52号│0898-5343901 │0898-│gyzc@sina.c││││││药品注册与医疗器械处│││5343985│om│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│祁昌宏│男│40│主任科员│青海省药品监督管理局│西宁市五四西路18号│0971-6304338 │0971-│││││││安监处(医疗器械处)│││6312865││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│XXX山│男│37│高级工程师│新疆自治区药品监督管│乌鲁木齐市新民路9号│0991-2629425 │0991-│││││││理局│830002││2630974││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│刘群│女│24││国家药品监督管理局上│上海市民和路154号│021-56635850 │021-│Nmdtcb@onl ││││││海市医疗器械质量监督│││56631202│││││││检验中心│││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│韩坚城│男│54│总工/│国家药品监督管理局杭│杭州市环城东路23号│0571-│0571-│Han-│││││高级工程师│州医疗器械质量监督检││87043175│87881112│**********││││││验中心│││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│任凤妹│女│37│工程师│国家药品监督管理局天│天津市南开区红旗南路237 │022-23690874 │022-│Tmiic@mail.││││││津医疗器械质量监督检│号││23690874│││││││验中心│││23365845││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│黄志新│女│25││国家药品监督管理局广│广州市寺右新马路寺右中街│020-87390917 │020-│************││││││东医疗器械质量监督检│九号││87390917│││││││验中心│││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│贺铭鸣│女│44│主管技师│国家药品监督管理局北│北京海淀区中关村南大街│010-│010-│││││││医医疗器械质量监督检│22 号│62179977-│62173402│││││││验中心││2267│││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│郑一菡│女│40│高工│国家药品监督管理局中│北京北三环中路2号│010-62013856 │010-│Cmdc-││││││国医疗器械质量认证中│││62013872│s@ ││││││心││││.cn│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│忙安石│男│52│高级工程师│国家药品监督管理局武│武汉市武昌中北路岳家嘴│027-86792293 │027-│nmutc@Publi││││││汉医疗器械质量监督检│││86786706│││││││验中心│││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│吴平│男│43│室主任/│国家药品监督管理局济│济南解放路11号250013│0531-8562174 │0531-│jczhx@jn-│││││研究员│南医疗器械质量监督检│││8937555│││││││验中心│││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│冯晓明│男│44│副研究员│国家药品监督管理局中│北京市天坛西里二号│010-│67020395│Cmd@nicpbp ││││││检所医疗器械质量监督│100050│67017755-563 │67020977│││││││检验中心│││││├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│宋连有│男│36│工程师│国家药品监督管理局北│北京北三环中路2号│ 010-│62025329│Songly@publi││││││京市医疗器械质量监督││62024422-││││││││检验中心││9258││nmsc2@yeah││││││││││.net│├────┼─┼─┼──────┼──────────┼────────────┼───────┼────────┼──────┤│牟莉│女│46│翻译│国家药品监督管理局沈│沈阳市铁西区重工北街22号│024-25827851 │024-│mulixlj@mail││││││阳医疗器械质量监督检│││25820569│││││││验中心│││││└────┴─┴─┴──────┴──────────┴────────────┴───────┴────────┴──────┘。
《医疗器械注册管理办法》 (2014国家食品药品监督管理总局局令第4号)

国家食品药品监督管理总局令第4 号《医疗器械注册管理办法》已于2014年6月27日经国家食品药品监督管理总局局务会议审议通过,现予公布,自2014年10月1日起施行。
局长张勇2014年7月30日医疗器械注册管理办法第一章总则第一条为规范医疗器械的注册与备案管理,保证医疗器械的安全、有效,根据《医疗器械监督管理条例》,制定本办法。
第二条在中华人民共和国境内销售、使用的医疗器械,应当按照本办法的规定申请注册或者办理备案。
第三条医疗器械注册是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其结果进行系统评价,以决定是否同意其申请的过程。
医疗器械备案是医疗器械备案人向食品药品监督管理部门提交备案资料,食品药品监督管理部门对提交的备案资料存档备查。
第四条医疗器械注册与备案应当遵循公开、公平、公正的原则。
第五条第一类医疗器械实行备案管理。
第二类、第三类医疗器械实行注册管理。
境内第一类医疗器械备案,备案人向设区的市级食品药品监督管理部门提交备案资料。
境内第二类医疗器械由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。
境内第三类医疗器械由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
进口第一类医疗器械备案,备案人向国家食品药品监督管理总局提交备案资料。
进口第二类、第三类医疗器械由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
香港、澳门、台湾地区医疗器械的注册、备案,参照进口医疗器械办理。
第六条医疗器械注册人、备案人以自己名义把产品推向市场,对产品负法律责任。
第七条食品药品监督管理部门依法及时公布医疗器械注册、备案相关信息。
申请人可以查询审批进度和结果,公众可以查阅审批结果。
第八条国家鼓励医疗器械的研究与创新,对创新医疗器械实行特别审批,促进医疗器械新技术的推广与应用,推动医疗器械产业的发展。
第二章基本要求第九条医疗器械注册申请人和备案人应当建立与产品研制、生产有关的质量管理体系,并保持有效运行。
国家食品药品监督管理局关于表彰全国食品药品监督管理系统先进集

国家食品药品监督管理局关于表彰全国食品药品监督管理系
统先进集体和先进个人的通报
【法规类别】药品管理
【发文字号】国食药监人[2010]13号
【发布部门】国家食品药品监督管理局(原国家药品监督管理局)(已撤销)
【发布日期】2010.01.15
【实施日期】2010.01.15
【时效性】现行有效
【效力级别】XE0303
国家食品药品监督管理局关于表彰全国食品药品监督管理系统先进集体和先进个人的通
报
(国食药监人[2010]13号)
各省、自治区、直辖市食品药品监督管理局(药品监督管理局),国家食品药品监督管理局机关各司局、各直属单位:
近年来,全国食品药品监督管理系统广大干部职工坚持以邓小平理论和“三个代表”重要思想为指导,深入贯彻落实科学发展观,认真实践科学监管理念,求真务实,开拓创新,在整顿和规范食品药品市场秩序、保障公众饮食用药安全各项工作中,涌现出一大批先进集体和先进个人。
为鼓励先进,弘扬正气,国家食品药品监督管理局决定:授予辽宁省食品药品监督管理
局技术审评中心等19个单位“全国食品药品监督管理系统先进集体”荣誉称号;授予刘建国等21名同志“全国食品药品监督管理系统先进个人”荣誉称号。
希望受表彰的先进集体和先进个人珍惜荣誉,谦虚谨慎,发扬成绩,再创佳绩。
全国食品药品监督管理系统广大干部职工要以受表彰的先进集体和先进个人为榜样,全面贯彻落实党的十七大精神,不断加强和改进食品药品监管工作,为开创我国食品药品监管工作新局面,全面建设小康社会做出新的更大的贡献!
附件:1.全国食品药品监督管理系统先进集体名单
2.全国食品药品监督。
医疗器械技术审评专家咨询函审通知

医疗器械技术审评专家咨询函审通知专家:国家食品药品监督管理局医疗器械技术审评中心是国家食品药品监督管理局负责对申请注册的进口医疗器械产品、医疗器械新产品、国产第三类医疗器械产品进行技术审评的直属机构。
工作的基本依据为《医疗器械监督管理条例》和《医疗器械注册管理办法》等相关规章,详情请查阅网。
我中心决定对(受理号:)进行函审,诚邀您作为本次函审的专家,希望您通过审阅邮寄给您的相关资料,对我们提出的咨询问题发表书面意见,如该申报资料中存在其它问题,请一并提出。
为了做好本次函审工作,现就有关事宜通知如下:一、请您务必在接到本通知和相关资料(附后)后,于年月日(星期)前将回执传真至我中心,或者通过电话方式告知我中心已收悉。
二、在进行函审时,请您注意以下事项:1、请您根据附后的函审资料在“医疗器械技术审评专家咨询意见表”中填写专家意见,并在规定时间内(一般为收到资料后10个工作日内)将函审书面意见寄回我中心;2、请您签署《专家承诺书》等文件(附后),并将《专家承诺书》等文件随注册申报资料一并寄回我中心;3、本通知所附快递到付单供您邮寄资料时使用,费用由我中心支付;4、请您将专家签字表填写完整,以供我中心报销使用。
5、请您在回执中写明您的银行账号,我们将向您所提供的账号中支付专家审评费,届时请注意查收。
感谢您对我们工作的支持!国家食品药品监督管理局医疗器械技术审评中心年月日电话:联系人:传真:地址:邮编:100044 ———————————————————————————回执:受理号为的产品函审通知及所附资料已于年月日全部收悉。
本人将按照要求及时将函审意见及相关资料寄回。
专家审评费汇入账号:(注:该账号仅限于在中国工商银行、中国建设银行或中国银行开设的账号)专家签名:年月日。
国家食品药品监督管理局关于印发保健食品审评专家管理办法的通知-国食药监许[2010]282号
![国家食品药品监督管理局关于印发保健食品审评专家管理办法的通知-国食药监许[2010]282号](https://img.taocdn.com/s3/m/60b9e7cfc0c708a1284ac850ad02de80d4d806a9.png)
国家食品药品监督管理局关于印发保健食品审评专家管理办法的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 国家食品药品监督管理局关于印发保健食品审评专家管理办法的通知(国食药监许[2010]282号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局),国家食品药品监督管理局保健食品审评中心:为进一步加强保健食品审评工作,规范保健食品审评专家管理,保证保健食品注册工作的科学、规范、公平、公正,国家局制定了《保健食品审评专家管理办法》,现予印发。
国家食品药品监督管理局二○一○年七月十九日保健食品审评专家管理办法第一条为加强和规范保健食品审评专家(以下简称审评专家)的聘用与管理,促进审评工作科学化和规范化,保证技术审评的公正、公平、公开,根据《保健食品注册管理办法(试行)》,制定本办法。
第二条国家食品药品监督管理局负责审评专家的聘用和管理,并设立保健食品审评专家库(以下称审评专家库)。
国家食品药品监督管理局委托保健食品审评中心承担审评专家库的日常管理工作。
第三条审评专家库由食品科学与工程、基础医学、临床医学、公共卫生与预防医学、中医学、中西医结合、药学、中药学、化学等相关领域的专家组成。
第四条审评专家应当具备以下基本条件:(一)作风正派、科学公正、认真负责、坚持原则;(二)熟悉掌握食品安全、保健食品及相关领域的法律法规、标准规范等;(三)具备大学本科以上(含大学本科)学历;(四)具有相应专业的正高级专业技术职称或具有博士学位副高级专业职称;(五)在本专业具有较高的学术造诣和丰富的实践工作经验,在相应专业岗位工作5年以上;(六)身体健康,原则上年龄在65周岁以下(院士除外);(七)能正常参加保健食品的技术审评会议,并能按要求承担和完成保健食品技术审评工作;(八)本人不在保健食品相关企业任职或兼职。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
□儿科(内外)
□新生儿——□培养箱
□呼吸——□呼吸机 □重症监护 □支气管内窥镜
□消化——□胃肠 □肝胆 □内窥镜
□心血管 □肾病 □血液、传染病 □神经 □内分泌 免疫
□其它(请说明)
□眼科
□角膜、屈光/视光学、准分子激光 □青光眼、激光 □白内障、晶状体
□视网膜、眼底、激光 □眼外伤、眼整形 □其它(请说明)
□眼科电生理 □介入放射 □其它(请说明)
□辅助科室
□麻醉 □重症监护,护理 □理疗、康复医学、运动医学
□病理 □临床统计 □其它(请说明)
□血站
□采血 □血液处理 □其它(请说明)
近五年论著,或在国家级专业刊物上发表论文情况
论文名称
刊物名称
期卷页
作者名次
本人保证以上信息真实、准确。
本人签名: 年 月 日
(不超过三项)
备注
□有源设备类
□电子仪器 □物理治疗设备 □麻醉和呼吸设备 □体外循环设备
□口腔设备□消毒设备 □高频、电磁场与微波技术
□光学和光学仪器 □超声设备□声学设备、听力仪器
□核物理——□医用X设备及用具 □放射治疗、核医学和放射剂量学设备
□压力容器 □医学检验设备 □磁学 □热学、低温技术
单位(盖章)
年 月 日
□药学
□药理 □毒理 □制剂 □中医药 □其它(请说明)
□内科
□呼吸 □消化——□胃肠 □肝胆
□神经 □心血管 □血液 □肾病——□透析
□内分泌与代谢 □免疫、变态反应 □传染 □其它(请说明)
□外科
□普外——□胃肠 □肝胆 □综合(请说明)
□神经外科——□神经系统外伤 □脊髓脊柱疾病
□脑血管病和老年神外疾病 □脑瘤专业 □内窥镜
□耳鼻喉科
□耳科 □鼻科 □咽喉科 □其它(请说明)
□口腔科
□口腔修复、正畸、整形 □内科 □其它(请说明)
□皮肤科
□皮肤病 □性传播疾病 □整形、美容 □其它(请说明)
□肿瘤科
□肿瘤——□放疗 □热疗 □介入治疗 □其它(请说明)
□医学影象科
□X线诊断 □CT □磁共振 □核医学 □超声诊断
□心电诊断 □脑电及脑血流图诊断 □神经肌肉电图
□基因工程 □免疫学 □遗传学
□口腔科材料及器具 □眼科器具
□神经、心血管器具、血液处理材料及器具、注射输液器具
□外科植入物和矫形器械、外科器械、计划生育器械、敷料
□生物学试验及评价 □其它(请说明)
□体外诊断试剂类
□体液、血液 □微生物 □化学检验 □免疫、血清学
□细胞分子遗传学 □其它(请说明)
国家医疗器械审评专家库审评专家推荐表
姓 名
性 别
2吋近期免冠照片
出生年月
身份证号
学 位
技术职称
工作单位
行 政
职 务
单位地址
电 话
传 真
通信地址
和邮编
电子信箱
移动电话
专业教育经历(从大专、大学填起,包括培训经历)
在企业兼职情况
参加技术审评的专业或领域
专 业
(限选一项)
研究方向及涉及领域(“——”号后为典型科目)
□骨科——□脊柱 □运动 □关节/关节镜、矫形 □骨肿瘤 □小儿骨科
□创伤 □综合(请说明)
□泌尿——□综合(请说明) □前列腺 □内窥镜
□胸外——□心血管 □介入 □内窥镜
□移植 □烧伤 □整形 □其它(请说明)
□妇科
□妇科 □产科 □计划生育、优生、生殖健康与不孕
□妇女保健(青春期、围产期、更年期、心理卫生、营养)
提名专家
提名专家单位:提名专家职来自:提名专家签名: 年 月 日
专家所在
单位意见
本表所填信息真实、准确,经我单位审核,同意推荐该同志成为国家食品药品监督管理局医疗器械审评专家库备选人员。
单位(盖章)
年 月 日
省级药监部门意见
单位(盖章)
年 月 日
国家局医疗器械审评中
心意见
单位(盖章)
年 月 日
国家局意见
□工程力学 □制造工艺 □测量学、统计学
□电气安全(GB9706) □软件 □其它(请说明)
□医用材料类
□化学——□无机化学 □有机化学 □物理化学 □生物化学
□分析化学 □化学工程
□材料——□金属材料 □无机非金属材料 □高分子材料 □生物材料
□光学材料 □纳米材料 □材料力学
□生物——□细胞生物学 □微生物 □动物学 □生物力学 □组织工程
