浙江大学有机化学乙 exercise 7
物理有机化学浙江大学年第7章消去反应幻灯片

k 1 B +HCCX B H + +CCX
k -1
CCXk 2 CC +X
B + ( D ) H C C XB H + C C + X 反 应 机 理 及 特 征
机理
(E1)anion (E1cB)r (E1cB)ip
反应级 β-H交换比消 普遍碱催化
N E t 3 + B H rC C H B rk k 1 - 1 B H rC C B H r N E t 3 k 2H C C B r + H N E t 3 B r
最后是(E1cB)irr机理。在这种反应中,离去基团的离去能力很强,
以致去氢成了决速步,对于这种情况(k2 >>k-1[BH]), 速率方程
就成为
ratke 1[B]C [ ]H
因此,这类反应的速率是与碱的浓度有关的,即,这类反应应是 受general-base催化的。从下列化合物消除一分子苯甲酸是受 普遍碱催化的,其速率与苯环上的取代基的性质无关。普遍碱催 化这一点排除了(ElcB)R机理,而离去基性质对反应速率没影响 排除了所有在过渡态还有碳-离去基键的机理.
例如,Skell and Hall研究了赤式-3-D代-2-丁醇对甲苯磺酸 酯。Syn消除将得到非氘代的cis-2-丁烯,和氘代的trans-2丁烯。但反式消除将产生氘代的cis-和非氘代的trans-2-丁烯。 实验中,在电离能力较差的硝基甲烷中,产物几乎完全是syn 消除的;但在乙醇和水的混合溶剂中,顺式和反式消除都有。
(E1)anion:
K1>>k-1、k2, 特点:β-氢的酸性很强,质子可以认为是自动离
有机化学课件浙江大学第7章有机波谱分析基础

3.红外光谱的分区 按吸收的特征,通常将4000-400 cm-1范围的红外光谱分为官
能团吸收区和指纹区。 (1)官能团吸收区 在1250-3700cm-1区域,称为高频区,有机化合物各种官能团
的吸收峰都在此区,可用来鉴定官能团。
(2)指纹区 所谓指纹区是指频率小于1250 cm-1的低频区,主要代表某些 分子骨架的特征振动以及C—C、C—O、C—N等单键的伸缩 振动和各种弯曲振动的吸收。只有结构完全相同的化合物,其 指纹区才相同。
红外光谱波长范围 波长范围为780-5×105 nm. 三个区域:
近红外(λ=780-2500 nm,υ=12820-4000 cm-1); 中红外(λ=2500-25000nm,υ=4000-400cm-1); 远红外(25000-5×105 nm,υ=400-20 cm-1)。
一般红外光谱仪使用的波数为4000-400cm-1,属中红外区,相 当于分子的振动能量,红外光谱也称为振动光谱。
7.2.1 分子的振动形式和红外光谱
红外光谱的基本原理
• 分子是由各种原子通过化学键互相连接而成的。 • 分子的振动是键合的原子通过化学键而引起的伸缩或弯曲运
动。
• 物质吸收红外光的能量大小与原子振动能级能量相当,就产
生振动能级跃迁,产生红外吸收光谱,振动能级的大小与化学 键的类型和其振动方式有关。
C-H键伸缩振动
C-H键伸缩振动所产生的吸收峰在高频区 CSP3—H :2800-3000cm-1, CSP2—H :3000-3100cm-1处, CSP—H :3300cm-1
(2)芳烃的红外光谱
芳烃的红外吸收主要为苯环上的C—H键及环骨架中 的C=C键振动所引起。芳烃主要有三种特征吸收。
浙江大学有机100题
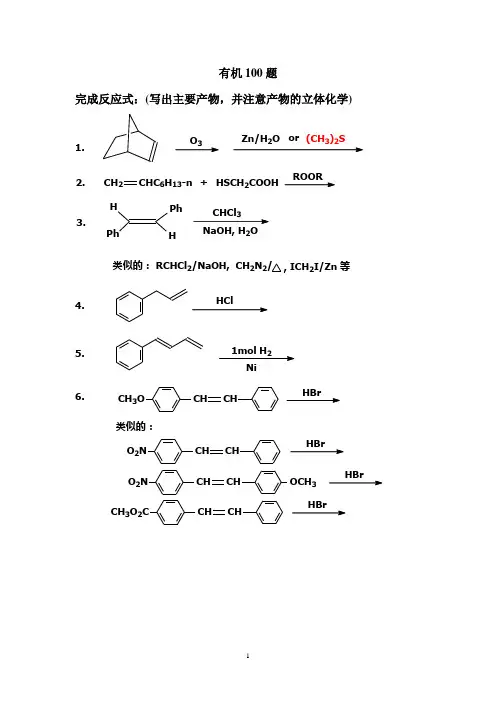
有机100题完成反应式:(写出主要产物,并注意产物的立体化学)1.O Z n /H 2Oo r (C H 3)2S2.C H 2C H C 6H 13-n+H S C H 2C O O H R O O R3.P h HHP hC H C l N a O H , H 2O类似的: R C H C l 2/N a O H , C H 2N 2/,IC H 2I/Z n 等4.5.1m o l H 2N i6.C H 3O C H CHH B r类似的: O 2N C H CH O 2N C H C H O C H3C H 3O 2CC HCH7.类似的:+ClA lC l+ClA lC l+ClA lC l+H8.C H 3+N a S H9.C lC H =C H C H 2C l +C H 3C O O N a N a 2C O 3/H 2ON a O RN aS H N a C N R CC N aN H 3N a N O 310.C H 2C H C H (C H 3)2O HH11.CH 2C H C H 2C H =C H C H 3HS O 12.C H 2C H 2C H C H 2CC H 3C H 3O HH S O13.C H2C H2C H2C H2CC H3C H3OHH S O14.C H3OC H3O C H2C H C H2C O C lA lC lO2N O2N C H2C H C H2C O ClA lC l15.A lC l+OH2O16.O2N217.ClClN aI(1mol)33CH318.324C HO19.C l20.SO3HOOO( )O21.NOOB r+22.BrN aO H ( )C l , H O( )23.C H 2=C HC F 3C H 2=C H N O 2C H 2=C HN (C H 3)3H B r+24.ORO H25.(C H 3)2CC H =C H 2C l(C H 3)2C =CH C H 2Cl23226.N OOC H 3H N O 2427.H N O 24OC O28.C H 3B H H O O H42329.BrCH 2CH 2CH 2CH 2BrH O30.C H 3O 22531.C CC H 3H H 3CHC C C H 3H H 3CH B r 432.C C C H 2C H 3H H 3CHC C C H 2C H 3H H 3CHB r 433.H BrCH 3CH 3CH 334.C H 3C H 3H O C l35.F C C O H (1m ol)36.C O O HC H 3H N O 2437.B rB rC H O H38.CCH 3C H 3CH 3C H 2ClA g H 2O39.C H 3C (C H 3)3C H 3C O C l A lC l 340.C O 2M e C O 2M eH41.Br 2-60C42.( )C OCH243.HOCH 2CH 2CH 2CH 2Cl44.OC H 3C 2H5+OCO C H 345.C H 3HH 3CHHH+C NC NN CN C46.+AlCl47.C l C H 3HC H 3HD (C H )C O K (C H 3)3C O H48.C H 2C H 349.C H 2C H 3C CH O H50.C F 3C l23C H 3C l 2351.写机理H 3B r 2) HH 3O H52.写机理HOH53.写机理H+O54.写机理C O C lO C H 3+C H 2=C H 2A lC l OC H 3O2255.写机理2H 3OH56.写机理O A cO T sO A c O A c57.写机理H OO HH O258.写机理H 2OH 3CC H 3O HC H 3H 3C59.写机理HO H60.写机理H OOHO H O H61.写机理OH+O HH OO HO62.写机理P h P hF C C O HOP h P hH 3CORRC H 3O HRO H C H 3+64.写机理C =C H C H 2C H 2C C H =C H 2C H 3C H 3C H 3O HH B rC H 3H 3CC H 3Br65.写机理1) C H C O OH /H 2HO H66.写机理H OC H 3+C H 3C O O HC H 3O C C H 3O67.写机理+C H 3C O C lA lC l C C H 3C lO68.写机理C H 2OHH69.写机理H C lC 2H 5S C H C H 2O HC H 3C 2H 5S C H 2C H C H 3C lOOH C 6H 53OOC 6H 571.写机理H72.写机理OO+M eO 2C C C C O 2M eCO 2M eC O 2Me+C O 273.写机理N EtC H 2C lN EtC l74.写机理O P h P h O H C P h 2O H75.写机理III+76.写机理(C H 3)2C =C H C H 2C H 2C H =C (C H 3)2H 3CC H 3CC H 3C H 377.写机理H B r378.写机理C H 2=CC H 3C H 2CC H 2O H C H 2C H =C H 2C H 2O HH OOC H 3C H 3C H 2C H =C H 2C H 2O H79.写机理NH B r NH B rB r80.写机理3H 3CC H 3H 3CC O O HH 3CC H 3H 3CC O O HC H 381.写机理N H C C 6H 5B rS K N H 3NS C 6H 582.写机理C 6H 5H 5C 6H 5C 6HHHC 6H 5C 6H 583.写机理HRO R 84.写机理O HC H3H OSO3N a +B r2225CO HC H3B rB r+OC H3B rO85.写机理O C H3F n-C H Li H O O C H3C H2O HC H2C H2C H2C H386.写机理(C H3)2CO H C(C H3)2C lA g N O C H3COC(C H3)387.将下表中的空白处分别用后面所写的“供选择用的答案”填入,只须填“供选择用答案”前面的号码(每一格中只能填一个号码):“供选择用答案”:(1)构型翻转。
2020版浙江选考化学大二轮复习讲义:专题七 第6讲 有机化学实验 Word版含答案
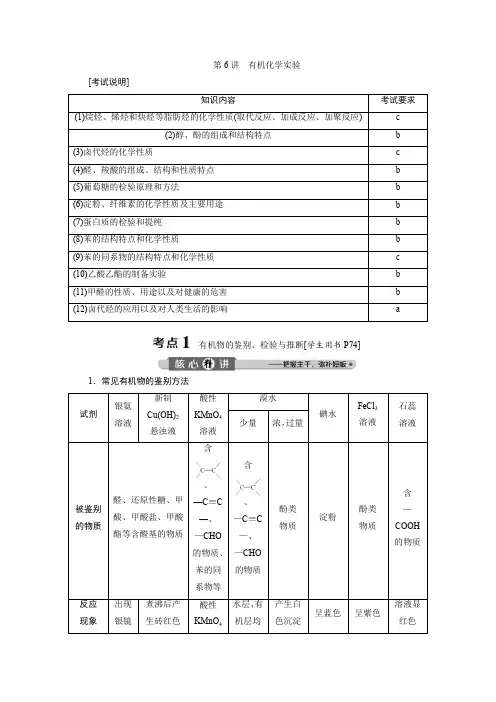
第6讲 有机化学实验[考试说明]有机物的鉴别、检验与推断[学生用书P74]1.常见有机物的鉴别方法、、2.有机物的检验与推断 (1)卤代烃中卤族元素的检验 ①原理⎭⎪⎬⎪⎫R —X +NaOH ――→H 2O△R —OH +NaX NaX +AgNO 3===AgX ↓+NaNO 3 ⇒根据沉淀AgX 颜色判断X 是Cl 、Br 还是I⎭⎪⎬⎪⎫R —CH 2—CH 2—X +NaOH ――→醇△R —CH===CH 2+NaX +H 2O NaX +AgNO 3===AgX ↓+NaNO 3⇒同上原理判断X 的类型(此方法只适用于能发生消去反应的卤代烃)②步骤:取少量卤代烃―→加NaOH(醇)溶液―→加热―→冷却―→加足量稀HNO 3―→加AgNO 3。
(2)淀粉水解程度的推断①原理:(C 6H 10O5)n +n H 2O ――→H 2SO 4微热n C 6H 12O 6; 淀粉遇碘水变蓝;CH 2OH(CHOH)4CHO +2Ag(NH 3)2OH ――→水浴加热CH 2OH(CHOH)4COONH 4+H 2O +2Ag ↓+3NH 3。
③现象与结论:A 为出现银镜,B 为无明显变化,则淀粉完全水解。
A 为出现银镜,B 为变蓝,则淀粉部分水解。
A 为无明显变化,B 为变蓝,则淀粉未水解。
(3)醛基的检验①原理:R —CHO +2Ag(NH 3)2OH ――→水浴加热RCOONH 4+3NH 3+2Ag ↓+H 2O 或R —CHO +2Cu(OH)2+NaOH ――→△RCOONa +Cu 2O ↓+3H 2O 。
②步骤:取少量待检液――→加新制银氨溶液或新制Cu(OH)2摇匀――→水浴加热或加热煮沸 出现银镜或砖红色沉淀③现象与结论:出现银镜或砖红色沉淀,则含有醛基。
④银氨溶液与新制氢氧化铜悬浊液配制a.取1 mL 2%的硝酸银溶液于试管中,在不断振荡试管的同时向试管中滴加2%的稀氨水,直至产生的沉淀恰好完全溶解。
浙大有机化学课件

浙大有机化学课件浙大有机化学课件有机化学是综合性大学化学系的基础课之一,也是生物化学、药物化学、医学、高分子化学、农业化学等学科的基础。
以下是小编整理的浙大有机化学课件,欢迎阅读。
教学目的和基本要求通过有机化学这门课程的学习,要使学生在有机化学知识上达到掌握烷、烯、炔、二烯烃、芳香烃、卤代烃化合物、醇、酚、醚、醛、酮、不饱和醛酮、取代醛酮、羧酸、羧酸衍生物、不饱和羧酸和取代羧酸、胺及其他含氮、硫、磷化合物的结构、性质,五元、六元杂环化合物的结构、性质,碳水化合物、氨基酸、肽等化合物的结构、性质及用途,周环反应。
掌握化合物的构型、构象等立体表达形式,及有关反应的立体专一性。
初步了解核磁共振、红外、质谱的基本原理,能对简单的结构进行解析。
目录1 有机分子的结构与性质2 饱和脂肪烃3 不饱和脂肪烃4 芳香烃5 立体化学6 核磁共振、质谱和红外光谱7 卤代烃8 醇和酚9 醚10 醛和酮11 不饱和醛酮和取代醛酮12 羧酸13 羧酸衍生物14 不饱和羧酸和取代羧酸16 其他含氮化合物18 杂环化合物19 碳水化合物20 氨基酸、蛋白质和核酸21 类脂、萜类化合物、甾族化合物和生物碱22 周环反应23 有机合成1 有机化合物的结构和性质1.1了解有机化学的发展史以及有机化学与生命科学的关系;1.2 有机分子的结构:共价键、碳原子的特性及有机化合物分子的立体形象;1.3 有机化合物分子的表示法:实验式、结构式、投影式;1.4 有机化合物中的共价键:碳原子的杂化轨道;?键和?键;1.5 价键理论;分子轨道理论;共振论;1.6 共价键的属性;键长、键角、键能、极性和极化度;1.7 酸碱理论:布朗斯特酸碱和路易斯酸碱理论;1.8 有机化合物结构和物理性质的关系,分子间力(范德华力和氢键)对溶解度、沸点、熔点、比重的影响。
2 饱和脂肪烃2.1 烷烃的结构:sp杂化;同系列;烷基的概念;同分异构现象;伯、仲、叔、季碳原子的概念;烷烃分子的构象:Newman投影式,重叠式与交叉式构象及能垒。
基础有机化学实验智慧树知到课后章节答案2023年下浙江大学

基础有机化学实验智慧树知到课后章节答案2023年下浙江大学浙江大学第一章测试1.以下物质中,哪些应该在通风橱内操作? ()答案:氯化氢2.高温实验装置使用注意事项错误的是:()答案:使用高温装置的实验,要求在防火建筑内或配备有防火设施的室内进行,并要求密闭,减少热量损失3.取用化学药品时,以下哪些事项操作是正确的?()答案:其余选项都是4.用剩的活泼金属残渣的正确处理方法是:()答案:在氮气保护下,缓慢滴加乙醇,进行搅拌使所有金属反应完毕后,整体作为废液处理5.试剂或异物溅到皮肤上,处理措施正确的是:()答案:其余选项都是第二章测试1.关于蒸馏,下列描述正确的是()答案:通过蒸馏可以测定液体化合物的沸点。
2.简单蒸馏时,蒸馏物的体积一般在蒸馏瓶容积的()答案:1/3-2/33.液体的沸点高于140℃时用()冷凝管答案:空气4.简单蒸馏时,温度水银球对应蒸馏头侧管下线位置偏高,会导致测得沸点()答案:偏低5.蒸馏不能分离以下哪种混合物:()答案:乙醇(95%)与5%水的混合液第三章测试1.关于Rf值,下列说法错误的是:()答案:同一物质的Rf值是一常数2.薄层层析上行法操作程序,按正确顺序排列:()a.加盖密闭,展开剂借毛细作用慢慢上移b.当展开剂的前沿距薄板另一端约1 cm左右时,取出薄层板,用铅笔轻轻画下溶剂前沿,然后让板上的溶剂自然挥发c.把一定量的展开溶剂倒入层析缸d.将薄层板点样端朝下以一定角度小心地放置在层析缸中,层析缸中溶剂的液面应在离样品原点0.5 cm以下答案:3、4、1、23.点样量的多少分析错误的是()答案:点样量随薄层厚度和分离目的而定,在0.25 mm厚度的薄层上,作定性分离时,一般点样量为点样量可达几十毫克~几百毫克4.薄层色谱的基本操作过程的正确顺序()1 薄层板的制备 2选择吸附剂 3展开4 点样5 记录6 显色,7 展开剂的选择答案:2,1,4,7,3,6,55.薄层色谱可用于:()答案:其余选项都是第四章测试1.关于柱层析中的洗脱剂,下列说法错误的是:()答案:一般要求该溶剂的极性应大于样品极性2.装柱时若柱中形成气泡或裂缝,会造成:()答案:样品分离不均匀,造成组分重叠,影响分离效果3.现有少量下列几种物质,纯度都不是很高。
浙江大学考研1991-2008年有机化学 反应式及答案
浙江大学考研1991-2008年有机化学反应式及答案浙江大学1991-2008年考研方程式答案张力学20091017浙大1991年反应式6题18分1 环酮扩环。
2 Cannizzaro 反应。
3 2,5-环己二烯酮酸性条件下重排成苯酚。
4 酯水解酰氧断裂5 CRAM 规则。
6 二卤卡宾对烯键加成,生成三元环。
浙大 1991-1OHNH2NaNOHClOOHNH2NaNOHClOOHN2+- N2CH2+CH2+-H+说明:这题的正确答案是环己酮。
这是环戊酮扩环的步骤的一部分。
OOO CNO CNH LiAlH 4OH NH 2CN--HOH浙大 1991-2CHO NaOHCOONa 2OH说明:碱性条件,答案要写羧酸钠,不写羧基。
浙大 1991-3OOHH+20091014说明OHOHOH浙大 1991-3+H +说明+-H+说明: 题目一共11个碳,答案有一个七元环。
浙大 1991-4OO 18]OH O OH18浙大 1991-5C 3H 7CH 3OHi LiAlH HOHC 3H 7H CH 3HOHiEtO CH 3HEt HOH3H C 3H 7CH 3O Hi C 3H 7O EtCH 3HC 3H7CH 3EtHH OH或表示为]题目羰基旁的手性碳是S 构型,答案这个手性碳当然还是S 构型,本题答案新形成带羟基手性碳是R 构型。
浙大 1991-6PhHgCBr 3Br Br浙大1992年6题14分。
1992-1 Michael 加成,取代丙二酸酯酸性条件下水解,加热脱羧,腈水解生成羧酸。
1992-2 烯烃亲电加成。
三氯化铝作用促进叔丁基氯生成叔丁基碳正离子。
1992-3 醇脱水生成烯烃1992-4 苯环比吡啶环易被氧化。
1992-5 季铵碱热分解。
原题目少了氢氧根,已补上。
产物是烯烃。
1992-6 Wittig反应,在指定位置形成烯键。
CNCOOEtCOOEtEtONaCOOEtCOOEtCNH O+heatrefluxCOOH浙大 1992-1COOH说明:本题答案即为戊二酸。
浙江大学有机化学试题库(推导结构)
1.某化合物分子式为C 6H 12O ,不能起银镜反应,但能与羟胺作用生成肟,在铂催化下加氢可生成一种醇,该醇经去水,臭氧分解后,得到两种液体,其中之一能起碘仿反应但不能与菲林试剂反应,另一种则能起银镜反应,但不起碘仿反应。
试写出该化合物结构式。
(CH 3)2CHCOCH 2CH 32.分子式为C 8H 14O 的化合物A ,与NH 2OH 作用、并可以很快使溴褪色。
A 被热KMnO 4氧化后可生成丙酮及另一化合物B 。
B 具有酸性,和NaOCl 反应可生成氯仿及丁二酸,试写出A 、B 的结构式。
A : (CH 3)2C=CCH 2CH 2CHOB : CH 3COCH 2CH 2COOH3.某醇经氧化脱氢生成一种酮。
该酮分子式为C 5H 10O ,经氧化后可生成乙酸和丙酸。
试推导该醇的结构。
CH 3CH 2CH(OH) CH 2CH 34.某化合物A 的分子式为C 5H 12O 、经K 2Cr 2O 7、H 2SO 4氧化后生成分子式C 5H 10O 的化合物B 。
B 不能起碘仿反应,亦不起银镜反应,B 与金属镁作用生成C 10H 22O 2化合物C ,C 能与高碘酸作用又可生成B 。
C 与浓H 2SO 4作用生成C 10H 20O 化合物D 。
D 能与氨基脲(NH 2NHCONH 2)作用生成结晶,D 不能起银镜反应。
试写出A 、B 、C 、D 结构及相关反应式。
CH 3CH 2CH(OH) CH 2CH 3 CH 3CH 2COCH 2CH 3 (CH 3CH 2)3CCOCH 2CH 35.分子式为C 12H 18N 2的苯腙用盐酸处理后生成的羰基化合物,不与多伦试剂、亚硫酸氢钠作用。
试写出该苯腙的可能结构。
6.分子式为C 8H 16化合物A ,经臭氧分解后生成B 、C 两种化合物。
B 能起银镜反应,但不起碘仿反应。
C 能与苯肼作用,但不与NaHSO 3作用。
试推导A 、B 、C 的结构。
浙江大学 动物科学(特种经济动物科学方向) 专业培养方案
浙江大学动物科学(特种经济动物科学方向) 专业培养方案培养目标本专业培养具有动物科学方面的基本知识、基本理论和基本技能,能在动物基因工程、克隆技术、胚胎移植、动物营养调控、特种经济动物产品的生产、加工和贸易等领域从事科研、教学、管理、生产和贸易等工作的知识、能力、素质俱佳,具有该领域国际视野的未来领导者。
培养要求本专业的学生主要学习现代动物科学的基本知识和基本理论,接受动物遗传繁育、营养调控、饲养管理、特种经济动物产品加工、疾病预防等基本技能的训练;具有分析和解决特种经济动物生产与经营管理实际问题的基本能力。
毕业生将获得以下几方面知识、能力和素质:1、具备扎实的数学、物理、化学和生物学等基本理论知识;2、掌握动物遗传繁育、动物营养、饲料加工、特种经济动物产品加工、经济管理和疾病预防等方面的理论知识;3、具备特种经济动物生产和动物生物技术应用的基本技能与实践能力,掌握解决特种经济动物生产实际问题的初步能力;4、了解特种经济动物产品与饲料贸易、动物防疫、环境保护等有关方针、政策和法规;5、掌握文献检索、资料查询的基本方法,具有一定的科学研究和实验工作能力;6、有较强的调查研究与决策、组织管理、口头与文字表达能力,具有独立获取知识、信息处理和创新的基本能力。
专业核心课程动物分子生物学、动物生理学、动物遗传学、动物营养学、饲料学、猪禽生产学、特种经济动物学、家蚕生物学、综合蚕丝学、蜜蜂学、水生生物资源学、生物资源工程学教学特色课程全英文教学课程:动物遗传学双语教学课程:动物营养学、家蚕生物学、动物分子生物学研究型课程:猪禽生产学、综合蚕丝学讨论型课程:动物生理学计划学制 4年毕业最低学分 160+4+5授予学位农学学士辅修专业说明辅修专业:12门课程,30学分,标注“*”号的课程。
课程设置与学分分布1、通识课程 48+5学分(1)思政类11.5+2 学分021E0010 思想道德修养与法律基础 2.5 1秋冬021E0020 中国近现代史纲要 2.5 1春夏021E0030 毛泽东思想、邓小平理论和“三个代表”重要思想概论 4 2秋冬021E0040 马克思主义基本原理概论 2.5 3秋冬02110081 形势与政策+2(2)军体类 5.5+3 学分第1、2学年的体育Ⅰ、Ⅱ、Ⅲ、Ⅳ为必修,每门课程1学分;高年级的体育课程为选修。
浙江大学有机化学乙 exercise 1
a. b. c. d.
-1 and +1 -1 and 0 0 and +1 0 and 0
25. Which one of the following species is formed when diazomethane loses a nitrogen molecule?
19. Predict which bond is the most polar in ethanol, CH3CH2OH? a. C-C b. C-H c. C-O d. O-H 15. What is the formal charge on the carbon atom?
a. b. C d.
a. b. c. d. 3
anti gauche skewed eclipsed What is the dihedral (torsion) angle between the two bromine atoms in the following sawhorse drawing?
a. b. c. d. 4
1
Organic Chemistry 2007-8 Exercise 1 Date (21/9)
5
Identify the spatial relationship of the two chlorine atoms.
a. b. c. d. 6
gauche anti eclipsed twist Which statement is correct concerning the relative stabilities of the two conformations, A and B, below?
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Organic Chemistry Exercise 7Nov. 22th within 20 min
1.Predict the effect the substituent attached to the benzene ring below would have on electrophilic aromatic
substitution reactions?
A. ortho/para director, activator
B. ortho/para director, deactivator
C. meta director, activator
D. meta director, deactivator
2.In the Friedel-Crafts alkylation of benzene, dialkylation is often a significant by-product. In the Friedel-
Crafts acylation of benzene, diacylation is not a significant by-product. Which of the following is the primary reason for this difference?
A. Alkyl groups activate the ring to further substitution, acyl groups deactivate it.
B. Alkyl groups are less sterically hindered than acyl groups.
C. Acyl cations are more difficult to make with Lewis acids.
D. Unlike acyl cations, carbocations can undergo rearrangements.
3.Which isomer of dichlorobenzene gives a single mononitration product?
A. ortho
B. meta
C. para
D. none of them
4.Salicylic acid reacts with two equivalents of ICl to give one of the products below. Which one is it? (Hint:
Cl is more electronegative than I.)
A. A
B. B
C. C
D. D
5.Identify the preferred site(s) of electrophilic attack on the following compound.
A. ortho/para positions on ring 1
B. meta position on ring 1
C. ortho/para positions on ring 2
D. meta position on ring 2
6.Which of the following is the best method to make meta-bromoethylbenzene from benzene?
A. A
B. B
C. C
D. D
7.Which one of the following compounds undergoes electrophilic aromatic sulfonation at the fastest rate?
8.What is the product of the following series of reactions?
9.What is the major product of the Friedel-Crafts alkylation of benzene with (CH3)2CHCH2Cl and AlCl3?
A. isobutylbenzene
B. tert-butylbenzene
C. sec-butylbenzene
D. butylbenzene
10.Where would the compound shown below undergo bromination with Br2/FeBr3?
A. ortho/para position on ring 1
B. meta position on ring 1
C. ortho/para position on ring 2
D. meta position on ring 2
11.Based on directing effects in electrophilic aromatic substitution reactions, predict the major addition product
of the following reaction.
12.Predict which position of the naphthalene compound below is the most reactive with electrophiles in
electrophilic aromatic substitution?
13.Starting with toluene, which of the following is the best method to make the ether shown below? (Assume
you can separate ortho and para isomers.)
14.Identify the major product(s) of the reaction sequence shown below.
A. ortho and para-chloroacetophenone
B. meta-chloroacetophenone
C. ortho and para-chlorobenzaldehyde
D. meta-chlorobenzaldehyde
15.Which point on the potential energy diagram corresponds to the species shown to the right for the
electrophilic nitration of benzene with HNO3/H2SO4?
A. A
B. B
C. C
D. D
16.Rank the following compounds in order of decreasing reactivity to aromatic electrophilic bromination.
I. benzene II. toluene III. benzoic acid IV. phenol
A. IV > II > I > III
B. IV > III > II > I
C. II > I > IV > III
D. II > III > IV > I。
