第三章 第1节 第三章第1节弱电解质的电离(选修4)
高中化学 人教版选修4 课件:第三章 第一节 第2课时 弱电解质的电离(36张PPT)

五、设计实验验证时注意等物质的量浓度和等pH的两种 酸的性质差异。
实验设计思路:以证明某酸(HA) 是弱酸为例
栏 目 链 接
尝试
应用 2.常温下,下列有关酸HA的叙述中,不能说明HA是弱 酸的是( ) ②测0.01 mol/L
栏 目 链 接
①取0.1 mol/L HA溶液,其溶液pH为2 NaA溶液,其溶液pH大于7 泡发光很暗 HA酸加水量多
第三章
水溶液中的离子平衡第一节
第一节 弱电解质的电离
第2课时 弱电解质的电离
栏 目 链 接
1.掌握弱电解质的电离平衡。
2.了解影响电离平衡的因素。
3.了解电离常数的意义。
栏 目 链 接
栏 目 链 接
要点一
1.概念
弱电解质的电离平衡
在一定条件(如温度、浓度一定)下,弱电解质在溶液中 电离成离子 __________的速率和 离子结合成分子 __________ 的速率相等,电离过程 就达到了平衡状态。 2.电离平衡的建立过程(用vt图象描述)
栏 目 链 接
多元弱酸各步电离常数大小的比较为K1≫K2≫K3,因此
多元弱酸的酸性主要由第一步电离所决定 (八字诀:分步进 行,一步定性)。
栏 目 链 接
四、一元强酸与一元弱酸的比较
♨ 特别提示:判断一种酸是强酸还是弱酸时,实质是 看它在水溶液中的电离程度,完全电离即为强酸,不完全电 离即为弱酸。
mol/L的NaA溶液,其溶液的pH大于7,说明NaA是强碱弱
酸盐,所以能说明HA是弱酸,故不选;③用HA溶液做导电 性实验,灯泡发光很暗,只能说明溶液中氢离子浓度较小,
栏 目 不能说明该酸的电离程度,所以不能说明该酸是弱酸,故选; 链 ④等体积pH=4的盐酸和HA稀释到pH=5,HA加水量多, 接
人教版新课程高中化学选修4《化学反应原理》第三章第一节《弱电解质的电离》说课稿

于培 养 学 生 应 用 化 学 知 识 解 决 实 际 问 题 的 能 力 .发 展 学 生 自 主 获 取 知 识 的 愿 望 和 能 力 ,把 知 识 学 习 、能 力培 养 与 情 感 体 验 有 机 结 合 起 来 ,实 现 自我 、社 会 与 自然 的 和 谐 有 着 广 泛 的 意 义 。
墨
Байду номын сангаас
人 教 版 新 课 程 高 中 化 学 选 修 4《化 学 反 应 原 理 》 第 三 章 第 一 节 《弱 电 解 质 的 电 离 》说 课 稿
郭 俊 辉
(通 钢 一 中 ,吉 林 通 化 134003)
一 、 解 读 课 程 标 准 .分 析 教 材 地 位 本 章 内 容 理 论 性 强 ,知 识 点 之 间 环 环 相 扣 、循 序 渐 进 ,理 论 与 实 际 、知 识 与 技 能 并 举 ,而 本 节 内 容 义 是 化 学 平 衡 理 论 的 延 伸 和 拓 展 .是 化 学 平 衡 与 溶 解 平 衡 的桥 梁 和 纽 带 ,是 学 生 学 好 本 章 的前 提 和 基 础 ,有 利 于 引 导 学 生 根 据 已有 的 知 识 和 生 活 经 验 去 探 究 和 认 识 化 学 , 激 发 学 生 探 究 和 学 习 的 兴 趣 对 于 促 进 学 生 学 习 方 式 的 多 样 化 ,建 构 自然 界 物 质 问 相 互 依 存 、相 互 制 约 的 思 想 有 着 重 要 的 作 用 。 电 离 平 衡 知 识 在 生 产 和 生 活 巾有 着 非 常 广 泛 的 应用 ,能 充 分 体 现 化 学 理 沦 对 实 际 的 指 导 作 用 .可 以让 学 生 了 解 化 学 知识 的 社 会 价 值 .对
高中化学-3.1 弱电解质的电离

3.下列各组物质的反应中,溶液的导电性比反应前明显增强的是
(A)
A.向亚硫酸钠饱和溶液中通入适量氯气 B.向硝酸银溶液通入少量HCl C.向氢氧化钠溶液中通入少量Cl2 D.向NaOH溶液中加入醋酸
4.醋酸的下列性质中可以证明它是弱电解质的是( AD )
A.1mol·L-1的醋酸溶液的C(H+)约为0.01 mol·L-1 B.醋酸与水以任意比例互溶 C.10mL 1mol·L-1醋酸恰好与10mL 1mol·L-1NaOH溶液完全反应
H++HS- K1=1.3×10-7 H++S2- K2=1.3×10-15
可记忆为: 分步进行,一步定性
因为多元弱酸的第一步电离产生的H+对其第二步、第三步 电离起抑制作用
Ka或Kb的应用②:
利用酸性相对强的酸可以制取酸性相对弱的酸原理,从K理解, 即相同条件下,K大的酸可制取K小的酸(多元弱酸看K1) 例:
(4)分析醋酸电离过程中,溶液中各粒子浓度的变化,填写下表:
粒子浓度
c(H+)
醋酸初溶于水 达到电离平衡前 达到电离平衡时
_接__近__于__0 增__大__ _不__变_
c(CH3COO-) _接__近__于__0 _增__大_ 不__变__
c(CH3COOH) 最__大__ _减__小_ _不__变__
0.1 mol·L-1的醋酸溶液中加水稀释时, 图像如下, 电
离程度_变__大__,离子浓度 __变__小____导电能力_变__小__
O点的导电能力为什么不为0?
O点含水,醋酸是共价化 合物,在水中能电离
讨论完成表格:HAc
Ac- + H+ HAc为CH3COOH的简写
弱电解质的电离 说课
一、强弱电解质
强电解质:在水溶液里全部电离成离子的电解质..如强碱、强酸和绝大多数盐.. 弱电解质:只有一部分分子电离成离子的电解质..如弱酸、弱碱和水..
二、弱电解质的电离平衡
为例 CH3COOH
CH3COO - + H+
2、在一定条件如温度、浓度下;当电解质分子电离成离子的速率和离子重新 结合生成分子的速率相等时;电离过程就达到了平衡状态;这叫电离平衡..
H2SO3>H3PO4>HF>CH3COOH>H2CO3>H2S>HClO
小 结 §3.1 弱电解质的电离
一、强弱电解质
强电解质 弱电解质
二、弱电解质的电离
电离平衡状态 电离平衡状态的特征 电解质的电离方程式的书写 影响电离平衡的因素 电离平衡常数
板书设计
第三章 水溶液中的离子平衡
第一节 弱电解质的电离平衡
cH+ 小
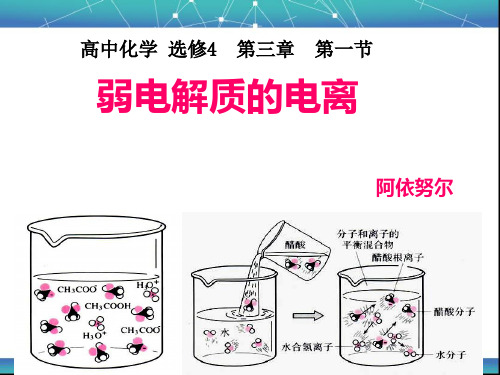
盐酸与醋酸在水中的电离示意图
盐酸在水中的电离示意图 醋酸在水中的电离示意图
溶液
溶液里 的粒子
H2O、H+ 、Cl-
H2O、CH3COOH H+、CH3COO-
§3.1 弱电解质的电离
一、强弱电解质
强电解质
弱电解质
定义
在水溶液中能够全 部电离的电解质
在水溶液中部分电离的 电解质
物质类别
电离特点
2. 意义:K值越大;电离程度越大; 相应酸 或碱的酸或碱性越强..
3.K 值只随温度变化..
探究实验: 向两支分别盛有0.1mol/L醋酸和饱和硼酸
溶液的试管中滴加等浓度Na2CO3溶液;观察现 象..
CH3COOH+Na2CO3=
化学选修4:第三章第一节 弱电解质的电离(第一课时)

盐酸完全电离, 电离程度(即电离度)为100%; 醋酸不完全电离, 电离程度较小,且小于100%, 即醋酸的电离是可逆的。
东北师大附中高中部化学组 柳西
盐酸中存在H+、Cl无HCl分子
醋酸溶液中存在 H+、CH3COO和CH COOH分子 东北师大附中高中部化学组 柳西 3
电解质有强弱之分
分别试验等体积、等浓度的盐酸、醋酸溶液与等量 镁条的反应;并测这两种酸的pH
醋酸
盐酸
对实验现象的解释
溶液的pH 与镁条反应
东北师大附中高中部化学组 柳西
【实验3-1】分别实验等体积、等浓度的盐酸、 醋酸与等量镁条的反应。 【实验要点】 盐酸和醋酸浓度均为1mol/L; 镁条用砂纸打磨、长度相同(表面积相同); 观察、比较气球鼓起的快慢等现象。
东北师大附中高中部化学组 柳西
讨论以下几种说法是否正确,并说明原因。 1.石墨能导电,所以是电解质。 2.由于BaSO4不溶于水,所以不是电解质 3.盐酸能导电,所以盐酸是电解质。 4.SO2、NH3、Na2O溶于水可导电,所以均 为电解质。
东北师大附中高中部化学组 柳西
【练习】
• 电解质:
②③④⑧⑩⑿
【例6】下图为一定量的冰醋酸加水稀释的变化 曲线思考: (1)稀释过程中,溶液的导电能力将如何变化? 先变大后变小 (2)稀释过程中,冰醋酸的电离程度如何变化? 一直变大 (3)若将冰醋酸改为1mol/L的醋酸溶液,c(H+)将 如何变化? C(H )
+
一直变小直至平衡
东北师大附中高中部化学组 柳西
东北师大附中高中部化学组 柳西
三、影响电离平衡的因素
(1)内因:电解质本性。通常电解质越弱, 电离程度越小。 (2)外因: A.浓度:浓度越大,电离程度 越小 。 在稀释溶液时,电离平衡 向右 移动,而 离子浓度一般会 减少 。 B.温度:温度越高,电离程度 越大 。 因电离是 吸 热反应。
高中化学:3.1《弱电解质的电离》教案(新人教版选修4)

第一节弱电解质的电离一、教学设计本章引言开门见山地指明了即将进一步研究的知识范围——酸、碱、盐在水溶液中发生的离子反应及其影响因素,并简要揭示了应用这类反应的广泛领域,给人以开阔的视野,感受到天地之间的生态平衡、自然奇观、矿产资源以及许多现代科技的应用都与离子的存在、迁移和物质间的转化有着密切联系。
使学生意识到:整个自然界实际就是各类物种相互依存、各种变化相互制约的复杂的平衡体系,而离子平衡就是其中的一个重要方面。
这种理念在教学中的贯彻对学生在学习过程中开阔思路、完善知识体系是有帮助的。
从具体知识结构来看,化学平衡、电离平衡、溶解平衡是研究电解质在溶液中发生各种变化的理论基础,而电离理论又是联系化学平衡与溶解平衡的纽带。
因此,本节知识对于后续章节的学习有着重要的指导作用。
本节包括两大部分:一是“电解质有强弱之分”;二是“弱电解质的电离过程是可逆的”,并存在着电离平衡。
要求学生在已经学过化学平衡理论并了解电解质发生电离和发生离子反应的条件等知识的基础上,进一步学习强电解质和弱电解质的概念,了解强、弱电解质与酸、碱、盐在物质类别方面的联系,及弱电解质的电离平衡以及浓度等条件对电离平衡的影响。
本节教学重点:强、弱电解质的概念和弱电解质的电离平衡。
本节教学难点:弱电解质的电离平衡。
教学建议如下:1.新课导入。
可以依据引言选择几幅有代表性的画面展示自然奇观和科技时事资料,帮助学生了解:为什么说地球上广阔的水域是离子反应广泛存在的先决条件,为什么说离子反应是了解生命过程的基础,以及研究离子反应在现代化工生产和环保建设中有何意义。
2.【实验3-1】的目的是帮助学生建立强电解质和弱电解质的概念,是本课的基本要求,实验中应强调以下知识点:(1)HCl和CH3COOH都是电解质,在水溶液中都能发生电离;(2)镁无论是与盐酸还是醋酸反应,其实质都是与溶液中的H+反应;(3)由于酸液浓度、温度、体积均相同,且镁条的量也相同,因此,实验中影响反应速率的因素只能是溶液中c(H+)的大小,通过对溶液pH的测定也能证实这一点;(4)对于学习基础较好的学生,可以向他们说明pH的实际意义是指溶液中c(H+)的负对数,以利于学生对盐酸中HCl的完全电离有更为确切的理解。
化学:第三章第一节《弱电解质的电离》原创课件(人教版选修4)

③同离子效应
加入同弱电解质电离所产生的离子相同 离子,电离平衡向逆方向移动
④化学反应
加入能与弱电解质电离产生的离子反应的 物质时,使电离平衡向电离方向移动
思考与讨论:
NH3+H2O
NH3·H-2O
NH4+ + OH
例:在氨水中存在怎样的电离平衡?若向
其中分别加入:
①升高温度
②加氨气
③水
④ NH4Cl溶液
问题:怎样定量的比较弱电解质的相
对强弱?电离程度相对大小怎么比较?
第三课时三、电离平衡常数(K)
看课本自学相关内容并思考: (1)什么叫电离平衡常数? (2)电离平衡常数的化学含义是什么? (3)怎样用电离平衡常数比较弱电解质的相 对强弱? (4)影响电离平衡常数的因素是什么?
知识回顾:
一、电解质与非电解质
电解质
在水溶液中或熔融状态下能 导电的化合物
(如:酸、碱、盐、水、大多数金属氧化物、 活泼金属过氧化物)
非电解质 在水溶液中和熔融状态下都不 导电的化合物
(如:多数有机物、某些非金属氧化物、某些非 金属氢化物如 NH3 等 )
物质
混合物
单质 纯净物
化合物
既不是电解质也 不是非电解质
冰醋酸加水稀释,醋酸在稀释的 过程中微粒的变化包含哪些过程?
CH3COOH
电离 结合
CH3COO - + H+
1、弱电解质的电离
CH3COOH
离子化 分子化
CH3COO - + H+
醋酸在电离过程中各微粒浓度的变化
C(H+)
HAc初溶于水 0
紧接着
最后
不变
高中化学 人教版选修4 课件:第三章 第一节 第1课时 强弱电解质(36张PPT)

5.强、弱电解质在熔融态的导电性: 离子型的强电解质由离子构成,在熔融态时产生自由移 动的离子,可以导电;而共价型的强电解质以及弱电解质 由分子构成,熔融态时仍以分子形式存在,所以不导电。
栏 目 链 接
尝试
应用
1 .下列物质的水溶液能导电,但属于非电解质的是
( ) A.CH3COOH C.NH4HCO3 B.Cl2 D.SO2
栏 目 链 接
尝试
应用 解析:选项中的四种物质的水溶液都能导电,但原因有 所不同。CH3COOH和NH4HCO3均为电解质,水溶液理应 能导电;Cl2和SO2水溶液能导电,是因为它们与水反应的生
成物均为电解质,故溶液也导电(Cl2+H2O
SO2+H2O 为非电解质。 答案:D
HCl+HClO,
H2SO3)。电解质和非电解质都属于化合物,
栏 目 链 接
♨ 特别提示: 1. 强、弱电解质的范围: , 强电解质:强 酸、强碱、绝大多数盐,弱电解质:弱酸、弱碱、水。 2. 强、弱电解质与溶解性的关系: , 电解质的强弱取决 于电解质在水溶液中是否完全电离,与溶解度的大小无关。 一些难溶的电解质,但溶解的部分能全部电离,则仍属强电 解质;如:BaSO4、BaCO3等。
栏 目 链 接
Cl2是单质,它既不是电解质又不是非电解质,因此只有SO2
要点二
强弱电解质电离方程式的书写
电离:电解质在水溶液或熔融状态下离解成自由移动离 子的过程。电离不需要通电,且一般为吸热的。电离方程式 的书写如下: 1.强电解质 完全 电离,符号用“________” ,如 HCl_________________________________________________ === H++Cl- _______________________; CH3COONH4____________________________________ ===CH3COO-+NH ____________________________________; Ba(OH)2_________________________________________ ===Ba2++2OH- _______________________________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三章第1节弱电解质的电离
课前预习学案
一、预习目标:
1. 了解电离、电解质、强电解质和弱电解质的概念
2. 了解弱电解质在水溶液中的电离平衡
3. 初步了解电离平衡常数及其意义。
二、预习内容:
阅读课本P39---P43内容,完成以下预习内容。
⒈电解质:(思考比较非电解质)_____________________________ _______ ___ 强电解质:___________________________ _
弱电解质
2.写出下列物质的电离方程式:
NaCl:__________________________ NaOH :____________________________
H2SO4:_______________ ___ NaHCO3____________________________ NaHSO4(水溶液):__________________________
3.思考并完成课本实验3-1表格
1mol/LHCl 1mol/LCH3COOH 与镁条反应现象
溶液的pH值
4.结合下图分析醋酸溶液的电离平衡的建立,并试着填写P42表格空白。
5.写出下列弱电解质电离方程式:
NH3·H2O:_____________________ __________
H2O:___________________________________
CH3COOH: ______________________________
6.阅读科学视野,思考电离平衡与化学平衡有何联系?
电离常数:叫做电离常数。
根据实验3-2和弱酸的电离常数,判断推测醋酸、碳酸和硼酸三种弱酸的相对强弱有几种方法?
多元弱酸的电离是分步进行的,试写出碳酸的分步电离的方程式,并写出电离常数的表达式。
思考:多元弱碱Al(OH)3的电离是分步的吗?
三、提出疑惑
同学们,通过你的自主学习,你还有哪些疑惑,请把它填在下面的表格中
疑惑点疑惑内容
课内探究学案
一、学习目标:
1.记住电解质、强电解质和弱电解质的概念,学会区分强弱电解质。
2.会正确书写弱电解质的电离方程式。
3.会分析弱电解质在水溶液中的电离平衡及平衡的影响因素
4.了解电离平衡常数及其意义。
二、学习重难点:正确书写弱电解质的电离方程式并分析弱电解质在水溶液中的电离平衡及影响因素
三、学习过程
实验探究1:相同浓度的盐酸和醋酸PH值相同吗?与镁条的反应现象相同吗?
实验3-1演示讨论,完善预习学案表格。
我们的结论是:。
讨论:
1.HCl和CH3COOH的浓溶液在水中的电离程度如何?
2.用下图解释醋酸电离平衡的形成过程。
3.写出醋酸的电离方程式。
精讲点拨:电离平衡:在一定条件(如温度、浓度)下,当电解质分子电离成离子的速率和离子重新结合生成分子的速率相等时,电离过程就达到了平衡状态,这叫电离平衡。
