7章-芳烃10.4
第七章-芳烃-习题-答案
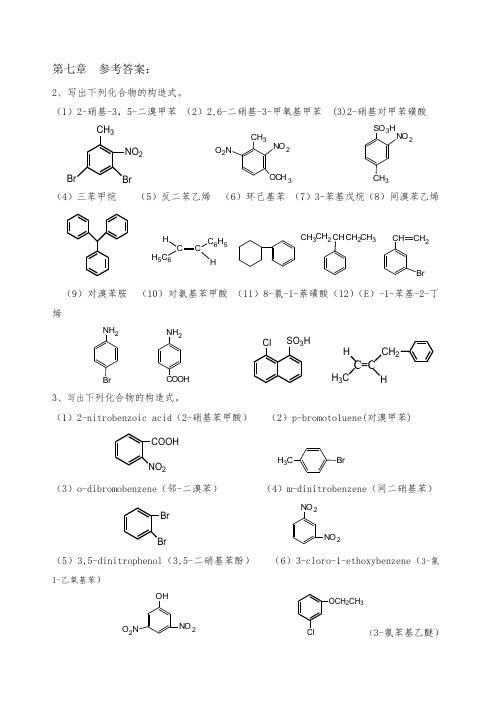
第七章 参考答案:2、写出下列化合物的构造式。
(1)2-硝基-3,5-二溴甲苯 (2)2,6-二硝基-3-甲氧基甲苯 (3)2-硝基对甲苯磺酸CH 3NO 2BrBrCH 3NO 2O 2NOC H 3SO 3HNO 23(4)三苯甲烷 (5)反二苯乙烯 (6)环己基苯 (7)3-苯基戊烷(8)间溴苯乙烯CCC 6H 5H 5C 6HH CH 3CH 2CHCH 2CH 3CHCH 2Br(9)对溴苯胺 (10)对氨基苯甲酸 (11)8-氯-1-萘磺酸(12)(E )-1-苯基-2-丁烯NH 2BrNH 2SO 3HClC=CHHH 3CCH 23、写出下列化合物的构造式。
(1)2-nitrobenzoic acid (2-硝基苯甲酸) (2)p-bromotoluene(对溴甲苯)COOH NO 2CH 3Br(3)o-dibromobenzene (邻-二溴苯) (4)m-dinitrobenzene (间二硝基苯)BrBrNO 2NO 2(5)3,5-dinitrophenol (3,5-二硝基苯酚) (6)3-cloro-1-ethoxybenzene (3-氯1-乙氧基苯)OHNO 2O 2NOCH 2CH 3(3-氯苯基乙醚)(7)2-methyl-3-phenyl-1-butanol (2-甲基-3-苯基1-丁醇)CH 3CHCHCH 2OHCH 3(8)p-chlorobenzenesulfonic acid (对氯苯磺酸)(9)benzyl bromide (苄基溴)SO 3HClCH 2Br(11)o-xyene (邻二甲苯)(12)tert-butylbenzene (叔丁基苯)(13)p-cresol (对甲苯酚)CH 3CH 3C(CH 3)3CH 3OH (14)3-phenylcyclohexanol (3-苯环己醇)(15)2-phenyl-2-butene (16)naphthalene(萘)HO5、写出下列反应的反应物构造式。
第七章 芳烃

7.1 芳烃的分类
芳烃按其结构分为四类:
单环芳烃 苯 甲苯 H C 联苯 三苯甲烷 CH3 CH3 二甲苯 CH3
芳烃
多环芳烃
稠环芳烃 萘
非苯芳烃
菲
7.2 单环芳烃的构造异构和命名
7.2.1 构造异构
一元取代只有一个结构式,二、三、四元取代各有 三个异构体。例:
CH3
甲苯
CH2CH3
乙苯
CH(CH3)2
SO3H SO3H
+ H2O
CH3 + H2SO4(浓) 室温
CH3 SO3H +
CH3
32%
SO3H 62%
苯环上已有一个-SO3H后,苯环钝化,且第二个基团上间位;
苯环上已有一个-CH3后,苯环活化,且第二个基团上邻、对位。
注意:磺化反应可逆!
+ H2SO4(浓) 800C 180 C
0
SO3H
(a) 硝化反应机理
硝化反应中进攻试剂是NO2+,浓硫酸的作用是促进 NO2+的生成:
HOSO2OH + HO-NO2 H-O-NO2 H
+
H-O-NO2 + HSO4H
+
+
NO2 + H2O
亲电试剂
NO2
+ NO2
+
+
H
-H+
NO2
σ-络合物
(b) 卤化反应机理
无Fe或FeX3存在时,苯不与溴或氯发生反应,所以苯 不能使溴的四氯化碳溶液褪色。 但有Fe或FeX3存在时,苯可与溴或氯发生反应,其中 FeX3的作用是促进X2极化离解:
有机化学第七章 芳烃

H
H
H
H
H
H
可以解释:为什么苯分子特别稳定? 为什么苯分子中碳碳键长完全等同? 为什么邻位二取代物只有一种?
(b)分子轨道理论 分子轨道理论认为:苯分子形成σ键后,苯的
六个碳原子上的六个P 轨道经线性组合可以形成六 个分子轨道,其中ψ1 、ψ2 和ψ3 是成键轨道,ψ4、 ψ5和 ψ6是反键轨道。当苯分子处于基态时六个电 子填满三个成键轨道,反键轨道则是空的。
-络合物
(b)硝化反应
2 H2SO4 HNO3
NO2
HNO3 H2SO4,45℃
CH3
HNO3 H2SO4,30℃
NO2
CH3 NO2
CH3
NO2
HNO3 H2SO4,95℃
NO2
NO2
NO2
H3O 2 HSO4
反应比苯容易 反应比苯困难
硝化反应机理
硝化反应中进攻试剂是NO2+,浓硫酸的作 用促进NO2+的生成:
苯环的特殊稳定性可以从它具有较低的氢化热 得到证明:
环己三烯氢化热=360kj/mol(假想值) 苯环氢化热=208kj/mol 相差152kj/mol
氢化热简图:
环己三烯+3H2
环己二烯+2H2
苯+3H2
环己烯+H2
231kj/mol
120kj/mol
208kj/mol
360kj/mol
环己烷
苯分子的近代概念
ቤተ መጻሕፍቲ ባይዱ
(1)煤的干馏
煤隔绝空气加热至1000~1300℃时分解所得到的 液态产物——煤焦油,其中含有大量芳烃化合物。 再经分馏得到各类芳烃。
馏分名称 轻油 酚油 萘油 洗油 蒽油
有机化学第七章 芳烃

1
一、教学目的和要求 通过对本章的学习,掌握芳烃的定义、分类、苯的结构、 闭合共轭体系、芳香性及苯的同系物的命名,掌握苯环上 的亲电取代反应及定位规则,侧链卤代和氧化反应,掌握 萘的结构及命名,萘的亲电取代反应、氧化反应;熟悉休 克尔规则及非苯芳烃的芳香性判断;了解联苯、蒽、菲的 结构及命名以及苯及其同系物的主要物理性质(易燃性)。 二、教学重点内容 芳烃的结构、闭合共轭体系、命名、亲电取代反应及其定 位规律、侧链氧化、萘的结构、命名及亲电取代反应、非 苯芳烃芳香性的判断是本章的重点。
CH3 CH3 CH3
(1)单环芳烃
苯 甲苯 间二甲苯
(2)多环芳烃
连 苯 三
C H 苯 甲
烷
(3)稠环芳烃
萘 蒽 菲
4
5.1
芳烃的构造异构和命名
5.1.1 构造异构
苯及其同系物的通式为:CnH2n-6。 例如苯有六个碳和六个氢,其六个碳和六个氢是等同的; 结构异构: 一元取代:只有一种
CH3 CH CH2 H3C CH CH3
(a)
(b) (c) (d) (e)
卤化
硝化 磺化 Friedel-Crafts反应 氯甲基化
17
(1)亲电取代反应
(a) 卤化
苯环上和卤代反应较困难,常用FeX3(Lewis酸)作催化剂。
+ Cl2
FeCl3,25oC 90%
Cl + HCl
控制苯过量,不要太激烈,避免二卤代。 因是亲电反应,所以苯的同系物(甲苯)比苯更易反应。 Cl 卤代活性: F2>Cl2>Br2>ICH CH3 CH3 CH3 2。 3
14
5.3
单环芳烃的物理性质
有机化学第七章 芳烃

2-甲基-3-苯基戊烷 2-methyl-3-phenylpentane
烃链上含有多个苯环时,一般 把苯作取代基,烃作母体。
C H
三苯甲烷
2. 二烃基取代苯:有三种异构体,取代基的位置可以用 阿拉伯数字标出,或用邻、间、对(o-, m-, p-)表示。
CH3 CH3
CH 3 CH3
CH3
CH3
1, 2-二甲苯 1, 3-二甲苯 1, 4-二甲苯
O + N + O
H
E
⑤原子不具有完整的价电子层且带电荷的极限结构稳定性 差,对真实分子贡献小。 CH2=O-CH3 · ·
稳定 +
CH2-O-CH3
不稳定 碳不具有完整的价电子层
+
在共振式中,稳定的经典结构式越多,其杂化体越稳定。 4. 关于共振论应用的几点说明: ①共振论在有机化学上有重要的作用,能解释并预测一些 有机化合物的基本的化学性质; ②共振论是一种理论,共振式是理论上存在的,无法测得; ③共振论引入了一些人为规定,对某些化学现象尚不能给
苄基(Benzyl):甲苯的甲基上去掉一个H后的基团,用Bz 表示。
CH2
苯 Benzen 苯基 phenyl 苄基 benzyl ( phenyl methyl)
CH2Cl
苄氯(氯化苄) Benzyl chloride
三、芳香族化合物
1. 取代基若为硝基或卤素,应以苯环为母体来命名。
NO2
Br
共振能152kJ/mol 共振能12kJ/mol
(3)不同的极限式对共振杂化体的贡献大小不一样,能量 越低、越稳定的极限式的贡献越大。
+
贡献大 贡献小
(4)这些极限结构式均不是这一分子、离子或自由基的真 实结构,其真实结构为所有经典结构式的共振杂化体。
有机化学第七章 芳烃

苯甲醛 benzaldehyde
COOH
苯甲酸 benzoic acid
SO3H
苯磺酸 benzenesulfonic acid
29
有两种以上取代基时,选择母体的顺序为:
—OR,—R,—NH2,—OH,—COR,—CHO, —CN,—CONH2,—COCl,—COOR,—SO3H, —COOH,正离子等。
NH2
对氨基苯磺酸 4-aminobenzenesulfonic acid
SO3H
31
苯环上连有三个及三个以上取代基时,只能用阿拉伯数 字编号。
COOH
O2N
NO2
3,5-二硝基苯甲酸 3,5-dinitrobenzoic acid
NH2 CH3
2-甲基-4-氯苯胺 4-chloro-2-methylaniline
16
(3) 对共振杂化体中不同经典结构式的贡献 越稳定的经典结构式在共振杂化体中占的分量越大。 经典结构式稳定性的确定: 共价键数目最多的经典结构式最稳定; 经典结构式的正负电荷越分散越稳定,即电荷分离的经 典结构式稳定性差; 经典结构式中所有原子都具有完整的价电子层的较稳定; 负电荷在电负性大的原子上的经典结构式较稳定。
CH3
CH2CH3
CH(CH3)2
甲苯 methylbenzene
乙苯
异丙苯
ethylbenzene propan-2-ylbenzene
23
烃基较复杂或有不饱和键时,把链烃当作母体,苯环 作为取代基。
苯基的英文名称为 phenyl。
CH2CH CH2
CH3CH2CHCH(CH3)2
3-苯基-1-丙烯 3-phenylprop-1-ene prop-2-en-1-ylbenzene
Cp07-芳烃

AlCl3 0 C
o
CH2CH2CH3 + 30 %
+
–
CH(CH3) 2 70 %
+ 重排 +
CH3CH2CH2 Cl AlCl 3
– + AlCl CH3CH2CH2 4
CH3CHCH3
◎
2、酰基化反应
O R C X + AlX3
+
O 无水AlX3 + R C X
(2) 参与共振的极限式必须符合下列原则:
z 价键原则:必须遵循价键理论 z 原子核的相对位置不变原则 (构型不变原则) z 成对电子数或未成对电子数不变原则 z 共振体系中原子的共平面原则
共振论(Resonance theory)的基本要点 (3) 对于某一化合物分子来说,每个极限式对共振杂 化体的贡献是不同的,越稳定的极限式,贡献越 大,与共振杂化体的结构越接近。
P2O5
R C O C R (RCO)2O 酸酐
O 无水AlCl 3 + CH3CH2 C Cl (1.7eq.)
O O
84 %
O C CH2CH3
多聚磷酸
+ CH3 C O C CH3
无水AlCl3 (>2eq.)
85 %
O C CH3
COOH O
Friedel-Crafts 酰基化反应
O 无水AlX3 + R C X
H3C
苄基 (benzyl)
C6H5CH2
Bz
邻甲苯基
o-CH3C6H4
间甲苯基
m-CH3C6H4
对甲苯基
p-CH3C6H4
第七章芳烃

注意:①各经典结构式之间只是电子排列不同;②共 振杂化体不是经典结构式混合物;③共振杂化体也不是 互变平衡体系。
共振论
基本要点如下: 3.书写极限式必须遵守一定的规则:
(3)在所有极限式中,未共用电子数必需相等。
CH3
间甲基苯胺
3-甲基苯胺
NH2 m-toluidine
NH2
对氨基苯磺酸
SO3H
OH
邻氯苯酚
Cl 2-氯苯酚
COOH NO2
间硝基苯甲酸 m-nitrobenzoic acid
COOH
O2N
NO2
3,5-二硝基苯甲酸 3,5-binitrobenzoic acid
NO2 Cl
SO3H CHO
Organic Chemistry
第七章 芳烃 (aromatic hydrocarbons)
第七章 芳 烃
制备
研究思路
分类和命名
性质
结构
研究重点放在芳环官能团上。
芳香烃的分类
H3C CH CH3 CH2 CH3
H C CH2
单环芳烃
苯
系
苯
乙苯
异丙苯
苯乙烯
芳
烃
联苯
芳
联苯
对三联苯
香
多环芳烃
烃
稠环芳烃
CH2CH3
思考题
H+ OH
H3C CHCH2Cl
AlCl3
?
H3C
能产生碳正离子的试剂均可,例:卤代烷、烯烃、醇等。 但卤代苯、乙烯卤不能做烷基化试剂
Cl
C C Cl
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(CH)x , x>=10
H H HHH
[18][18]-轮烯
H
芳香性
化合物的结构为:环状平面的共轭体系,其 化合物的结构为:环状平面的共轭体系, 平面的共轭体系 中π电子数等于4n+2 (n=0,1,2……)。这个规则 电子数等于4n 4n+ 称为Huckel规则。 称为Huckel规则。 Huckel规则
(Aryl), Ar表示 表示。 三、芳基 (Aryl),用Ar表示。
CH2
C6H5
Ph或φ 或 苯基
phenyl
C6H5CH2 Bz 苯 甲基 或 苄基
benzyl ( phenyl methyl)
第三节 单环芳烃的化学性质
一、亲电取代反应
1. 硝化反应
NO2
H2SO4 55-60 C -
。
+ HONO2
一、休克尔规则(Huckel’s Rule) 休克尔规则(Huckel (Huckel’
1.芳香性 1.芳香性
环丁二烯
环辛四烯
2.含(4n+2)个 2.含(4n+2)个π电子的芳烃实例
环丙烯正离子
萘
蒽
HH
[10]-轮烯 [10]-
H
HH
H
[14][14]-轮烯
轮烯:具有交替的单双键的单环多烯烃 轮烯:
70%
CH3CH2CH2
重排
CH3CHCH3
二、反应不易控制在一元取代阶段,常常得到 反应不易控制在一元取代阶段, 一元、二元、 一元、二元、多元取代产物的混合物
CH3
CH3Cl AlCl3
CH3 CH3 +
CH3
CH3
CH3Cl AlCl3
CH3
CH3 CH3
烷基化试剂除卤代烃外还有: 烷基化试剂除卤代烃外还有:
A)傅-克烷基化
+ C2H5Br
无水AlCl3
C2H5 + HBr
烷基化历程
CH3CH2Cl
+
AlCl3
_ δ+ δ CH3CH2AlCl4
+
亲电试剂
CH3CH2 + AlCl4
_
傅-克烷基化反应的特点
一、烷基化反应易发生重排
+ CH3CH2CH2Cl
AlCl3
CH2CH2CH3 +
30%
+ +
CH(CH3)2
CH3 CH3 CH3
CH3
H3C
CH3ห้องสมุดไป่ตู้
3.几个取代基不同类型: 3.几个取代基不同类型: 几个取代基不同类型
确定主官能团 见P152
CH3
OH
CHO
COOH
对甲苯甲酸
NH2
2-氨基-5-羟基苯甲醛 氨基-
4.苯环为取代基的情况 4.苯环为取代基的情况
CH3
CH3 CCH2CH2CH2CH3
2-甲基-2-苯基己烷 甲基-
三、苯分子结构的共振论解释
苯的共振式
Dewar 苯
(1)
(2)
+
(3)
(4)
极限式又称为 共振贡献式
(5)
_
…….
极限式的书写原则: 极限式的书写原则: P149
1. 原子核的位置必须相同,只允许电子的排布有 原子核的位置必须相同, 差异。 差异。 2.共振结构必须符合价键的规则 2.共振结构必须符合价键的规则 3. 各极限式必须具有相同数目的未共用电子数
H H C C C C H C C H
简写为:
H
H
二、苯分子结构的价键解释
H H H
0.1 39 7n m
。 120
0.109nm
C:SP2杂化
H H
H
苯的平面正六边形构型
BENZENE
氢化热 120kJ/mol 208kJ/mol
- = ( ) 离域能, 离域能,共轭能 120× 3-208=152(kJ/mol)
B) 傅-克酰基化
酰基化历程
酰基化反应不会发生重排
CH3
二、侧链上的氧化反应 侧链上的氧化 氧化反应
COOK
CH(CH3)2
KMnO4 OH-
C(CH3)3
×
KMnO4 OH-
三、加成与还原反应
1. 加氢
2. 与氯加成
第四节 苯环的亲电取代定位规则
一、定位基分类 P165
邻对位定位基 间位定位基
亲电 试剂
NO2 + +H
O N O
NO2
+ HNO3(发烟) 发 H2SO4(浓) 浓
NO2
NO2 93%
2. 卤代反应
催化剂:Fe粉或FeX 催化剂:Fe粉或FeX3 粉或
X
+ X2
Fe or FeX3
卤苯
+ HX
卤代反应历程(以溴代为例) 卤代反应历程(以溴代为例)
+ Br
2
FeBr3
Br Br
+ H2O 硝 基苯
硫酸起何作用? 硫酸起何作用?
硝化反应历程
P154
H2O NO2 + HSO4+ NO2
+
H2SO4 + HONO2
H2O NO2
+
slow
+ H2O
+ HSO4
-
H2O + H2SO4
2H 2SO4 HNO3
H3O +
H3 O
+
2HSO4
NO2+
+ NO2
NO2 H
σ-络合物
第七章 芳 烃 Aromatic hydrocarbon
芳烃: 芳烃:芳香族碳氢化合物 通常所说的芳烃是指苯系芳烃。 通常所说的芳烃是指苯系芳烃。
第一节 苯的结构
一、苯的Kekule式 苯的Kekule Kekule式
苯的分子式: 苯的分子式:C6H6 1865年 Kekule式 1865年,Kekule式
(1)两个定位基同类 (1)两个定位基同类
NH2
COOH
CH3
NO2
(2)两个定位基不同类 (2)两个定位基不同类
NHCOCH3
NO2
例1
NO2
Cl
A)硝化、氯代 硝化、 B)氯代、硝化 氯代、
•√
例2
CH3 O2N COOH NO2
磺化、硝化、脱磺酸基、 磺化、硝化、脱磺酸基、氧化
第七节 非苯系芳烃
δ+
δ_
FeBr3
Br H
+
Br + H
Br
+
FeBr3
芳烃侧链卤代
CH3 Cl2 hν 或高温
CH2Cl
3. 磺化反应
SO3H
H2SO4, SO3 30-50 C -
。
+ H2O 苯磺酸
磺化反应历程
2 H 2SO4
+ H 3O +
HSO4
-
+
SO3
亲电试剂
4. Friedel-Crafts反应 Friedel-Crafts反应
OH
+C\> -I
(3)氯苯 (3)氯苯
Cl
-I > +C
2. 间位定位基
(1)硝基苯 (1)硝基苯 a.用电子效应解释 a.用电子效应解释
N O
O
-C -I
三、二取代苯的定位规律
1. 两个取代基定位效应一致
CH3
CH3
位阻大
NO2
Cl
2.两个取代基定位效应不一致 2.两个取代基定位效应不一致
kC6H5Z/C6H6
速率常数
>1
致活基
<1
钝化基
二、取代定位效应解释
1.邻对位定位基 1.邻对位定位基
(1)甲苯 (1)甲苯 a.用电子效应解释 a.用电子效应解释
0.96
CH3
1.017 0.999 1.011
+C +I
b.中间体的稳定性- b.中间体的稳定性-共振论解释 中间体的稳定性
(2)苯酚 (2)苯酚
共振的结果使键长平均化, 共振的结果使键长平均化,使体系能量降低
第二节 单环芳烃的同分异构和命名
一、一取代苯的命名 二、二取代苯的命名
1. 2个取代基相同: 2个取代基相同: 个取代基相同
CH3 CH3
CH3
CH3
CH3
CH3
3个取代基相同 个取代基相同: 2. 3个取代基相同:
CH3 CH3 CH3
