第11章 多肽与蛋白质类药物
生物制药多肽与蛋白质类药物

• c.种子摇瓶培养 在4个1000mL三角瓶中, 分别装入250mL种子培养基,分别接种人干 扰素αⅡb基因工程菌,30℃摇床培养10h,
第28页/共46页
• d.发酵培养基 1%蛋白胨、0.5%酵母提取物、 0.01%NH4Cl、0.05%NaCl,0.6% Na2HPO4、0.001%CaCl2、0.3%KH2PO4、 0.01%MgSO4、0.4%葡萄糖、50mg/ml氨 苄西林、少量消泡剂。
第9页/共46页
• 沉淀4加原体积l/25000量pH=8.0的 0.1mol/L PBS溶解,调至pH=7~7.5,对 PBS(pH=7.3)透析,过夜,离心,收集上清液, 检测,得IFN-B。上清液3中加盐酸使pH值降 至3.0,离心,得沉淀5。沉淀5加入原体积 1/5000量的pH=8、0.1mol/L PBS溶解,加 NaOH调节pH=7~7.5,对PBS(pH=7.3)透 析过夜,离心收集上清液,检测,得IFN-A。 每份灰黄层约能制备100万单价的纯化干扰素。
第10页/共46页
• 此法特点是一次纯化量大,回收率高于60%; 经济,简便,易于普及。效价可达1.2×108 U/ml,比活2.2×106 U/mg(蛋白)。IFNA中干扰素含量占回收干扰素的82%,比活 也比较高。IFN1的比活较低[5×104 U/mg (蛋白)],一般可作外用滴鼻剂或点眼剂等。
第14页/共46页
• 将0.5µg平头末端cDNA用末端转移酶加15 个dC,并将2µg质粒pBB322在PstⅠ位点 线性化,用末端转移酶加15个dG,再将两者 连接,利用这种方法可产生新的PstⅠ位点, 利于从载体上再次切下cDNA。将产生的质 粒转化大肠杆菌HB101后,用微量板培养。 合成引物5′-CCTTCTGGAACTG- 3′,该序 列是IFN-α、β最长的不间断保守序列,用其 作引物可同时调出IFN-α、β。
多肽与蛋白质类药物

B. 对蛋白质类药物进行结构修饰
多肽、蛋白质类药物分类
3.3.1 反相高效液相色谱
3.3.1 反相高效液相色谱
分离机理:
①用C4~C8烷基作配基,将配基键合在固定基质上作为固定相 ,以水溶性有机溶剂(如甲醇、乙腈、异丙醇)加强酸作流 动相(流动相极性大于固定相)。
②蛋白质分子中既有亲水性基团(-OH,-NH、-COOH、SH 等),也有疏水性基团(如苯环、-CH3、-CH2和-CH等)。
理论上,每公顷红花田可生产出1公斤人胰岛素原料药。
3.2 多肽和蛋白质药物的生产方法
加拿大渥太华大学生物技术研究中心的科研人员也利 用另两种高产作物——烟草和水稻植株生产出了一种 名为“胰岛素样生长因子”(ILGF)的新型降血糖药物 。
据称,ILGF的降糖效果甚至优于常规口服降糖药。 如果ILGF能通过临床试验并成功上市,或将成为前景
3.2 多肽和蛋白质药物的生产方法
加拿大SembioSys生物工程公司利用北美洲普遍栽培的高 产油料作物——红花作为转基因植物“平台”,成功生 产出“红花子来源人胰岛素”,
该胰岛素顺利通过动物实验与Ⅰ~Ⅱ期临床试验,其药 代动力学与药效学试验结果与美国礼来利用大肠杆菌表 述胰岛素基因生产的重组DNA人胰岛素基本一样。
多肽和蛋白质的物化性质
4. 变性 ➢ 天然蛋白质的严密结构在某些物理或化学因素作用下,
其特定的空间结构被破坏,从而导致理化性质改变和生 物学活性的丧失,如酶失去催化活力,激素丧失活性, 称之为蛋白质的变性作用(denaturation)。 ➢ 变性蛋白质和天然蛋白质最明显的区别是溶解度降低
多肽、蛋白质类药物的质量研究和质量标准建立
三、生物制品质量研究的内容
应包括对原液、、t"-成品和成晶的质撮研究,Ici材料的质量控制研究,以及生产T艺的质量控制 研究。 (‘)肠i液、、仁成品和成晶质馈研究:应建立有关产6自的鉴别、纯度、稳定性和活性等方研i的 试验方法 在物理化学方嘶的研究内窬包括,氨坫酸成份分析;N端15个氨些酸序列分析;肽图分析;聚 丙烯酰胺凝胶电泳(PAGE)及等电聚焦纯度分析;高效液市【{色谱(HPLC)纯度分析;残余细胞DNA 测定:其它外源性物质检奄等。 往生物学测定方而包括,鉴别试验;效价测定;特异比活性测定:热原质试验:病毒污染检企; 无菌试验:抗原一陀物质检仓;毒・陀试验等。 (.:)戍i材料的质键控制研究,以人用霞组DNA制品为例,应对表达找体和宿丰细胞进行研究: 对克降丛『丈J的序列进行研究;埘其他原材料的研究,包括细胞培养刷小个血清、培养液等。 (■)生,托』二艺的质蛩控制研究,包括)(寸细胞库的研究:对纯化上艺的研究,应特别沣意污染
HO HO
GR
F
5.FU
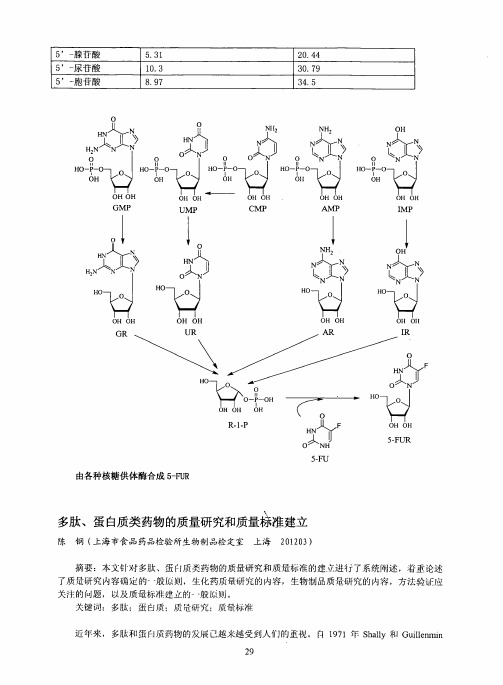
由各种核糖供体酶合成5-FUR
、
多肽、蛋白质类药物的质量研究和质量标准建立
陈钢(上海市食品药品检验所生物制品检定室上海201
203)
摘要:本文钊‘对多肽、蛋Fj质类药物的质量研究和质量标准的建立进行了系统闸述,着重论述 了质量研究内容确定的一‘般历i则,生化药质量研究的内容,生物制品质量研究的内容,方法验证应 关注的I’uJ题,以及质量标准建立的一一般原则。 关键词:多肽:蛋白质;质最研究;质最标准
五、质量标准建立的一般原则
质量标准建立的一般原则:质鼍标准主要由检测项F1、分析方法和限度组成:在全面、有针对 性的质最研究基础上,充分考虑药物的安伞。陀和有效性,以及生产、流通、使用各个环节的影响, 确定控制产品质量的项日和限度:质趟标准应能反映产品特征和质量变化,有效控制产品批f刚质最, 验证生产T艺的稳定性;所用的分析方法应经过方法学验证,具有一‘定的适用性和重现性,同时还 应考虑原料药和其制剂质量标准的关联性。 多肽药物质量标准项F1一‘般有,外观性状;比旋度;氨基酸分析;反离子的含量;水分:多肽 纯度:多肽序列;残留溶剂;氟化物残留量;肽图;多肽的结构;生物或免疫活性;多肽含量等。 提取物药物质量标准项FI应尽可能用理化检测,不能用的应以工艺、安全。件检测和效价测定(或 活一P_-I-:fN定)结合来控制质量。 蛋白质药物以重组治疗蛋白药品为例,质韪标准项F1 1般有,比活;肽图;纯度(HPLC);纯 度(SDS—PAGE);分子量;等电点;最大的紫外吸收波长;残留DNA;残留宿主细胞蛋白:残留抗 生素:N端氮基酸序列:细菌内毒素等
多肽、蛋白质类药物给药系统

多肽、蛋白质类药物给药系统摘要随着重组DNA技术的发展.基因工程肽和蛋白质药物的大规模生产已成现实,这类药物应用于临床的数量越来越多。
与传统的化学合成约物相比,其优点受到了广泛的关注,即与体内正常生理物质十分接近,更易为机体吸收,其药理活性高、针对性强、毒性低。
但由丁多肽、蛋门质类约物(1)分子质量大、稳定性高、易被胃肠道中的的蛋白水解酶降解;(2)生物半衰期短、生物膜渗透性差、生物利用度不高、不易通过生物屏障等,故其给药系统的研究一直足约剂学领域的一个热点。
许多学者曾尝试对肽类、蛋白质类约物进衍化学修饰、制成前体药物、应用吸收促进剂、使用酶抑制刺、采用离子电渗法皮肤给药以及设计各种给药系统解决上述问题.此炎药物一般注射给药,基本剂型足注射剂和冻粉针剂,常需频繁注射,患者顺从性差,且加重了患者的身体、心理和经济负担。
近年来,脂质体、微球、纳米粒等制剂新技术发展迅述歼逐渐完善,国内外学者将其广泛应用于多肽、蛋白质炎约物给约系统(drug deiivery system,DDS)的研究中,为此炎药物的临床应用铺平了道路。
本文就多肽、蛋白质类约物的给药系统及新技术进行综述。
主要介绍注射给药系统和非注射给约系统,及其下属几个分支。
重点介绍非注射给药系统。
关键字给药系统注射非注射l 新型注射给药系统1.1 控释微球制剂为了达到多肽、蛋白质类药物控制释放,可将其制成生物可降解的微球制剂。
目前已经实际应用的生物可降解材料主要有淀粉、明胶、葡糖糖、清蛋白、聚乳酸(PLA)、聚乳酸乙醇酸共聚物(PIGA)、聚邻酯、聚内酯和聚酐等;其中PLGA最为常用,改变乳酸乙醇酸的比例或相对分子质量,可得到不同降解时间的微球。
PLGA 微球相对于常规注射剂具有如下优点:(1)释药周期长,避免频繁给药;(2)使用安全;(3)药理作用增强;(4)避免发生明显的不良反应;(5)生物利用度显著提高。
1.2 脉冲式给药系统普通注射剂(疫苗、类毒素)一般至少接种3次,才能确保免疫效果,血药浓度波动大,且不能保证在疾病发作时相应的血药浓度。
《多肽、蛋白质药物》课件

目录
• 多肽、蛋白质药物的概述 • 多肽、蛋白质药物的合成与制备 • 多肽、蛋白质药物的特性与优势 • 多肽、蛋白质药物的应用领域 • 多肽、蛋白质药物的研发与审批 • 多肽、蛋白质药物的挑战与前景
01
多肽、蛋白质药物的概述
定义与分类
定义
多肽和蛋白质药物是指利用基因工程 技术、蛋白质工程技术或化学合成等 方法制备的,具有治疗、预防或诊断 疾病作用的大分子化合物。
感谢观看
研究与开发阶段
确定药物靶点
首先需要确定药物作用的生物靶点,即药物作用的生物分子,如蛋 白质或基因。
多肽、蛋白质设计
基于靶点的结构和功能,设计能够与靶点相互作用的多肽或蛋白质 药物。
合成与优化
通过化学或生物方法合成多肽或蛋白质药物,并进行药效和药代动力 学优化。
临床试验阶段
Ⅰ期临床试验
评估药物的安全性和耐受性,确定药物剂量和给药方案。
神经性疾病治疗
神经保护剂
01
多肽、蛋白质药物可以保护神经元免受损伤,用于治疗帕金森
病、阿尔茨海默病等神经退行性疾病。
镇痛剂
02
一些多肽、蛋白质药物具有镇痛作用,可以用于治疗疼痛性疾
病,如偏头痛、神经痛等。
促进神经再生
03
多肽、蛋白质药物可以促进神经细胞的再生和修复,用于治疗
脑外伤、脊髓损伤等。
心血管疾病治疗
药物作用机制
01
02
03
靶点识别与结合
多肽和蛋白质药物通过与 靶点分子结合,发挥其治 疗作用。
信号转导调控
一些多肽和蛋白质药物可 以调控细胞内的信号转导 通路,从而达到治疗目的 。
免疫调节
多肽和蛋白质药物还可以 调节机体的免疫反应,用 于治疗免疫相关疾病。
多肽、蛋白质类药物的质量研究和质量标准建立

5.31 lO.3 8.97
20.44 30.79 34.5
0 OH
O
lI
Ho—P
O
)H
U P
%)
O
I|
Ho—P—O
O
— O OiPIO H
0H
0H
GMP
。∥扒d一
o儿
1}
CM[P
∥久—√一一 ∥火吲
OH
O
P
●
O
蛐i州办
O
M』H
N/=i:\
HO HO
GR
F
5.FU
由各种核糖供体酶合成5-FUR
作者: 作者单位: 陈钢 上海市食品药品检验所生物制品检定室 上海 201203
本文链接:/Conference_6681585.aspx
、
多肽、蛋白质类药物的质量研究和质量标准建立
陈钢(上海市食品药品检验所生物制品检定室上海201
203)
摘要:本文钊‘对多肽、蛋Fj质类药物的质量研究和质量标准的建立进行了系统闸述,着重论述 了质量研究内容确定的一‘般历i则,生化药质量研究的内容,生物制品质量研究的内容,方法验证应 关注的I’uJ题,以及质量标准建立的一一般原则。 关键词:多肽:蛋白质;质最研究;质最标准
一、质量研究内容确定的一般原则
药物的质量研究足质奄标准制订的旗础。质量研究的内容应尽可能全面,既要考虑一1般性要求,
义要有针对性。确定质疑研究内容的1般历i则,应根据所研制药物的特性、所采用的制各I:艺、药
物的稳定性数据来定,生物制晶还要根据所使用的生物原材料及_『:艺束确定。
二、生化药质量研究的内容
五、质量标准建立的一般原则
质量标准建立的一般原则:质鼍标准主要由检测项F1、分析方法和限度组成:在全面、有针对 性的质最研究基础上,充分考虑药物的安伞。陀和有效性,以及生产、流通、使用各个环节的影响, 确定控制产品质量的项日和限度:质趟标准应能反映产品特征和质量变化,有效控制产品批f刚质最, 验证生产T艺的稳定性;所用的分析方法应经过方法学验证,具有一‘定的适用性和重现性,同时还 应考虑原料药和其制剂质量标准的关联性。 多肽药物质量标准项F1一‘般有,外观性状;比旋度;氨基酸分析;反离子的含量;水分:多肽 纯度:多肽序列;残留溶剂;氟化物残留量;肽图;多肽的结构;生物或免疫活性;多肽含量等。 提取物药物质量标准项FI应尽可能用理化检测,不能用的应以工艺、安全。件检测和效价测定(或 活一P_-I-:fN定)结合来控制质量。 蛋白质药物以重组治疗蛋白药品为例,质韪标准项F1 1般有,比活;肽图;纯度(HPLC);纯 度(SDS—PAGE);分子量;等电点;最大的紫外吸收波长;残留DNA;残留宿主细胞蛋白:残留抗 生素:N端氮基酸序列:细菌内毒素等
多肽与蛋白质类药物

两性物质的等电点会因条件不同(如在不同离子 强度的不同缓冲溶液中,或含有一定的有机溶媒的 溶液中)而改变。当盐存在时,蛋白质若结合了较 多的阳离子,则等电点向较高的pH值偏移。反之, 蛋白质若结合较多的阴离子,则等电点移向较低的 pH值。
用等电点法沉淀蛋白质常需配合盐析操作,而除 去不需要的杂蛋白时,常需配合热变性操作。
肝细胞生长因子是从肝细胞分化最旺盛阶段的胎 儿、胎猪或胎牛肝中获得的。若用成年动物,必须经 过肝脏部分切除手术后,才能获得富含肝细胞生长因 子的原料。
(3)生物状态 动物饱食后宰杀,胰脏中的胰岛素含 量增加,对提取胰岛素有利,但胆囊收缩素的分泌使 胆汁排空,对胆汁的收集不利。严重再生障碍性贫 血症患者尿中的EPO含量增加。
葡聚糖凝胶含有少量的酸性基团,故有较弱的离子 交换作用,此外还有吸附作用。在纯化蛋白质时,可 采用mol/L),或者用与待分离蛋白质相同的标准 蛋白质预先使凝胶柱平衡,以期不损失所分离的蛋白 质。
3、根据蛋白质溶解度的不同来纯化蛋自质
蛋白质的溶解度受溶液的pH、离子强度、溶剂的 电解质性质及温度等多种因素的影响。在同一特定条 件下,不同蛋白质有不同的溶解度,适当改变外界条 件,可以有选择地控制某一种蛋白质的溶解度,达到 分离的目的。
应用最多的氨基保护剂是苄氧羰酰氯(Cbz-Cl), 可用催化氢化法或钠氨法(用金属钠在液氨中处理) 除去保护基,也可用叔丁氧羰酰氯(BOC-Cl)作保 护剂,用稀盐酸或乙酸在室温除去保护基。
羧基保护剂通常用无水乙醇或甲醇在盐酸存在下 进行酯化,使羧基接上烷基。除去保护基可在常温下 用氢氧化钠皂化法。
等电聚焦电泳除了用于分离蛋白质外,也可用于 测定蛋白质的等电点。
2、根据蛋白质分子形状和大小的不同来纯化蛋白质
第十一章(1) 多肽与蛋白质类药物

根据等电点不同, 可以将胸腺素组分5 中所含多肽分为α、 β、 γ 三个区,
α区---pI5.0以下多肽。 β区---pI5.0~7.0以下多肽 γ区---pI7.0以上多肽(种类较少)
胸腺素组分5中,所含的多肽中并非每一种都有免疫 活性,有活性的称为胸腺素,如胸腺α1、 α5 、 α7 , 无活性的称为多肽,如β1 等。
的多肽----催产素。
(2)天然动植物及重组动植物提取法
通过生化工程技术,从天然动植物中分离纯化。由于 天然动植物中的有效成分含量过低,杂质太多,引起人们 对重组动植物的重视。 重组动植物只通过基因工程技术手段,将药物基因 或能对药物基因起调节作用的基因转导入动植物细胞,以 提高动植物合成药用成分的能力,再经过生化分离,制得 生物制品。
二、主要多肽类药物的制备
1、胸腺素(thymocin)
胸腺位于胸骨后面,紧靠心脏, 呈灰赤色,扁平椭圆形,分左、右 两叶,由淋巴组织构成。青春期前 发充良好,青春期后逐渐退化,为 脂肪组织所代替。 胸腺是造血器官, 分泌胸腺素,能产生淋巴细胞,并 运送到淋巴结和脾脏等处。这种淋 巴细胞对机体的细胞免疫具有重要 作用。 生长激素和甲状腺素能刺激胸腺 生长,而性激素则促使胸腺退化。
☆ (3)分子小,结构易于改造,可通过化学合成的方法生产。如
由中国首先合成的牛胰岛素,就属于一种含51个氨基酸的多肽。 ☆ (4)活性多肽的合成过程往往是由蛋白质精加工剪切转化而来 的,许多多肽之间都具有共同的来源、相似的结构。
2.多肽类药物的分类
主要多肽类药物
主要有多肽激素、多肽类细胞生长 调节因子、含有多肽成分的组织制剂:
人体和动物都有免疫系统,包括特异性免疫和非特异性 免疫,其中特异性免疫又分为体液免疫系统和细胞免疫系统。 当某些外源生物(如细菌)或生物大分子(如蛋白质),也叫 抗原,进入动物体后,会刺激动物体本能地产生相应的抗体, 引起免疫应答,从而将进入的外源生物或蛋白质分解或清除。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、概述
多肽类生化药物是以多肽激素和多肽细胞生长调节 因子为主的一大类内源性活性成分。 蛋白质生化药物包括蛋白质类激素、蛋白质细胞生 长调节因子、血浆蛋白质类、粘蛋白、胶原蛋白及蛋白 酶抑制剂等。
细胞生长调节因子系在体内和体外对效应细胞的生 长、增殖、和分化起调控作用的一类物质。 细胞生长刺激因子 高活性 低免疫原性 细胞生长抑制因子 人体可耐受剂量大
二、多肽类药物的制备
1、用传统的生化提取法和微生物发酵法生产 2、利用基因工程技术构建的工程菌(细胞)生产 多肽激素
垂体 下丘脑 甲状腺 胰岛 肠胃道 胸腺
多肽类细胞生长调节因子 含有多肽成分的组织制剂
表皮生长因子 转移因子 心钠素 蛇毒 蜂毒 胚胎素 花粉提取物
降钙素——甲状腺激素
降钙素是由甲状腺内的滤泡旁细胞( C细胞)分 泌的一种调节血钙浓度的多肽激素。 功能:抑制破骨细胞的活力,阻止钙的释放,降 低血钙 临床应用:骨质疏松、VD过多症、畸形性骨炎
发酵培养
半成品制备 包装
粗提
精提
附:传统方法生产干扰素
【启动诱生】 【正式诱生】
仙台病毒 37℃,12 h
【分离】
离心 2500r/min
人白细胞粉
溶解
人a-干扰素 37℃,2 h
启动白细胞
白细胞培养物
IFN1
沉淀2
上清液1 沉淀1 粗制a-干扰素 ︻ pH = pH = 3.5 5℃ 沉 上清液2 5.5~5.8 【溶解】 淀 NaOH PBS,NaOH 对PBS透析 分 pH = 8.0 沉淀4 溶解液 上清液 pH = 7.0~7.5 pH = 7.0~7.5 PBS,KSCN 离 (IFN-b) 沉淀 3 【酸沉淀】 【溶解】 ︼ pH = 5.2 HCl PBS,NaOH 沉淀5 溶解液 【KSCN处理】 上清液3
定义:由诱生剂诱导有关细胞所产生的一类高活性、多功能的诱 生蛋白质。具有广泛的抗病毒、抗肿瘤和免疫调节活性。
白细胞干扰素(IFN-a)
类淋巴细胞干扰素(IFN-a、b) 成纤维细胞干扰素(IFN-b) T细胞干扰素(IFN-g)
干扰素生物学活性
1.抑制病毒等细胞内微生物的增殖。 2.抗细胞增殖。
干扰素的生物学活性
DNA的PstⅠ酶切割段加 上dA或dG
(在b-内酰胺酶基因内)
将干扰素cDNA的克隆入 表达载体在E.coli中表达 采用杂交翻译法挑选含 有干扰素cDNA的克隆
扩增杂交质粒 筛选抗四环素但对氨苄 西林敏感的细菌克隆
基因工程干扰素的生产
基因工程干扰素的生产工艺:
启开种子
分装 冻干
制备种子液
半成品检定 成品检定
产品的不稳定性
诱生剂因厂家和批 号的不同而异
基因工程干扰素的生产
干扰素工程菌的构建:
诱生的白细胞或 成纤维细胞 提取全RNA 通过寡dT-纤 维素柱获得聚 A的mRNA 5%~23%蔗糖密 度梯度离心提取 12S的mRNA 自mRNA逆转录 成cDNA
pBR322质粒
双链cDNA用末端DNA转 移酶接上dT或dG尾 退火获得杂交质粒 转化大肠杆菌K12
降钙素——甲状腺激素
1、结构与性质 溶解性: 溶于水和碱性溶液
不溶于丙酮、乙醇
等有机溶剂,
难溶于有机酸。
稳定性:低温避光干燥条件下稳定,易被蛋白酶、氧 化剂破坏。 来源:甲状腺、甲状旁腺等组织,鲑、鳗、鳟等
降钙素——甲状腺激素
2、生产工艺——提取法
提取 沉淀 除杂蛋白
猪甲状腺丙酮粉
0.1 mol/L HCl
促性腺激素:SGH、HCG、NMG
其他蛋白质激素:胰岛素、松弛素
血浆蛋白质:Alb、免疫球蛋白、凝血因子—特异性
蛋白质类细胞生长调节因子:IFN、IL、t-PA、HGF 黏蛋白:胃膜素、硫酸糖肽等 胶原蛋白:明胶、阿胶、冻干猪皮等 碱性蛋白和蛋白酶抑制剂
干扰素——高度种属特异性
灭活流感病毒 鸡胚绒毛尿囊膜碎片 抗性、干扰因子释放
3.免疫调节。 4.改变细胞表面的状态,组织相容性 抗原表达增加。
5.增加细胞对双链DNA敏感性。
传统方法生产干扰素——弊端
成本高
45000L→200mg 1 kg → 220~440亿
组分多
类淋巴母细胞: 80% a-干扰素 + 20% b-干扰素
纯度低、活性低
传统生产的干扰素 纯度最高只有1%, 活性在105 U/mg
pH = 3.0 pH = 7.0~7.5
【二次酸 【除杂蛋白】 【KSCN处理】 除杂蛋白】 乙醇 KSCN,HCl
特点:一次纯化量大,回收
【干燥】
冻干
【除盐】
对PBS透析 离心
率高于 60% ;经济、简便, a-干扰素 易于普及。
(IFN-A)Biblioteka 透析清液60℃,1h
提取液
异戊醇-醋酸-水
50℃,过滤
沉淀物
pH = 2.5
0.3 mol/L NaCl, 10%HCl CMC 降钙素 解析液 离心清液 pH = 4.5 冷冻干燥
干燥 吸附、解析
NaCl盐析
3、生物活性测定: 原子吸收光谱法、标准曲线法
三、蛋白质类药物的制备
垂体蛋白质激素:GH、TSH、PRL 蛋白质类激素
