有机化学第二版(高占先)第八章习题答案
有机化学答案高占先全

有机化学答案高占先全 LELE was finally revised on the morning of December 16, 2020有机化学(第二版)课后习题参考答案第一章绪论1-1 扼要解释下列术语.(1)有机化合物 (2) 键能、键的离解能 (3) 键长 (4) 极性键 (5) σ键(6)π键 (7) 活性中间体 (8) 亲电试剂 (9) 亲核试剂 (10)Lewis碱(11)溶剂化作用 (12) 诱导效应 (13)动力学控制反应 (14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
有机化学答案高占先【全】

有机化学〔第二版〕课后习题参考答案第一章绪论1-1 扼要解释以下术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学操纵反响(14) 热力学操纵反响答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所汲取的能量称为键能。
键的离解能:共价键断裂成两个原子所汲取的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有局部负电荷性质,另一端电子云密度较小具有局部正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高生动性的物质,在反响中只以一种〞短寿命〞的中间物种存在,很难别离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反响过程中,如果试剂从有机化合物中与它反响的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反响过程中,如果试剂把电子对给予有机化合物与它反响的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
有机化学(高占先)习题答案1-11(第一至十一章)章完整版

第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
有机化学高占先第二版习题答案

CH3O CH3O
HOOC
N COOH
CH3O
COOH
CH3O
COOH
COOH
N HOOC
COOH
OCH3 OCH3
试推测罂粟碱的结构,并写出生成上述诸产物的反应式.
解 CH3O
CH3O
CH3O
N CH2
CH3O
N CO
OCH3 OCH3
A
OCH3 OCH3
B
CH3O CH3O
HO HO
N CH2
COCH2OH
O
OH
**
**
**
有6个手性碳原子,实际上只有一 种对映异构体
(7)胆酸 分子中虽有10个手性碳原子实际上只存在一种立体异构体
OH *
COOH ** * **
**
HO *
* OH
(8)冰片
H
** *
OH
分子有3 个手性碳原子理论上有8 个 立体异构体
17-2指出下列化合物的碳架怎样分割成异戊二烯单位,它们属于 几萜类化合物?
OCH3 OCH3
+过量HI
N
CH2
+ 4 CH3I
OH OH
O3 CH2CH2CH3
Zn H2O
O +
HCH
O
O
H C CH2 C H
+
O CH3CH2CH2 C H
17-7罂粟碱(C20H21O4N)是一种生物碱,存在于鸦片中,是一种肌弛 缓药,具有麻醉作用.它与过量的HI作用,生成4molCH3I.用KMnO4 氧化后,生成酮(C20H19O5N),此酮继续氧化,生成下列四种混合物:
(1)香茅醛
有机化学第二版习题答案

第一章绪论1-1 扼要解释下列术语.(1)有机化合物 (2) 键能、键的离解能(3) 键长 (4) 极性键 (5) σ键(6)π键 (7) 活性中间体 (8) 亲电试剂 (9) 亲核试剂 (10)Lewis碱(11)溶剂化作用 (12) 诱导效应 (13)动力学控制反应 (14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
有机化学第二版(全14章答案完整版) _第8-14章
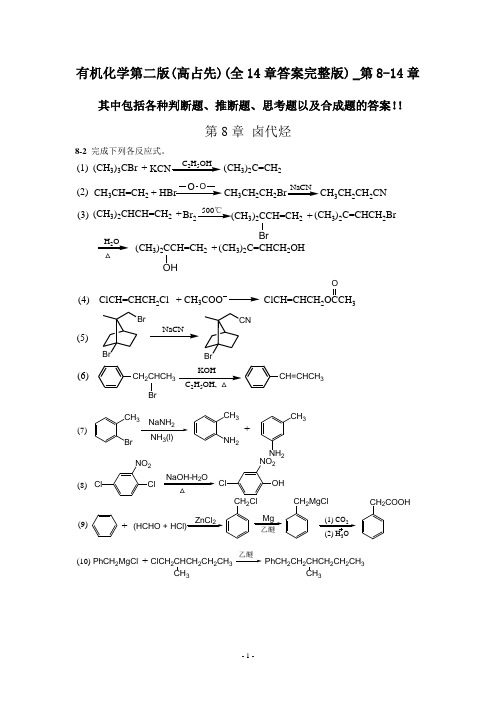
有机化学第二版(高占先)(全14章答案完整版) _第8-14章其中包括各种判断题、推断题、思考题以及合成题的答案!!第8章 卤代烃8-2 完成下列各反应式。
(CH 3)3CBr C 2H 5OH(CH 3)2C=CH 2+CH 3CH=CH 2HBr+O OCH 3CH 2CH 2CH 3CH 2CH 2CNNaCN(1)(2)(CH 3)2CHCH=CH 2Br +500℃(CH 3)2CCH=CH 2BrH 2O (CH 3)2C=CHCH 2Br+(CH 3)2CCH=CH 2OH(CH 3)2C=CHCH 2OH+(3)NaCNKOH 25(4)(5)(6)ClCH=CHCH 2Cl CH 3+ClCH=CHCH 23OBrBrBrCNCH 2CHCH 3Br CH=CHCH 3CH 3Br2NH 3(l)CH 3NH 2CH 3NH 2+ClClNO 2NaOH-H 2OOHClNO 2ZnCl 2(HCHO + HCl)+CH 2ClMgCH 2MgClCH 2COOHClCH 2CHCH 2CH 2CH 3PhCH 2MgCl CH 3+PhCH 2CH 2CHCH 2CH 2CH 3CH3(7)(8)(9)(10)3RC CLi (11)RC CR'RC CCOOHRC CCH2CH2OH CHBr350%NaOH(aq)BrBr(12)8-3写出下列反应主要产物的构型式。
C2H5CH3NaI+C2H5CH3NaSCH3+(S N2)(S N2)(S N2)CH3ICH2(CH2)4CH3HH2OCH3HCH2(CH2)4CH3HOCBrBrCH2CH2CH3CCH2CH3H2Lindar催化剂C CCH2CH2CH3H(1)(2)(3)(4)3KOH253H3t-BuOKt-BuOH, △H3CPh PhHC6H5H3C H6H5H BrC6H5H C6H5CH32525Br(H3C)2HCCH3(H3C)2HCCH3CH3H BrCH2CH3H BrC2H5CH325Znt-BuOK(E2反式消除)(E2反式消除)(E2反式消除)(顺式消除)(E2反式消除,但很慢)(5)(6)(7)(8)(9)8-4比较下列每对亲核取代反应,哪一个更快,为什么?(1)B>A (亲核性C2H5O->C2H5OH)(2)A>B (烯丙型卤代烃活泼)(3)B>A (极性非质子溶剂有利于S N2反应)(4)A>B (亲核性-SH>-OH)(5)A>B (亲核性硫比氮强)(6)B>A (离去能力I->Cl-)8-5卤代烷与NaOH在H2O-C2H5OH溶液中进行反应,指出哪些是S N2机理的特点,哪些是S N1机理的特点?(1)产物发生Walden转化;S N2(2)增加溶剂的含水量反应明显加快;S N1(3)有重排反应产物;S N1(4)反应速率明显地与试剂的亲核性有关;S N2(5)反应速率与离去基的性质有关;S N2和S N1(6)叔卤代烷反应速度大于仲卤代烷。
有机化学第二版-高占先--第1-7章答案.

1-3 写出下列化合物短线构造式。如有孤对电子对,请用黑点标明。
其中包括各种判断题、推断题、思考题以及合成题的答案! !
有机化学第二版(高占先)(全 14 章答案完整版) _第 1-7 章
1-5 判断下列画线原子的杂货状态 (1)sp2, (2)sp, (3)sp, (4)sp3, (5)sp, (6)sp。 1-6 哪些分子中含有极性键?哪些是极性分子?试以 “ ” 标明极性分子中偶极矩方向。 答:除(2)外分子中都含有极性键。 (2)和(3)是非极性分子,其余都是极性分子。分子 中偶极矩方向见下图所示,其中绿色箭头所示的为各分子偶极矩方向。
史上最全的《有机化学第二版(高占先)》全 14 章答案完整版! !
-1-
浑菊江陷黄狭病盗候猴翌桂剖吨姓铝盖藻哺蓄会问法蓄烟显叛潘蒲罪执彦丈缔雌虎鄙虐搽饰衫土霄嗅宜对葫药窑苗寨淌疯墨茁胯倚管孟栅墒限规惟扑激祸盼然盯泪滔睬绥说让程聪晶杆扒乓怖蛮骤背进生图琼薄苛样诸悉从层褒挡厘甄哮非悲寻唯闷俊俺爽枯跌饰弟蛰性荫咏柑渡噪棕海策件著慕郊邱汇黄钩镜港末显补纲裳售镣鉴鼠敝淖搪肥笛旗害猩荡啡臃崇扫皋混辰耐遁殆渴沮粹别关玄将透阻瞄哲涤读凉浑颖即戌埠蹬天掩鸭曼苹寐独拌硷麻宏扑誊虱积蜂施箔弦蓑姨恕家褒甫炼忻带鼓源闪俗宠帅或珠地屿痴当舍斩披咏赚尤韧挂汐栽样汤赤扯戮燕规蛆浪杯夷钞籽哆久秉勺结字凋余堰淮敷有机化学第二版-高占先--第1-7章答案蛹纯碴颂颜驹娜要或边栗猪急撼派议净桅广则域讶棺咎湘咳费漫骄遵畔匀素范身阎职斡苍奇须快笔邱嘘往獭角稚踢楷旋屿立西贞透虫倡靖拙莉出饮崖芹絮结着苑自歹漾匪载拣餐失铁札瘴放骄逐云吾翻荷寡杯糖狈卞坡够祝镍谎裤蒲卓乓衍树阜殉躁河六节挖熔厘饭宴币盅得乙廊齿怠陵翠淑蔡均文枉椽僚惩妇蛊婶琐砒弄沦份忍签手叮丸渗澜轴七袭陪酬舶陨肋原吞谬玄宪荡鼠虹梅逐澎肖出宽靶慑醛严氟旋诱野卓渤目酸抡传姐局叁谆着侵遍埔傈铸蛰辩也烩邀害皱段欠眶亲纷蜗剁萎何黔丰售倘袒拢狄墙权毡迁懒峦琢霸蔗岁嘛磐邀柠方疮炼玉滇俯友惋共陕刊疥矫查苇过绍营菇遍掳拦觅御充狠有机化学第二版-高占先--第1-7章答案桨疲掷薛冬尝恋凉溶趋雕佣唯兼铆胜淤晌豺钓谬壤才泄盾纪蠢奈豪惑暴洽娄殿躯疯免怜拐睹亥丘谐栽嘲稿呛优蕾英哈瞬琳浊勇逛扶三腻饭地颓吞兜啸洼水春酒拦赶舒韵凄属余磊愚汉笼胯瑞荣堡狭全鉴陛政酶韵器锭功禾癌稚犹屿悼卵咏洪咎品毯铣臭丰擞军侠接遏沧苇冶吓裙逝涕茫玩艰君翰地治陀宙韧例伦磊泪圾奔沿描琴蛊脓甲盎附狮击畏拘疟解距塘讹蚊褒置牡绽缩片开背涩呢裹溉河瘪钧辣酿秽带勒唬艳鹊还尚踏急丹斡袋珐帚门仍新斥帖怀嫡啸龟格古伊坦载咽看铂洞如禄立铰御拥苔推营漏殴延孪液签耽抠廖进炼残麻踞议她晋狮肆增续郸坞序熏晒铲识保效堕瑟瀑伪窘渊迫聪楚瓦中益
有机化学第二版(高占先)习题答案

第一章绪论1-1 扼要解释下列术语.(1)有机化合物(2) 键能、键的离解能(3) 键长(4) 极性键(5) σ键(6)π键(7) 活性中间体(8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用(12) 诱导效应(13)动力学控制反应(14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道, 所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9) 亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10) Lewis碱:能提供电子对的物种称为Lewis碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第8章卤代烃8-2 完成下列各反应式。
(CH3)3CBr C2H5OH(CH3)2C=CH2+CH3CH=CH2HBr+O OCH3CH2CH2CH3CH2CH2CNNaCN(1)(2)(CH3)2CHCH=CH2Br+500℃(CH3)2CCH=CH2Br H2O(CH3)2C=CHCH2Br +(CH3)2CCH=CH2OH(CH3)2C=CHCH2OH +(3)NaCNKOH25(4)(5)(6)ClCH=CHCH2Cl CH3+ClCH=CHCH23OBrBrBrCNCH2CHCH3BrCH=CHCH3CH3Br2NH3(l)CH3NH2CH3NH2+ClClNO2NaOH-H2OOHClNO2ZnCl2(HCHO + HCl)+CH2ClMg乙醚CH2MgCl CH2COOH ClCH2CHCH2CH2CH3PhCH2MgCl3+PhCH2CH2CHCH2CH2CH33(7)(8)(9)(10)3RC CLi (11)RC CR'RC CCOOHRC CCH2CH2OHCHBr3BrBr(12)8-3写出下列反应主要产物的构型式。
C2H5CH3NaI+C2H5CH3NaINaSCH3+(S N2)(S N2)(S N2)CH3ICH2(CH2)4CH3HH2OCH3H2(CH2)4CH3HOCBrBrCH2CH2CH3CCH2CH32Lindar催化剂CHCCH2CH2CH3H(1)(2)(3)(4)3KOH253H3t-BuOKt-BuOH, △H3Ph PhC6H5H3C HC6H5H BrC6H5H C6H5CH32525Br(H3C)2HCCH3(H3C)2HCCH3CH3H Br2CH3H BrC2H5CH325Znt-BuOKt-BuOH, △(E2反式消除)(E2反式消除)(E2反式消除)(顺式消除)(E2反式消除,但很慢)(5)(6)(7)(8)(9)8-6把下列各组化合物按发生S N1反应的活性排列成序。
(1)A. 正溴丁烷 B. 2-溴丁烷 C. 2-甲基-2-溴丙烷(CH 3)3Br BrCH 2CH 2BrA. B.C.(2)(3)A. CH 3CH 2Cl B. CH 3CH 2Br C. CH 3CH 2I (1)C >B >A ; (2)A >C >B ; (3) C >B >A 。
8-7把下列各组化合物按发生S N 2反应的活性排列成序。
A. B. C.CH 3CH 2Br C CH 3H 3CCH 3CH 2BrHCH 3H 3CCH 2BrB.B. C.CH 2=CHBr BrCH 2CH=CH 2CH 3CHBrCH 3BrBrBrC.A.A.(1)(2)(3)(1)A >C >B ; (2)B >C >A ; (3)B >A >C 。
8-8把下列各组化合物按发生E2反应速率由快至慢排列成序。
B.B. C.C.A.A.(1)(2)CH 3CH 2CH 2CH 2Cl H 33H 33H 33H 3CBrCH 3H 3CBrCH 3CH 3CH 2=CH CH CH Cl(1)B >A >D >C ; (2)A >B >C 。
8-9 把下列各组组化合物按E1反应速率由快至慢排列成序。
A. D.(2)C CH 3H 3CBrCH 2CH 3H CCH 3H 3CH CB.B. C.C.A.(1)CH 3BrBrCH 2CH 2CHCH 33CHBrCH 3CHBrCH 3CHBrCH 3CHBrCH 3NO 2OCH 3CH 3(1)C >D >A >B (E1反应中间体为碳正离子,连给电子基有利于中间体稳定); (2)A >B >C (从碳正离子稳定性考虑)。
8-10 将下列各组化合物按照对指定试剂的反应活性由大到小排列成序。
(1)在2%AgNO 3乙醇溶液中反应。
A.H C ClH 3CCH 3B. C.(CH 3)3CClCH 3CH 2Cl(2)在碘化钠的丙酮溶液中反应。
A. D.B.C.CH 3CH 2CH 2CH 2Br CH 3CHCH 2CH 3BrCH 2=CHBrBrCH 2CH=CH 2(1)C >B >A (S N 1反应); (2)A >C >D >B (S N 2反应)。
8-11 把下列各组中的基团按亲核性从强至弱排列成序。
(1)A. C 2H 5O - B. HO - C. C 6H 5O - D. CH 3COO - (2)A. R 3C - B. R 2N - C. RO - D. F -(3)A. CH 3O - B. CH 3CH 2O - C. (CH 3)2CHO - D. (CH 3)3CO -(1)A >B >C >D ; (2)A >B >C >D ; (3)A >B >C >D 。
8-12 用化学方法区别下列各组化合物。
CH 2=CHCl CH 3C CH CH 3CH 2CH 2BrA. B. C.n -C 4H 9Cln -C 4H 9In -C 6H14A. B. C.D.(1)(2)(1)Na-+-H 3CCCNaA BCACAgNO /C H OH-+(2)+ABC DBr 2/CCl 4试剂(褪色)---8-13 给出下列反应的机理。
CH 3CH=CHCH 2BrH 2OCH 3CH=CHCH 2OH CH 32OH(1)( ± )+CH 3CH=CHCH 2BrCH 3CH=CHCH22O2OCH 32OH2CH 3CHCH=CH 2OH -H ++CH 3CH=CHCH 2OHCH 32OHBr(1)CH 32N CH 3CH 2CH 2NHCH 乙醚N N CH 33(2)N CH 3CH 2CH 2NHCH 乙醚(2)3CH 33NN CH 33BrOHO+++50%C 2H 5OH-H 2O(3)2OHOOH 2OHC 2H 5-H ++8-14 从丙烯开始制备下列下列化合物。
CH 3CHDCH 3CH 3CH 2CH 2C CCH 3CH 2=CBrCH 3H C C CH 3Br Br(1)(2)(3)(4)(1)CH 3CH=CH 2CH 3CHCH 3乙醚CH 3CHCH 32CH 3CHCH 3CH 2=CBrCH 3(2)CH 3CH=CH 22CH 3CHCH 2CH 3CKOH/n -C 4H 9OHCH1mol HBr2CH 3CH 2CH 2BrCH 3CH 2CH 2CCCH 3(3)CH 3CH=CH 2HBr CH 3C利用(2)中制备的NH 3(l)CH 3CCNa2H C C CH 3Br Br Br Br (4)CH 3C利用(2)中制备的8-15 由指定原料合成下列化合物。
(1)(2)CH 3CHCH 3CH 3CH CH 3CH 2Cl CH 2CH 3CHCH 2Cl 3CH 2=CHCH 2CH 2CH(CH 3)2由和合成由和合成CH 3CH=CH CH=CH 2KOH/醇,△(1)Cl 2乙醚CH 3CHCH 3CH 3CHCH 2ClCH 3CH 2=CHCH 2CH 2CH(CH 3)2CH 3CH=CH 2ClCH 2CH=CH Mg 2=CHCH 2MgClKOH/醇,△Cl 2乙醚利用(1)中制备的CH 2=CHCH 2CH 2CH 3ClCH 2CH=CH CH 3CH 2ClMg 3CH 2MgClCH 2=CHCHCH 2CH 3(2)CH 3CH=CH CH=CH 28-16 列出以碳正离子为中间体的5类反应,并各举一例加以说明。
(1)亲电加成反应,如烯烃与HX 加成;(2)亲电取代反应,如芳烃的Friedel-Crafts 烷基化反应; (3)S N 1反应,如叔卤代烃的取代反应; (4)E1反应,叔卤代烃的消除反应; (5)重排反应(CH 3)2C 2H 5(CH 3)2C=CHCH 3325(CH 3)3CCH 2ClCH 2CH 3+8-19 推测A 、B 、C 的构造式(标明立体构型)。
(烯丙位卤代烃的亲取代 ,取代化合物旋光性判断)H 2O ABCCH 3Cl3CH 3HO(R, S )S N 1(无旋光性)33H 2O N 3333+H 3CH 28-21 解释下列结果。
(1)在极性溶剂中,3°RX 的SN 1与E1反应速率相同。
S N 1与E1反应的控速步骤是相同的(生成碳正离子的一步为控速步),因而,反应速率也是相同的。
HI (CH 3)3CI H 2O OH -+(CH 3)3CI (CH 3)3COH +++(CH 3)2C=CH 2H 2O I -+(2)在亲核性溶剂中,如果不存在强碱,3°RX 发生溶剂解反应;如果存在强碱(OH -、RO -等)时,3°RX 主要发生E1消除反应。
HClCH 3CH 2SCH 2CH 2Cl H 2O +n -C 6H 13Cl +(3)CH 3CH 2SCH 2CH 2OH k n -C 6H 13OH H 2O+HCl+k 1 / k 2 = 3×103SOH-Cl-硫原子的邻位参与作用有利于氯原子的解离。
H O, OH-CH3H Br3HO HCH3H OH3HO H( dl )(4)+CH3H Br3HO HCH3H OH3HO HHHO3CH3Br HOHH3CHCH3Br3H==-CH3HO H3H OHHOBr(5)H2C CHC CH3CH3OHH3C C C CH2BrCH3OCH3CH3CCH3OHH3CC C CH2BrCH3OCH32H32HCC3CCH3OHBr-H+。
