反应工程课后答案
化学反应工程第二章习题答案

化学反应工程第二章习题答案化工103班2-1银催化剂上进行甲醇氧化为甲醛的反应2CH3OHO22HCHO2H2O2CH3OH3O22CO24H2O进入反应器的原料中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇转化率达72%,甲醛的收率为69.2%,试计算:(1)反应的总选择性;(2)反应器出口组成。
解:根据甲醇:空气:水蒸气=2:4:1.3(摩尔比),以100mol进料为基准设χy分别为HCOH和co2生成量2CH3OHO22HCHO2H2O2CH3OH3O22CO24H2O对上式积分(n1)kct1cn1kcAcn1AOn111cn1n1AcA①0①式为无量纲对数形式可判别出kc的单位molm3n1kt111同理pn1pn1n1kn11ApAp的单位pa02-4在间歇反应器中进行等温二级、一级、零级均相反应,求出转化率由0变为0.9所需的时间,与转化率由0.9变为0.99所需时间之比。
解:等温二级反应111kt1ckt21AcA0cA2cA某A0.9某A0.999t190A0kcA0t1:t21:10等温一级反应ktlncA0cAln10同上解得t1t2kt1:t21:1等温零级反应ktcA0cA同上解得t10.9cA0A0kt20.09ck10:12-5某一反应在间歇反应器中进行,经8min后反应物转化了80%,经过18min后转化了90%,求表达此反应的动力学方程。
解dnrAAVdt积分后:tcA0dcArACcA0dcAcAcAn111n1n1AkcAkn1cA0cAt8min某A180%t18min某A290%28111kn1cn1cn1n1A0A01某A11811kn1cn11n1n1A0cA01某A2n2r2AkcA2-6某一气相一级反应A2RS,在恒温、恒压的实验反应器中进行,原料含75%A及25%惰性气体(摩尔比),经8min后其体积增加一倍。
求此时的转化率及该反应在此温度下的速率常数。
(完整版)化学反应工程课后习题答案.

积分之
2.10在催化剂上进行三甲基苯的氢解反应:
反应器进口原料气组成为66.67%H2,33.33%三甲基苯。在0.1Mpa及523K下等温反应,当反应器出口三甲基苯的转化率为80%时,其混合气体的氢含量为20%,试求:
(1)(1)此时反应器出口的气体组成。
(2)(2)若这两个反应的动力学方程分别为:
组分
摩尔分率yi0
摩尔数ni0(mol)
CH3OH
2/(2+4+1.3)=0.2740
27.40
空气
4/(2+4+1.3)=0.5479
54.79
水
1.3/(2+4+1.3)=0.1781
17.81
总计
1.000
100.0
设甲醇的转化率为XA,甲醛的收率为YP,根据(1.3)和(1.5)式可得反应器出口甲醇、甲醛和二氧化碳的摩尔数nA、nP和nc分别为:
组分
摩尔质量
摩尔分率yi
CO
28
15.49
H2
2
69.78
CO2
44
0.82
CH4
16
3.62
N2
28
10.29
总计
100
其中冷凝分离后气体平均分子量为
M’m=∑yiMi=9.554
又设放空气体流量为Akmol/h,粗甲醇的流量为Bkg/h。对整个系统的N2作衡算得:
5.38B/28×1000+0.1029A=2.92 (A)
20
30
40
50
60
70
试求当进口原料气体流量为50ml/min时CO的转化速率。
解:是一个流动反应器,其反应速率式可用(2.7)式来表示
化学反应工程答案

FA0
k[(FA0
dX / v0 )(1
X )]2
v02dX FA0k (1 X )2
V
X
v02dX FA0k (1 X )2
v02 FA0k
(1 1 X
1)
102 (L/h)2
1
(
5mol/h 3L/(mol h) 1 0.99
1)
660L
4
112
在一个20L的恒体积间歇反应器中进行等温气相反应
9
(3)在一个10.5L的CSTR反应器中, 能达到的最大转化率是多少? 因
解: 先将表格用polymath自动转换成以下形式 ?
为 是
绝
X
0
0.2
0.4
0.5
对PFR反应器 :
dFA dV
rA,
即
(2) rA kCA 对CST R反应器 :
V dFA dFA FA FA0 FA 99L
FA rA
k FA
k
k
V
0.99FA0 rA
0.99FA0 k CA
0.99FA0 k(0.01FA0 / v0 )
0.99 10L/s 0.0001s1 0.01 3600
消耗99%的组分A (即CA 0.01CA0)时, 对CSTR和PFR反应器需要的反应体积。 已知进料的体积流率
10L/h。[ 注意:F A CAv。 当体积流率恒定时, v v0, 因此, FA CAv。
故CA0 FA0 / v0 5(mol/h)/(10L/h) 0.5mol/L。] 解:
2ft3/ min 时, 所需的反应器体积。 该系统的空速是多少?
解: v0 2ft3/ min 28.32 2L/ min 56.64L/ min
化学反应工程许志美课后答案第一章

化学反应工程许志美课后答案第一章1、下列含有蒽醌类成分的中药是()*A丹参B决明子(正确答案)C芦荟(正确答案)D紫草2、下面化合物能与异羟肟酸铁反应的是()[单选题] *A花椒内酯(正确答案)B柠檬烯C色原酮D天精3、在结晶溶剂的选择过程中首先要遵循的是()[单选题] *A成分的纯度(正确答案)B相似相容原理C冷却热饱和原理D以上都不对4、四氢硼钠反应变红的是()[单选题] *A山柰酚B橙皮素(正确答案)C大豆素D红花苷5、木脂素是苯丙素衍生聚合而成的天然化合物,多为()[单选题] *A二聚体(正确答案)B三聚体C四聚体D五聚体6、在溶剂提取法中,更换新鲜溶剂可以创造新的(),从而使有效成分能够继续被提取出来。
()[单选题] *A极性差B压力差C浓度差(正确答案)D体积差7、E何首乌(正确答案)下列不含蒽醌类成分的中药是()*A丹参(正确答案)B决明子C芦荟D紫草(正确答案)8、下列基团在极性吸附色谱中的被吸附作用最强的是()[单选题] *A羧基(正确答案)B羟基C氨基D醛基9、E连续回流提取法(正确答案)用乙醇作溶剂提取时,下列说法正确的是()* A对植物细胞壁穿透力强(正确答案)B溶解范围广,提取较全面(正确答案)C提取液中蛋白质、多糖等水溶性杂质少(正确答案)D有防腐作用,提取液不易发霉变质(正确答案)10、四氢硼钠反应变红的是()[单选题] *A山柰酚B橙皮素(正确答案)C大豆素D红花苷11、乙醇不能提取出的成分类型是()[单选题] *A生物碱B苷C多糖D鞣质(正确答案)12、碱水提取芦丁时,若PH过高会使()[单选题] * A产品质量降低B产品收率降低(正确答案)C苷键水解断裂D内酯环开环13、很少含有挥发油的植物科为()[单选题] *A菊科B唇形科C茜草科(正确答案)D姜科14、挥发油常见属于哪类萜类化学物()[单选题] *A半萜与单萜B单贴与倍半萜(正确答案)C倍半萜与二萜D二萜与三萜15、与明胶反应生成沉淀的成分是()[单选题] *A强心苷B皂苷C有机酸D鞣质(正确答案)16、中药丹参中的主要有效成分属于()[单选题] *A苯醌类B萘醌类C蒽醌类D菲醌类(正确答案)17、连续回流提取法与回流提取法比较,其优越性是()[单选题] * A节省时间且效率高B节省溶剂且效率高(正确答案)C受热时间短D提取量较大18、有机溶剂加热提取中药成分应采用()[单选题] *A回流装置(正确答案)B蒸馏装置C萃取装置D分馏装置19、大黄素型蒽醌母核上的羟基分布情况是()[单选题] * A一个苯环的β位B苯环的β位C在两个苯环的α或β位(正确答案)D一个苯环的α或β位20、下列不能作为极性吸附剂的是()[单选题] *A活性炭(正确答案)B氧化铝C硅胶D氧化镁21、区别挥发油与油脂常用的方法是()[单选题] *A相对密度B溶解性C油迹试验(正确答案)D沸点22、组成木脂素的单体基本结构是()[单选题] *AC5-C3BC5-C2CC6-C3(正确答案)DC6-C423、香豆素与浓度高的碱长时间加热生成的产物是()[单选题] * A脱水化合物B顺式邻羟基桂皮酸(正确答案)C反式邻羟基桂皮酸D醌式结构24、具有光化学毒性的中药化学成分类型是()[单选题] *A多糖B无机酸C鞣质D呋喃香豆素(正确答案)25、属于挥发油特殊提取方法的是()[单选题] *A酸提碱沉B水蒸气蒸馏(正确答案)C煎煮法D浸渍法26、中药补骨脂中的补骨脂内脂具有()[单选题] *A抗菌作用B光敏作用(正确答案)C解痉利胆作用D抗维生素样作用27、E连续回流提取法(正确答案)能用乙醇作溶剂提取的方法有(多选)()* A浸渍法(正确答案)B渗漉法(正确答案)C煎煮法D回流提取法(正确答案)28、挥发性成分的提取,常用的是()[单选题] *A溶剂提取法B水蒸气蒸馏法(正确答案)C超临界液体萃取法D超声提取法29、以下哪种方法是利用混合中各成分在溶剂中的溶解度不同或在冷热情况下溶解度显著差异的原理而达到分离的()[单选题] *A沉淀法B分馏法C结晶法(正确答案)D升华法30、以葛根素为指标成分进行定性鉴别的中药是()[单选题] *A葛根(正确答案)B黄芩C槐花D陈皮。
(完整版)反应工程课后答案完整版.
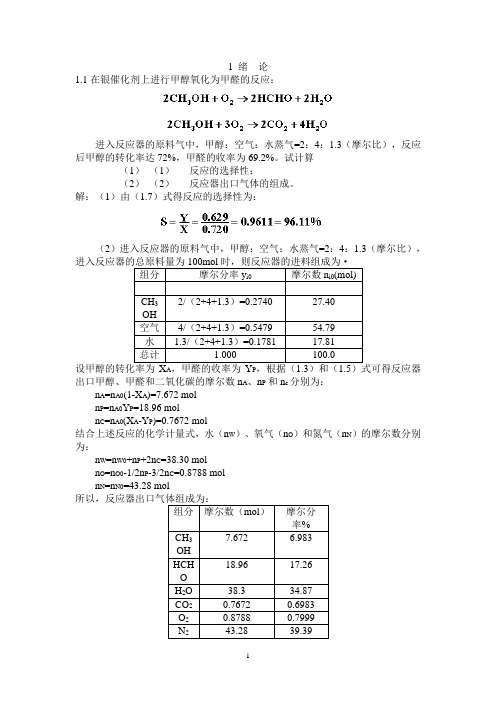
1 绪论1.1在银催化剂上进行甲醇氧化为甲醛的反应:进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1)(1)反应的选择性;(2)(2)反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),组分摩尔分率y i0 摩尔数n i0(mol)CH32/(2+4+1.3)=0.2740 27.40OH空气4/(2+4+1.3)=0.5479 54.79水 1.3/(2+4+1.3)=0.1781 17.81总计 1.000 100.0A P出口甲醇、甲醛和二氧化碳的摩尔数n A、n P和n c分别为:n A=n A0(1-X A)=7.672 moln P=n A0Y P=18.96 moln C=n A0(X A-Y P)=0.7672 mol结合上述反应的化学计量式,水(n W)、氧气(n O)和氮气(n N)的摩尔数分别为:n W=n W0+n P+2n C=38.30 moln O=n O0-1/2n P-3/2n C=0.8788 moln N=n N0=43.28 mol组分摩尔数(mol)摩尔分率%7.672 6.983CH3OH18.96 17.26HCHOH2O 38.3 34.87CO2 0.7672 0.6983O2 0.8788 0.7999N2 43.28 39.392 反应动力学基础2.4在等温下进行液相反应A+B→C+D,在该条件下的反应速率方程为:若将A和B的初始浓度均为3mol/l的原料混合进行反应,求反应4min时A的转化率。
解:由题中条件知是个等容反应过程,且A和B的初始浓度均相等,即为1.5mol/l,故可把反应速率式简化,得由(2.6)式可知代入速率方程式化简整理得积分得解得X A=82.76%。
2.6下面是两个反应的T-X图,图中AB是平衡曲线,NP是最佳温度曲线,AM是等温线,HB是等转化率线。
《化学反应工程》(第四版)课后习题答案详解

(3)两个CSTR串联
VR C A0 x A1 C A0 ( x A2 x A1 ) 根据 V0 rA1 rA2
m 1 m2
C A0 x A1 C A0 ( x A2 x A1 ) kCA0 (1 x A1 )C A0 x A1 kCA0 (1 x A2 )C A0 x A2 1 ( x A2 x A1 ) ; (1 x A1 ) (1 x A2 ) x A2
x A1
0
xA2 dxA dxA 4.35 2 2 x A1 (1 x ) (1 x A1 ) A1
1 1 1 1 4.35 1 x A1 1 x A2 1 x A1 1 1 4.35; 1 x A1 1 5.35 4.35; 1 x A2 1 5.35; x A1 0.81; 1 x A1
1 1 8.314 0.7 1 ln[ / ln ] 423 T2 83.681000 1 0.7 1 0.6 1 1 8.314 0.9347 ; 423 T2 83.681000
T2 441K
习题3-5解答
C A0
1 C B 0 2.0 1.0mol / L 2 CP 0 CR 0 0; xAf CB 0 xBf 1.0 0.8 0.533 xBf 0.8; ; C A0 1.5 CA 1.5 (1 0.533) 0.7; CP CR CB0 xBf 1.0 0.8 0.8;
1 5 0.99 t2 ln 5.81(h) 4 0.615 0.307 5 (1 0.99)
分析:等当量配料,随转化率提高,反应时间迅速增长; 若采用过量组分配料,随转化率提高,反应时间增长放慢。
李绍芬《反应工程》课后习题答案

李绍芬《反应工程》课后习题答案1 绪 论1.1在银催化剂上进行甲醇氧化为甲醛的反应:3222CH OH O 2HCHO 2H O +→+ 32222CH OH 3O 2CO 4H O +→+进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1) (1) 反应的选择性;(2) (2) 反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:0.629Y S 0.961196.11%X 0.720====(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),组分 摩尔分率y i0 摩尔数n i0(mol) CH 3OH 2/(2+4+1.3)=0.2740 27.40 空气 4/(2+4+1.3)=0.5479 54.79 水 1.3/(2+4+1.3)=0.1781 17.81 总计 1.000 100.0A P 出口甲醇、甲醛和二氧化碳的摩尔数n A 、n P 和n c 分别为:n A =n A0(1-X A )=7.672 mol n P =n A0Y P =18.96 moln C =n A0(X A -Y P )=0.7672 mol结合上述反应的化学计量式,水(n W )、氧气(n O )和氮气(n N )的摩尔数分别为:n W =n W0+n P +2n C =38.30 mol n O =n O0-1/2n P -3/2n C =0.8788 mol n N =n N0=43.28 mol组分 摩尔数(mol ) 摩尔分率% CH 3OH 7.672 6.983 HCHO 18.96 17.26 H 2O 38.3 34.87 CO 2 0.7672 0.6983 O 2 0.8788 0.7999 N 2 43.28 39.391. 1. 2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:23CO 2H CH OH +⇔23222CO 4H (CH )O H O +⇔+ 242CO 3H CH H O +⇔+24924CO 8H C H OH 3H O +⇔+222CO H O CO H +⇔+由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩原料气 Bkg/h 粗甲醇 Akmol/h100kmol 放空气体原料气和冷凝分离后的气体组成如下:(mol )组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 2 1.46 0.82 CH 4 0.55 3.62 N 2 2.92 10.29粗甲醇的组成为CH 3OH 89.15%,(CH 3)2O 3.55%,C 3H 9OH 1.10%,H 2O 6.20%,均为重量百分率。
化学反应工程(梁斌)习题答案

rA=kCACBb/a 请问后一种速率方程式是否正确,为什么?
习题 2.3
什么是基元反应?
反应物分子在碰撞中一步直接转化为生成物分子的反应.
通常对基元反应而言,可以说:单分子反应、双分 子反应、三分子反应
• r=k+θAθB-k-θCθV
• r=k(pApB-pc/K)/(1+KApA+KBpB+KcPc)2
• k=k+KAKB
K=k+KAKB/(k-KC)
习题2.10
• (2) 机理:A+σ1Aσ B+σ2Bσ2 Aσ1+Bσ2Cσ2+σ2 (控制步骤) Cσ2C+σ2
• 在210℃等温条件下,进行亚硝酸乙酯的气相分解反 应
C2H5ONO NO 0.5CH3CHO 0.5C2H5OH
该反应为一级不可逆反应,反应速率常数与温度的关系
为:
k 1.39 1014 exp( 37700)
RgT
活化能E的单位为cal/mol,若反应在恒容下进行,系统起 始状态为1at的纯亚硝酸乙酯,试计算亚硝酸乙酯分 解率为80%时,亚硝酸分解速率及乙醇的生成速率.
习题2.1
• C6H12O6+6O2+inert=6CO2+ 6H2O+inert
• mol
20.96 79 0.04
79 t=0
• mol 20.96(1-x) 79 0.04+20.96x 20.96x 79 t=t
• 反应前后O2与CO2摩尔数之和应不变,则反应后总 摩尔数为:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第二章均相反应动力学
1、有一反应在间歇反应器中进行,经过8min后,反应物转化掉80%,经过18min后,
转化掉90%,求表达此反应的动力学方程式。
3、在间歇反应器中有一级液相可逆反应,初始反应时C A0=0.5mol/L,C P0=0反应8min
后,A的转化率为1/3,而平衡转化率是2/3,求此反应的动力学方程式.
解:
根据一级可逆反应积分式
5、恒温恒容的气相反应A →3P,其动力学方程为,在反应过程中系统总压p t及组分A的分压均为变量,试推导的表达式.解:
8、纯气相组分A在一等温等容间歇反应器中按计量式进行反应,实验测得如下数据,
时间/min 0 2 4 6 8 10 12 14 ∝分压p A/MPa 0.1 0.08 0.0625 0.051 0.042 0.036 0。
032 0.028 0。
020 用积分法求此反应的动力学方程式.
解:由于当时,常数,因此假设为一级可逆反应.
第三章均相反应过程
1、液相一级等温反应在间歇釜中达到70%转化率需要12min,若此反应移到同温度下
平推流反应器和全混流反应器中进行时,所需要的空时和空速各为多少?解:
3、液相反应在一间歇反应器中进行,反应速率如下表所示:
C A/mol/L 0.1 0.2 0.3 0.4 0。
5 0.6 0。
7 0。
8 1。
0 1。
3 2.0
(—r A)/mol/(L.min)0.1 0.3 0.5 0.6 0。
5 0。
25 0.10 0。
06 0.05 0。
045
0.042
(2)
5、丙烷裂解为乙烯的反应可表示为
C3H8→C2H4+CH4(忽略副反应)
在772℃等温反应时,动力学方程为-,其中k=0。
4h-1。
若系统保持恒压p=0。
1MPa,ν0=0。
8m3/h(772℃,0。
1MPa),求当x A=0。
5时,所需平推流反应器的体积大小。
解:恒压变容反应
8、一级反应A→P,在一体积为VP的平推流反应器中进行,已知进料温度为150℃,活化能为84kJ·mol—1,如改用全混流反应器,其所需体积设为Vm,则Vm/Vp应有何关系?当转化率为0.6时,如果使Vm=Vp,反应温度应如何变化?如反应级数分别为n=2,1/2,−1时,全混流反应器的体积将怎样改变?
解:
PPT课件答案
1、在间歇反应器中进行液相反应A+B→P,C A0=0.307mol/L,测得二级反应速率常数
k=61.5×10—2L/(mol·h),计算当C B0/C AO=1和5时,转化率分别为0.5,0.9,0。
99所需要的反应时间,并对计算结果加以讨论。
2、已知:苯醌与环戊二烯在25℃下进行液相二烯合成反应A+B→C
(—r A)=;k=9。
92×10-3[m3/kmol·s];C AO=0。
1[kmol/m3];C BO=0.08[kmol/m3];x A=0。
95;
t/=1[h];每天处理300kg环戊二烯.求:反应器有效容积?
;(—r A)==
[h]
V=
3、在等温间歇反应器中进行乙酸乙酯皂化反应: CH3COOC2H5+NaOH→CH3COONa+C2H5OH 该反应对乙酸乙酯及氢氧化钠均为一级。
反应开始时乙酸乙酯及氢氧化钠的浓度均为 0.02mol/l,反应速率常数等于5。
6l/mol.min.要求最终转化率达到95%。
试问: (1)当反应器的反应体积为1m3时,需要多长的反应时间? (2)若反应器的反应体积为2m3时,所需的反应时间又是多少?
解:(1)t=C A0∫0XA f dX A/(—RA)=CA0∫0XAfdXA/[k2A0C2A0 (1-XA)2]
=1/(kCA0) ×XA/(1—XA) =1/(5。
6×0.02)×0。
95/(1-0。
95)
=169.6min(2.83h)
(2)因为间歇反应器的反应时间与反应器的大小无关,所以反应时间仍为2.83h。
4、平推流反应器中进行二级反应,当进料初浓度从30%降到4%,若要求反应结果的残余浓度维持在0。
1%,问进料流率应作如何调整?
5、。
