第六章 气体动理论 习题课
气体动理论习题课
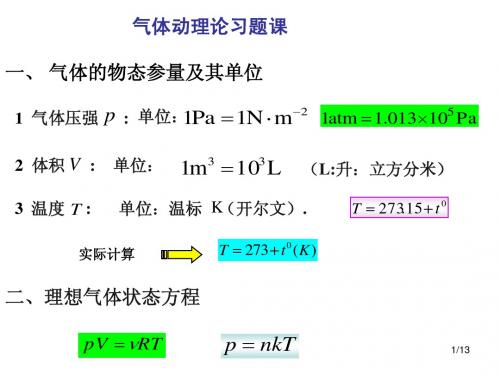
5 E氧 = ν RT 2
2 ε 转动 = ν RT 2
12/13
9 .某理想气体定压摩尔热容为 29.1J ⋅ mol −1 ⋅ K −1 。求它 某理想气体定压摩尔热容为 在温度为273 K时分子平均转动动能. = 1.38 × 10 −23 J ⋅ K −1 时分子平均转动动能. 在温度为 时分子平均转动动能 k
2/13
五、理想气体压强、温度的统计意义 理想气体压强、
2 P = nε k 3
εk
1 3 2 = m v = kT 2 2
p = nkT
六、三种速率
v =
2
3 kT = m
3 RT M
2kT 2 RT vp = = m M
v ≈ 1 . 60
kT = 1 . 60 m
RT M
3/13
七、理想气体自由度数目
i E = ν RT 2
pV氧 = ν 氧 RT
E氧 = ν 氧
5 RT 2
E氦 = ν 氦
3 RT 2
pV氦 = ν 氦 RT
2. 压强为 、体积为 的氢气(视为刚性分子理想气体)内能为: 压强为p、体积为V的氢气 视为刚性分子理想气体)内能为: 的氢气( (A)
5 PV 2 3 (B) PV 2
i C P = CV + R = R + R 2
2(C P − R ) CP i= = 2 − 1 = 5 R R
可见是双原子分子。 可见是双原子分子。只有两个转动自由度
2 ε r = kT = kT = 3.77 × 10 − 21 J 2
13/13
气体动理论习题课 一、 气体的物态参量及其单位
1 气体压强 2 体积 V : 3 温度 T :
气体动理论习题课(新)

∞
7、对分布曲线的进一步讨论
fm(v) 已知平衡态下的N个粒子系统 个粒子系统, 已知平衡态下的 个粒子系统,
f (v)
其速率分布曲线如图。 其速率分布曲线如图。求 (1) 速率 1 间的粒子数。 2 在V0 →2V0 间的粒子数。 (2) 速率 o 分布函数的极大值为多少? 分布函数的极大值为多少
∫
v2 v 1
v N d
N
速率间隔V 速率间隔 1 →V2内分子的速率之和占 总分子的比率。 总分子的比率。
5、求标准状态下氧气的 、 (1) 单位体积中分子数 单位体积中分子数n (2) 分子质量 分子质量m (3) 质量密度ρ 质量密度ρ
Mm m= = NA
P n= = K T
ρ = nm
2
(4) 分子间的平均距离 。 分子间的平均距离l。
1 (t +r +2s) RT —1mol气体的内能 m 气体的内能 2
2、容器中装有理想气体,容器以速率 运动,当容 、容器中装有理想气体,容器以速率v运动 运动, 器突然停止,则容器温度将升高。 器突然停止,则容器温度将升高。 若有两个容器,一个装有 ,另一装有H 若有两个容器,一个装有He,另一装有 2,如果它 们以相同速率运动,当它们突然停止时, 们以相同速率运动,当它们突然停止时,哪一个容器 的温度上升较高? 的温度上升较高
kT i = (t + r + 2s) ⋅ = kT 2 2
=
理想气体的内能: 理想气体的内能: U
1 du η = ρ vλ 黏性 dK = −η ( ) z0 A ⋅ dt 3 dz dT 1 非平衡态下的输运过程 热传导 dQ = −k( ) z0 A ⋅ dt k = ρ v λ C V 3 dz dρ 1 自扩散 dM = − D( ) z0 A ⋅ dt D = v λ 3 dz
物理答案第六章气体动理论答案-ZSH

物理答案第六章⽓体动理论答案-ZSH第六章⽓体动理论6-1 处于平衡状态的⼀瓶氦⽓和⼀瓶氮⽓的分⼦数密度相同,分⼦的平均平动动能也相同,则它们( C ) (A)温度、压强均不相同.(B)温度相同,但氦⽓压强⼤于氮⽓压强. (C)温度、压强都相同.(D)温度相同,但氦⽓压强⼩于氮⽓压强.6-2 三容器A 、B 、C 中装有同种理想⽓体,其分⼦数密度 n 相同,⽽⽅均根速率之⽐为4:2:1)(:)(:)(212212212=CBAv v v ,则其压强之⽐C B A P P P :: 为( C )(A) 4:2:1 (B) 8:4:1 (C) 16:4:1 (D) 1:2:46-3 在⼀个体积不变的容器中,储有⼀定量的某种理想⽓体,温度为0T 时,⽓体分⼦的平均速率为0v ,分⼦平均碰撞次数为0Z ,平均⾃由程为0λ,当⽓体温度升⾼为04T 时,⽓体分⼦的平均速率为v ,分⼦平均碰撞次数为Z ,平均⾃由程为λ分别为( B ) (A) 04v v =,04Z Z =,04λλ= (B) 02v v =,02Z Z =,0λλ= (C) 02v v =,02Z Z =,04= (D) 04v v =,02Z Z =,0=6-4 已知n 为单位体积的分⼦数,)(v f 为麦克斯韦速率分布函数,则dv v nf )(表⽰()(A) 速率v 附近,d v 区间内的分⼦数(B) 单位体积内速率在v ~ v +d v 区间内的分⼦数 (C) 速率v 附近d v 区间内分⼦数占总分⼦数⽐率(D) 单位时间内碰到单位器壁上速率在v ~ v +d v 区间内的分⼦数6-5 温度为0℃和100℃时理想⽓体分⼦的平均平动动能各为多少?欲使分⼦的平均平动动能等于1eV,⽓体的温度需多⾼?解:=1ε231kT =5.65×2110-J=2ε232kT =7.72×2110-J 由于1eV=1.6×1910-J , 所以理想⽓体对应的温度为:T=2ε/3k =7.73×310 K6-6 ⼀容器中储有氧⽓,其压强为0.1个标准⼤⽓压,温度为27℃,求:(1)氧⽓分⼦的数密度n ;(2)氧⽓密度ρ;(3)氧⽓分⼦的平均平动动能k ε?解: (1)由⽓体状态⽅程nkT p =得,242351045.23001038.110013.11.0?===-kT p n 3m - (2)由⽓体状态⽅程RT M MpV mol= (M ,mol M 分别为氧⽓质量和摩尔质量) 得氧⽓密度:13.030031.810013.11.0032.05mol ====RT p M V Mρ 3m kg -? (3) 氧⽓分⼦的平均平动动能21231021.63001038.12323--?===kT k ε6-7 在容积为2.0×33m 10-的容器中,有内能为6.75×210J 的刚性双原⼦理想⽓体分⼦,求(1)⽓体的压强;(2)设分⼦总数5.4×2210个,求⽓体温度;(3)⽓体分⼦的平均平动动能?解:(1)由2iRT M m =ε以及RT M mpV =可得⽓体压强 p =iVε2=1.35×510 Pa (2)分⼦数密度V Nn =, 得该⽓体的温度62.3===NkpV nk p T ×210K (3)⽓体分⼦的平均平动动能为=ε23kT =7.49×2110-J6-8 2100.2-?kg 氢⽓装在3100.4-?m 3的容器内,当容器内的压强为51090.3?Pa 时,氢⽓分⼦的平均平动动能为多⼤?解:由RT M m pV =得 mR MpV T = 所以221089.32323-?=?==mRMpVk kT εJ6-9 1mol 刚性双原⼦⽓体分⼦氢⽓,其温度为27℃,求其对应的平动动能、转动动能和内能各是多少?(求内能时可不考虑原⼦间势能)解:理想⽓体分⼦的能量为RT in E 2=,所以氢⽓对应的平动动能为(3=t ) 5.373930031.8231==t J转动动能为(2=r ) 249330031.8221==r εJ内能5=i 5.623230031.8251==i ε J6-10 设有N 个粒⼦的系统,其速率分布如图所⽰,求:(1)分布函数)(v f 的表达式; (2)速度在1.50v 到2.00v 之间的粒⼦数;(3) N 个粒⼦的平均速率;解:(1)从上图所给条件得:≥=≤≤=≤≤=)2(0)()2()()0(/)(00000v v v Nf v v v a v Nf v v v av v Nf 由此可得分布函数表达式为:≥≤≤≤≤=)2(0)2(/)0(/)(00000v v v v v Na v v Nv av v f 类似于概率密度的归⼀化条件,故)(v f 满⾜?+∞∞-1d )(=v v f ,即=+00020,1d d v v v v a v v av 计算得032v Na =,带⼊上式得分布函数)(v f 为:≥≤≤≤≤=)2(0)2(32)0(3/2)(0000020v v v v v v v v v v v f (2)该区间对应的)(v f 为常数32v N,所以可通过计算矩形⾯积得该区间粒⼦数为: N v v v N N 31)5.12(32000=-=(3) N 个粒⼦平均速率+===∞∞+∞-00020202d 32d 32d )(d )(v v v v v v v v v v v vf v v vf v 0911v = 6-11 设N 个粒⼦系统在各速率区间对应的粒⼦数变化率为:Kdv dN = (为常量K v V ,0>>),0=dN (V v >)(1)画出速率分布函数图;(2)⽤N 和V 表⽰常量K ;(3)⽤V 表⽰出平均速率和⽅均根速率。
普通物理学第五版第6章气体动理论答案(精品课件)

解:
μ gh
M gh
P = P0 e kT =P0 e RT
ln
P P0
=
Mg h RT
h=
RT Mg
ln P P0
=
8.31×273 28×10-3×9.8
ln
0.75
= 2.3km
结束 目录
6-15 求压强为1.013×105Pa、质量为 2×10-3kg、容积为1.54×10-3m3的氧气的 分子的平均平动动能。
结束 目录
解:P = ( h1 h2)d =(0.76 0.60)×1.33×105 Pa
V = 0.28×2.0×10-4 =5.6×10-4 m3
T = 273+27=300 K
M = 0.004 kg/mol
PV
=
m M
RT
m
=
M PV RT
=
0.04×0.16×1.33×105×5.6×10-4 8.31×300
提示:
2 p
01e- x2dx =0.847
2 p
0∞e- x2dx =1
结束 目录
解:(1)
v=
v0pv dN vp dN
0
=
vp 0
v
3e
vp 0
v
2e
dv v 2
v
2
p
dv v 2
v
2
p
令
x=
v vp
dv= vp dx
v
=
vp
1 0
1 0
x 3e-x
2 dx
x 2e-x 2 dx
结束 目录
6-3 一封闭的圆筒,内部被导热的不漏 气的可移动活塞隔为两部分。最初,活塞位 于筒中央,圆筒两侧的长度 l1= l2。 当两侧 各充以T1、p1,与T2、p2的相同气体后,问 平衡时活塞将在什么位置上( 即 l1/l2 是多 少)?已知 p1=1.013×105Pa, T2= 680K, p2 = 2.026×105Pa, T2 =280K。
气体分子动理论习题解PPT课件

1 mv2 3 kT,可得
2
2
N 1 mv2 3 NkT
2
2
即
N
1 2
mv2
3 2
RTN
/(Nd m)
3 (M 2
/
M mol )RT
3 2
(RT
/
M mol )V
7.31106
E
1 2
(M
/
M mol )iRT
(V
/
M mol )
1 2
iRT
4.16104
J
(v2 )1/2
(v
2 2
)1/
2
(v21)1/2
(1) 气体分子的平动动能总和. (2) 混合气体的压强. (普适气体常量R=8.31 J·mol-1·K-1 )
3 kT 8.281021 J
2
Ek
N
( N1
N2)
3 kT 2
4.14105 J
p nkT 2.76 105 Pa
第6页/共10页
17.一瓶氢气和一瓶氧气温度相同.若氢气分子的平均平动动能为 = 6.21×10-21
[B]
8.速率分布函数f(v)的物理意义为:
(A) 具有速率v的分子占总分子数的百分比.
(B) 速率分布在v附近的单位速率间隔中的分子数占总分子数的百分比.
(C) 具有速率v的分子数.
(D) 速率分布在v附近的单位速率间隔中的分子数.
[B ]
9.设某种气体的分子速率分布函数为f(v),则速率在v 1─v 2区间内的分子的平均速
4.一瓶氦气和一瓶氮气密度相同,分子平均平动动能相同,
而且它们都处于平衡状态,则它们
(A) 温度相同、压强相同.
大学物理热学习题课

dN m 32 4 ( ) e Ndv 2kT
v2
对于刚性分子自由度 单原子 双原子 多原子
i tr
(1)最概然速率
2kT 2 RT RT vp 1.41 m
(2)平均速率
i=t=3 i = t+r = 3+2 = 5 i = t+r = 3+3 =6
6、能均分定理
8kT 8 RT RT v 1.60 m
M V RT ln 2 M mol V1
QA
绝热过程
PV 常量
M E CV T M mol
(2)由两条等温线和两条绝热线 组成的循环叫做 卡诺循环。 •卡诺热机的效率
Q0
Q2 T2 卡诺 1 1 Q1 T1
M P1V1 P2V2 A CV T M mol 1
E 0
•热机效率
A Q1 Q2
M E CV T M mol M Q C P T M mol
A Q1 Q2 Q2 1 Q1 Q1 Q1
A=P(V2-V1) 等温过程
A
E 0
Q1 Q2 •致冷系数 e W Q1 Q2
热机效率总是小于1的, 而致冷系数e可以大于1。
定压摩尔热容
比热容比
CP ( dQ )P dT i2 i
8、平均碰撞次数 平均自由程
z
2d v n
2
CV •对于理想气体:
Cp
v z
1.热力学第一定律
1 2 2d n
二、热 力 学 基 础
Q ( E2 E1 ) A dQ dE dA
准静态过程的情况下
4. 摩尔数相同的两种理想气体 一种是氦气,一种是氢气,都从 相同的初态开始经等压膨胀为原 来体积的2倍,则两种气体( A ) (A) 对外做功相同,吸收的热量 不同. (B) 对外做功不同,吸收的热量 相同. (C) 对外做功和吸收的热量都不 同. (D) 对外做功和吸收的热量都相 同. A=P(V2-V1)
(完整版)《大学物理》习题册题目及答案第6单元 气体动理论

第6单元 气体动理论 序号 学号 姓名 专业、班级一 选择题[ C ]1.在标准状态下, 若氧气(视为刚性双原子分子的理想气体)和氦气的体积比2121=V V ,则其内能之比21/E E 为: (A) 1/2 (B) 5/3 (C) 5/6 (D) 3/10[ B ]2.若理想气体的体积为V ,压强为p ,温度为T ,一个分子的质量为m ,k 为玻耳兹曼常量,R 为摩尔气体常量,则该理想气体的分子数为(A) pV/m (B) pV/(kT)(C) pV/(RT) (D) pV/(mT)[ D ]3.若)(v f 为气体分子速率分布函数,N 为分子总数,m 为分子质量,则 )(21221v Nf mv v v ⎰ d v 的物理意义是 (A) 速率为v 2的各分子的总平均动能与速率为v 1的各分子的总平均动能之差。
(B) 速率为v 2的各分子的总平动动能与速率为v 1的各分子的总平动动能之和。
(C) 速率处在速率间隔v 1~ v 2之内的分子的平均平动动能。
(D) 速率处在速率间隔v 1~ v 2之内的分子平动动能之和。
[ D ]4.在一密闭容器中,储有A 、B 、C 三种理想气体,处于平衡状态,A 种气体的分子数密度为 1n ,它产生的压强为 1p ,B 种气体的分子数密度为 12n ,C 种气体的分子数密度为3n 1,则混合气体的压强p 为(A)31p (B)41p(C)51p (D)61p二 填空题1.在定压下加热一定量的理想气体,若使其温度升高1K 时,它的体积增加了0.005倍,则气体原来的温度是_________200k__________。
2.用总分子数N 、气体分子速率v 和速率分布函数f(v),表示下列各量:(1)速率大于0v 的分子数= ⎰∞0)(v dv v Nf ;(2)速率大于0v 的那些分子的平均速率=⎰⎰∞∞00)()(v v dv v f dv v vf ;(3)多次观察某一分子的速率,发现其速率大于0v 的概率=⎰∞0)(v dv v f 。
华东理工大学《大学物理》第六章 气体动理论习题及答案

ΔT = 2ΔE m Ri M
= 2 ×1012 ×1.6 ×10 −19 0.1× 8.31× 3
= 1.28×10 −7 K
6、质量为 50.0g、温度为 180c的氮气装在容积为 10.0 升的密闭绝热容器内,容器以 v=200m/s的速率作匀速直线运动,若容器突然停止运动,其定向运动的动能全部转化为 分子热运动的动能,那么,平衡后氮气的温度和压强将各增大多少?
解:(1)Q v = ∴z =
8RT
P = nkT
πM
2πd 2 vn = 4d 2 N 0 P 3πm
M
E
E = m 6 RT M2
(2) v p =
2RT = M
2E 3m
(3) εk
=
3 2
kT
=
ME 2N A m
(其中NA为阿伏伽德罗常数)
12、一真空管的真空度为 1.33×10-3Pa,试求在 270C时单位体积的分子数及分子平均自 由程。设分子的有效直径d=3.0×10-10m。 解: n = P = 1.33 × 10 −3 = 3.22 × 1017 个 m 3
× 300
= 1.00 ×10 −8 J
3) εk转总 = NkT = 1.61×1012 ×1.38×10−23 × 300 = 6.67 ×10−9 J
4) εk总 = εk平总 + εk转总 = 1.67 ×10−8 J
39
大学物理习题册题解
5、一能量为 1012eV的宇宙射线粒子,射入一氖管中,氖管中含有氖气 0.1mol。如果宇 宙射线粒子的能量全部被氖气分子所吸收而变为热运动能量,问氖气温度升高多少度? 解:等容吸热 ΔE = m i RΔT
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
vp =
m f ( v p ) = 4π e 2π kT
T1(> T2)
2 kT m m − 2 kT
2kT m
=
4 m e 2π kT
1 2
O
vp1 vp2
v
5.理想气体处于平衡状态设温度为T气体的自由度为 则每个 .理想气体处于平衡状态设温度为 气体的自由度为 气体的自由度为i,则每个 气体分子所具有的[ 气体分子所具有的 C ]
i A:动能为 2 kT : i C:平均动能为 kT : 2
i B:动能为 2 RT :
i D:平均平动动能为 2 RT :
6. 1mol刚性双原子分子理想气体,当温度为 时,其内能为 . 刚性双原子分子理想气体, 刚性双原子分子理想气体 当温度为T时 [C]
3 A: 2 RT
3 B: kT 2
5 C: 2 RT
2 E转 = RT 5 E = RT 2
5.平衡状态下,温度为127℃的氢气分子的平均速率 .平衡状态下,温度为 ℃ 3 3 为 2.06×10 m/ s,方均根速率为 2.23×10 m/ s ,最可几速率 3 为 1.82×10 m/ s。 解: v = 8 RT
πµ
v =
2
3RT
µ
vp =
2 RT
2 2
=1
EHe EO2
3 ( nRT ) He 3 =2 = 5 ( nRT )O2 5 2
三、计算题
3 1.体积 V = 1m 的容器内混有 N1 = 1.0 × 10 25 个氧气分子和 .
N 2 = 4.0 × 10 25 氮气分子 混合气体压强为 2.76 × 10 5 Pa 。求 氮气分子, (1) 气体分子的平均平动动能;(2) 气体的温度。 气体分子的平均平动动能; 气体的温度。
3 D: kT 2
7.下列各图所示的速率分布曲线,哪一图中的两条曲线是 .下列各图所示的速率分布曲线, 同一温度下氮气和氦气的分子速率分布曲线? [ 同一温度下氮气和氦气的分子速率分布曲线 B ]
f (v )
f ( v)
f (v )
f ( v)
(A)
(B)
O
O
(C)
(D)
O
v O
v
v
v
二、填空题 1.一容器内储有氧气,其压强为1.01×103Pa,温度为27℃则气 .一容器内储有氧气,其压强为 ,温度为 ℃ 2.44×1025 m-3 ,氧气的密度为 1.3 体分子的数密度为 kg/m3 ;分子的平均平动动能 6.21×10-25 J 。 解: P = nkT
第6章 气体动理论 习题课 章
一、选择题 1.在一个密闭容器中储存有ABC三种气体,处于平衡状态, .在一个密闭容器中储存有 三种气体, 三种气体 处于平衡状态, A种气体的分子数密度为 1,它产生的压强为 1,B种气体的 种气体的分子数密度为n 它产生的压强为P 种气体的分子数密度为 种气体的 分子数密度为2n 气体的分子数密度为3n 分子数密度为 1,C气体的分子数密度为 1,则混合气体的 气体的分子数密度为 压强为 [ D ] A:3P1 : B: 4P1 : C: 5P1 : D: 6P1 :
解:(1) 由 f(v) 的归一化条件 得 (2) a
∫
∫
∞ 0
∞
0
f (v)dv = 1 ⇒ ∫ Nf (v)dv = N
0
∞
1 2N Nf (v)dv = N = v0 a + v0 a ⇒ a = 2 3v0
(3) N ′ = (4)
∫
3 v0 2 v0 2
av v0N f (v) = aN 1 1 v0 a 1 7N Nf (v)dv = v0 a − + v0 a = 2 2 2 2 2 12
解:(1) Ek =
3 3 p 3 pV kT = = 2 2 n 2 N1 + N 2
2.76 ×105 ×1 = 1.5 × = 8.3 ×10−21 J 5.0 ×1025 pV 2.76 ×105 ×1 = = 400k (2) T = ( n1 + n2 ) R (16.6 + 66.4 ) × 8.31
3m PV A: : 2M
3 3M B: : : PV C: 2 PV 2µ
3µ D: 2M N A PV :
3 3 P 3 PV M 3 m 解:P = nkT ⇒ ε k = kT = = = PV 2 2n 2 N M 2M
4.已知一定量的某种理想气体,在温度为T1与T2时的分子最可 .已知一定量的某种理想气体,在温度为 几速率分别为v 分子速率分布函数的最大值分别为f(v 几速率分别为 p1和vp2,分子速率分布函数的最大值分别为 p1) 和f(vp2),若T1>T2,则 [ B ] , A:vp1 >vp2 f(vp1)> f(vp2) B:vp1>vp2 f(vp1) < f(vp2) : > : C:vp1<vp2 f(vp1) < f(vp2) D:vp1<vp2 f(vp1) > f(vp2) : : 解:
3.下列各式中,表示气体分子的平均平动动能的是(式中,M .下列各式中,表示气体分子的平均平动动能的是(式中, µ 为气体质量, 为气体的摩尔质量, 为气体分子质量 为气体分子质量, 为气 为气体质量, 为气体的摩尔质量,m为气体分子质量,N为气 体分子数目, 为气体分子数密度 为气体分子数密度, 为阿伏加德罗常数) 体分子数目,n为气体分子数密度,NA为阿伏加德罗常数) [ A]
2.储有氧气的容器以速率100 m/s运动,假设该容器突然停止, .储有氧气的容器以速率 运动, 运动 假设该容器突然停止, 全部定向运动的动能都变为气体分子热运动的动能, 全部定向运动的动能都变为气体分子热运动的动能,问容器中 氧气的温度将会上升多少? 氧气的温度将会上升多少? 解:
1 2 5m mv = RT 2 2µ
v =
2
解:
3RT
µ
3PV µ 3P = = µ M ρ
−2 3.已知氧气的压强 p = 2.026 Pa,体积 V = 3.0 × 10 m3,则其 . , 。 内能 E = 0.15J M 5 5 解: E = RT = PV µ 2 2
4.1摩尔 ℃氢气具有的总的平动动能为 3739.5J ,总的转动 . 摩尔 摩尔27℃ 动能为 2493J ,内能为 6232.5J 。 解: E平 = 3 RT
µ
6. 两容器中分别贮有氦气和氧气(视为刚性双原子分子的理想 两容器中分别贮有氦气和氧气( 气体)已知氦气的压强是氧气压强的1/2,氦气容积是氧气的2 气体)已知氦气的压强是氧气压强的 ,氦气容积是氧气的 试问, 倍,试问,氦气内能是氧气内能的 35 倍。 解:
M i PV = RT µ 2
( pV )He ( nRT ) He = ( pV )O ( nRT )O
3 3P ε k = kT = 2 2n
M Pµ ρ= = V RT
5
2.某理想气体处于平衡状态,已知压强为 p = 1.013 × 10 Pa,密 .某理想气体处于平衡状态, , 度为 ρ = 1.24 × 10 −2 kg/m3,则该气体分子的方均根速率为 v 2 =
4.95×103 m/ s 。
32 × 10−3 ×1002 T= = = 7.7k 5R 5 × 8.31
µv2
3.有N个质量均为 的同种气体分子,它们的速率分布如图所 . 个质量均为m的同种气体分子 个质量均为 的同种气体分子, 说明曲线与横坐标所包围面积的含义; 示 (1) 说明曲线与横坐标所包围面积的含义; (2) 由N和v0求a值;(3) 求速率在 v0 和 3v0 间的分子数; 间的分子数; 和 值 2 2 (4) 求分子的平均平动动能 Nf (v)
0
v0
2v0
v
ε kt = ∫
∞
0
v0 1 2 v0 1 1 2 31 2 2 av 2 a mv f (v )dv = ∫ mv dv + ∫ mv dv = mv0 0 2 v0 2 2 v0 N N 36
P 解: P = n1kT ⇒ kT = 1 1 n1
P = nkT = (n1 + n2 + n3 )kT = 6n1kT = 6 P 1
2.速率分布函数f(v)的物理意义为 [ B ] .速率分布函数 的物理意义为 A:具有速率 的分子占总分子数的百分比 :具有速率v的分子占总分子数的百分比 B:速率分布在 附近的单位速率间隔中的分子数占总分子数的 :速率分布在v附近的单位速率间隔中的分子数占总分子数的 百分比 C:具有速率 的分子数 :具有速率v的分子数 D:速率分布在 附近的单位速率间隔中的分子数 :速率分布在v附近的单位速率间隔中的分子数
