2011年哈工大物理化学考研真题
2011年全国硕士研究生入学统一考试农学门类联考化学真题及详解【圣才出品】

圣才电子书
【答案】D
十万种考研考证电子书、题库视频学习平 台
【解析】选项中 3 种化合物,均为第 V 主族元素的氢化物,是化学性质相似的同系物。
NH3(l)中存在分子间氢键,分子间力最强,相同温度下蒸汽压最低;AsH3(l)分子变
形性比 PH3(l)大,故分子间色散力较强,相同温度下蒸汽压较低。
B.-270.8kJ·mol-1
十万种考研考证电子书、题库视频学习平 台
C.-343.3kJ·mol-1
D.-541.6kJ·mol-1
【答案】B
【解析】由 ×反应式(1)+ ×反应式(2)+反应式(3)得
故
3.用 HCl 标准溶液标定 NaOH 溶液,由于滴定管读数时最后一位数字估测不准而产 生误差,为减少这种误差可以采用的方法是( )。
圣才电子书
十万种考研考证电子书、题库视频学习平
台
2011 年全国硕士研究生入学统一考试农学门类联考化学真题及详解
一、单项选择题:1~30 小题,每小题 2 分,共 60 分。下列每题给出的四个选项中, 只有一个选项是符合题目要求的。
1.在 298K 和标准状态时,下列反应均为非自发反应,其中在高温时仍为非自发的反 应是( )。
6.将 AgNO3 溶液和 KI 溶液混合制得 AgI 溶胶,测得该溶胶的聚沉值为: Na2SO4,140mmol;Mg(NO3)2,6.0mmol。该溶胶的胶团结构式为( )。
A. B. C. D. 【答案】A 【解析】离子所带的电荷越高,其聚沉能力越强;聚沉值越小,表示该电解质对溶胶 的聚沉能力越大,该溶胶应为负电溶胶。A 项,为负电溶胶;B 项,胶团结构式错误。
A.零级 B.一级 C.二级 D.三级 【答案】C 【解析】一个复杂的化学反应速率由最慢的基元反应(定速步骤)的速率来决定。反 应 2NO+H2=N2+H2O2 为定速步骤,其速率正比于 NO 浓度的二次方,所以该反应对于 NO 是二级反应。
哈工大复材所考研-初试-2011

2011年研究生入学考试材料学(航天学院)专业试题一、概念题(每题5分,8题共40分)1.晶界工程:玻璃相处于陶瓷结构中的晶界位置,是影响陶瓷性能的重要显微组成,提高晶界的结晶化程度可以改善陶瓷的高温性能。
此项研究称为“晶界工程”。
2.玻璃陶瓷:对于某些玻璃,通过适当控制反玻璃化过程,可以得到无残余应力的微晶玻璃,这种材料称为玻璃陶瓷。
3.RTM:RTM是“Resin Transfer Molding”的缩写,意思为树脂传递模塑工艺,它是一种先进的、聚合物基复合材料闭模成型的工艺方法。
4.烧蚀型防热:是利用材料的分解、解聚、蒸发、气化及离子化等化学和物理过程带走大量热能,并利用消耗材料本身来换取隔热效果。
5.材料设计:材料设计是指在材料科学的理论知识和已有经验的基础上,利用计算机技术,按预定性能要求,确定材料组分和结构,并预测达到预定性能要求应选择的工艺手段和工艺参数。
6.相变增韧:陶瓷中裂纹尖端的应力场引起裂纹尖端附近的晶体结构发生相变,当相变使该局部区域发生体积膨胀时,体积膨胀会使基体裂纹闭合,从而改善了陶瓷材料的断裂韧性。
7.界面:复合材料的界面是指基体与增强物之间化学成分有显著变化的、构成彼此结合的、能起载荷传递作用的微小区域。
8.微观复合材料:增强相的尺寸为纳米等级的材料称为纳米复合材料,增强相尺寸控制在埃级,即原子或分子水平的称为杂化材料,两者统称为微观复合材料,它们主要用作新型结构材料或功能材料。
二、问答题(每题10分,8题共80分)1.聚合物基复合材料的功能性有哪几种?答:五种:耐烧蚀性好;有良好的摩擦性能,包括良好的摩阻特性及减摩特性;高度的电绝缘性能;优良的耐腐蚀性能;有特殊的光学、电学、磁学的特性。
2.根据使用温度范围,金属基体分哪几类?答:金属与合金种类繁多,目前用作金属基复合材料的金属有铝及铝合金,镁合金,钛合金,镍合金,铜与铜合金,锌合金,铅,钛铝、镍铝金属间化合物等。
哈工大化学系考研真题

哈工大化学系考研真题哈工大化学系考研真题考研,对于许多大学生来说,是他们迈向更高学术层次的一道门槛。
而在众多考研科目中,化学系的考研难度一直以来都是备受关注的。
作为中国著名的高校之一,哈尔滨工业大学化学系的考研真题更是备受瞩目。
本文将围绕哈工大化学系考研真题展开讨论,探究其特点和应对策略。
首先,我们来了解一下哈工大化学系考研真题的特点。
从往年的考研真题中可以看出,哈工大化学系注重考察学生的基础知识和应用能力。
在选择题方面,往往会涉及到化学的基本概念、原理和实验技术等方面的内容。
而在解答题方面,重点考察学生对于化学原理的理解和应用能力。
此外,哈工大化学系的考研真题还注重对学生的综合能力的考察,往往会涉及到跨学科的知识点,要求学生能够灵活运用所学的化学知识。
那么,面对哈工大化学系考研真题,我们应该如何应对呢?首先,我们要重视基础知识的学习。
化学是一门基础学科,掌握好基础知识是考研成功的关键。
我们可以从课本出发,系统地学习化学的基本概念、原理和实验技术等方面的内容。
此外,我们还可以通过参加化学系的学术讲座和实验室实践等活动,加深对化学知识的理解和应用。
其次,我们要注重解题技巧的培养。
解答题是哈工大化学系考研真题的重点,而解答题的得分往往取决于解题的方法和策略。
在解答题时,我们可以先通读题目,理清思路,确定解题的步骤和方法。
在解题过程中,我们要注重逻辑推理和实际应用,灵活运用所学的化学知识。
此外,我们还要注重解题的细节,注意计算和单位的转换等问题,避免因为细节错误导致失分。
最后,我们要注重综合能力的培养。
哈工大化学系考研真题往往会涉及到跨学科的知识点,要求学生能够将所学的化学知识与其他学科进行结合,解决实际问题。
因此,我们要注重跨学科的学习,积极参加相关的学术讲座和研讨会,拓宽自己的学术视野。
同时,我们还可以通过参加科研项目和实验室实践等活动,提升自己的实际操作和实验设计能力。
综上所述,哈工大化学系考研真题的特点和应对策略是我们备战考研的重要参考。
2011年真题801物理化学

(a) 标准状态下自发变化的方向 (b) 在 ∆ r Gm 所对应的温度下的平衡位置 (c) 在标准状态下体系所能作的最大非膨胀功 (d) 提高温度反应速率的变化趋势
�
第 1 页 共 6 页
7. 在通常情况下,对于二组分物系能平衡共存的最多相为: (a ) 1 (b)2 (c ) 3 (d)4 8. 下列说法中,哪些是不正确的 : (a)沸点随压力增加而增加 (c)升华温度随压力增加而增加
二、计算题(90 分)
°C、101.325kPa 下恒压加热至体 1.(10 分)1mol 氨气(NH3)(可视为理想气体 )于 25 25° 积为原来的三倍,已知氨气的恒压摩尔热容为
−1 −1 C� = 25.89 + 33.0 ×10−3 T − 30.46 ×10−7 T 2 p , m / J ⋅ K ⋅ mol
(d) 无法确定
14. 已知如下图示,玻璃管两端各有一大小不等的肥皂泡,中间用活塞相连,打开 活塞后_______。 (a) 两泡的大小保持不变 (b) 两泡均变小 (c) 大泡变小,小泡变大 (d) 小泡变小,大泡变大
r1
r2
15. 反应 2O3 → 3O 2 的速率方程为 −
d[O3 ] = k[O3 ]2 [O2 ]−1 ,或者 dt
(b)熔点随压力增加而增加 (d)蒸气压随压力增加而增加
9. 电解质溶液导电性能理解,正确的是: (a)与金属铜导电性能一样 (b)温度升高导电能力减小; (c)浓度增大导电能力增大 (d)导电机理是离子定向迁移和电极反应 10. 用电导仪测未知溶液的电导, 将一定浓度的标准 KCl 溶液注入电导池中进行测 定,其目的是: (a)做空白试验 (b)校正零点 (c)求电导池常数 (d)作工作曲线 11. 用对消法测定电池电动势,若实验中发现检流计始终偏向一边,则可能原因是: (a)测定电池温度不均匀 (b)测定电池的两极接反了 (c)搅拌不充分使浓度不均匀 (d)检流计灵敏度差 12. 玻璃毛细管中汞面上的饱和蒸气压比水平汞表面上的饱和蒸气压 _______。 (a ) 小 ( b) 大 (c) 相等 (d)不能确定 13. 硅胶吸水后其表面吉布斯自由能将 _______。 (a) 降低 (b) 升高 (c) 不变
哈工大 2011工程流体力学

,d=60mm,h=3m。
管路的沿程阻
2
三、证明:超声速气流通过正激波后必然变成亚声速流动。
(10分)
四、绝能等熵空气流动中,已知点1的马赫角μ
1=27.70,点2的马赫角μ
2
=35.80,
请问这是等熵膨胀还是等熵压缩流动?这两点的压强比p
1/p
2
=?(20分)
3.根据泽尔多维奇、弗兰克-卡门涅茨基和谢苗诺夫理论,分析在一维圆管内流动条件下,预混可燃气体的层流火焰传播速度受哪些因素的影响?(10分)
4.煤粉燃烧的方式主要包括旋流煤粉燃烧和直流煤粉燃烧两大类。
请从煤种
适应性、着火稳定性、燃尽性能,以及运行经济性等方面对上述两种燃烧方式进行综合评价。
(15分)。
2011年物理化学试题

2011年攻读硕士学位研究生入学考试北京市联合命题物理化学试题(请把答案写在答题纸上)一.选择正确的答案:(每小题2分,共计50分)1.下列说法中不正确的是:( 1 )用热力学方法不能测热力学能的绝对值;( 2 )理想气体的热力学能只与温度有关,且与气体物质的量成正比;( 3 ) N种气体混合物的热力学能等于混合前N种气体的热力学能之和;( 4 ) 热力学能是系统状态的单值函数。
2. 在隔离系统内( 1 ) 热力学能守恒,焓守恒;( 2 ) 热力学能守恒,焓不一定守恒;( 3 )热力学能不一定守恒,焓守恒;( 4 ) 热力学能、焓均不一定守恒。
3. 理想气体从状态I等温自由膨胀到状态II,可用哪个状态函数的变量来判断过程的自发性。
(1)∆G(2)∆U(3)∆S(4)∆H4. 公式d G =-S d T + V d p可适用下述哪一过程:(1) 在298 K,100 kPa下水蒸气凝结成水的过程;(2) 在一定温度压力下,由N2( g ) + 3H2( g )合成NH3( g )的过程;(3) 电解水制H2( g )和O2( g )的过程;(4)理想气体膨胀过程。
5. 下述说法哪个是正确?(1) 水的生成焓即是氧的燃烧焓 (2) 水蒸气的生成焓即是氧的燃烧焓(3)水的生成焓即是氢气的燃烧焓(4) 水蒸气的生成焓即是氢气的燃烧焓6. 对一个化学反应,若知其∑νB C p, m(B) > 0 ,则:(1)∆r H随温度升高而减小;(2)∆r H随温度升高而增大;(3)∆r H不随温度升高而改变;(4)∆r H随温度变化没有规律;7. 克拉贝龙-克劳修斯方程式可用于:(1)固气两相平衡;(2)固液两相平衡;(3)固固两相平衡;(4)液液两相平衡。
8. 下列关于偏摩尔量的理解,错误的是:( 1 )只有广度性质的物理量才有偏摩尔量;( 2 )偏摩尔量是广度性质;( 3 )纯物质的偏摩尔量就是其摩尔量(4)偏摩尔Gibbs自由能是化学势9. 指出关于亨利定律的下列几点说明中,错误的是:(1)溶质在气相和在溶剂中的分子状态必须相同;(2)溶质必须是非挥发性溶质;(3)温度愈高或压力愈低,溶液愈稀,亨利定律愈准确;(4)对于混合气体,在总压力不太大时,亨利定律能分别适用于每一种气体,与其他气体的分压力无关。
哈尔滨工业大学2007-2011年硕士研究生入学考试复试试题
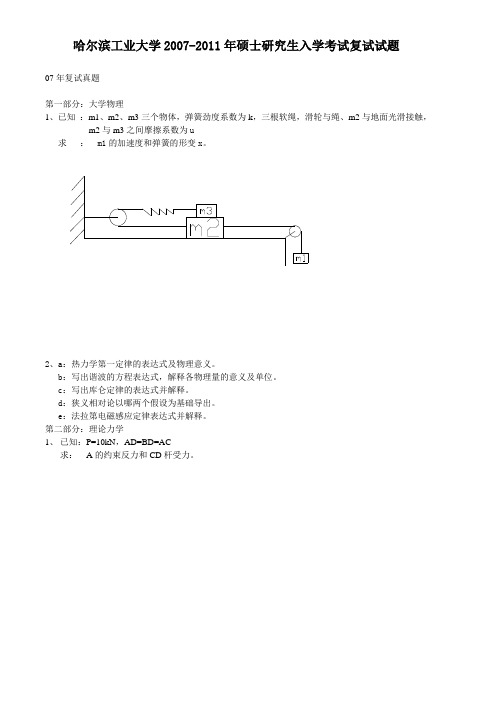
哈尔滨工业大学2007-2011年硕士研究生入学考试复试试题07年复试真题第一部分:大学物理1、已知:m1、m2、m3三个物体,弹簧劲度系数为k,三根软绳,滑轮与绳、m2与地面光滑接触,m2与m3之间摩擦系数为u求: m1的加速度和弹簧的形变x。
2、a:热力学第一定律的表达式及物理意义。
b:写出谐波的方程表达式,解释各物理量的意义及单位。
c:写出库仑定律的表达式并解释。
d:狭义相对论以哪两个假设为基础导出。
e:法拉第电磁感应定律表达式并解释。
第二部分:理论力学1、已知:P=10kN,AD=BD=AC求:A的约束反力和CD杆受力。
2、已知:一光滑圆柱体用绳子缠绕,如图下落,从起点下落h 时质心速度v =32gh 3求:圆柱体平面运动方程第三部分:材料力学1、L=11 h=8 b=10求Me= ,d= ,[bs δ] [τ] 。
校核2、 已知:J2=2J1求:最大挠度第四部分:电工技术1、求电流的初始值2、a:叠加定理b:把电阻性负载联结到三相电路中,分别联成星形和三角形。
c:已知:u=310sinwt,f=50HZ求:U的有效值和当t=0.1s时的瞬时值d:叙述基尔霍夫电压和电流定律e:可编程控制器的英文缩写是什么?工作方式是什么?f:用电流表、电压表测电流、电压时与电路或负载如何联结?第五部分:电子技术1、已知:三人表决器设计,原则:少数服从多数,不可弃权写出真值表及逻辑表达式推理过程,并用“与非”门设计电路。
2、a:什么叫反馈、正反馈及负反馈?b:二极管主要参数是什么?第六部分:自动控制1、已知:施加一外力f(t),求:物体的运动微分方程和传递函数G(S)=Y(s)/F(S)。
S+23S +32S+4S+52、a:已知系统的特征方程为 D(s)=4用劳斯稳定判据判断其稳定性。
b:自动控制系统稳定性的概念。
c:写出控制系统典型输入信号的函数表达式:脉冲函数,阶跃函数,速度函数。
d:开环传递系统和闭环传递系统的定义。
2011年硕士研究生招生入学考试试题A

5、水能完全润湿洁净玻璃,而水银则不能。现将一根玻璃毛细管插入水中,管内液面将,若在管内液面处加热,则液面将;当玻璃毛细管插入水银中时,管内液面将,若在管内液面处加热,则液面将。(请填写上升、下降或不变)
6、所谓临界温度是指。已知CO2的临界温度约为31.0℃,临界压力约为7.38 MPa,则在40 ℃和10 MPa时,CO2以液态存在。(请填能或不能)
(A)左移(B)右移(C)不动(D)无法判断
7、20℃时,浓度均为10 mmol·kg-1的LaCl3、CaCl2、NaCl三种水溶液,离子平均活度因子γ±由大到小的顺序为:
(A)LaCl3>CaCl2>NaCl(B)LaCl3> NaCl > CaCl2
(C)CaCl2>LaCl3>NaCl(D)NaCl >CaCl2> LaCl3
4、(本题15分)有一原电池Ag | AgCl(s) | Cl-(a=1)||Cu2+(a=0.01)| Cu。
(1)写出上述原电池的反应式;
(2)计算该原电池在25℃时的电动势E;
(3)25℃时,原电池反应的吉布斯函数变(rGm)和平衡常数K 各为多少?
已知:E (Cu2+|Cu) = 0.3402V,E (Cl-|AgCl|Ag) =0.2223 V。
(A)0.993(B)0.812(C)0.181(D)0.0183
14、下列体系属于两相体系的是哪个?
(A)左旋酒石酸和右旋酒石酸的固态混合物
(B)水-乙醇的液态混合物
(C)金属铜和镍形成的固溶体
(D)大小不一的一堆纯净冰决
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
哈尔滨工业大学
2010年硕士研究生考试物理化学试题
一.填空题(20分)
1、C (s )和CO (g )、CO 2(g )、O 2在700℃达到平衡,则该系统的自由度数为( )
2、某一化学反应在一定条件下的平衡转化率为50%,加入催化剂后,保持其他反应条件不变,反应速率增加了20倍,此时的平衡转化率将是( )
3、在T 、P 恒定的条件下,某反应达到平衡时A 的平衡转化率为x A ,1,
保
持T 、P 不变,加入惰性气体,此时A 的平衡装化率为x A ,2,那么 x A ,1、 x A ,
2的大小关系为(
)
4、电极的极化现象是( )
5、1mol 双原子分子理想气体B 从300K 分别经恒温和恒压过程升温至400K ,则两过程熵变之差为,即∆S (恒压)−∆S (恒容)=( )
6、写出(ðV/ðT)P 、(ðP/ðT)V 、(ðS/ðV)T 、(ðS/ðP)T 这四个量之间的两个等量关系式( )
7、在一定温度下,当KCl 溶液中KCl 的物质的量浓度c = ( )时,该溶液的电导率与其摩尔电导率数值上相等。
8、在101.325 kPa 的压力下,I 2在液态水和四氯化碳中达到分配平衡(无固态碘存在),则该系统的条件自由度( )
9、将克拉贝龙方程用于水的液固两相平衡,因为()()m 2m 2V H O,l V H O,s 〈,所以随着压力的增加,()2H O l 的凝固点将( ) 二. 选择题(20分) 1、在隔离系统内( )
A. 热力学能守恒,焓变守恒
B. 热力学不一定守恒,焓变守恒
C. 热力学能守恒,焓变不一定守恒
D. 热力学能,焓变均不一定守恒 2、戊烷标准摩尔燃烧焓−35201KJ mol -⋅,()2CO g 和()2H O g 标准摩尔生成焓分别为−3951KJ mol -⋅和−2861KJ mol -⋅,则戊烷标准摩尔生成焓为( ) A. 28391KJ mol -⋅ B. −28391KJ mol -⋅ C. 1711KJ mol -⋅ D. −1711KJ mol -⋅
3、有一连串反应12
K K A B C −−→−−→,
下列哪些情况可能使B 的产率提高( ) A. B 很不活泼,A 很活泼 B. 反应速率关系12k k
C. A 不活泼,B 活泼
D. 尽可能延长反应时间 4、()γP,m V,m pV γ=C /C = 常量适用的条件是( )
A. 绝热过程
B. 理想气体绝热过程
C. 理想气体绝热可逆过程
D. 绝热可逆过程
5、恒温恒压下,某反应的1r m G 5kJ mol θ-∆=⋅该反应能否进行( )
A. 能正向自发进行
B. 能逆向自发进行
C. 不能判断
D. 不能进行 6、关于亨利系数,下列说法正确的是( )
A. 其值与温度、浓度、压力有关
B. 其值只与温度、溶质性质和浓度标度有关
C. 其值与溶剂性质、温度以及浓度大小有关
D. 其值与温度、溶剂和溶质的性质以及浓度标度等性质有关 7、已知373K 时液体A 的饱和蒸汽压为133.24 kPa ,液体B 的饱和蒸汽压为
66.62KPa ,设A 和B 形成理想溶液,当溶液中A 的物质量分数为0.5时,在气相中A 的物质的量分数为( )
A. 1
B. 1/2
C. 2/3
D. 1/3
8、在一定温度和压力下,对于一个化学反应,能用于判断其方向的是( ) A. r m G θ∆ B. P K C. r m G ∆ D. r m H ∆
9、某温度下,()4NH Cl s 的分解压力为p θ,则分解反应的平衡常数为p K θ为( ) A. 1 B. 1/2 C. 1/4 D. 1/8
10、某物质溶于互不相容的两液相α和β中,该物质在α相以A 的形式存在,在β相以2A 的形式存在,则定温定压下,两相平衡时( ) A. ()()2A A θθμ=μ B. ()()2A 2A θθμ=μ C. ()()22A A θθμ=μ D. 无法确定 三. 简答题(20分)
1、用3AlCl 水解制备3AlOH 溶胶,(1)请画出胶团结构;(2)用3LaNO 和NaCl 聚沉,何者聚沉能力强 ?
2、Zn 和稀硫酸作用:(a )在敞口瓶中进行(b )在封口瓶中进行,请问何者放热多?为什么?
3、在一个底部为光滑平面的抽真空的玻璃容器中,有半径大小不同的圆形汞滴,请问恒温放置一段时间后,会发生什么现象?请分别用拉普拉斯方程和开尔文方程解释这种现象。
4、为什么晴朗的天空是蓝色的? 四、计算题(90分)
1、1mol 单原子理想气体,始态为273 K ,1013225 Pa ,分别经历下列可逆变化:
(1)恒温下压力加倍(2)绝热不可逆反抗恒外压0.5×1013225 Pa 膨胀至平衡。
试计算上述两个过程的Q ,W ,∆U ,∆H ,∆S ,∆G ,∆A 。
已知,在273K ,1013225 Pa 下气体的摩尔熵为11100J mol K --⋅⋅(15分)
2、理想气体A 和B 发生化学反应,当保持B 的压力(1.33kPa )不变,改变A 的压力,测得反应初试速率的数据如下:
当保持A 的压力(1.33kPa )不变,改变B 的压力,测得反应初试速率的数据如下:
试计算:(1)该反应对A 和B 的级数以及总的反应级数(2)以压力表示反应速率常数(3)以浓度表示反应速率常数(反应温度为673.2K )。
(15分) 3、在一个体积恒定为V 的容器中装有A 和B 两种理想气体。
在373K ,A 和B 的压力分别是A,0P /kPa = 47.8 ,B,0P /kPa =44.8。
经下列反应:
()()()373K A g B g D g +−
−−→ 到达平衡以后系统的总压力为86.0 KPa 。
试求373K 时,(1)()D g 的平衡分压D P 及平衡组成D y (2)反应的标准平衡常数K θ (10分) 4、已知298.15K 下,有: (1)
()()()()
122424Pt,H p H SO 7mol kg Hg SO s ,Hg l θ-⋅的
1E 0.5655V,
=1E 0.61515V θ=;(2)()()()()122442Pt,H p H SO 7mol kg PbSO s ,PbO s θ-⋅的
2E 1.750V,=2E 1.68488V θ=,试求此溶液水的活度。
(15分)
5、20℃时分压为101.325 kPa 的HCl 溶于66C H 中达到平衡后,溶液中HCl 的摩尔分数是0.0425。
已知纯66C H 的饱和蒸汽压为10.01kPa 。
若HCl 和66C H 的总压为101.325 kPa ,问20℃时100g 66C H 中可以溶解多少克HCl ?(10分)
6、在100℃的水中如果只有直径为1m μ 的水泡,要是这样的水开始沸腾需要过热多少度 ?已知100℃时水的表面张力为10.0589N m -⋅,水的汽化热
1
vap m H 40.656kJ mol θ-∆=⋅。
(10分) 7、A-B 二元相图如下所示。
(1)指出各区域所存在的是什么相?(2)画出含B 40%(质量)的系统(图中R 点)从1700℃冷却至1000℃时的冷却曲线示意图。
请注明每一阶段系统有那些相?发生了哪些变化?指出自由度为多少?(3)含B 10%(质量)的系统9 Kg ,冷却至1400℃时液相中含A 多少克?(15分)。
