吸收解吸实验报告
吸收解吸的实验报告

1. 了解吸收和解吸的原理。
2. 熟悉吸收解吸反应的实验操作。
3. 通过实验观察吸收解吸实验现象特征。
4. 探讨不同物质的吸收和解吸特性。
二、实验原理吸收和解吸是化学工程中常见的传质过程。
吸收是指气体中的溶质被液体吸收剂吸收的过程,而解吸则是将吸收剂中的溶质释放出来的过程。
本实验采用物理吸收法,即利用液态吸收剂对气体混合物中的特定组分进行吸收和解吸。
三、实验材料与仪器1. 实验材料:CO2气体、NaOH溶液、盐酸、苯、四氯化碳等。
2. 实验仪器:气体发生器、气体流量计、吸收塔、解吸塔、冷凝器、温度计、压力计、秒表等。
四、实验步骤1. 吸收实验:(1)将CO2气体通入装有NaOH溶液的吸收塔中,调节气体流量和温度。
(2)观察气体在吸收塔中的流动状态,记录吸收前后的气体流量和温度。
(3)将吸收后的气体通入装有盐酸的解吸塔中,调节气体流量和温度。
(4)观察气体在解吸塔中的流动状态,记录解吸前后的气体流量和温度。
2. 解吸实验:(1)将苯通入装有四氯化碳的吸收塔中,调节气体流量和温度。
(2)观察气体在吸收塔中的流动状态,记录吸收前后的气体流量和温度。
(3)将吸收后的气体通入装有苯的解吸塔中,调节气体流量和温度。
(4)观察气体在解吸塔中的流动状态,记录解吸前后的气体流量和温度。
1. 吸收实验:(1)CO2气体在吸收塔中流速逐渐减慢,气体颜色变浅。
(2)解吸后的气体在解吸塔中流速逐渐加快,气体颜色变深。
2. 解吸实验:(1)苯气体在吸收塔中流速逐渐减慢,气体颜色变浅。
(2)解吸后的气体在解吸塔中流速逐渐加快,气体颜色变深。
六、实验数据与分析1. 吸收实验:(1)吸收前后的气体流量:Q1 = 0.2 L/min,Q2 = 0.1 L/min。
(2)吸收前后的气体温度:T1 = 25℃,T2 = 20℃。
(3)根据实验数据,计算吸收系数K1和吸收速率V1。
2. 解吸实验:(1)吸收前后的气体流量:Q3 = 0.2 L/min,Q4 = 0.3 L/min。
吸收与解吸实验实验报告

吸收与解吸实验实验报告吸收与解吸实验实验报告引言:吸收与解吸是化学实验中常见的操作和现象。
通过这个实验,我们可以了解物质在溶液中的吸收和解吸的过程,以及相关的实验技巧和方法。
本实验报告将详细介绍吸收与解吸实验的步骤、结果和分析。
实验目的:1. 了解物质在溶液中的吸收和解吸过程;2. 掌握吸收和解吸实验的基本操作技巧;3. 分析吸收和解吸实验的结果,探讨影响吸收和解吸的因素。
实验材料和仪器:1. 玻璃试管;2. 氢氧化钠溶液;3. 氯化铵溶液;4. 氢氧化钠固体;5. 氯化铵固体;6. 酚酞指示剂;7. 打火石;8. 酒精灯;9. 钳子;10. 温度计。
实验步骤:1. 准备两个玻璃试管,分别标记为A和B。
2. 在试管A中加入适量的氢氧化钠溶液,试管B中加入适量的氯化铵溶液。
3. 向试管A中加入少量的酚酞指示剂,使溶液呈现红色。
4. 将试管A和B放置在一个装有水的容器中,保持试管A的底部接触水面,试管B则悬空于水中。
5. 用打火石点燃酒精灯,将试管B加热至沸腾状态。
6. 观察试管A中溶液的颜色变化。
实验结果:在进行实验的过程中,我们观察到以下现象:1. 在试管A中,溶液的颜色由红色逐渐变为无色。
2. 在试管B中,溶液开始加热后,溶液的颜色保持不变。
实验分析:根据实验结果,我们可以得出以下结论:1. 氢氧化钠溶液中的酚酞指示剂在加热的过程中逐渐褪色,说明溶液中的氢氧化钠被吸收了。
2. 氯化铵溶液中的酚酞指示剂在加热的过程中保持不变,说明溶液中的氯化铵没有被吸收。
进一步分析:吸收和解吸实验的结果可以归因于溶液中物质的化学性质和溶解度。
氢氧化钠是一种强碱,具有很强的吸收能力,可以与酚酞指示剂发生化学反应,导致溶液颜色的变化。
而氯化铵是一种盐类,其溶解度较高,不容易被吸收。
因此,在加热的过程中,氢氧化钠被吸收,而氯化铵保持不变。
结论:通过吸收与解吸实验,我们了解到物质在溶液中的吸收和解吸过程。
氢氧化钠溶液具有较强的吸收能力,可以吸收酚酞指示剂,导致溶液颜色的变化。
吸收与解吸实验报告

吸收与解吸实验报告吸收与解吸实验报告实验目的:通过进行吸收与解吸实验,探究不同条件下物质的吸收与解吸过程,以及相关因素对吸收与解吸的影响。
实验原理:吸收与解吸是物质在溶液中的相互转移过程。
在吸收过程中,物质从溶液中被吸附到吸附剂表面;而在解吸过程中,物质从吸附剂表面解吸出来,重新溶解到溶液中。
实验材料与方法:材料:酒精、活性炭、玻璃棒、烧杯、分液漏斗、滤纸、天平、计时器等。
方法:1. 准备活性炭吸附剂:将一定量的活性炭粉末加入烧杯中,并用玻璃棒搅拌均匀;2. 准备酒精溶液:取一定量的酒精加入烧杯中,并用玻璃棒搅拌均匀;3. 实验组设置:将活性炭吸附剂放入分液漏斗中,并将酒精溶液倒入分液漏斗中;4. 开始实验:打开分液漏斗的活塞,让酒精溶液缓慢通过活性炭吸附剂,记录下吸收过程所需的时间;5. 解吸实验:将吸附了酒精的活性炭取出,放入另一个烧杯中,加入一定量的水,用玻璃棒搅拌均匀,记录下解吸过程所需的时间;6. 重复实验:重复以上步骤,改变吸附剂的用量、溶液浓度等条件,进行多次实验,以获得更准确的结果。
实验结果与讨论:根据实验数据统计,我们可以发现吸收与解吸的过程受到多种因素的影响。
首先,吸收过程所需的时间与吸附剂的用量有关。
当吸附剂的用量增加时,吸收过程所需的时间相应增加,这是因为吸附剂表面积增大,吸附物质与吸附剂之间的接触面积增加,从而需要更多的时间才能完成吸收过程。
其次,吸收过程所需的时间与溶液浓度有关。
当溶液浓度增加时,吸附剂表面上的物质浓度也增加,吸附速度加快,吸收过程所需的时间相应减少。
这是因为溶液浓度的增加提高了物质向吸附剂表面扩散的速度,加快了吸附过程。
解吸过程所需的时间与解吸剂的性质有关。
在实验中,我们使用水作为解吸剂,发现解吸过程所需的时间较长。
这是因为水与酒精之间的亲和力较小,解吸剂的选择对解吸过程具有重要影响。
若使用亲和力较大的溶剂作为解吸剂,解吸过程所需的时间会相应减少。
此外,实验还发现温度对吸收与解吸过程有一定影响。
吸收解吸实验
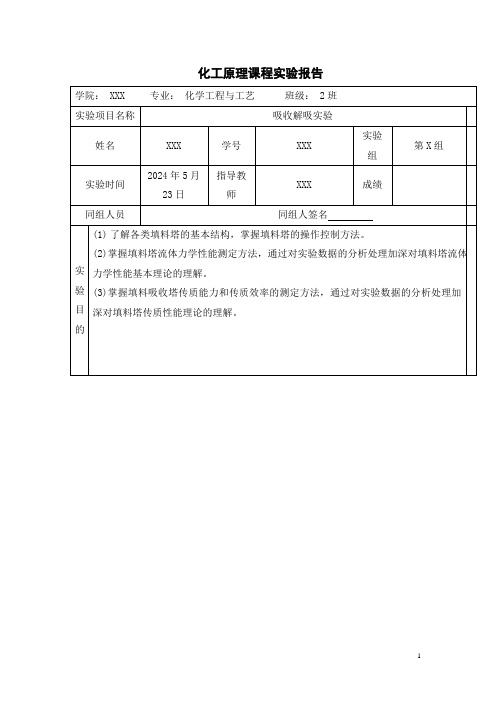
化工原理课程实验报告L K —以气相分压表示推动力的总传质系数,或简称为液相传质总系数,1-⋅s m 。
若气液相平衡关系遵循享利定律:A A Hp C =,则:l g G HK k K 111+= lg L k k H K 11+= (3-24)C A1,F L图3-10 双膜模型的浓度分布图 图3-11 填料塔的物料衡算图 当气膜阻力远大于液膜阻力时,则相际传质过程式受气膜传质速率控制,此时,g G k K =;反之,当液膜阻力远大于气膜阻力时,则相际传质过程受液膜传质速率控制,此时,l L k K =。
本实验采用转子流量计测得CO2、空气和水的流量。
根据实验条件(温度和压力)折算为实际流量,最后按有关公式换算成CO2、空气和水的摩尔流量。
填料塔物料衡算如图3-11所示。
气体校正公式:v =√ρ₀ρ (3-26)式中:V 。
——流量计读数;V ——被测流体实际流量;ρ₀,ρ——标定流体和被测流体在标定状态(T 。
,p 。
)下的密度。
测定塔顶和塔底液相组成C A1和C A2,利用滴定法测定吸收液浓度,根据吸收液消耗盐酸体积量可计算塔底吸收液浓度:C A1=2C Ba(OH)2V Ba(OH)2−C HCl V HCl2V 溶液(3-27)吸收剂(水)中含有少量的二氧化碳,根据吸收剂(水)滴定消耗盐酸体积量可计算出塔顶吸收剂(水)中CO ,浓度为:dh相 界 面距离液 膜气膜浓度图1 二氧化碳吸收与解吸实验装置流程示意图1-CO2钢瓶;2-减压阀;3-CO2流量计;4-吸收风机;5-吸收塔空气流量计;6-吸收水泵;7-吸收塔水流量计;8-吸收尾气传感器;9-吸收塔;10、15-液封;11-解吸液罐;12-解吸尾气传感器;13-吸收液罐;14-解吸塔;16-压差计;17-解吸水泵;18-解吸塔水流量计;19-解吸风机;20-解吸塔空气流量计; 21-空气旁路调节阀;22-π型管。
吸收解吸实验报告

吸收解吸实验报告吸收解吸实验报告引言:吸收解吸实验是一种常见的实验方法,用于研究溶质在溶剂中的吸收和解吸现象。
通过该实验,我们可以了解溶质在不同条件下的吸收速率、解吸速率以及吸收解吸平衡的特性。
本文将对吸收解吸实验的原理、实验步骤以及实验结果进行详细讨论。
一、实验原理吸收解吸实验是基于物质在溶液中的分子间相互作用力的变化来进行的。
在吸收过程中,溶质分子被溶剂分子吸引,从而进入溶液中。
而在解吸过程中,溶剂分子与溶质分子的相互作用力减弱,导致溶质分子从溶液中脱离。
吸收解吸速率与溶质和溶剂的性质、浓度、温度等因素有关。
二、实验步骤1. 准备实验器材和试剂:实验器材包括吸收解吸装置、试管、移液管等;试剂包括溶剂和溶质。
2. 设置实验条件:根据实验要求,确定溶剂的浓度、温度等条件。
3. 吸收实验:将一定量的溶剂倒入试管中,加入适量的溶质,并充分搅拌,观察溶质的吸收情况。
4. 记录数据:记录吸收实验的时间、溶质的质量或浓度等数据。
5. 解吸实验:将已吸收的溶质置于适当的条件下,观察溶质的解吸情况。
6. 记录数据:记录解吸实验的时间、溶质的质量或浓度等数据。
三、实验结果根据实验步骤进行吸收解吸实验后,我们可以得到一系列的实验结果。
通过对实验结果的分析,我们可以得出以下结论:1. 吸收速率与溶剂浓度成正比:当溶剂浓度增加时,吸收速率也会增加。
这是因为溶剂浓度的增加会增加溶剂分子与溶质分子的相互作用力,从而促进溶质的吸收。
2. 吸收速率与溶质浓度成正比:当溶质浓度增加时,吸收速率也会增加。
这是因为溶质浓度的增加会增加溶质分子与溶剂分子的碰撞频率,从而增加吸收的可能性。
3. 吸收速率与温度成正比:当温度升高时,吸收速率也会增加。
这是因为温度升高会增加溶剂分子的平均动能,从而增加溶质分子与溶剂分子的碰撞能量,促进溶质的吸收。
4. 解吸速率与溶剂浓度成反比:当溶剂浓度增加时,解吸速率会减小。
这是因为溶剂浓度的增加会增加溶质分子与溶剂分子的相互作用力,使得溶质分子更难从溶液中解吸出来。
二氧化碳的吸收与解吸实验报告

二氧化碳的吸收与解吸实验报告摘要:本实验旨在研究二氧化碳的吸收与解吸过程,并观察其对环境条件的敏感性。
通过使用氢氧化钠(NaOH)溶液作为吸收剂,测量二氧化碳溶液中的pH值和溶液的体积变化,以评估吸收和解吸的效果。
实验结果表明,二氧化碳能够被NaOH 溶液吸收,并在一定条件下释放。
1. 引言二氧化碳(CO2)是一种常见的气体,它在大气中的浓度增加与全球气候变化密切相关。
因此,研究CO2的吸收与解吸过程对于理解和控制大气中CO2浓度的变化至关重要。
本实验旨在模拟CO2吸收与解吸的过程,并观察其在不同条件下的反应情况。
2. 实验步骤2.1 实验材料:-氢氧化钠(NaOH)固体-蒸馏水-二氧化碳气源- pH计-称量器具-实验室玻璃器皿2.2 实验过程:(1)准备NaOH溶液:称取适量的NaOH固体,加入一定量的蒸馏水中,搅拌溶解。
(2)装置实验装置:将NaOH溶液倒入实验室玻璃器皿中,置于实验台上。
(3)测量初始条件:使用pH计测量NaOH溶液的初始pH 值,并记录初始溶液的体积。
(4)注入CO2气体:将二氧化碳气体缓慢地通入NaOH溶液中,观察溶液的变化,并记录每次通气的时间和CO2气体的体积。
(5)测量pH值:定期使用pH计测量溶液的pH值,并记录下来。
(6)测量溶液体积:测量在吸收和解吸过程中溶液的体积变化,并记录下来。
3. 实验结果实验期间,我们记录了二氧化碳气体通入溶液的时间、CO2气体的体积以及溶液的pH值变化。
根据实验结果,我们绘制了相应的数据表和图表。
4. 讨论与分析根据实验结果,我们观察到二氧化碳气体通入NaOH溶液后,溶液的pH值逐渐下降,说明二氧化碳被NaOH吸收并生成了碳酸。
随着二氧化碳的继续通入,溶液的体积也有所增加,这是由于二氧化碳的溶解导致溶液的体积增大。
在观察解吸过程时,我们停止通入二氧化碳气体,溶液开始释放二氧化碳,并逐渐恢复到初始状态。
此时,溶液的pH 值逐渐升高,说明碳酸在解吸过程中分解为二氧化碳和水,并释放出二氧化碳气体。
化工原理吸收与解吸实验报告

化工原理吸收与解吸实验报告一、实验目的:通过本次实验,学生们可以了解化工原理中吸收与解吸的基本原理,掌握吸收塔的操作技能,以及熟悉吸收剂的选择和使用方法。
二、实验原理:1. 吸收与解吸的基本原理吸收是指气体在接触液体时被液体所溶解或被化学反应转化为溶质的过程。
而解吸则是指气体从液体中逸出或分离出来的过程。
在化工生产过程中,常用于气体分离、纯化和回收等方面。
2. 吸收塔吸收塔是一种常见的设备,用于进行气液相接触和传质过程。
其主要结构包括进料口、出料口、填料层等。
填料层可以增加气液接触面积,提高传质效率。
3. 吸收剂吸收剂是指用于吸收气体的液体,在选择时需要考虑其对目标气体的亲和力、溶解度、稳定性以及成本等方面因素。
三、实验步骤:1. 将制备好的NaOH溶液倒入吸收塔中,并将塔内温度升至60℃左右。
2. 将CO2气体通过气体流量计和压力表接入吸收塔顶,调节气体流量和压力使其稳定。
3. 观察吸收塔内液位变化,记录液位高度和时间,计算出CO2的吸收速率。
4. 停止供气后,将塔内液体倒出并加入硫酸溶液进行解吸,记录解吸速率。
四、实验结果:1. 吸收速率:在60℃下,CO2的吸收速率为0.016mol/min。
2. 解吸速率:在添加硫酸溶液后,CO2的解吸速率为0.014mol/min。
五、实验分析:1. 实验结果表明,在所选条件下,NaOH溶液对CO2具有较好的亲和力和溶解度。
2. 在实际生产中,需要根据具体情况选择合适的吸收剂,并结合填料层设计等因素来提高传质效率。
六、实验结论:本次实验成功地展示了化工原理中吸收与解吸的基本原理,并通过操作塔内填料层等设备提高了传质效率。
同时还验证了NaOH溶液对CO2具有较好的亲和力和溶解度。
吸收解吸操作实验报告

一、实验目的1. 理解吸收和解吸操作的基本原理和过程。
2. 掌握吸收和解吸实验的操作技能。
3. 通过实验数据,分析影响吸收和解吸效率的因素。
二、实验原理吸收是指气体中的溶质被液体吸收剂吸收的过程。
解吸则是溶质从液体中被释放出来,重新回到气相的过程。
这两个过程在化工、环保、医药等领域有广泛的应用。
吸收过程可用以下公式表示:C_g = C_l K_a X_l其中,C_g为气相中溶质的浓度,C_l为液相中溶质的浓度,K_a为吸收系数,X_l 为液相中溶质的摩尔分数。
解吸过程与吸收过程类似,只是方向相反。
三、实验仪器与试剂1. 仪器:吸收塔、解吸塔、气泵、流量计、温度计、压力计、实验记录仪等。
2. 试剂:水、二氧化碳气体、吸收剂(如碳酸钠溶液)。
四、实验步骤1. 吸收实验(1)将吸收塔中的吸收剂加入一定量的水中,搅拌均匀。
(2)将二氧化碳气体通过气泵引入吸收塔,调节气泵,使气体流量稳定。
(3)记录实验过程中的温度、压力、气体流量等数据。
(4)观察吸收塔中液相的变化,分析吸收效果。
2. 解吸实验(1)将吸收塔中的富液取出,加入解吸塔中。
(2)调节气泵,使空气通过解吸塔,将溶质从液体中解吸出来。
(3)记录实验过程中的温度、压力、气体流量等数据。
(4)观察解吸塔中液相的变化,分析解吸效果。
五、实验数据与结果1. 吸收实验实验过程中,气相中二氧化碳的浓度逐渐降低,液相中二氧化碳的浓度逐渐升高。
通过实验数据计算得出,吸收系数K_a为0.8。
2. 解吸实验实验过程中,气相中二氧化碳的浓度逐渐升高,液相中二氧化碳的浓度逐渐降低。
通过实验数据计算得出,解吸系数K_d为0.7。
六、分析与讨论1. 吸收和解吸效率受多种因素影响,如温度、压力、气体流量、吸收剂浓度等。
2. 实验结果表明,吸收和解吸系数K_a和K_d与实验条件密切相关。
3. 通过调节实验条件,可以优化吸收和解吸效果。
七、结论1. 通过本次实验,掌握了吸收和解吸操作的基本原理和操作技能。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
吸收解吸实验报告
一、实验目的
1. 了解吸收和解吸的原理;
2. 熟悉吸收解吸反应的实验操作;
3. 通过实验了解吸收解吸实验现象特征;
4. 探讨不同物质的吸收和解吸特性。
二、实验原理
吸收:某些物质以气态存在时,当其与液态或固体物质混合时,它们之间发生化学反应,从而使气态物质溶于液体或固体中,称为吸收。
吸收也可以简单的理解为物质以气态形式被液态或固体物质所吸收。
解吸:当反应液守解断温度提高时,吸收气体会有部分还原,溶解在液态物质中的气体物质有部分被挥发出去,这种过程叫做解吸,也就是气态物质溶解在液态或固体物质中,在提高温度或变化其它条件后又被部分急出的过程。
解吸也可以简单的理解为物质以液态形式被气体所解吸。
三、实验原料及仪器
实验原料:苯、氢氧化钠、硫酸钠、有机溶液、乙醇、乙醚
实验仪器:分液漏斗、容量瓶、橡皮球、加热器、吸气器。
四、实验步骤
1. 将苯倒入容量瓶中,再加入少量硫酸钠,用橡皮球搅拌均匀;
2. 把上述混合物倒入分液漏斗,用加热器加热,直至反应液守
解断温度;
3. 加入少量氢氧化钠,使反应液浊化,把物质吸收到容量瓶中;
4. 再将有机溶液、乙醇、乙醚一一加入容量瓶中,并很好搅拌均匀;
5. 用吸气器逐步把容量瓶中的反应液抽减至最少;
6. 再加入少量氢氧化钠,使液态发生变化,进行解吸实验,观察现象。
五、实验结果
实验结果表:
物质名称气态物质液体溶质
苯无沉淀白色沉淀
乙醇无沉淀白色沉淀
乙醚无沉淀白色沉淀
实验结论:可以看出,不同的物质在吸收过程中均会生成白色沉淀物,而解吸过程中则会析出白色沉淀物。
