最新第九章B有机化学基础第三节烃的含氧衍生物资料讲解
烃的含氧衍生物课件

细读教材记主干 一、醇 1.概念 羟基与 烃基 或 苯环侧链 上的碳原子相连的 化合物称为醇。
2.分类 根据醇分子里含羟基的数目,醇可分为: (1)一元醇:如甲醇的结构简式: CH3OH 。 (2)二元醇:如乙二醇的结构简式:
(3)多元醇:如丙三醇的结构简式:
3.分子通式 饱和一元醇的分子通式为 CnH2n+1OH 。 4.醇的物理性质 (1)沸点 ①随着碳原子数的增多,饱和一元醇的沸点逐渐 升高 。 ②饱和一元醇的沸点比与它相对分子质量相近的烷烃或 烯烃的 高 ,因为分子间存在 氢键 。 (2)溶解性:甲醇、乙醇、丙醇与水 以任意比例混溶 , 因为与水形成了 氢键 。
取代 反应
氧化 反应
浓硫酸 70 ℃
浓硫酸 140 ℃
②④ ①或②
CH3CH2OH― 浓17― 硫0 ℃→ 酸 CH2===CH2↑+H2O
CH3CH2OH+ HOCH2CH3― 浓14― 硫0 ℃→ 酸 CH3CH2OCH2CH3+H2O
消去 反应
取代 反应
酸性 KMnO4 或 K2Cr2O7
知识点 3 苯酚 [新知探究]
1.分子组成与结构
2.物理性质 (1)颜色: 无 色,放置时间较长时因被空气中的氧气 氧化呈 粉红 色。 (2)状态:晶体。 (3)气味: 特殊气味 。 (4)熔点:43 ℃。 (5)毒性: 有 毒,对皮肤有 腐蚀性 。 (6)溶解性:室温下在水中溶解度为 9.3 g ,温度高于 65 ℃时,能与水 混溶 ,易溶于 有机溶剂 。
Na
①
反应物 或条件
HBr △
断键 位置
②
O2(Cu) ①③ △
化学方程式
2CH3CH2OH+2Na―→ 2CH3CH2ONa+H2↑ 化学方程式
烃的含氧衍生物

②、饱和一元醇,随分子中碳原子数的增加,沸点逐渐升高。
③、醇分子中羟基数目越多,分子间形成的氢键就越强,沸点越高。
④、通常情况下,含1~11个碳原子的直链饱和一元醇为液体,含12个碳原子以上的醇为无色蜡状固体。
2CH3CH2OH+ O2 2 CH3CHO + 2 H2O,反应实质是铜先与氧气反应生成氧化铜,氧化铜再与乙醇反应。
③、被强氧化剂如酸性高锰酸钾溶液、酸性重铬酸钾溶液直接氧化成乙酸。
(3)、与HX发生取代反应:CH3CH2OH+ HX→CH3CH2X + H2O
(4)、分子间脱水:CH3CH2OH+CH3CH2OH CH3CH2OCH2CH3(乙醚)+ H2O
5、同分异构现象:(1)、碳链异构;(2)、位置异构;(3)、官能团异构:醇和醚。
二、酚
(一)、苯酚( )
1、分子结构:分子式、结构简式。
2、物理性质:纯净的苯酚是无色的晶体,露置在空气中会因被氧化而呈粉红色。苯酚具有特殊气味,熔点为43℃,在水中溶解度不大,但当温度高于65℃时,则能与水以任意比互溶。苯酚易溶于乙醇、乙醚等有机溶剂,有毒,腐蚀皮肤。
(2)、酯化反应
①、实验操作:在大试管中加入3mL乙醇,边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸;按图连好装置,用酒精灯小心均匀的加热试管3~5min,产生的蒸气经导管通到饱和碳酸钠溶液液面上。
②、实验现象:碳酸钠饱和溶液的液面上有透明的油状液体产生,并可闻到香味。
+ CH3CH2OH (乙酸乙酯)+ H2O
3、化学性质
高考化学一轮复习 第九章 有机化学基础(必考+选考)第三讲 烃的含氧衍生物课件

4.化学性质 以断键方式理解醇的化学性质(以乙醇为例):
反应 断裂的化学键
化学方程式
与活泼 金属反应
催化氧 化反应
① ①③
2CH3CH2OH+ 2Na―→2CH3CH2ONa+H2↑
2_C_H__3C_H__2O_H__+__O_2―__C△ ―_u_→_2_C_H__3C__H_O_+__2_H_2_O
官能团
—OH
结构 —OH 与链烃基相 —OH 与芳香烃 —OH 与苯环直接
特点 连
侧链相连
相连
(1)与钠反应(置换反应); 主要化 (2)取代反应;(3)消去反应; 学性质 (4)氧化反应;(5)酯化反应;
(6)脱水反应 特性 将红热的铜丝插入醇中有刺激性气
味产生(生成醛或酮)
(1)弱酸性; (2)取代反应; (3)显色反应
第九章 有机化学基础(必修2+选修5)
第三讲 烃的含氧衍生物
第九章 有机化学基础(必修2+选修5)
1.掌握醇、酚、醛、羧酸、酯的结构与性质,以及它们之间 的相互转化。 2.了解有机分子中官能团之间的相互影响。 3.了解烃的衍生物的重要应用以及合成方法。
醇酚
[知识梳理] 一、醇 1.概念 羟基与烃基或苯环侧链上的碳原子相连的化合物称为醇。饱和 一元醇的分子通式为__C_n_H__2n_+__1O__H__或 CnH2n+2O(n≥1)。
(1)1mol 汉黄芩素与足量 H2 反应,消耗 H2 的物质的量是多少? (2)1mol 汉黄芩素与足量的 NaOH 溶液反应,消耗 NaOH 的物 质的量是多少?
答案:(1)8mol (2)2mol
脂肪醇、芳香醇、酚的比较
类别
第三节烃的含氧衍生物考点(二)醛、酮-课件新高考化学一轮复习

2.最简单的酮——丙酮 (1)物理性质:无色透明的液体,沸点 56.2 ℃,易挥发,能与水、乙醇等互 溶。 (2)化学性质:丙酮不能被银氨溶液,新制的 Cu(OH)2 等弱氧化剂氧化,在 催化剂条件下,可与 H2 发生加成 反应,生成 2-丙醇,反应的方程式为
3.酮的应用 酮是重要的有机溶剂和化工原料。如丙酮可以做化学纤维等的溶剂,还用 于生产有机玻璃、农药和涂料等。 [微点拨] 酮和同碳原子数的醛属于同分异构体,如丙酮和丙醛互为同分异构体。
式
CH3COONa+Cu2O↓+3H2O
[微点拨] 乙醛与银氨溶液或者新制氢氧化铜反应均在碱性环境中,所以乙 醛被氧化后的乙酸均以羧酸盐的形式存在。
③催化氧化 乙醛在有催化剂并加热的条件下,能被氧气氧化为乙酸,反应的化学方程式
催化剂 为 2CH3CHO+O2 ―△―→ 2CH3COOH 。
[微点拨] —CHO 具有明显的还原性,能被酸性高锰酸钾溶液等强氧化剂氧 化为—COOH,故能使酸性高锰酸钾溶液褪色。
[题点全盘查] 1.判断正误(正确的打“√”,错误的打“×”)。
(1)
属于饱和一元醛
(2)乙醛是无色体,不溶于水
(3)乙醛既能发生氧化反应又能发生还原反应
(4)能发生银镜反应的有机物都属于醛类有机物
(5)甲醛常温下为气体,其水溶液可用于浸制生物标本
答案:(1)× (2)× (3)√ (4)× (5)√
⑥银镜可用稀 HNO3 浸泡洗涤除去
色沉淀,这是 Cu(OH)2 受热分解生 成 CuO 所致
【解析】
A. O
B. P
C. Mn
D. Cr
D. 自由电子受外力作用时能迅速传递能量
谢 谢观
【答案】D
烃的含氧衍生物知识点讲解103页PPT

25、学习是劳动,是充满思想的劳动。——乌申斯基
谢谢!Βιβλιοθήκη 60、人民的幸福是至高无个的法。— —西塞 罗
21、要知道对好事的称颂过于夸大,也会招来人们的反感轻蔑和嫉妒。——培根 22、业精于勤,荒于嬉;行成于思,毁于随。——韩愈
烃的含氧衍生物知识点讲解
56、极端的法规,就是极端的不公。 ——西 塞罗 57、法律一旦成为人们的需要,人们 就不再 配享受 自由了 。—— 毕达哥 拉斯 58、法律规定的惩罚不是为了私人的 利益, 而是为 了公共 的利益 ;一部 分靠有 害的强 制,一 部分靠 榜样的 效力。 ——格 老秀斯 59、假如没有法律他们会更快乐的话 ,那么 法律作 为一件 无用之 物自己 就会消 灭。— —洛克
烃的含氧衍生物

拓展思维: 乙醛也能和一些极性试剂发生加成反应。请写出乙醛与氢化氰HCN反应化学方程式。
甲醛的结构 甲醛的化学性质
甲醛的氧化反应 1 mol HCHO~4 mol Cu(OH)2~2 mol Cu2O
计算题:
1. 3 g某醛和足量的银氨溶液反应,结果析出43.2 g Ag,则该醛为
A.甲醛 B.乙醛
②催化氧化 乙醇在铜或银作催化剂加热的条件下与空气中的氧气反应生成乙醛
有机化合物分子中失去氢原子或加入氧原子的 反应叫做氧化反应。 得氧去氢
2CH3CH2OH+O2―C――u或―△―A―→g 2CH3CHO+2H2O
③醇还能被KMnO4酸性溶液或K2Cr2O7酸性溶液氧化
CH3CH2OH ――氧―化―→ CH3COOH
根据工业废水中苯酚的处理流程填空
①流程图设备Ⅰ中进行的操作是 萃取、分液
(填操作名称)。
②由设备Ⅱ进入设备Ⅲ的物质A是 C6H5ONa 。由设备Ⅲ进入设备Ⅳ的物 质B是 NaHCO。3
③在设备Ⅲ中发生反应的化学方程式为
为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是
苯酚乳浊液,静置分层,最后通过分液即可得到苯酚
归纳总结
(1)苯酚在水中可发生微弱的电离
苯酚的水溶液呈弱酸性。
(2)由于酸性:H2CO3>苯酚> HCO- 3 , 向苯酚钠溶液中通入CO2,无论是否过量,只能生成NaHCO3。
(2)取代反应 羟基影响苯环 向盛有少量苯酚稀溶液的试管中滴加过量的饱和溴水,现象为 有白色沉淀生成 。
乙醚是一种优良溶剂。
讨论:1-丙醇、2-丙醇和乙醇分子间脱水生成醚的可能产物
以乙烯为基本原料,合成六元环状化合物D(C4H8O2)de部分反应如下(部分试剂、产物及反应条件略去)
2024版新教材高考化学全程一轮总复习第九章有机化学基础第33讲烃的含氧衍生物学生用书
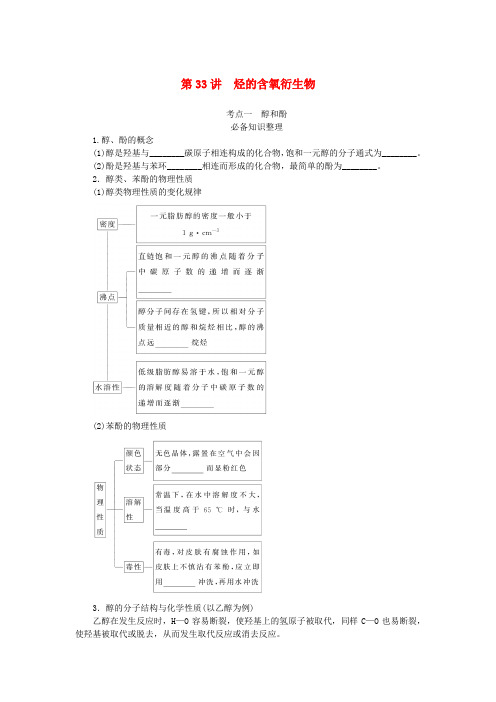
第33讲烃的含氧衍生物考点一醇和酚必备知识整理1.醇、酚的概念(1)醇是羟基与________碳原子相连构成的化合物,饱和一元醇的分子通式为________。
(2)酚是羟基与苯环________相连而形成的化合物,最简单的酚为________。
2.醇类、苯酚的物理性质(1)醇类物理性质的变化规律(2)苯酚的物理性质3.醇的分子结构与化学性质(以乙醇为例)乙醇在发生反应时,H—O容易断裂,使羟基上的氢原子被取代,同样C—O也易断裂,使羟基被取代或脱去,从而发生取代反应或消去反应。
完成下列条件下反应的化学方程式,并指出反应类型。
(1)与Na反应:_______________________________________________。
(2)与HBr的取代:________________________________。
(3)催化氧化:___________________________________。
(4)①浓硫酸,加热分子内脱水:_______________________________________。
②浓硫酸,加热分子间脱水:__________________________________________。
(5)与乙酸的酯化反应:________________________________________________。
4.由基团之间的相互影响理解酚的化学性质(1)苯环对羟基的影响——弱酸性由于苯环对羟基的影响,使酚羟基比醇羟基更活泼,可以发生电离。
①苯酚的电离方程式为____________________。
苯酚俗称石炭酸,但酸性________,________使石蕊溶液变红。
②与碱的反应:苯酚的浑浊液加入NaOH溶液→现象为________再通入CO2气体→ 现象为________。
该过程中发生反应的化学方程式分别为③与活泼金属反应:(2)羟基对苯环的影响——苯环上羟基邻、对位氢原子的取代反应由于羟基对苯环的影响,使苯酚中苯环上的氢原子比苯分子中的氢原子________。
烃的含氧衍生物知识点讲解共103页文档

44、卓越的人一大优点是:在不利与艰 难的遭遇里百联
41、学问是异常珍贵的东西,从任何源泉吸 收都不可耻。——阿卜·日·法拉兹
42、只有在人群中间,才能认识自 己。——德国
烃的含氧衍生物知识点讲解
11、获得的成功越大,就越令人高兴 。野心 是使人 勤奋的 原因, 节制使 人枯萎 。 12、不问收获,只问耕耘。如同种树 ,先有 根茎, 再有枝 叶,尔 后花实 ,好好 劳动, 不要想 太多, 那样只 会使人 胆孝懒 惰,因 为不实 践,甚 至不接 触社会 ,难道 你是野 人。(名 言网) 13、不怕,不悔(虽然只有四个字,但 常看常 新。 14、我在心里默默地为每一个人祝福 。我爱 自己, 我用清 洁与节 制来珍 惜我的 身体, 我用智 慧和知 识充实 我的头 脑。 15、这世上的一切都借希望而完成。 农夫不 会播下 一粒玉 米,如 果他不 曾希望 它长成 种籽; 单身汉 不会娶 妻,如 果他不 曾希望 有小孩 ;商人 或手艺 人不会 工作, 如果他 不曾希 望因此 而有收 益。-- 马钉路 德。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(4) 氧化反应
(5) 氧化反应
(6) 缩聚反应
羟基上 活泼性
酚羟基 ( 弱酸性 )> 醇羟基 ( 中性 )
的氢
原因
由于苯环的影响使连在苯环上的羟基上的氢活泼性增强
特别提示: (1) 醇和酚均含有羟基,根据与羟基相连的烃基不同区分醇类和酚类。
(2)
醇羟基、 酚羟基都能与 Na 反应,酚羟基还能与 NaOH、Na2CO3 反应,两者都不与 NaHCO3 反应, 苯酚的酸性比碳酸还弱,比 HCO-3 的酸性强,故二氧化碳通入苯酚钠溶液中发生
学而不思则惘,思而不学则殆
沸点: 直链饱和一元醇的沸点随着分子中碳原子数的增加而逐渐升高; 键,所以相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
(2) 醇类的化学性质 ( 以乙醇为例 )
醇分子间存在氢
反应物及条件
Na
HBr, △
O2(Cu) , △
断键位置 ① ②
①③
浓硫酸, 170℃
②④
学而不思则惘,思而不学则殆
第九章
有机化学基础
第三节烃的含氧衍生物
| 考点一
醇类的结构与性质
[ 教材知识层面 ]
1.醇类的结构 (1) 醇类的概念 羟基与烃基或苯环侧链上的碳原子相连的化合物称为醇, +1OH或 CnH2n+2O。 (2) 醇类的分类
饱和一元醇的组成通式为 CnH2n
2.醇类的性质 (1) 醇类物理性质的变化规律 ①在水中的溶解性:低级脂肪醇易溶于水。 ②密度:一元脂肪醇的密度一般小于 1 g/cm 3。
乙二醇
结构简 式
CH3OH
状态 溶解性
液体
液体 易溶于水和乙醇
丙三醇 甘油
液体
3.醇类物质的反应规律 (1) 醇的催化氧化反应规律: 醇的催化氧化的反应情况与跟羟基 ( — OH)相连的碳原子上的氢原子的个数有关。
(2) 醇的消去反应规律:
①结构条件: 醇分子中连有羟基的碳原子必须有相邻的碳原子,
该相邻的碳原子上必须
浓硫酸, 140℃
①②
CH3COOH (浓硫酸 )
①
(3) 几种常见的醇
反应类型 置换反应 取代反应 氧化反应 消去反应 取代反应
取代反应
化学方程式 2CH3CH2OH+ 2Na―→
2CH3CH2ONa+ H2↑ CH3CH2OH+ HBr△
CH3CH2Br +H2O Cu
2CH3CH2OH+ O2――△→ 2CH3CHO+ 2H2O
2.有机物 C7H15OH,若它的消去反应产物有三种,则它的结构简式为
()
学而不思则惘,思而不学则殆
解析:选 D 若 C7 H15OH发生消去反应生成三种产物,则必须符合:连有— 必须连接着三个不同的烃基,且烃基中邻位碳原子上连有氢原子。
OH的碳原子
| 考点二
苯酚的结构与性质
1.组成与结构 分子式
。
③与碱的反应:
加入 NaOH溶液
再通入 CO2
苯酚的浑浊液中― ――――――――→液体变澄清― ―――――→溶液又变浑浊。
该过程中发生反应的化学方程式分别为
(2) 苯环上氢原子的取代反应 苯酚与饱和溴水反应的化学方程式为:
反应产生白色沉淀,此反应常用于苯酚的定性检验和定量测定。 (3) 显色反应 苯酚跟 FeCl 3 溶液作用产生紫色溶液,利用这一反应可以检验苯酚的存在。 4.脂肪醇、芳香醇、酚类物质的比较
CH3 CH2OH浓―17―H02℃→SO4 CH2===CH2↑+ H2O 浓 H2SO4 2CH3CH2OH―14―0℃→
CH3CH2OCH2CH3+ H2O CH3 COO+H
浓H2 SO4 CH3 CH2OH △
CH3 COOC2HCH3+ H2O
学而不思则惘,思而不学则殆
名称 俗称
甲醇 木精、木醇
连有氢原子。 CH3OH(无相邻碳原子 ) , 等结构的醇不能发生消去反应。
( 相邻碳原子上无氢原子 )
学而不思则惘,思而不学则殆
②醇消去反应的条件是浓硫酸、加热。 ③一元醇消去反应生成的烯烃种数等于连羟基的碳原子的邻位碳原子上不同化学环境 下的氢原子的种数。
如
的消去产物有 2 种。
[ 考点达标层面 ]
学而不思则惘,思而不学则殆
物质
脂肪醇
芳香醇
酚
实例
CH3CH2OH
C6H5CH2OH
C6H5— OH
官能团
— OH
结构特点
— OH与链烃基相 连
—OH与芳香烃侧 链相连
—OH与苯环直接相连
(1) 弱酸性
(1) 与活泼金属反应
(2) 取代反应
主要化学性质
(2) 取代反应
1.下列醇类物质中既能发生消去反应, 又能发生催化氧化反应生成醛类的物质是 ( )
解析:选 C 醇类发生消去反应的条件是与— OH相连的碳原子的相邻碳原子上有 H原子,
上述醇中, B 不符合。与— OH相连的碳原子上有 H 原子的醇可被氧化,但只有含有两个
H
原子的醇 ( 即含有— CH2OH)才能转化为醛。
。因为
,所以, 上面的反应生
成
同时生成 NaHCO3 而不生成 Na2CO3。
5.官能团异构——酚、芳香醇与芳香醚
含相同碳原子数的酚、芳香醇与芳香醚互为同分异构体,但不属于同类物质。
如 C7H8O属于芳香族化合物的同分异构体有:
学而不思则惘,思而不学则殆
[ 考点达标层面 ]
1.下列四种有机化合物的结构简式如下所示,均含有多个官能团,下列有关说法中正 确的是 ( )
C6H6O 2. 物理性质
[ 教材知识层面 ] 结构简式
结构特点
羟基与苯环 直接相连
3. 化学性质 (1) 羟基中氢原子的反应
学而不思则惘,思而不学则殆
①弱酸性: 苯酚的电离方程式为 C6H5 蕊溶液变红。 ②与活泼金属反应: 与 Na反应的化学方程式为
6H5O- +H+,俗称石炭酸,但酸性很弱,不能使紫色石
A.①属于酚类,可与 NaHCO3 溶液反应产生 CO2 B.②属于酚类,能使 FeCl3 溶液显紫色 C.1 mol ③最多能与 3 mol Br 2 发生反应 D.④属于醇类,可以发生消去反应 解析:选 D ①属于酚类,与 NaHCO3 溶液不反应, A 错误;②属于醇类,不能与 FeCl3 溶液发生显色反应, B 错误; 1 mol ③中的物质最多能与 2 mol Br 2 发生反应, C 错误;④ 中的物质属于醇类,能发生消去反应。
2. 茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的
抗氧化剂和自由基净化剂。 其中没食子儿茶素 (EGC)的结构如图所示。
