弱电解质的电离平衡
弱电解质的电离平衡名词解释

弱电解质的电离平衡名词解释
弱电解质的电离平衡是指在特定条件下,弱电解质在水溶液中分解成离子的速率和离子结合成弱电解质分子的速率相等时的状态。
这种状态是一种暂时的、相对的动态平衡,因为弱电解质分子和离子的浓度会随时间而变化。
当外界条件 (如温度、浓度、溶剂化能力等) 改变时,弱电解质的电离平衡会发生变化,从而产生移动。
例如,增加弱电解质的浓度会导致平衡向电离方向移动,而稀释溶液则会促使平衡向水解方向移动。
电离平衡是化学中一个重要的概念,对于理解化学反应的进行和溶液的配制等方面都有重要的作用。
高二化学弱电解质的电离平衡

B.
C ( NH 4 ) C (OH )
C.
C ( NH 3 H 2 O) C ( NH 4 )
D.
C (OH )
4.相同温度下,两种稀氨水A和B,浓 度分别为0.2mol/L和0.1mol/L,
则A、B的OH-浓度之比为( B ) A.大于2 B. 小于2 C. 等于2 D. 不能肯定
RNH3++OH-的 )
平衡中,要使RNH2· H2O的电离程度
及c(OH-)都增大,可采取的措施( D
A.通入氯化氢
B.加少量氢氧化钠固体 C.加水 D.升温
3.在25℃时,用蒸馏水稀释氨水,随溶 液的稀释,下列各项中始终保持增大趋 势的是( A )
A.
C (OH ) C ( NH 3 H 2 O)
5. 1mol/L的盐酸、醋酸、硫酸各
1L,分别加入足量的铁。 开始反应时产生氢气的速率
________
硫酸>盐酸>醋酸
,
。
最终收集到的氢气的物质的量
硫酸>盐酸 = 醋酸 ______
6. 冰醋酸加水溶解并不断稀释过程中,溶液导电 能力与加入水的体积有如下变化关系:试回答:
⑴“0”点导电能力为0的理由是: 冰醋酸中只 存在醋酸分子,无离子。 ⑵a、b、c三点对应溶液的PH值由大到小的 顺序是 a﹥c﹥ b ⑶a、b、c三点中电离程度最大的是 C 。电 离平衡常数的关系 相等 . ⑷若使c点溶液中C(Ac-)、PH 值均增大,可采取的措施有: ①加碱②加碳酸钠③加镁或锌
升温
四. 弱电解质电离程度的电离常数:
对于一元弱酸:HA H++A-,平衡时
Ka=
c ( H+) .c( A-) c(HA) M++OH-,平衡时
弱电解质的电离平衡

稀释相 同倍数 后pH 小 大
相同pH、相同体积时 pH、 同体积时 比较 C(H+) 项目 HA HB 相同 相同 C(酸 C(酸) 中和碱 与活泼金 与金属反 的能力 属反应产 应的开始 生H2的量 速率 小 大 小 大 相同 相同 稀释相 同倍数 后pH 大 小
小 大
四、强电解质和弱电解质的证明方法
冰醋酸加水溶解并不断稀释过程中, 1、冰醋酸加水溶解并不断稀释过程中,溶 液导电能力与加入水的体积有如下变化关系: 液导电能力与加入水的体积有如下变化关系 : 试回答: 试回答: 点导电能力为0 ⑴“0”点导电能力为0的理由是: 冰醋酸中只 0 点导电能力为 的理由是: 存在醋酸分子,无离子。 存在醋酸分子,无离子。 ⑵a、b、c三点对应溶液的PH值由大到小的 顺序是 a﹥c﹥ b ⑶a、b、c三点中电离程度最大的是 C 。电 离平衡常数的关系 相等 . 若使c点溶液中C(Ac ⑷若使c点溶液中C(Ac-)、PH 值均增大,可采取的措施有: 值均增大,可采取的措施有: ①加碱②加碳酸钠③加镁或锌 加碱②加碳酸钠③
下表是常见弱酸的电离平衡常数(25℃) 下表是常见弱酸的电离平衡常数(25℃)
酸 醋酸 碳酸 氢硫酸 电离方程式 电离平衡常数K 电离平衡常数K
CH3COOH ⇌ CH3COO-+H+
H2CO3 ⇌ H++HCO3HCO3- ⇌ H++ CO32H2S ⇌ H++HSHS- ⇌ H++ S2H3PO4 ⇌ H++H2PO4H2PO4— ⇌ H++HPO42HPO42— ⇌ H++PO43-
回答下列各问题: 回答下列各问题:
弱电解质的电离平衡

弱电解质的电离一、电离平衡常数(1)概念:在一定条件下达到平衡时,弱电解质电离形成的各种离子浓度的乘积与溶液中未电离的物质的浓度之比是一个常数,该常数成为电离平衡常数,简称电离常数。
(2)表达式:弱酸的电离平衡常数用Ka表示,如: HA H+ + A-,则Ka=弱碱的电离平衡常数用Kb表示,如:MOH M++ OH-,则Kb=多元弱酸电离是电离,以第步电离为主;多元弱碱电离一般认为一步电离完成。
(3)意义:电离平衡常数表征了弱电解质的电力能力,根据同温下电离常数的大小可以判断弱电解质电离能力的相对强弱。
K值越大,电离程度,弱酸酸性(弱碱碱性)。
(4)影响因素:电离平衡常数只随的变化而变化,升高温度,K值。
二、弱电解质电离平衡的特点和影响因素(1)电离平衡特点为:动、等、定、变(2)弱电解质稀溶液加水稀释时,电离平衡向电离方向移动,促进电离,平衡混合物中微粒总浓度、离子数、离子浓度与溶质分子浓度的比值均增大,但离子总浓度减小,导电能力减弱。
(3)条件改变时,弱电解质的电离平衡会发生移动,但K值只随温度的改变而改变。
例1:向0.1 mol/L的CH3COOH溶液中加水或加入少量的CH3COONa晶体时,下列有关叙述不正确的是() A.都能使溶液的pH增大 B.都能使溶液中c(H+)·c(CH3COO-)增大C.溶液中的c(H+)·c(OH-)不变D.都能使溶液中c(CH3COO-)/c(CH3COOH)增大例2:用水稀释0.1 mol/L NH3·H2O时,溶液中随着水量的增加而减小的是( )A.c(OH-)/c(NH3·H2O) B.c(NH3·H2O)/ c(OH-)C.c(H+)和c(OH-)的乘积 D.OH-的物质的量三、强酸与弱酸的比较及判断电解质强弱的方法(1)等物质的量浓度或等pH的强酸与弱酸的比较等物质的量浓度盐酸(a)与醋酸溶液(b)等pH的盐酸(a)与醋酸(b)pH或物质的量浓度 pH: 物质的量浓度:溶液的导电能力水的电离程度c(cl-)与c(CH3COO-)等体积溶液中和NaOH的量分别加该酸的钠盐固体后pH变化开始与金属反应的速率M A B 等体积溶液与金属反应长生H 2量(2)判断电解质强弱的方法 a.浓度与pH 的关系。
弱电解质的电离平衡及溶液的PH值的计算

4、弱电解质电离方程式书写规律:
1.弱电解质在溶液中部分电离,用“ ”
2.强酸酸式盐电离时H+分开写,弱酸酸式盐电离时 H+不能拆开.
3.多元弱酸的电离 应分步完成电离方程式,多元 弱碱则一步完成电离方程式。
写出电解质NaCl、 NaHSO4、NaHCO3、 CH3COOH、 H3PO4的电离方程式 NaCl = Na++Cl- NaHSO4= Na++ H ++ SO42NaHCO3= Na++HCO3CH3COOH H3PO4 H++CH3COO- H ++H2PO42-
练习
PH=10的氢氧化钠溶液与PH=10的氨水,稀释 NaOH < NH3 H 相同倍数,其PH大小关系是______________· 2O ,
即弱碱在稀释时电离平衡被破坏,要不断电 离出OH-,所以稀释相同倍数后,其碱性应 比强碱强一些,因而PH值应大一些 如稀释后溶液的PH值仍然相同,则稀释 NaOH<NH3· 2O H 倍数大小关系是_______
例:在一定温度下,冰醋酸加水稀释的过程中,溶液的 导电能力如图所示,请回答:(1)“o”点导电能力为 0的理由是 在O点处醋酸没电离,无离子存在 。
(2) a、b、c三点溶液PH由大到小的顺序是 C、a、b 。 导 C 。 电 (3) a、b、c三点中电离程度最大的是 能 力 b (4)若使c点溶液中C(Ac-)增大,
关键:抓住氢离子进行计ቤተ መጻሕፍቲ ባይዱ!
b、
强碱与强碱混合
例题:在25℃时,pH=9和pH=11的两种氢
氧化钠溶液等体积混合pH值等于多少? 关键:抓住氢氧根离子离子进行计算!
C、强酸与强碱混合
【知识解析】弱电解质的电离平衡
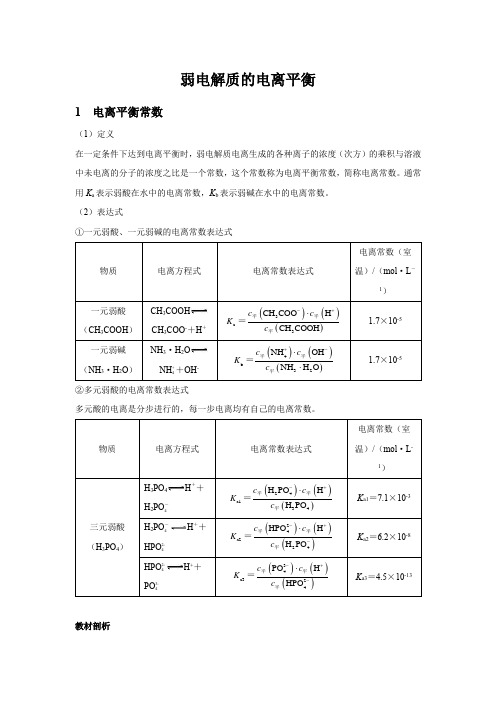
弱电解质的电离平衡1 电离平衡常数(1)定义在一定条件下达到电离平衡时,弱电解质电离生成的各种离子的浓度(次方)的乘积与溶液中未电离的分子的浓度之比是一个常数,这个常数称为电离平衡常数,简称电离常数。
通常用K a表示弱酸在水中的电离常数,K b表示弱碱在水中的电离常数。
(2)表达式①一元弱酸、一元弱碱的电离常数表达式CH3COOHCH3COO-+H+NH3·H2ONH ++OH-4②多元弱酸的电离常数表达式多元酸的电离是分步进行的,每一步电离均有自己的电离常数。
H3PO4H++H2PO-4H2PO-H++4HPO2-4H++HPO2-4PO3-4教材剖析【教材P98】 “多元弱酸的各级电离常数逐级减小。
对于各级电离常数相差很大的多元弱酸,其水溶液中的H +主要是由第一步电离产生的。
”【教材剖析】 多元弱酸第一步电离出H +后,剩余的酸根离子带负电荷,对H +的吸引力增强,使其电离出H +更困难,故一般K a1>>K a2>>K a3……。
因此计算多元弱酸溶液中的c (H+)或比较弱酸酸性的相对强弱时,通常只考虑第一步电离。
(3)意义电离常数表征了弱电解质的电离能力,根据相同温度下电离常数的大小可以判断弱电解质电离能力的相对强弱。
弱酸的电离常数越大,弱酸电离出H +的能力就越强,酸性也就越强;反之,酸性越弱。
如:名师提醒(1)电离常数服从化学平衡常数的一般规律,只受温度的影响。
(2)电离常数相对较大、电离能力较强的弱电解质,其溶液的导电能力不一定强。
这是因为溶液的导电能力与溶液中的离子浓度和离子所带电荷数有关。
(3)相同温度下,等浓度的多种一元弱酸溶液,弱酸的电离常数越大,溶液中c (H +)越大,溶液的导电能力也就越强。
2 电离度(1)定义弱电解质在水中的电离达到平衡状态时,已电离的溶质的分子数占原有溶质分子总数(包括已电离的和未电离的)的百分率称为电离度,通常用α表示。
弱电解质的电离平衡

例 5-3 计算 °C时 0.10molL - 1H2S水溶液的 计算25 时 水溶液的
pH值及 2-的浓度. 值及S -的浓度. 值及 已知: 已知:Ka1=1.3×10-7 × Ka2=7.1×10-15 ×
13
∴
pH=8.77 .
返回1 返回1
16
六,酸碱平衡的移动
1,同离子效应 , 作用原理:平衡移动原理用于溶液体系. 作用原理:平衡移动原理用于溶液体系. + 如: HAc ←V → H + Ac
V分
加 NaAc Na+ + Ac― Ac―为同名离子;NaAc同名离子强电解质. 为同名离子; 同名离子强电解质. 同名离子强电解质 ∵[Ac―]↑↑,使平衡向左移 ,
§6-1 弱电解质的电离平衡
一,一元弱酸,弱碱的电离 一元弱酸, 一元弱酸HAc: 一元弱酸 : HAc+H2O Ac-+ H3O+ 简写为: HAc Ac-+ H+ 简写为: 则电离常数为: 则电离常数为:
K
θ a
[c(H )/c ] [c(Ac )/c ] = θ [c(HAc)/c ]
θ θ
0.1moll -1HAc和0.5moll -1HAc, 和 , 0.1HAc 0.5HAc 0.593% 经测 α : 1.33% > [离子 = 离子] 离子
+
②根据
α C
3 1
1 3
[ H 3 O ]0.1 HAc = 0.1 × 1.33% = 1.33 × 10 mol l
2.弱电解质的电离平衡

根据对0.1
mol· L-1的醋酸溶液进行的下列有关 变化,完成表格
电离平衡移动方向 c(H+) c(CH3COO—)
加热 加水 加CH3COOH 加NaOH
加HCl
2、电离方程式的书写 强电解质电离用等号,弱电解质电离用可逆号 多元弱酸分步电离 多元弱碱写成一步电离的形式 强酸酸式盐一步电离到各离子,用等号; 弱酸酸式盐第一步电离到阳离子和酸式酸根离子,用 等号;酸式酸根离子再电离,遵照分步电离,用可逆 号
一定能在下列溶液中大量共存的离子组是
A.含有大量Al3+的溶液:Na+、NH4+、SO42-、ClB.c(H+)=1×10-13mol· -1 的 溶 液 : Na+ 、 Ca2+ 、 L SO42-、CO32C. 含 有 大 量 Fe3+ 的 溶 液 : Na+ 、 Mg2+ 、 NO3- 、 SCND.含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl-
浓度均为0.1
mol· -1的三种溶液等体积混合,充 L 分反应后没有沉淀的一组溶液是( ) A.BaCl2 、NaOH 、 NaHCO3 B. Na2CO3 、 MgCl2 、 H2SO4 C.AlCl3 、 NH3· 2O 、 NaOH H D.Ba(OH)2 、 CaCl2 、 Na2SO4
下 列 各 组 离 子 能 大 量 共 存 , 当 溶 液 中
c(H+)=10—10 mol•L—1时,有气体产生;而 当溶液中c(H+)=10—13 mol•L—1时,又能生 出沉淀。该组离子可能是( ) A.Na+、Cu2+、NO3—、CO32— B.Ba2+、K+、Cl—、HCO3— C.Fe2+、Na+、SO42—、NO3— D.Mg2+、NH4+、SO42—、Cl—
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
弱电解质的电离平衡考点一弱电解质的电离平衡一.强、弱电解质(1)定义与物质类别(2)电离方程式的书写——“强等号,弱可逆,多元弱酸分步离”①强电解质:如H2SO4:H2SO4===2H++SO2-4。
②弱电解质:a.一元弱酸,如CH3COOH:b.多元弱酸,分步电离,分步书写且第一步电离程度远远大于第二步的电离程度,如H2CO3:c.多元弱碱,分步电离,一步书写。
如Fe(OH)3:③酸式盐:a.强酸的酸式盐:NaHSO4在水溶液中:;熔融时:b.弱酸的酸式盐:“强中有弱”,如NaHCO3:(3)外界条件对电离平衡的影响①温度:温度升高,电离平衡移动,电离程度。
②浓度:稀释溶液,电离平衡移动,电离程度。
③同离子效应:加入与弱电解质具有相同离子的强电解质,电离平衡移动,电离程度。
④实例展示+稀释一弱电解质溶液时,所有粒子浓度都会减小吗?练习:1、一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:(1)O点为什么不导电:_______________________。
(2)a 、b 、c 三点溶液的pH 由小到大的顺序是_______________。
(3)H +的物质的量最大的是________(填“a”“b”或“c”)。
(4)若使c 点溶液中的c(CH 3COO -)增大,可以采取下列措施中的________(填字母序号)。
A .加热 B.加很稀的NaOH 溶液 C .加NaOH 固体 D.加水E .加CH 3COONa 固体 F .加入锌粒要证明某电解质是弱电解质,关键在于一个“弱”字,即证明它只是部分电离或其溶液中存在电离平衡。
以一元酸HA 为例,证明它是弱电解质的常用方法有:3.25 ℃时,把0.2 mol·L -1的醋酸加水稀释,则图中的纵轴y 表示的是( )A .溶液中OH -的物质的量浓度 B .溶液的导电能力C .溶液中c (CH 3COO -)c (CH 3COOH )D .CH 3COOH 的电离程度4.稀氨水中存在着下列平衡:NH3·H2O NH+4+OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是()①NH4Cl固体②硫酸③NaOH固体④水⑤加热⑥加入少量MgSO4固体A.①②③⑤ B.③⑥C.③ D.③⑤5.H2S水溶液中存在电离平衡H2S H++HS-和HS-H++S2-。
若向H2S 溶液中()A.加水,平衡向右移动,溶液中氢离子浓度增大B.通入过量SO2气体,平衡向左移动,溶液pH增大C.滴加新制氯水,平衡向左移动,溶液pH减小D.加入少量硫酸铜晶体(忽略体积变化),溶液中所有离子浓度都减小6.关于常温下,pH=2的醋酸溶液,下列叙述正确的是()A.c(CH3COOH)=0.01 mol/L B.c(H+)=c(CH3COO-)C.加水稀释100倍后,pH=4 D.加入醋酸铵固体,可抑制醋酸的电离考点二电离平衡常数1.表达式(1)对于一元弱酸HAHA H++A-,平衡常数K=c(H+)·c(A-)c(HA);(2)对于一元弱碱BOHBOH B++OH-,平衡常数K=c(OH-)·c(B+)c(BOH)。
2.意义相同条件下,K值越大,表示该弱电解质电离,所对应的酸性或碱性相对3.特点(1)多元弱酸是分步电离的,各级电离常数的大小关系是K1≫K2……,所以其酸性主要决定于第一步电离。
判断正误(正确的打“√”,错误的打“×”)(1)电离平衡常数(K)越小,表示弱电解质电离能力越弱。
()(2)不同浓度的同一弱电解质,其电离平衡常数(K)不同。
()(3)电离平衡右移,电离平衡常数一定增大。
()(4)温度不变,向NH3·H2O溶液中加入NH4Cl,平衡左移,电离平衡常数减小。
()(5)电离平衡常数大的酸溶液中c(H+)一定比电离平衡常数小的酸溶液中c(H+)大。
()(6)H2CO3的电离平衡常数表达式:K a=c(H+)·c(CO2-3)c(H2CO3)。
()归纳:有关电离平衡常数的计算以弱酸HX为例:(1)已知c(HX)和c(H+),求电离平衡常数(2)已知c(HX)和电离平衡常数,求c(H+)考法一:电离平衡常数的定性分析1、丙酸的Ka和丙二酸的K1、K2的大小次序应该是?为什么?2.25 ℃时,部分物质的电离平衡常数如表所示;(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序________________________________。
(2)同浓度的CH3COO-、HCO-3、CO2-3、ClO-结合H+的能力由强到弱的顺序为__________________________。
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式______________________。
(4)物质的量浓度均为0.1 mol·L-1的下列四种物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3,pH由大到小的顺序是________(填字母)。
(5)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,填写下列表达式中的数据变化情况(填“变大”“变小”或“不变”)①c(CH3COOH)c(H+)____________________;②c(CH3COO-)·c(H+)c(CH3COOH)_____________;③c(CH3COO-)c(CH3COOH)__________________;④c(CH3COO-)c(CH3COOH)·c(OH-)____________________。
3、今有HA、H2B、H3C三种一元、二元、三元弱酸,根据”较强酸+较弱酸盐较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:①HA+HC2- (少量)A﹣+H2C﹣;②H2B(少量)+2A﹣B2-+ 2HA;③H2 B (少量)+H2C﹣HB﹣+H3C。
回答下列问题:(1)在相同条件下,HA、H2B、H3C三种酸中酸性最强的是________。
(2)A﹣、B2﹣、C3﹣、HB﹣、H2C﹣、HC2﹣六种离子中,最易结合质子的是_________,最难结合质子的是_________。
(3)下列反应的离子方程式书写正确的是_________。
A. H3C+3A﹣3HA+C3﹣B. HB﹣+A﹣HA+B2-C.H3C+B2-HB﹣ +H2C-(4)完成下列反应的离子方程式:①H3C+OH﹣(过量)__________________;②HA (过量)+C3-___________________________。
考法二有关电离平衡常数的定量计算4、已知H2CO3的二级电离常数为K2,a mol/L NaHCO3溶液(PH=8.3)中CO32-的浓度为_______. 5.已知室温时,0.1 mol·L-1某一元酸HA在水中有1.0%电离,此酸的电离平衡常数为________。
6.在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH+4)=c(Cl-),则溶液显__________(填“酸”“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数K b=__________。
7、常温下,将a mol·L-1CH3COONa溶于水配成溶液,向其中滴加等体积的b mol·L-1的盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),用含a和b的代数式表示醋酸的电离常数K a=________。
8、已知硫酸的第一步电离(H2SO4=H++HSO4-)是完全的,但第二步电离(HSO4-⇌H++SO42-)并不完全.如果25℃时,0.1mol/L H2SO4溶液中c(SO42-)=0.010mol/L,0.1mol/L NaHSO4溶液中c(SO42-)=0.029mol/L,试回答:(1)25℃时,0.1mol/L H2SO4溶液中pH=______;(可用对数表示)(2)为何0.1mol/L的H2SO4溶液中c(SO42-)比0.1mol/L的NaHSO4溶液中c(SO42-)小?______(3)0.1mol/L Na2SO4溶液的pH值______7(填大于、小于或等于)(4)常温下测得0.25mol/L的CuSO4溶液的pH值为5,0.25mol/L Cu(ClO4)2溶液的pH值为4.5,其原因是______.考点三强酸(碱)与弱酸(碱)的比较练习:1.体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01 mol,下列叙述错误的是( )A.与NaOH完全中和时,醋酸所消耗的NaOH多B.分别与足量CaCO3反应时,放出的CO2一样多C.两种溶液的pH相等D.分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-)2.pH=12的NaOH溶液与氨水:(1)c(NaOH)________c(NH3·H2O)(填“>”“<”或“=”)。
(2)加水稀释10倍后,两溶液的pH各是多少?(3)若稀释后两溶液的pH仍然相等,则加水量有何关系?考向一强酸(碱)与弱酸(碱)的比较1.pH=2的两种一元酸X和Y的溶液,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示。
分别滴加NaOH溶液(c=0.1 mol/L)至pH=7,消耗NaOH溶液的体积为V X、V Y,则( )A.X为弱酸,V X<V YB.X为强酸,V X>V YC.Y为弱酸,V X<V YD.Y为强酸,V X>V Y2.现有室温下四种溶液,有关叙述不正确的是( )B.②③两溶液等体积混合,所得溶液中c(H+)>c(OH-)C.分别加水稀释10倍,四种溶液的pH:①>②>④>③D.V1L④与V2L①混合,若混合后溶液pH=7,则V1<V2考向二强、弱电解质的图象分析3.(2018·山东临沂模拟)向体积均为1 L、pH=2的盐酸和醋酸溶液中分别投入0.2 g Ca,则下图中比较符合反应事实的曲线是( )考向三 判断弱酸(碱)的方法4.为了证明醋酸是弱电解质,甲、乙、丙、丁四人分别选用下列试剂进行实验:0.1 mol·L -1醋酸溶液、0.1 mol·L -1盐酸、pH =3的盐酸、pH =3的醋酸、CH 3COONa 晶体、NaCl 晶体、CH 3COONH 4晶体、蒸馏水、锌粒、pH 试纸、酚酞、NaOH 溶液等。
