循环过程
(2)循环过程

准静态循环过程旳描述
以蒸汽机为例
高温热源(热库)
在整个循环过程中 系统对外做净功:
Q1
锅炉 蒸汽
A A1 A2
A2
泵
A1
系统吸收旳净热量: Q Q1 Q2
水 冷凝器
汽缸
整个循环过程旳特征 从初态出发经过一种
Q2
低温热源(冷库)
循环过程回到原来状态后,系统旳内能不变
E E2 E1 0
=1-300/400=25%
Q1=A/ =8000/0.25=32023(J)
Q2=Q1-A=24000(J)
0
a d Q2
Q1 b
c 15 V
(1) 据题意Q'2=Q2=24000J
P a'
A' =10000J
a
Q'1= Q'2+ A'=Q2+ A'=34000J
Q'1
b' Q1 b
∴ ' = A'/ Q'1
提高c
T1 T2
提升高温热源旳温度现实些
9
3)理论阐明低温热源温度
阐明热机效率 c 1
进一步阐明
T2 0 且有 T2 T1
且只能 c 1
热机循环不向低温热源放热是不可能旳
热机循环至少需要两个热源
4)疑问:由热一定律,在循环过程中,假如 1
相当于把吸收旳热量全作功。从能量转换看 不 违反热力学第一定律,但为何实际做不到?
阐明:必然还有一种独立于热力学一定律旳定律 存在。 这就是热力学第二定律。
10
四、卡诺致冷机
卡诺热机作逆循环就叫卡诺致冷机
卡诺致冷机旳制冷系数
循环过程:系统经过一系列状态变化过程以后,又回到原来状态的过程。 循环特征:系统经历一个循环之后,内能

在上述高温压缩气体中,用电火花或其他方式引起气
体燃烧爆炸,气体压强随之骤增,由于爆炸时间短促,
活塞在这一瞬间移动的距离极小,这 p
近似是个等体过程(图中过程cd)。
d
这一巨大的压强把活塞向右推动而作
功,同时压强也随着气体的膨胀而降 c 低,爆炸后的作功过程可看成一绝热
e
过程(图中过程de)。
p0
a
b
(1)吸入燃料过程
气缸开始吸入汽油蒸气及
c
助燃空气,此时压强约等于
e
1.0105Pa ,这是个等压过程
p0
a
b
(图中过程ab)。
O
V0
VV
上页 下页 返回 退出
(2)压缩过程
活塞自右向左移动,将已吸入汽缸内的混合气体加以
压缩,使之体积减小,温度升高,压强增大。由于压缩较
快,汽缸散热较慢,可看作一绝热过程(图中过程bc)。 (3)爆炸、作功过程
亦即
Te
Td
Tb
Tc
V0 V
1
p
d
1
1
1
1 1
1
V V0
r
c
e
式中r= V/V0叫做压缩比。
p0
a
O
V0
b VV
上页 下页 返回 退出
计算表明,压缩比愈大,效率愈高。汽油内燃机
的压缩比不能大于7,否则汽油蒸气与空气的混合气 体在尚未压缩至c点时温度已高到足以引起混合气体
上页 下页 返回 退出
例题6-5 内燃机的循环之一——奥托循环。内燃机利 用液体或气体燃料,直接在气缸中燃烧,产生巨大的压 强而作功。内燃机的种类很多,我们只举活塞经过四 个过程完成一个循环(如图)的四动程汽油内燃机(奥 托循环)为例。说明整个循环中各个分过程的特征,并 计算这一循环的效率。
5.3 循环过程

É· ú Q2 ÉÉ 氨 É ÷° É 0 0 20 C 70 C 10atm É É É ÉÉ ÷ É ú
1
A外 A
Q1 Q2
Í Î µ Â È Ô ´
(ÉÉ É)
第5章 热力学定律
5.3 循环过程
第5章 热力学定律
5.3 循环过程
二卡诺循环 1824年,法国青年科学家卡诺 *
(N. L. S. Carnot, 1796 ~1832)发
第5章 热力学定律
5.3 循环过程
第5章 热力学定律
5.3 循环过程
2 逆循环 反时针方向的循环. 一般从低温热库吸热, 向高温热库放热
逆循环过程对应制冷机(refrigerator)
在P-V图
P
逆循环
V
第5章 热力学定律
5.3 循环过程
逆循环对应制冷机利用外界做功获得低温的机器.
T可调 高温热源 A
表了他关于热机效率的理论。为提 高热机效率指明方向。
第5章 热力学定律
5.3 循环过程
卡诺循环 由两条绝热线和两条等温线构成 (为双热源循环)
第5章 热力学定律
5.3 循环过程
卡诺循环的效率
高温热源 A 低温热源
P
a
Q1
Q2
b
c
d
O
V
第5章 热力学定律
5.3 循环过程 吸收热量
P
a
Q1
dQ 0
A
高温热源
低温热源
第5章 热力学定律
逆循环
制冷系数:
T可调 低温热源
Q2 Q2 w A Q1 Q2
第5章 热力学定律
5.3 循环过程
例:电冰箱的工作原理 :氨 、氟利昂
热力学3 循环过程
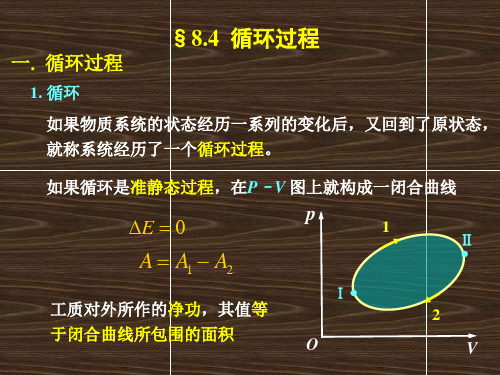
§8.4 循环过程一.循环过程如果循环是准静态过程,在P –V 图上就构成一闭合曲线如果物质系统的状态经历一系列的变化后,又回到了原状态,就称系统经历了一个循环过程。
=∆E 1. 循环VpOⅡⅠ··12工质对外所作的净功,其值等于闭合曲线所包围的面积21A A A -=21>-=A A A 21Q Q A -=2. 正循环、逆循环正循环(循环沿顺时针方向进行)逆循环(循环沿逆时针方向进行)(系统对外作功)21Q A Q +=ⅠⅡQ 1Q 2ab V pO根据热力学第一定律,有021<-=A A A (系统对外作负功)正循环也称为热机循环逆循环也称为致冷循环··ⅠⅡQ 1Q 2ab VpO····热库热库冷库冷库二. 循环效率1212111Q Q Q Q Q Q A -=-==η在热机循环中,工质对外所作的功A 与它吸收的热量Q 1的比值,称为热机效率在制冷循环中,工质从冷库中吸取的热量Q 2与外界对工质作所的功A 的比值,称为循环的致冷系数2122Q Q Q A Q w -==热机的能流图2Q 1Q 2T 低温热源致冷机的能流图2T 低温热源1Q 1T 高温热源热机能流图制冷机能流图1T 高温热源2Q AA1 mol 单原子分子理想气体的循环过程如图所示。
(1) 作出p -V 图(2) 此循环效率解例求cab 600211632T (K )V (10-3m 3)O2ln 600lnR V V RT A Q abab ===V (10-3m 3)OP (105R )(2) ab 是等温过程,有bc 是等压过程,有750bc p Q C T Rν=∆=-(1) p -V 图abc300ca 是等体过程R p p V T T C E Q c a c a V ca 450)(23)(=-=-=∆=ν循环过程中系统吸热RR R Q Q Q ca ab 8664502ln 6001=+=+=循环过程中系统放热RQ Q bc 7502==00124.1386675011=-=-=RRQ Q η此循环效率一定量的理想气体经历如图所示的循环过程。
8.4 循环过程

位置
热力学基础
第一定律
定律 在等值、绝热过程
定律的应用 循环过程
第二定律
§8.4 循环过程
8.4.1 循环过程 1.概念 循环过程: 工作物质(工质): p
2.特征 ①在p-V图中为一闭合曲线
(若是准静态过程)
② E 0
3.正循环与逆循环
O
(1)正循环
A净
V
①概念 ——沿顺时针 ②特点 ⅰ系统对外做的净功 A 0
M M mol CV,m (Tc Tb )
M M mol
5 2 R(Tc Tb )
5 2
V1
(
pc
pa
)
Abc 0
0 吸热
例
以双原子理想气体为工质的热机,过程如图
求:η
P(Pa)
c
解:
Qab
7 2
pa (V1
V2 )放热
Qbc
5 2 V1( pc
pa )吸热
Aab pa (V1 V2 ) Abc 0
(2)逆循环
ⅱA净=闭合曲线所围面积
①概念 ——沿逆时针 ②特点 ⅰ系统对外做的净功 A 0 (即外对系统做的净功>0)
4.为什么要研究循环 ●需求:如:不断地Q→A
ⅱA净值=闭合曲线所围面积
●可:正循环
§8.4 循环过程(一循环)
8.4.2 热机和热机循环
1.热机 持续地→Q吸收→A对外的机器 (如:蒸汽机)
Q放1 :对1循环 abcda
1
1 T2 T1
1 27 273 127 273
25%
2
T2
又1
A净1 Q吸1
Q吸1
8000 25%
3 循环过程解读

1 循环过程
热力学系统经历了一系列热力学过程后 又回到初始状态,这个过程为循环过程。 循环过程的重要特征: E 0 如果循环过程中各个分过 程都是准静态过程,这个 过程为准静态循环过程。
P
1 2
V1
准静循环过程可以在状态 图上用一个闭合曲线表示。 o
V2
V
循环曲线所包围的面积为系统做的净功。
1→2 等温膨胀过程, 吸热 Q1 = A= RT1 ln(V2/V1)
P
1
Q1
绝热
4
2 等温T1
绝热
3→4 等温压缩过程, 放热的大小为 Q2= RT2 ln(V3/V4)
1
Q2
3
等温T2 V
V1 V4 V2 V3
1
1、4两点在同一绝热线上, T1V1 T2V4 2、3两点在同一绝热线上, T V 1 T V 1 1 2 2 3 得
高温热源T1
Q1
热机效率
A Q1 Q2 Q1 Q1
热机
Q2
A
热机效率通常用百分数来表示 如果从高温源吸取的热量转变 成功越多,则热机效率就越大。
低温热源T2
逆循环
循环曲线逆时针,这 种循环叫做逆循环。 逆循环能量转化特征: 系统吸热,对外做正功; 返回时,系统放热,对外 做负功;循环面积为负值。 逆循环对应致冷机循环
Q1
致冷机
Q2
低温热源T2 室内
A
例1 燃烧汽油的四冲程内燃机 中进行的循环过程叫奥托循环。
这一过程不是同一工质反 复进行的循环,但在理论 P 上研究这一过程的能量转 化时,总是用一定量的理 想气体的下述准静态循环 过程来代替:两条绝热线 和两条等容线构成准静态 循环过程。 证明:奥托机效率为:
大学物理(13.4.1)--循环过程

一、循环过程的定义及其特点1.定义:工作物质的状态经过一系列变化过程后,又回到原来状态的过程称为热力学系统的循环过程,简称循环。
2.特点:1)系统的内能没有变化 0=∆E 2)如果组成某一循环的各个过程都是准静态过程,则此循环过程可以用P —V 图上的一条闭合曲线来表示。
系统完成一个循环所做的净功等于P —V 图上循环过程曲线所围的面积。
二、循环过程的分类及其应用1.正循环:在P —V 图上按顺时针方向进行的循环过程。
热机:工作物质作正循环的机器。
1)工作原理:从高温热源吸收热量Q 1,一部分用来对外做功W ,一部分向低温热源放出热量Q 2(在计算中取正值)。
2)循环的效率:1211 Q Q Q W -==η吸收同样多的热量,对外界作的功越多,表明热机把热量转化为有用功的本领越大,效率就越高。
2.逆循环:在P—V 图上按逆时针方向进行的循环过程致冷机:工作物质作逆循环的机器。
1)工作原理:从低温热源吸收热量Q 2,外界做功W ,向高温热源放出热量Q 1。
2)制冷系数:2122Q Q Q W Q e -==三、卡诺循环1.卡诺循环1)定义:卡诺循环:两个等温过程和两个绝热过程组成的循环。
2)分类正循环——卡诺热机逆循环——卡诺制冷机2.卡诺热机的效率1)卡诺热机的四个过程中功、内能增量和热量(1)AB:等温膨胀过程,内能变化为零,吸收的热量全部用来对外做功12111ln V V RT M m Q W == (1)(2)BC 绝热膨胀过程:系统不吸收热量,对外所作的功等于系统减少的内能 )(21,2T T C Mm E W m V -=∆-= (2)(3)CD 等温压缩过程:内能变化为零,外界对系统做功等于向低温热源放出的热量 34223ln V V RT M m Q W ==-- (3)(4)DA 绝热压缩过程:系统不吸收热量,外界对系统做功等于系统增加的内能 )(21,4T T C Mm E W m V -=∆=- (4)把以上四式左、右两边相加得系统对外界所作的净功为⎪⎪⎭⎫ ⎝⎛=432121ln ln V V T V V T R M m W -总的内能变化 0=E ∆从高温热源吸收的热量1211ln V V RT M m Q =向低温热源放出的热量4322ln V V RT M m Q =2)卡诺热机的效率由热机效率定义: 121432121ln ln11V V T V V T Q Q Q W -=-==η应用绝热方程const T V =-1γ得BC 过程 213112T V T V --=γγDA 过程 214111T V T V --=γγ两式相除得4312V V V V = 因而 121 T T -=η——仅适宜卡诺热机3)说明:(1)要完成一个卡诺循环必须有个热源。
循环过程

锅炉
按卡诺循环计算:
C 1 273 30 64.5%
273 580
36 实际最高效率: %
发电机
冷凝塔
非卡诺循环、散热、摩擦等 原因:
12
2.卡诺逆循环的致冷系数:
取绝对值
Q2 Q2 T2 wC W Q1 Q2 T1 T2
取绝对值
100 5 1
若T1 = 293 K(室温),
C V
CA为等温过程E 0
WCA QCA 400 J
8
W =WAC WABC
WABC 500 J
卡诺循环(Carnot cycle )
一、卡诺循环
卡诺循环:只和两个恒温热库传递热量并对外作 功的准静态、无摩擦循环。卡诺循环是由两个等 温过程和两个绝热过程组成的理想化循环。 不计摩擦、热损失及漏气,视为理想热机。
P
1
高温热库T1
Q1
绝热
4
2 等温T1
Q1
Q2
绝热
W Q1 Q2
Q2
卡诺循环
3
等温T2
V1 V4 V2 V3
V
低温热库T2 卡诺循环能流图
9
二、卡诺循环的效率
1→2 等温膨胀过程,吸热 Q1 = W= RT1 ln(V2/V1) 3→4 等温压缩过程,放热
P
1
Q1
绝热
4
2 等温T1
绝热
| Q2 | RT2 ln(V3 / V4 )
(3) 如果提高高温热源的温度,让热机仍工作在与 (1)相同的两条绝 热线之间,但每次循环净功比(1)增加20,求此时高温热源的温度。
W T2 0 W Q1 1500J 解 : (1) 1 25 0 Q1 T1 Q2 Q1 W 4500J T2 Q2 (2) w 3 Q1 8000 J w 3 T1 T2 Q1 Q2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
温过程 , 设T1 = 300 K , T2 = 200 K , V2 = 2pV1. 求循环效率.
解:
QAB
W AB
m RT ln V2 M 1 V1
吸热
A T1=300K
QBC
ΔE BC
m M
5 2
R
(T2
T1 )
放热
BDBiblioteka QCDW CDm M
RT 2
ln
V1 V2
放热
T2=200K C
15% QDA
ΔE DA
m M
5 2
R
(T1
T2 ) 吸热
V1
W
WAB WCD
T1
ln
V2 V1
T2
ln V1 V2
V2
Q1
QAB QDA
T1
ln V2 V1
5 2
(T1
T2 )
V
Va
Vb V
结论: 在任何一个循环过程中, 系统所做的净功在数值上 等于p –V 图上循环曲线所包围的面积.
循环过程的分类:
正循环: 在p –V 图上循环过程按顺时针进行 . 逆循环: 在p –V 图上循环过程按逆时针进行 . 热机: 工作物质作正循环的机器.
制设冷: 系机统: 工吸作热物Q质1 ,作系逆统循放环热的Q机2 器. 循环过程的热力学第一定律: Q1 Q2 W
大学物理
热力学
第7讲 循环过程
循环过程: 系统经历了一系列状态变化 过 程以后,又回到原来状态的过程.
循环特征: 经历一个循环过 程后, 内能不变.
ΔE 0
蒸汽机的工作原理
气体做功:
aIb 为膨胀过程: WaIb
p a
bIIa为压缩过程: WbIIa
pa
I
净功:
II
pb
b
W W aIb W bIIa 0
➢ 热机效率 W
在一次循环过程中, 工作物质对 外作的净功与它从高温热源 吸 收的总热量之比.
W
Q吸
Q 吸 Q放 W
热机效率
W 1 Q放
Q吸
Q吸
➢ 制冷系数 W
制冷过程: 外界作功W, 系统吸热 Q吸,放热Q放.
W Q放 Q吸
制冷系数:
Q吸 Q吸
W Q放 Q吸
例题 3.210 -2 kg 氧气作ABCD循环. AB和C D都为等
