17_第17课时 无机化工流程图问题
无机化工流程题解题方法指导-副本
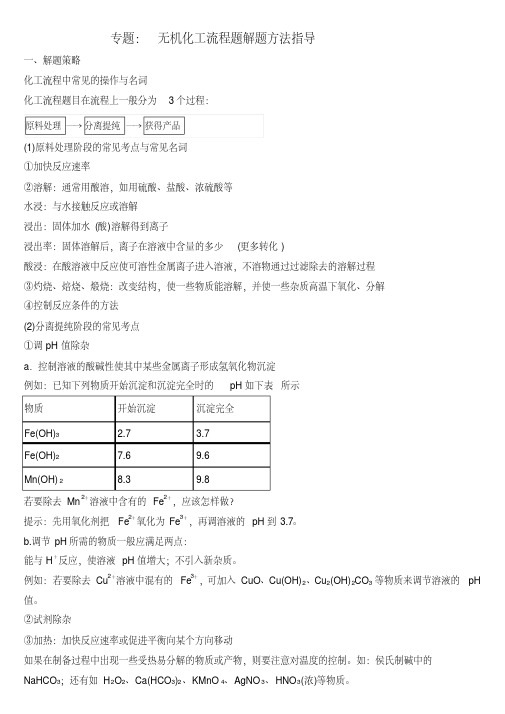
专题:无机化工流程题解题方法指导一、解题策略化工流程中常见的操作与名词化工流程题目在流程上一般分为3个过程:原料处理―→分离提纯―→获得产品(1)原料处理阶段的常见考点与常见名词①加快反应速率②溶解:通常用酸溶,如用硫酸、盐酸、浓硫酸等水浸:与水接触反应或溶解浸出:固体加水(酸)溶解得到离子浸出率:固体溶解后,离子在溶液中含量的多少(更多转化)酸浸:在酸溶液中反应使可溶性金属离子进入溶液,不溶物通过过滤除去的溶解过程③灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质高温下氧化、分解④控制反应条件的方法(2)分离提纯阶段的常见考点①调pH值除杂a.控制溶液的酸碱性使其中某些金属离子形成氢氧化物沉淀例如:已知下列物质开始沉淀和沉淀完全时的pH如下表所示物质开始沉淀沉淀完全Fe(OH)3 2.7 3.7Fe(OH)27.6 9.6Mn(OH)28.3 9.8若要除去Mn2+溶液中含有的Fe2+,应该怎样做?提示:先用氧化剂把Fe2+氧化为Fe3+,再调溶液的pH到3.7。
b.调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH值增大;不引入新杂质。
例如:若要除去Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH 值。
②试剂除杂③加热:加快反应速率或促进平衡向某个方向移动如果在制备过程中出现一些受热易分解的物质或产物,则要注意对温度的控制。
如:侯氏制碱中的NaHCO3;还有如H2O2、Ca(HCO3)2、KMnO4、AgNO3、HNO3(浓)等物质。
④降温:防止某物质在高温时会溶解(或分解)、为使化学平衡向着题目要求的方向移动⑤萃取(3)获得产品阶段的常见考点①洗涤(冰水、热水):洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
②蒸发、反应时的气体氛围抑制水解:如从溶液中析出FeCl3、AlCl3、MgCl2等溶质时,应在HCl的气流中加热,以防其水解。
公开课无机化工流程题解题策略

Mg(OH)2
12.4
2,题干:用框图形式将主要产工艺流程表示出来。
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
(2)滤渣I的主要成分有 (3)从滤液Ⅱ中可回收利用的主要物质有 。
部分阳离子以氢氧化物形式完全深沉时溶液的pH由见上表。
(写两条)
3,题尾:设问
。
二,设问特点
1,以点的形式设问。 即不需要理清工业生成流程图的主线即可以答题。
KCl 稀硫酸 NH4HCO3溶液 FeSO4溶液 反应I CO2(g) 过滤 反应II 反应IV CO2(g) FeCO3(s) 空气中煅烧 反应III 过滤 K2SO4(s) NH4Cl溶液 H2(g) (NH4)2S2O8溶液 Fe2O3(s)
FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O (3)反应Ⅰ需控制反应温度低于35 ℃,其目的是________。 防止NH4HCO3分解(或减少Fe2+的水解)
(4)使用合适的催化剂。加快反应速率,缩短达到平衡所需要的时间。
练习2: 钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSiO3 BaSO3、Ba(FeO2)2等]。某主要生产BaCl2、BaCO3、BaSO4的化 工厂利用钡泥制取Ba(NO3)2,其部分工艺流程如下:
(2)酸溶时通常控制反应温度不超过70 ℃,且不使用浓硝酸, 原因是________、______。 防止反应速率过快、浓HNO3易挥发、分解
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
(写两条)
2,以线的形式设问。 即必须先理解工业生产流程图主线与核心部分才能答题。
(2)滤渣I的主要成分有 。
无机化工流程图题的解答方法及常见答题技巧

无机化工流程图题的解答方法及常见答题技巧(1)增大原料浸出率(离子在溶液中的含量多少)的措施:搅拌、升高温度、延长浸出时间、增大气体的流速(浓度、压强),增大气液或固液接触面积(2)加热的目的:加快反应速率或促进平衡向某个方向(一般是有利于生成物生成的方向)移动(3)温度不高于××℃的原因适当加快反应速率, 但温度过高会造成(如浓硝酸)挥发//(如H2O2、NH4HCO3)分解//(如Na2SO3)氧化或促进(如AlCl3)水解等,影响产品的生成(4)从滤液中提取一般晶体(溶解度随温度升高而增大的晶体)的方法【蒸发浓缩<至有晶膜出现>、冷却结晶、过滤、洗涤(冰水洗、热水洗、乙醇洗)、干燥】(5)从滤液中提取溶解度受温度影响较小或随温度升高而减小的晶体的方法(蒸发浓缩、趁热过滤 <如果温度下降,杂质也会以晶体的形式析出来>、洗涤、干燥)(6)溶液配制、灼烧、蒸发、过滤用到的仪器(7)控制某反应的pH值使某些金属离子以氢氧化物的形式沉淀(调节pH所用试剂为主要元素对应的氧化物、碳酸盐、碱,以避免引入新的杂质;pH分离时的范围确定、范围过小的后果<导致某离子沉淀不完全>或过大的后果<导致主要离子开始沉淀>)(8)减压蒸馏(减压蒸发)的原因:减小压强,使液体沸点降低,防止(如H2O2、浓硝酸、NH4HCO3)受热分解\挥发(9)检验溶液中离子是否沉淀完全的方法:将溶液静置一段时间后,向上层清夜中滴入沉淀剂,若无沉淀生成,则离子沉淀完全(10)洗涤沉淀:沿玻璃棒往漏斗中加蒸馏水至液面浸没沉淀,待水自然流下后,重复操作2-3次(11)检验沉淀是否洗涤干净的方法:取少量最后一次的洗涤液于试管中,向其中滴入某试剂,若———–,则沉淀洗涤干净(13)冰水洗涤的目的:洗去晶体表面的杂质离子并降低被洗涤物质的溶解度,减少其在洗涤过程中的溶解损耗(14)乙醇洗涤的目的:降低被洗涤物质的溶解度,减少其在洗涤过程中的溶解损耗,得到较干燥的产物(15)蒸发、反应时的气体氛围:抑制某离子的水解,如加热蒸发AlCl3溶液时为获得AlCl3需在HCl气流中进行(16)事先煮沸溶液的原因:除去溶解在溶液中的(如氧气)防止某物质被氧化工业流程常见的操作与名词工业流程题目在流程上一般分为3个过程:(1)原料处理阶段的常见考点与常见名词①加快反应速率②溶解:通常用酸溶。
无机化工流程解题方法总结
无机化工流程题复习解题指导1.无机化工流程题的特点无机工业流程题能够以真实的工业生产过程为背景,体现能力立意的命题为指导思想,能够综合考查学生各方面的基础知识及将已有知识灵活应用在生产实际中解决问题的能力。
所以这类题成为近年来高考的必考题型。
这类题常呈现的形式:流程图、表格、图像这类题常围绕以下几个知识点进行设问:(1)反应速率与平衡理论的运用;反应物颗粒大小:反应速率、原料的利用率等温度:反应速率、物质的稳定性、物质的结晶等(2)氧化还原反应的判断、化学方程式或离子方程式的书写;(3)利用控制pH分离除杂;(4)化学反应的能量变化;(5)实验基本操作:除杂、分离、检验、洗涤、干燥等;(6)流程中的物质转化和循环,资源的回收和利用;(7)环境保护与绿色化学评价。
2.工业生产流程主线规律:主线主产品、分支副产品、回头为循环核心考点:物质的分离操作、除杂试剂的选择、生产条件的控制3.解答无机化工流程试题的程序基本步骤:①从题干中获取有用信息,了解生产的产品。
②然后整体浏览一下流程,基本辨别出预处理、反应、提纯、分离等阶段。
③分析流程中的每一步骤,从几个方面了解流程:A、反应物是什么B、发生了什么反应C、该反应造成了什么后果,对制造产品有什么作用;抓住一个关键点:一切反应或操作都是为获得产品而服务。
④从问题中获取信息,帮助解题。
解题思路:明确整个流程及每一部分的目的→仔细分析每步反应发生的条件以及得到的产物的物理或化学性质→结合基础理论与实际问题思考→注意答题的模式与要点4.熟悉工业流程常见的操作与名词工业流程题目在流程上一般分为3个过程:原料处理→分离提纯→获得产品(1)原料处理阶段的常见考点与常见名词①加快反应速率②溶解:通常用酸溶。
如用硫酸、盐酸、浓硫酸等水浸:与水接触反应或溶解浸出:固体加水(酸)溶解得到离子浸出率:固体溶解后,离子在溶液中的含量的多少(更多转化)酸浸:在酸溶液中反应使可溶性金属离子进入溶液,不溶物通过过滤除去的溶解过程③灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质高温下氧化、分解④控制反应条件的方法(2)分离提纯阶段的常见考点①调pH值除杂a.控制溶液的酸碱性使其某些金属离子形成氢氧化物沉淀例如:已知下列物质开始沉淀和沉淀完全时的pH如下表所示物质开始沉淀沉淀完全Fe(OH)3 2.7 3.7Fe(OH)27.6 9.6Mn(OH)28.3 9.8若要除去Mn2+溶液中含有的Fe2+,应该怎样做?提示:先用氧化剂把Fe2+氧化为Fe3+,再调溶液的pH到3.7。
《无机化工流程题解题方法指导》

专题讲座无机化工流程题解题方法指导一、解题策略化工流程中常见的操作与名词化工流程题目在流程上一般分为3个过程:原料处理―→分离提纯―→获得产品(1)原料处理阶段的常见考点与常见名词①加快反应速率②溶解:通常用酸溶,如用硫酸、盐酸、浓硫酸等水浸:与水接触反应或溶解浸出:固体加水(酸)溶解得到离子浸出率:固体溶解后,离子在溶液中含量的多少(更多转化)酸浸:在酸溶液中反应使可溶性金属离子进入溶液,不溶物通过过滤除去的溶解过程③灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质高温下氧化、分解④控制反应条件的方法(2)分离提纯阶段的常见考点①调pH值除杂a.控制溶液的酸碱性使其中某些金属离子形成氢氧化物沉淀例如:已知下列物质开始沉淀和沉淀完全时的pH如下表所示若要除去Mn2+提示:先用氧化剂把Fe2+氧化为Fe3+,再调溶液的pH到3.7。
b.调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH值增大;不引入新杂质。
例如:若要除去Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH值。
②试剂除杂③加热:加快反应速率或促进平衡向某个方向移动如果在制备过程中出现一些受热易分解的物质或产物,则要注意对温度的控制。
如:侯氏制碱中的NaHCO3;还有如H2O2、Ca(HCO3)2、KMnO4、AgNO3、HNO3(浓)等物质。
④降温:防止某物质在高温时会溶解(或分解)、为使化学平衡向着题目要求的方向移动⑤萃取(3)获得产品阶段的常见考点①洗涤(冰水、热水):洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
②蒸发、反应时的气体氛围抑制水解:如从溶液中析出FeCl3、AlCl3、MgCl2等溶质时,应在HCl的气流中加热,以防其水解。
③蒸发浓缩、冷却结晶:如除去KNO3中的少量NaCl。
④蒸发结晶、趁热过滤:如除去NaCl中的少量KNO3。
⑤重结晶(4)其他常见考点①化学方程式②实验仪器③计算④信息二、热点题型探究热点1碱金属及其矿物的开发利用[例1](2012·广东理综,32)难溶性杂卤石(KSO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水2中存在如下平衡:K2SO4·MgSO4·2CaSO4·2H2O(s) 2Ca2++2K++Mg2++4SO2-4+2H2O为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:(1)滤渣主要成分有________和________以及未溶杂卤石。
无机化工流程题的解题策略

无机化工流程题的解题策略《无机化工流程题的解题策略》嘿,同学们!今天咱们来唠唠无机化工流程题的解题策略。
这无机化工流程题啊,就像一个神秘的大工厂里的探险之旅,可有意思啦。
我记得有一次做一道无机化工流程题,那图就像一个超级复杂的迷宫一样。
我当时就懵了,心里想:“这都是啥呀?”可是呢,我知道不能就这么被它吓倒。
咱们得像勇敢的小探险家一样,一点一点去摸索。
在做这种题的时候,咱们第一步要做啥呢?首先得看原料和目标产物。
这就好比你要从一个地方走到另一个地方,你得知道自己从哪出发,要到哪去呀。
比如说,原料是一种矿石,目标产物是一种金属单质。
那你就得想啦,矿石里有好多杂质呢,怎么才能把那些杂质去掉,把金属单质提炼出来呢?这就像你从一堆杂物里找一个宝贝一样,得想办法把那些没用的东西挑出去。
然后呢,咱们就得顺着流程走啦。
流程里那些箭头就像一条条小路,引导着我们前进。
有时候会看到有什么“酸浸”“碱浸”的步骤。
这是啥意思呢?这就像是给原料洗个特殊的澡,酸浸就像是用酸性的水来洗,能把一些碱性的杂质或者能和酸反应的物质给去掉。
我就想啊,这原料就像一个脏娃娃,得用不同的东西把它洗干净。
我和我的同桌还经常讨论这种题呢。
有一回,他就说:“你看这个‘氧化’步骤,为啥要加这个氧化剂呢?”我就回答他:“你想啊,就像我们要把一个调皮捣蛋的小坏蛋变成乖乖听话的好孩子,得用点特别的办法。
这里加氧化剂就是把那些化合价低的元素变成化合价高的元素,这样才能让它朝着我们想要的目标产物的方向去变化呀。
”他听了之后,就像突然开窍了一样,说:“哦,原来是这样啊,真好玩。
”再看看那些反应条件,什么温度啦、压强啦。
这就像做菜的时候,火候和压力的控制一样重要。
温度高一点或者低一点,可能就会得到不一样的东西。
我就想啊,如果把这个反应当成做蛋糕,温度不对,那蛋糕可能就烤糊了或者没烤熟呢。
有一次考试,我没太注意这个温度条件,结果算出的答案就错得离谱。
我当时那个懊悔呀,就像丢了最心爱的玩具一样。
高考 无机化工流程图题 较基础 简

无机化工流程图题要点介绍1.化工生产选择适宜条件的原则化工生产选择适宜条件的目的是尽可能加快反应速率和提高反应进行的程度,依据外界条件对化学反应速率和化学平衡影响的规律确定,其原则是:(1)对任一可逆反应,增大反应物浓度,能提高反应速率和转化率。
故生产中常使廉价易得的原料适当过量,以提高另一原料的利用率,如氮气与氢气的配比为1.07∶3。
(2)对气体分子数减少的反应,增大总压使平衡向增大生成物的的方向移动。
但压强太大,动力消耗,设备要求、成本增高,故必须综合考虑。
(3)对放热反应,升温,提高反应速率,但转化率降低,若温度太低,反应速率又太慢,故需使用适当的催化剂。
对吸热反应,升温,加快反应速率,又能提高转化率,但要避免反应物或生成物过热分解。
(4)使用催化剂可大大提高反应速率且不影响化学平衡,但使用时必须注意其活性温度范围,且防止催化剂“中毒”,延长使用寿命。
合成氨适宜条件:500℃、铁触媒、2×107~5×107、循环操作。
2.绿色化学(1)节省资源,提高原料转化率和利用率。
例如在合成氨工业,硝酸工业,接触法制硫酸,联合制碱法等工艺流程中采取了循环操作,体现了绿色化学中节省能源的基本原理。
(2)化工生产中均介绍了尾气回收方法和处理装置以防止或减少环境污染。
例如:氨氧化法制硝酸、接触法制硫酸、炼钢、炼铁等均介绍了尾气处理或尾气吸收装置。
★化学工艺流程题的结构、特点与解法1. 工艺流程题的结构、特点和作用工艺流程题的结构分题头、题干和题尾三部分。
题头一般是简单介绍该工艺生产的原材料和工艺生产的目的(包括附产品);题干部分主要用框图形式将原料到产品的主要生产工艺流程表示出来;题尾主要是根据生产过程中涉及到的化学知识设制成系列问题,构成一道完整的化学试题。
其特点与作用有三:一是源于生产实际,以解决化学实际问题作思路进行设问,情境真实,能培养学生理论联系实际,学以致用的学习观;二是内容丰富,涉及化学基础知识方方面面,能考查学生化学双基知识的掌握情况和应用双基知识解决化工生产中有关问题的迁移推理能力;三是试题新颖,阅读量大,能考查学生的阅读能力和资料的收集处理能力。
无机化工流程图题的解答方法及常见答题技巧.

无机化工流程图题的解答方法及常见答题技巧工艺流程题的结构分题头、题干和题尾三部分。
题头一般是简单介绍该工艺生产的原材料和工艺生产的目的(包括副产品);题干部分主要用框图形式将原料到产品的主要生产工艺流程表示出来;题尾主要是根据生产过程中涉及到的化学知识设制成系列问题,构成一道完整的化学试题。
因此解答化工工艺流程题的基本步骤是:推荐阅读:运用规律解工艺流程题——“模型解题法”一、读题头,得目的,划原料明产品,解决“干什么”通过阅读题头,了解流程图以外的文字描述、表格信息、后续设问中的提示性信息,通过对比分析工业流程示意图中的第一种物质(原材料)与最后一种物质(产品),弄清从原料出发,要得到最终产品,必须除去什么元素、引进什么元素?阅读题干时要随手画出题目提供的一些课本上未出现过的诸如溶解度、物质的热稳定性和熔沸点等不知何用的信息,以便在后面阅读流程图和解题时随时调用。
二、读题干,析过程,看措施推用意,解决“怎么做”题干部分主要用框图形式将原料到产品的主要生产工艺流程表示出来。
分析流程中的每一步骤的反应物是什么?发生了什么反应?利用了什么原理(氧化还原、溶解度、电离平衡、水解平衡、溶解平衡)?该反应造成了什么后果(除目标物质外还产生了什么杂质或副产物?这些物质又是如何分离、提纯和循环利用的?如何体现绿色化学思想?)?每一步操作进行到什么程度最佳?在此过程中抓住一个关键点:一切反应或操作都是为获得产品而服务,在回答相关操作的原因或目的时要从对产品的影响层面作答。
我们把它分为三个层次:读得懂的;读得不太懂但根据上下文可以勉强懂的;完全读不懂的。
快读读得懂的,对于读得懂的,往往是常见的化学反应、化学实验操作等基础知识,是要求学生必须掌握的。
出题者常在这些环节设问,让大部分学生都能得到这些分。
因此要克服恐惧心理意识到,无论流程图如何复杂都会有简单的得分题。
例如一些灼烧、水浸及过滤的目的。
细读读得不太懂但根据上下文可以勉强懂的,这部分需要运用已有的基础知识,根据学习过的化学反应原理,联系实验工业生产及题目信息等进行知识的整合方可得到结论的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
②试剂除杂 ③加热:加快反应速率或促使平衡向某个方向移动。 如果在制备过程中出现一些受热易分解的物质或产物,则要注意对温度的 控制。 ④降温:防止某物质在高温时溶解(或分解)或使化学平衡向着题目要求的 方向移动。 ⑤萃取 (3)获得产品阶段 ①洗涤(冷水、热水):洗去晶体表面的杂质离子,并减少晶体在洗涤过程中 的溶解损耗。 ②蒸发浓缩、冷却结晶:如除去KNO3中的少量NaCl。
典例1 (2015山东威海一模)氯化亚铜(CuCl)常用作有机合成工业中的催 化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。下图是工业上用 印刷电路的蚀刻液的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:
(2)选择的还原剂是否能用铁 (填“是”或“否”),原因是 。
(3)若滴定用掉c mol/L KMnO4溶液b mL,则样品中铁元素的质量分数是 。
考点突破
考点 工艺流程题的解题方法
1.通过学过的化学知识明确原料和产品(包括副产品)间的转化关系,即箭头 方向所代表的含义。
2.依据流程图搞清流程中每一步发生了什么反应(可能发生的副反应),弄清 有关反应原理,发生的副反应会对产品有何影响、如何消除(除杂、分 离)。 3.由于该类试题多是与实际的工业生产相联系,有些问题就需要从生产成 本、物质的循环利用、环境污染等角度进行考虑。 4.注意审题技巧 化工生产流程图题中经常会出现一些表述性词语,这些表述性词语就是隐 含信息,可以暗示我们审题应考虑的角度。常见的有: (1)“控制较低温度”——常考虑物质的挥发,物质的不稳定性和物质的转 化等。 (2)“加过量试剂”——常考虑反应完全或增大转化率、产率等。
③蒸发结晶、趁热过滤:如除去NaCl中的少量KNO3。 ④重结晶。 自测1 MgSO4·7H2O在医药上常用作泻药,工业上可用氯碱工业中的一次 盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和 碳酸盐等成分。其主要工艺如下:
(1)用H2SO4调节溶液pH至1~2,H2SO4的作用是 。
(6)流程中的物质转化和循环,资源的回收和利用; (7)环境保护与绿色化学评价。 2.工业生产流程主线 规律:主线主产品、分支副产品、回头为循环。 核心考点:物质的分离操作、除杂试剂的选择、生产条件的控制。 3.工业流程常见的操作 工业流程题目在流程上一般分为三个过程: 原料处理→分离提纯→获得产品 (1)原料处理阶段。 ①粉碎:加快反应速率。 ②溶解:通常用酸溶,如稀硫酸、盐酸、浓硫酸等。
不断搅拌下滴加足量2 mol·L-1 BaCl2溶液,充分反应后,得沉淀4.46 g,则样品
纯度为
。
自测2 某氯化亚铁和氯化铁的混合物,现要测定其中铁元素的质量分数, 按以下步骤进行实验:
Ⅰ.请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
、
(填仪器名称)。
(2)请写出加入溴水发生反应的离子方程式:
。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至
室温称量其质量为b2 g,若b1-b2=0.3,则接下来还应进行的操作是
。若蒸发皿质量是W1 g,蒸发皿与加热后固体总
质量是W2 g,则样品中铁元素的质量分数是
。
Ⅱ.有同学提出,还可以采用以下方法来测定:
(1)溶解样品改用了硫酸,而不再用盐酸,原因是 。
9T; 2015年安徽理综,27T。
教材研读
无机化工流程问题中涉及的基础知识 1.无机化工流程题的特点 无机化工流程题以真实的工业生产过程为背景,能够综合考查学生各方面 的基础知识及将已有知识灵活应用在生产实际中解决问题的能力。 这类题常呈现的形式:流程图、表格、图像。 这类题常围绕以下几个知识点进行设问: (1)反应速率与平衡理论的运用; (2)氧化还原反应的判断、化学方程式或离子方程式的书写; (3)通过控制pH除杂; (4)化学反应的能量变化; (5)实验基本操作:除杂、分离、检验、洗涤、干燥等;
3.提取信息、分析问题,将新信息与已 的化学实验与探究能力、分析和解决 的知识。
有知识整合,并组织化学术语进行表 (解答)化学问题的能力以及获取化学
达。
信息的能力,突出对学生分析与综
合、类比与比较、判断和推理等思维
能力的要求。如2015年课标Ⅰ,27T;2
015年课标Ⅱ,28T; 2015年山东理综,2
(3)“能否加其他物质”——常考虑会不会引入杂质或是否影响产品的纯 度。 (4)“在空气中或在其他气体中”——主要考虑O2、H2O、CO2或其他气体 是否参与反应或达到防氧化、防水解、防潮解等目的。 (5)“控制pH”——常考虑防水解、促进生成沉淀或除去杂质等。 (6)“用某些有机试剂清洗”——常考虑降低物质溶解度有利于析出、减 少损耗和提高利用率等。
(2)加NaClO溶液至pH=5~6并加热煮沸5~10分钟,沉淀2中主要含有MnO2和
另外两种难溶物,这两种难溶物的化学式分别为
、
;其中NaClO溶液将MnSO4转化为MnO2的离子方程式为 。
(3)检验滤液Ⅱ中是否含有Fe3+的实验方法是 。
(4)“操作X”是将溶液
、、过Βιβλιοθήκη 洗涤,即得到MgSO4·7H2O晶体。 (5)准确称量制得的样品5 g,用200 mL水溶解,加入2 mol·L-1的盐酸5 mL,在
课标版 化学
第17课时 无机化工流程图问题
考纲导学
考试要点
命题规律
备考策略
1.综合掌握元素化合物的性质。
无机化工流程图题是综合题,综合考 复习备考时注意挖掘题目中的有用信
2.将化学知识迁移到生产实际中解决 查元素化合物、基本概念和理论、实 息。熟练掌握基本概念、基本理论、
实际问题。
验与探究等相关知识,综合考查学生 元素化合物知识以及与化学实验相关
水浸:与水接触反应或溶解。 浸出:固体加水(或酸)溶解得到离子。 浸出率:固体溶解后,离子在溶液中的含量的多少。 ③灼烧、焙烧、煅烧:改变结构,使一些杂质在高温下氧化、分解。 (2)分离提纯阶段 ①调pH除杂 a.控制溶液的酸碱性使某些金属离子形成氢氧化物沉淀。 b.调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH增大;不引入 新杂质。 例如:若要除去含Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH)2、Cu2(OH)2 CO3等物质来调节溶液的pH。
