实验八片剂的制备及质量检查
片剂制备实验报告

片剂制备实验报告实验目的本实验旨在探究片剂的制备过程,通过了解片剂制备的基本原理和步骤,提高学生对药物制剂的认识和理解。
实验材料•主要药物原料•辅助药物原料•药品配方•制剂设备实验步骤1. 原料准备首先,根据药品配方,准备所需的主要药物原料和辅助药物原料。
确保原料的质量和纯度达到要求,并按照配方要求进行称量和筛选。
2. 混合制备将称量好的主要药物和辅助药物原料放入制剂设备中,进行均匀混合。
混合过程中需要注意控制温度、湿度和混合时间,保证药物原料的充分混合。
3. 加工制备经过混合的药物原料,进一步进行加工制备。
这一步骤包括湿法制粒、干法制粒、干燥等工艺。
制粒过程中需要掌握加液量、湿度和制粒时间的合理控制,保证制粒的质量和大小均匀。
干燥过程中需要控制温度和湿度,确保制剂的干燥程度符合要求。
4. 造粒和压片经过加工制备的药物原料,进一步进行造粒和压片。
造粒是将制粒好的药物原料进行分级筛选,保证颗粒大小的一致性。
压片是将造粒好的药物原料放入片剂机中,通过压制形成片剂。
这一步骤需要掌握合适的压片力度和速度,保证片剂的质量和形状。
5. 表面处理制备好的片剂需要进行表面处理,以提高片剂的外观和稳定性。
表面处理可以采用磨光、薄膜包衣等方法,根据药物特性选择合适的表面处理工艺。
6. 包装和贮存最后,制备好的片剂需要进行包装和贮存。
包装过程中需要注意选择合适的包装材料,保证片剂的密封性和防潮性。
贮存条件也需要注意,确保片剂在合适的温度和湿度下储存,避免药物的变质和降解。
实验结果与分析经过以上步骤,成功制备了一批片剂。
经实验测试,片剂的外观良好,质量符合药典要求。
通过对片剂的制备过程的分析,可以得出以下结论:1.片剂制备过程中需要掌握一定的药物制剂原理和工艺知识,确保制剂的质量和稳定性。
2.不同药物原料和配方需要选择合适的制剂设备和工艺方法,以保证最佳的制剂效果。
3.片剂制备过程中的环境条件和操作控制对最终产品的质量有重要影响,需要严格遵守操作规程。
实验二-片剂的制备与质量检查
实验二 水杨酸片的制备及质量检查一、实验目的1. 通过片剂制备,掌握湿法制粒压片的工艺过程。
2. 掌握单冲压片机的使用方法及片剂质量的检查方法。
3. 掌握片剂的质量检查方法,并了解压片力对片剂硬度或崩解的影响。
二、实验指导片剂是应用最为广泛的药物剂型之一。
片剂的制备方法有制颗粒压片(分为湿法制粒和干法制粒),粉末直接压片和结晶直接压片。
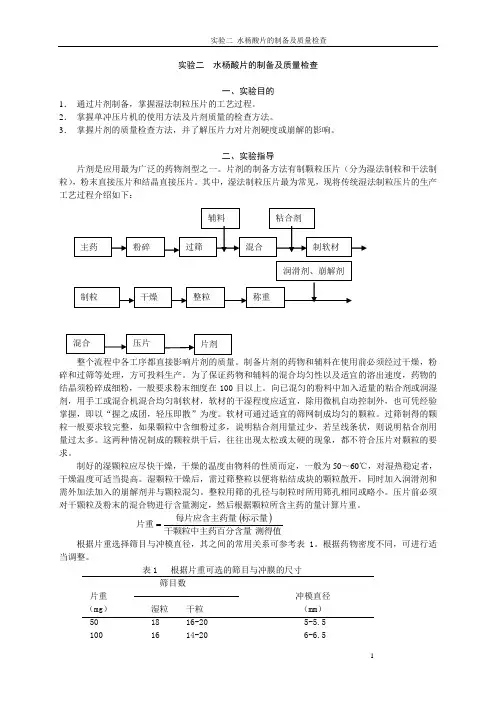
其中,湿法制粒压片最为常见,现将传统湿法制粒压片的生产工艺过程介绍如下:整个流程中各工序都直接影响片剂的质量。
制备片剂的药物和辅料在使用前必须经过干燥,粉碎和过筛等处理,方可投料生产。
为了保证药物和辅料的混合均匀性以及适宜的溶出速度,药物的结晶须粉碎成细粉,一般要求粉末细度在100目以上。
向已混匀的粉料中加入适量的粘合剂或润湿剂,用手工或混合机混合均匀制软材,软材的干湿程度应适宜,除用微机自动控制外,也可凭经验掌握,即以“握之成团,轻压即散”为度。
软材可通过适宜的筛网制成均匀的颗粒。
过筛制得的颗粒一般要求较完整,如果颗粒中含细粉过多,说明粘合剂用量过少,若呈线条状,则说明粘合剂用量过太多。
这两种情况制成的颗粒烘干后,往往出现太松或太硬的现象,都不符合压片对颗粒的要求。
制好的湿颗粒应尽快干燥,干燥的温度由物料的性质而定,一般为50~60℃,对湿热稳定者,干燥温度可适当提高。
湿颗粒干燥后,需过筛整粒以便将粘结成块的颗粒散开,同时加入润滑剂和需外加法加入的崩解剂并与颗粒混匀。
整粒用筛的孔径与制粒时所用筛孔相同或略小。
压片前必须对干颗粒及粉末的混合物进行含量测定,然后根据颗粒所含主药的量计算片重。
()测得值干颗粒中主药百分含量标示量每片应含主药量片重=根据片重选择筛目与冲模直径,其之间的常用关系可参考表1。
根据药物密度不同,可进行适当调整。
表1 根据片重可选的筛目与冲膜的尺寸筛目数片重 冲模直径(mg ) 湿粒 干粒 (mm )50 18 16-20 5-5.5100 16 14-20 6-6.5150 16 14-20 7-8200 14 12-16 8-8.5300 12 10-16 9-10.5500 10 10-12 12制成的片剂需按照《中国药典》规定的片剂的质量检查项目进行检查。
实验2药物片剂的质量检查PPT课件

硬度测试
硬度测试
硬度适中的片剂有利于药物的崩 解和溶出,提高药物的生物利用
度。
硬度计
使用硬度计对片剂进行硬度测试, 记录每个片剂的硬度值。
操作方法
按照规定的操作方法进行硬度测试, 确保测量结果准确可靠。
崩解时限
崩解时限
崩解时限是衡量片剂质量的重要 指标之一,合格的片剂应在规定
的时间内完成崩解。
崩解设备
通过测定药物片剂的重量差异、硬度、崩解度、溶出度等指标,可以评估药物片剂 的质量
本实验将采用仪器法进行上述指标的测定
实验步骤概览
01
02
03
04
准备实验仪器和试剂
制备不同批次的药物片剂样品
进行药物片剂的质量检查,记 录数据
分析数据,得出结论
02 药物片剂的质量标准
外观质量
01
02
03
外观质量
片剂表面应光滑、色泽均 匀,无裂片、黑点、粘连、 变形等缺陷。
根据实验数据的分析结果,判断药物 片剂的质量是否符合规定的要求。
04 实验结论与讨论
实验结论总结
实验目的
通过实验了解药物片剂的质量检查方 法,确保药物片剂的质量符合标准。
实验原理
基于药物片剂的质量标准,采用不同 的检测方法对片剂的外观、硬度、崩 解时限等指标进行检测。
实验步骤
详细记录了实验的操作过程,包括样 品的选取、仪器的使用、数据的记录 等。
实验2药物片剂的质量检查ppt课 件
目录
• 实验简介 • 药物片剂的质量标准 • 实验操作与结果分析 • 实验结论与讨论 •的
掌握药物片剂的质量 检查方法
学会使用相关仪器进 行药物片剂的质量检 查
片剂制备-片剂质量检验
课程名称
药物制剂
课题
片剂制备-片剂质量检测
审批
授课日期
年月日
授课时数
10节
教学班级
12药物班
教材名称及版本
药物制剂技术(医药出版社)
教学方法
项目教学法、任务驱动法、归纳法
教学媒体(含教具)
黑板、粉笔、多媒体、教具
学习
目标
一、知识目标:
1、片剂质量要求-外观、硬度、片重差异、崩解时限。
规定
片重质量
重量差异限度
0.3克以下
±7.5%
0.3克或以上
±5%
三、硬度分析:空抛两米两次,落地不裂者合格
四、崩解时限:37度,15分钟,缓慢搅动
讲授法
任务准备(15分钟)
项目实施(8课时)
评价(15分钟)
布置作业
分组实施:
1、更衣、洗手消毒
2、按要求准备好各组器具
在工作任务指导下,分小组完成工作任务:
3、学生小组示范展示操作、互评。
教学准备
教材学材:
1、《药物制剂技术》,中国劳动和社会保障出版社
工具设备:
药片、天平、水浴锅
任务书
项目
内容
课题
片剂制备-片剂质量检验
学习材料
教程片剂内容+补充内容
引导问题
1.片剂质量要求包括哪几个方面?
任务咨询
明确任务:对片剂进行质量检验。
1、任务一:对片剂外观进行质量检验-松片、裂片、以及在生产过程中产生的粘冲等的原因分析。
2、任务二:片重差异检验-分析影响片重差异的原因
3、任务三:硬度检验-分析影响硬度的原因
4、任务四:崩解时限检验-分析超限原因
片剂的制备及其质量考察

二、实验指导
• 湿法制粒压片的生产工艺过程
辅料 主药 粉碎 过筛 混合 粘合剂 制软材
混合
称重
整粒
干燥
制粒
润滑剂、崩解剂 压片 片剂
三、仪器与材料
• 仪器:高速粉碎机,普通天平,混合机,快速搅 拌制粒机,电热干燥箱,单冲压片机,片剂硬度 测试仪,脆碎度测试仪,崩解时限测试仪 • 材料:乙酰水杨酸,维生素C,糊精,淀粉,枸 橼酸,滑石粉,硬脂酸镁,50% 乙醇,酒石酸
3. 操作注意
干淀粉应在105℃干燥约2小时,使含水量在8~10% 之间。黑点。
四、实验内容与操作
(三)疏水性润滑剂对碳酸氢钠片剂崩解的影响
1. 处方:
碳酸氢钠 淀粉 硬脂酸镁 20g 2g 适量
2. 操作:
• ① 10% 淀粉浆的制备:称取淀粉2g,加入到20ml蒸馏水 中均匀分散,加热糊化,即可。 • ② 碳酸氢钠颗粒的制备:称取碳酸氢钠细粉20g与淀粉2g ,混匀,加10%淀粉浆适量,制软材,过16目筛制粒。湿 颗粒在50℃干燥,干颗粒过16目筛整粒。 • ③ 加入不同比例疏水性润滑剂:将②中碳酸氢钠干颗粒 平均分为两份,称重,其中一份中加入0.6% 硬脂酸镁, 另一份加入3% 硬脂酸镁,混匀,在相同压力下压片,测 定两种片剂的崩解时间。
重量差异限度平均片重重量差异限度030g以下75030g或030g以上5五实验结果与讨论将上述实验结果列表硬度kg崩解时间min结论五实验结果与讨论名称硬度kg崩解时间min复方甘草片思考题分析并讨论实验结果总结出影响片剂崩解的因素及原理
实验一 片剂的制备及其质量考察
一、实验目的
1. 通过片剂制备,掌握湿法制粒压片的工艺过程。 2. 掌握单冲压片机的基本构造、使用方法及片剂 质量的检查方法。 3. 考察压片力及崩解剂等对片剂的硬度或崩解的 影响。
药学基础实验 片剂制备

将吊篮通过上端的不锈钢轴悬挂于金属支架上,
浸入温度为 37 ± 1 ℃的恒温水浴中,调节水位高
度使吊篮上升时筛网在水面下 15mm 处,下降时
筛网距烧杯底部 25mm ,支架上下移动的距离为
55 ± 2mm ,往返频率为每分钟 30-32 次。取滴ຫໍສະໝຸດ 6粒,分别置于上述吊篮的玻璃管中,
每管各加一粒,启动崩解仪进行检查。各丸应在
片剂的制备方法主要有湿法制粒压片、干法制粒压 片和直接压片法。
片剂的分类方法有多种,其中根据给药途径分为口 服用片剂、口腔用片剂、非口服片剂、外用片剂等。
主药及辅料的预处理
1.主药及辅料的处理
制备片剂用的主药及辅料一般要先经粉碎、过筛、 混合操作。当主药为难溶性药物时,必须有足够 的细度以保证混合均匀及溶出度符合要求。
颗粒的大小一般根据片剂大小由筛网孔径来控 制,一般大片(片重0.3~0.5g)选用14~16目 筛,小片(片重0.3以下)选用18~20目筛制粒。
颗粒一般要求较圆整,可含有一部分小颗粒。如 果颗粒中含细粉太多,说明粘合剂用量太少;
如果颗粒呈长条状,则粘合剂用量太多。
这两种颗粒烘干后往往会太松或太硬,都不符合 压片用颗粒要求。
(2)在处方中加入酒石酸的目的是防止Vc遇金属离子变色(酒石酸对 金属离子有络合作用)。也可改2%的枸橼酸,同样具有稳定Vc的作 用。
(3)由于酒石酸量小,为混合均匀,宜先融入粘合剂(50%乙醇)中。
【质量检查】
崩解时限:取药片6片,分别置于吊篮的玻璃管中, 每管各加1片,吊篮浸入盛有37±1℃水的1000ml烧 杯中,开动马达按一定的频率和幅度往复运动(每分 钟30-32次)。从片剂置于玻璃管时开始计时,至片 剂全部崩解成碎片并全部通过管底筛网止,该时间 即为崩解时间,应符合规定崩解时限。如有1片崩解 不全,应另取6片复试,均应符合规定。
药剂学实验——片剂的制备与质量检查
实验六 片剂的制备及质量检查
润滑剂 黏合剂 崩解剂
润滑剂 崩解剂
主
药粉
碎混 和
制 制干 整 软湿
混压
辅 料
过 筛
合
材 粒燥 粒 填充
合 挥发
片
剂
物
湿法制粒压片工艺流程
实验六 片剂的制备及质量检查
实验内容与操作
➢实验材料与设备 实验材料:蓝淀粉、糖粉、糊精、淀粉、50%乙 醇、硬脂酸镁等 实验器材:单冲压片机、药筛、搪瓷盆、片剂崩 解仪、不同冲头和冲模(模圈)
实验六 片剂的制备及质量检查
➢实验内容与操作
1.空白片的制备 操作
2.空白片质量检查
操作
实验六 片剂的制备及质量检查
实验报告
实验六 片剂的制备及质量检查
思考题
1.制湿粒之前过两次筛的目的是什么?如果不 过筛会出现什么问题? 2.造成片剂重量差异和崩解时限检查不合格 的主要原因是什么?ຫໍສະໝຸດ 实验六 片剂的制备及质量检查
实验目的 实验指导 实验内容与操作 实验报告 思考题
实验六 片剂的制备及质量检查
实验目的
初步掌握湿法制粒压片的过程的技术 会分析片剂处方的组成和各种辅料在压片 过程中的作用 正确使用单冲压片机 熟悉处片重差异、崩解时限的检查方法
实验六 片剂的制备及质量检查
实验指导
片剂(tablets)系指药物与适宜的辅料混匀压制 而成的圆片状或异形片状的固体制剂(见图6-1)
片剂的生产工艺及质量检测培训教材
片剂的生产工艺及质量检测培训教材1. 引言片剂是一种固体制剂,常用于口服给药。
片剂的生产工艺决定了其质量和药效,而质量检测是保证片剂安全和可靠性的重要环节。
本文档将介绍片剂的生产工艺及质量检测相关知识,帮助读者了解片剂的制备过程和质量控制。
2. 片剂的生产工艺片剂的生产工艺包括原料准备、混合、造粒、湿法制片、干燥、包衣和包装等环节。
下面将对每个环节进行详细介绍。
2.1 原料准备原料准备是片剂生产的第一步,包括活性成分、辅料和溶剂等的准备与称量。
合理的原料准备能够确保片剂的药效和质量。
2.2 混合混合是将活性成分、辅料和溶剂等按照一定比例混合均匀的过程。
混合方式通常有干混法和湿混法两种,根据不同药物的特性选择适合的混合方式。
2.3 造粒造粒是将混合后的物料进行颗粒化处理,以便更好地制备成片剂。
造粒方法有湿法造粒和干法造粒两种,根据原料的特性选择适合的造粒方法。
2.4 湿法制片湿法制片是将颗粒化的物料与黏合剂混合后通过压片机进行制片。
制片的压力、时间和速度等参数需要严格控制,以保证片剂的质量和一致性。
2.5 干燥湿法制片后的片剂需要进行干燥处理,以去除水分并增加片剂的稳定性。
干燥的方法常用的有烘箱干燥和流化床干燥两种。
2.6 包衣某些片剂需要进行包衣操作,以改善药物的外观和稳定性。
常用的包衣方法有薄膜包衣、糖衣和乳糖包衣等。
2.7 包装片剂制备完成后需要进行包装,以确保片剂的质量和保存期限。
常见的包装方式有铝塑包装、泡罩包装和瓶装等。
3. 片剂的质量检测片剂的质量检测是保证片剂质量和药效的重要环节。
下面将介绍片剂常见的质量检测项目。
3.1 外观检查外观检查是片剂质量检测的第一步,通过目视观察片剂的颜色、形状、表面光滑度等指标进行判断。
3.2 重量和尺寸通过称重和测量片剂的尺寸,可以判断片剂的重量和大小是否符合要求。
3.3 含量测定含量测定是判断片剂中活性成分含量的关键指标,常用的方法有高效液相色谱法和紫外分光光度法等。
片剂实验报告是什么
片剂实验报告是什么实验目的本实验旨在通过制备片剂,掌握片剂的制备工艺和质量控制方法。
同时,了解片剂的物理性质和化学性质。
实验原理片剂的定义片剂是一种固体制剂,主要由药物和辅料组成,通过压制方法制成,具有平坦的表面和固定的形状。
片剂的制备工艺片剂的制备主要包括下列几个步骤:1. 原料准备:选择适当的活性成分和辅料,根据药物的特性和所需要的剂量确定配方。
2. 研磨:将药物和辅料粉碎成合适的粒度,以确保均一性和可压性。
3. 混合:将药物和辅料充分混合,以确保均匀分布。
4. 加水:适量加入水或其他添加剂,以增加片剂的可塑性。
5. 压制:将混合物填入模具中,用适当的压力进行压制,形成片剂的形状。
6. 干燥:将刚制成的片剂置于通风良好的地方,以去除水分,增加片剂的硬度。
片剂的质量控制片剂的质量控制主要包括外观质量、尺寸质量和化学成分质量等方面的检测。
- 外观质量:检查片剂的形状、颜色、表面光滑度等。
- 尺寸质量:测定片剂的厚度、直径和重量等。
- 化学成分质量:通过化学分析方法,检测片剂中的活性成分含量、杂质含量和溶出度等指标。
实验步骤1. 准备所需原料和设备:药物粉末、辅料、模具、研磨机、混合器、压片机等。
2. 研磨:将药物和辅料进行研磨,使其达到合适的粒度。
3. 混合:将药物和辅料充分混合,以确保均匀分布。
4. 加水:根据所需的可塑性和可压性,适当加入适量的水。
5. 压制:将混合物填入模具中,用压片机进行压制。
6. 干燥:将制成的片剂放置于通风良好的地方进行干燥。
7. 质量控制:检查片剂的外观质量、尺寸质量和化学成分质量。
实验结果经过制备的片剂外观圆形,色泽一致,表面光滑。
厚度、直径和重量均符合预定要求。
化学分析结果显示,片剂中的活性成分含量符合规定要求,杂质含量和溶出度也在合理范围内。
实验结论本实验通过制备片剂,掌握了片剂的制备工艺和质量控制方法。
片剂制备过程中的各个环节都十分重要,任何细微的差异都可能影响到片剂的质量。
实验药物片剂的质量检查PPT课件
在预实验中, 维生素C片可以15分钟内全部崩解, 西地碘含片在20分钟内也可全部崩解, 阿莫西林胶囊可在30分钟内全部崩解
实验药物片剂的质量检查
实验目的
• 掌握药物片剂的质量检查方法; • 熟悉中国药典中收载的三种溶出测定方法
(大杯法、转蓝法和小杯法)及其在仪器 装置,以及测定方法等方面的差异; • 掌握片剂溶出度测定的方法以及药物溶出 度测定仪的调试与使用;
• 掌握实验中影响溶出度测定结果的因素以及实验 设计中针对这些影响因素所采取的措施;
7 设定停机时间,按选择键选择设定“时”或 “分”按“∧”“∨”键增减。取待测样品6片,分 别投入吊篮的6个玻璃管中,(每管1片) 完成后按启动键,按药典要求进行崩解试 验,并判定结果。
• 如需复试则应按规定加上挡板。
• 两套吊篮均可独立工作,停机时蜂鸣器报 警,按“∧”“∨”可计学评价方法, 利用威布尔概率值拟合求算溶出参数的方法和单 因素随机变量的方差分析方法;
• 熟悉溶出度的概念,了解溶出度与口服固体制剂 中药物吸收的关系,以及溶出度的测定在药物评 价中的意义和运用。
实验原理
• 片剂成品的质量评价可以分为化学评价、 物理评价、微生物评价、生物学评价及稳 定性评价。而物理评价包括片剂的质量差 异、崩解时限、溶出度、硬度、脆碎度、 厚度、含水量等指标。
仪器与试剂
• 仪器:电子分析天平、崩解仪。 • 试剂:维生素C片、西地碘含片、阿莫西林
胶囊、穿心莲片、对乙酰氨基酚片等
实验步骤
1 质量差异测定
• 随机抽取药片20片,准确称取总质量,求 得药片平均质量后,再分别准确称取各药 片的质量,按下式计算药片质量差异限度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验八片剂的制备及质量检查
一、实验目的
1.通过片剂制备,掌握湿法制粒压片的工艺过程。
2.掌握单冲压片机的使用方法及片剂质量的检查方法。
3.考察压片力及崩解剂等对片剂的硬度及崩解度的影响。
二、实验原理
片剂是应用最为广泛的药物剂型之一。
片剂的制备方法有制颗粒压片(分为湿法制粒和干法制粒),粉末直接压片和结晶直接压片。
其中,湿法制粒压片最为常见,现将传统湿法制粒压片的生产工艺过程介绍如下:
和过筛等处理,方可投料生产。
为了保证药物和辅料的混合均匀性以及适宜的溶出速度,药物的结晶须粉碎成细粉,一般要求粉末细度在100目以上。
向已混匀的粉料中加入适量的粘合剂或润湿剂、崩解剂,用手工或混合机混合均匀制软材,软材的干湿程度应适宜,除用微机自动控制外,也可凭经验掌握,即以“握之成团,轻压即散”为度。
软材可通过适宜的筛网制成均匀的颗粒。
过筛制得的颗粒一般要求较完整,如果颗粒中含细粉过多,说明粘合剂用量过少,若呈线条状,则说明粘合剂用量过多。
这两种情况制成的颗粒烘干后,往往出现太松或太硬的现象,都不符合压片对颗粒的要求。
制好的湿颗粒应尽快干燥,干燥的温度由物料的性质而定,一般为50~60℃,对湿热稳定者,干燥温度可适当提高。
湿颗粒干燥后,需过筛整粒以便将粘结成块的颗粒散开,同时加入润滑剂和需外加法加入的崩解剂并与颗粒混匀。
整粒用筛的孔径与制粒时所用筛孔相同或略小。
压片前必须对干颗粒及粉末的混合物进行含量测定,然后根据颗粒所含主药的量计算片重。
根据片重选择筛目与冲膜直径,其之间的常用关系可参考下表。
根据药物密度不同,可进行适当调整。
表1 片重、筛目与冲模直径
筛号(目)
片重冲模直径
(mg)湿粒干粒(mm)
50 18 16-20 5-5.5
100 16 14-20 6-6.5
150 16 14-20 7-8
200 14 12-16 8-8.5
300 12 10-16 9-10.5
500 10 10-12 12
制成的片剂需按照中国药典规定的片剂质量标准进行检查。
检查的项目,除片剂的外观应完整、光洁、色泽均匀、硬度适当、含量准确外,必须检查重量差异和崩解时限。
对有些片剂产品,药典还规定检查溶出度和含量均匀度,并规定凡检查溶出度的片剂,不再检查崩解时限,凡检查含量均匀度的片剂,不再检查重量差异。
另外,在片剂的制备过程中,所施加的压片力不同,所用的润滑剂、崩解剂等的种类不同,都会对片剂的硬度或崩解时限产生影响。
三、实验内容
(一)阿司匹林片的制备
【处方】
阿司匹林30g
淀粉3g
枸椽酸适量
10%淀粉浆适量
滑石粉适量共制100片
【操作】
1.10%淀粉浆的制备:将0.2g枸椽酸(或酒石酸)溶于约20ml蒸馏水中,再加入淀粉约2g分散均匀,加热糊化,制成10%淀粉浆。
2.制颗粒:取处方量阿司匹林与淀粉混合均匀,加适量10%淀粉浆制软材, 过16目筛制粒,将湿颗粒于40-60℃干燥,过16目筛整粒并与滑石粉混匀(5%)。
3.在不同压力下压片:将上述制好的颗粒在单冲打片机中压片。
【注】
1.乙酰水杨酸在润湿状态下遇铁器易变为淡红色。
因此,宜尽量避免铁器,如过筛时宜用尼龙筛网,并迅速干燥。
在干燥时温度不宜过高,以避免药物加速水解。
2.在实验室中配制淀粉浆:可用直火加热,也可以水浴加热。
若用直火时,需不停搅拌,防止焦化而使片面产生黑点。
3.加浆的温度,以温浆为宜,温度太高不利药物稳定,太低不宜分散均匀。
(二)质量检查与评定
本实验检查重量差异、硬度和崩解时限。
1.重量差异检查
取药片20片,精密称定总重量,求得平均片重后,再分别精密称定各片的重量。
每片重量与平均片重相比较(凡无含量测定的片剂,每片重量应与标示片重比较)超出重量差异限度(见表2)的药片不得多于2片,并不得有1片超出限度1倍。
2.硬度检查
采用破碎强度法,采用片剂四用测定仪进行测定。
方法如下:将药片径向固定在两横杆之间,其中的活动柱杆借助弹簧沿水平方向对片剂径向加压,当片剂破碎时,活动柱杆的弹簧停止加压,仪器刻度盘所指示的压力即为片子的硬度。
测定6片,取平均值。
结果列于表3。
3.崩解时限检查
应用片剂四用测定仪进行测定。
采用吊篮法,方法如下:取药片6片,分别置于吊篮的玻璃管中,每管各加一片,开动仪器使吊篮浸入37±1.0℃的水中,按一定的频率(30-32次/min)和幅度(55±2mm)往复运动。
从片剂置于玻璃管开始计时,至片剂破碎并全部固体粒子都通过玻璃管底部的筛网(Φ2mm)为止,该时间即为该片剂的崩解时间,应符合规定崩解时限(一般压制片为15min)。
如有1片不符合要求,应另取6片复试,均应符合规定。
结果列于表3。
表3 片剂硬度和崩解性能的检查
硬度(kg) 崩解时间(min)
1 2 3 4 5 6 平均 1 2 3 4 5 6 平均
结论
五、思考题
1.分析并讨论实验结果,总结出影响片剂崩解的因素及原理。
2.根据实验结果,总结出主药性质与辅料选择的关系。
实验六胶囊剂的制备
一、实验目的
1.掌握硬胶囊剂的制备工艺流程及手工填充胶囊的方法。
2.了解硬胶囊剂的质量检查方法。
二、实验原理
硬胶囊剂是将药物粉末直接填充于空胶囊中,或是将一定量的药物加适宜辅料制成均匀的粉末或颗粒,填充于空胶囊中,或取一种或多种速释小丸或缓释、控释小丸,单独填充或混合后填充,必要时加入适当空白小丸作填充剂填充于空胶囊中制成缓控释胶囊。
硬胶囊剂制备的关键在于药物的填充,以保障药物剂量均匀,装量差异符合要求。
药物的流动性是影响填充均匀性的主要因素,对于流动性差的药物,需加入适宜辅料或制成颗粒以增加流动性,减少分层。
填充方法有手工填充和机械灌装两种。
手工填充的方法:将药物粉末置于白纸或洁净的玻璃板上,用药匙铺平并压紧,厚度约为胶囊体高度的1/4或1/3;手持胶囊体,口垂直向下插入药物粉末,使药粉压入胶囊内,同法操作数次,至胶囊被填满,使其达到规定的重量后,套上胶囊帽。
填充过程中所施压力应均匀,还应随时称重,以使每粒胶囊的装量准确。
为使填充好的胶囊剂外观美观、光亮,可用喷有少许液状石蜡的洁净纱布轻轻滚搓,擦去胶囊剂外面粘附的药粉。
本次实验采用胶囊装药器手工填充(实验内容中具体介绍)。
三、实验内容
【制法】
选择适宜的药物粉末(将散剂制备实验中的阿司匹林散混匀)及适当规格的空胶囊,用胶囊装药器进行手工填充硬胶囊。
胶囊装药器手工填充硬胶囊:采用有机玻璃制成的胶囊板填充。
板分上下两层,上层有数百孔洞。
先将囊帽、囊体分开,囊体插入胶囊板孔洞中,调节上下层距离,使胶囊口与胶囊板表面相平。
将药物粉末铺于板面,轻轻振动胶囊板,使药物粉末填充均匀并填满,多余的粉末用刮板刮平并清除,顶起囊身,套合囊帽,取出胶囊,即得。
【质量检查】
①外观:表面光滑、整洁、不得粘连、变形和破裂,无异臭。
检查方法:取供试品20 粒,分别精密称定重量后,倾出内容物(不能损失囊壳),硬胶囊壳用小刷或其它适宜的用具(如棉签等)拭净,再分别精密称定囊壳重量,求得每粒内容物装量与平均装量。
每粒装量与平均装量相比较,超出装量差异限度的胶囊不得多于 2 粒,并不得有 1 粒超出装量差异
限度的 1 倍。
四、思考题
1.胶囊剂与片剂相比,有何特点?
2.胶囊剂有哪几类?两者有何不同?分别适用于哪些药物?
实验九栓剂的制备(开放性设计实验)
一、实验目的
1. 通过开放性设计实验使学生了解科学研究的基本程序和方法
2. 学生自行设计实验,提高自主学习的能力,激发学生的学习兴趣。
3. 掌握置换价的测定方法及栓剂处方的设计方法。
4. 通过实验掌握热熔法制备栓剂的工艺过程。
二、实验内容
(一)课前预习
1. 要求学生在课前要做好实验预习,掌握栓剂制备的原理,置换价测定的方法及2005年版《中国药典》附录中规定的栓剂质量检查项目及方法。
2. 认真完成实验预习报告,内容如下:
(1)实验原理
要求写出栓剂基质的种类、常用的基质、栓剂制备的常用方法以及如何测定药物的置换价。
(2)处方设计
以阿司匹林为主药,半合成脂肪酸酯为基质,采用热熔法,按2005年版《中国药典》规定的规格自行设计一个制备20枚肛门栓的处方。
(注意:在处方设计前应首先测定阿司匹林对半合成脂肪酸酯的置换价)
①工艺流程:
以框图的形式表示出栓剂置换价测定及栓剂制备的工艺流程。
②操作方法:
写出本实验的具体操作步骤。
③质量检查:
查阅2005年版《中国药典》,写出栓剂质量检查的项目及方法。
(二)课堂实验
1. 实验带教教师首先对学生的实验预习报告进行检查,合格后方可进行实验。
2. 学生按照自行设计的实验方案进行实验。
3. 对所制备的栓剂进行性状、鉴别、重量差异和融变时限的检查和质量评价并认真详实地做好实验记录。
三、思考题
1.热熔法制备阿司匹林栓应注意哪些问题?
2.测定药物的置换价在栓剂制备中有何意义?什么情况下可考虑不用测定置换价?
3. 此次开放性实验你有何体会?。
