2015-2019年安徽省中考化学试题分类汇编计算题
2019年安徽省市中考化学试卷(Word版-含答案)

2019年安徽省初中毕业学业考试化学注意事项:1.本卷共三大题16小题,满分60分。
化学与物理的考试时间共120分钟。
2.试卷包括“试题卷”和“答题卷”两部分,“试题卷”共4页,“答题卷”共2页。
3.请务必在“答题卷”上答题,在“试题卷”上答题是无效的。
4.考试结束后,请将“试题卷”和“答题卷”一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Fe-56一、本大题包括10小题,每小题2分,共20分。
每小题的4个选项中只有1个符合题意。
1.下列生产、生活中的变化,属于化学变化的是2.2019年世界环境日的主题是“促进可持续的生活方式”,核心是倡导良好的生活习惯。
小明的下列做法符合这一主题的是A.去超市购物,用布袋购物B.上购买大量闲置物品C.节假日随父母出游,经常开私家车D.外出就餐,超量点菜3.学校食堂提供了下列5种食物:小亮为自己安排的午餐食谱中,较合理的是A.①②③B.①③⑤C.①④⑤D.③④⑤4.重铬酸钾(K2Cr2O7)可用于测定酒驾中的酒精(C2H5OH)含量。
下列说法正确的是A.K2Cr2O7中铬元素的化合价为+7 B.K2Cr2O7属于氧化物C.C2H5OH的相对分子质量为46 D.C2H5OH中C、H、O的原子个数比为2:5:15.钒被誉为“合金的维生素”,钒元素的相关信息如下。
下列有关钒的说法正确的是A.属于非金属元素B.原子序数为23C.原子核外电子数为28D.相对原子质量为50.94g6.“超临界水”因具有许多优良特质而被科学家追捧,它是指当气压和温度达到一定值时,水的液态和气态完全交融在一起的流体。
下面有关“超临界水”的说法正确的是A.它是混合物B.它是一种不同于水的物质C.它的分子之间有间隔D.它的一个分子由4个氢原子和2个氧原子构成7.下列实验操作符合安全要求的是A.验证氢气的可燃性B.闻气体气味C.移走蒸发皿D.稀释浓硫酸的是8.下图为汽车尾气净化装置中发生反应的微观示意图,有关叙述错误..A.该反应是置换反应B.图中单质的化学式为N2C.反应后分子总数减少D.该装置可净化汽车尾气9.研究和学习化学,有许多方法。
2015-2019年安徽省中考化学试题分类汇编:科学探究题(含附加分)(解析版)

2015-2019年安徽省中考化学试题分类汇编第15题——科学探究题(含附加分)【2019年第15题】(7分)某兴趣小组为探究金属活动性强弱,分别做了镁、铝、铜与稀盐酸反应的实验。
(1)比较金属活动性强弱:铝比铜______(填“强”或“弱”)。
写出镁与稀盐酸反应的化学方程式:_____________________________________(2)小芳同学做镁与稀盐酸反应的实验时,发现试管中出现灰白色沉淀,该小组同学对灰白色沉淀的成分进行如下探究:[提出假设]假设一:含有氯化镁假设二:含有镁粉假设三:含有氢氧化镁……[查阅资料]①氯化镁易溶于水:②在一定条件下镁可与冷水缓慢反应。
[[得出结论]由实验1可知,假设___不成立;由实验2可知,沉淀中不含___。
假设三__________(填“成立”或“可能成立”或“不成立”)。
[实验反思]实验后同学们请教老师得知,灰白色沉淀的主要成分是碱式氯化镁,碱式氯化镁受热易分解产生氯化氢气体。
于是小芳再取少量灰白色沉淀于试管中加热,并将蘸有紫色石蕊溶液的滤纸条悬于试管口,预期的实验现象是__________________________注意:若答对第(3)小题奖励4分.化学试卷总分不超过60分。
(3)为探究镁与稀盐酸反应生成碱式氯化镁的条件.该小组同学进行了如下实验:在小烧杯中加入一定量的盐酸和去除氧化膜的镁带,观察实验现象,并测量溶液pH的变化。
结果见下根据表中信息回答下列问题:①请描述溶液pH变化的规律并解释原因:____________________②请对生成碱式氯化镁的条件提出猜想,并设计实验证明猜想:____________________ 【解析】(1)根据金属活动性表,铝活动性比铜强,镁与稀盐酸反应的化学方程式:Mg+2HCl=MgCl2+H2↑,故填:强; Mg+2HCl=MgCl2+H2↑(2)根据实验现象分析,由实验1可知,假设一不成立;由实验2可知,沉淀中不含镁粉假设三可能成立。
2019年安徽省中考化学试卷(解析版)
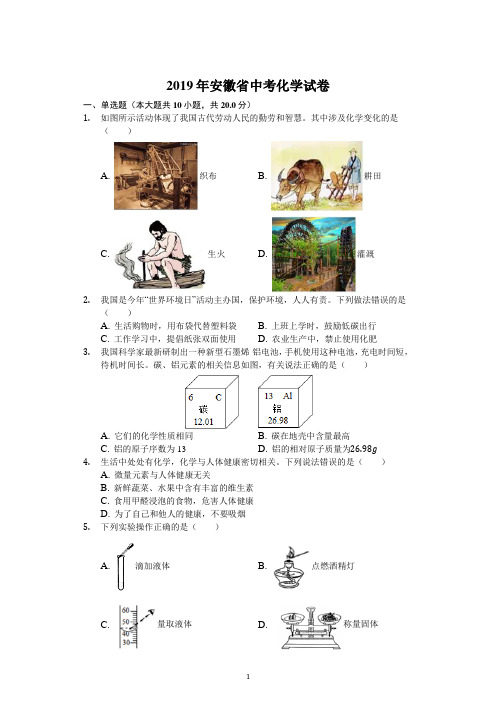
2019年安徽省中考化学试卷一、单选题(本大题共10小题,共20.0分)1.如图所示活动体现了我国古代劳动人民的勤劳和智慧。
其中涉及化学变化的是()A. 织布B. 耕田C. 生火D. 灌溉2.我国是今年“世界环境日”活动主办国,保护环境,人人有责。
下列做法错误的是()A. 生活购物时,用布袋代替塑料袋B. 上班上学时,鼓励低碳出行C. 工作学习中,提倡纸张双面使用D. 农业生产中,禁止使用化肥3.我国科学家最新研制出一种新型石墨烯-铝电池,手机使用这种电池,充电时间短,待机时间长。
碳、铝元素的相关信息如图,有关说法正确的是()A. 它们的化学性质相同B. 碳在地壳中含量最高C. 铝的原子序数为13D. 铝的相对原子质量为4.生活中处处有化学,化学与人体健康密切相关。
下列说法错误的是()A. 微量元素与人体健康无关B. 新鲜蔬菜、水果中含有丰富的维生素C. 食用甲醛浸泡的食物,危害人体健康D. 为了自己和他人的健康,不要吸烟5.下列实验操作正确的是()A. 滴加液体B. 点燃酒精灯C. 量取液体D. 称量固体6.我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式为H25N34O3Cl),该物质是超高能材料,在航空航天上可做推进剂。
下列有关该物质的说法正确是()A. 属于有机物B. 由四种非金属元素组成C. 中原子总数为62D. 氢、氮、氧、氯的原子个数比为1:7:8:177.如图是一种处理汽车尾气的反应微观示意图,有关说法正确的是()A. 反应前后分子总数不变B. 反应前后原子种类发生变化C. 反应前后均为纯净物D. 该反应可以减少二氧化氮的排放8.某同学用一系列实验探究物质的燃烧,得到下列结论,其中不正确的是()A. 镁条在氧气和二氧化碳中均能燃烧,说明二氧化碳分子中有氧气B. 玻璃棒不能燃烧而火柴棒可以燃烧,说明燃烧与物质本身性质有关C. 蜡烛在氧气中比在空气中燃烧更旺,说明燃烧与氧气的浓度有关D. 燃烧是一种化学反应,需考虑两方面因素:反应物内因和反应条件外因9.学习化学,提高学科核心素养,学会从化学的角度分析问题。
完整版2019年安徽省中考化学试题答案解析版

2019年安徽省中考化学试题、答案(解析版)本试卷满分60分,考试时间50分钟H—1可能用到的相对原子质量:35.5—ClO—16C—12N—1455—MnCa—40K—39第Ⅰ卷(选择题共20分)一、选择题(本题共10小题,每小题2分,共20分。
每小题只有一个选项符合题意)1.如图所示活动体现了我国古代劳动人民的勤劳和智慧。
其中涉及化学变化的是( )...CDB灌溉耕田生火A织布.2我国是今年“世界环境日”活动主办国,保护环境,人人有责。
下列做法错误的是 . )(..B A生活购物时,用布袋代替塑料袋上班上学时,鼓励低碳出行..DC 农业生产中,禁止使用化肥工作学习中,提倡纸张双面使用-3铝电池,手机使用这种电池,充电时间短,待机时我国科学家最新研制出一种新型石墨烯. 间长。
碳、铝元素的相关信息如图,有关说法正确的是().BA .它们的化学性质相同碳在地壳中含量最高..26.98 g13 CD铝的相对原子质量为铝的原子序数为4 .()生活中处处有化学,化学与人体健康密切相关。
下列说法错误的是AB 新鲜蔬菜、水果中含有丰富的维生素.微量元素与人体健康无关 .CD .食用甲醛浸泡的食物,危害人体健康.为了自己和他人的健康,不要吸烟)(5.下列实验操作正确的是.. CA量取液体滴加液体称量固体D..B点燃酒精灯我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式为.6ClNOH,该物质是超)33425高能材料,在航空航天上可做推进剂。
下列有关该物质的说法正确是()A.属于有机物.由四种非金属元素组成lHNO62中原子总数为32534.17:871::氢、氮、氧、氯的原子个数比为D7.(如图是一种处理汽车尾气的反应微观示意图,有关说法正确的是). A B反应前后原子种类发生变化.反应前后分子总数不变DC该反应可以减少二氧化氮的排放..反应前后均为纯净物8某同学用一系列实验探究物质的燃烧,得到下列结论,其中不正确的是.(). A镁条在氧气和二氧化碳中均能燃烧,说明二氧化碳分子中有氧气B玻璃棒不能燃烧而火柴棒可以燃烧,说明燃烧与物质本身性质有关.. C蜡烛在氧气中比在空气中燃烧更旺,说明燃烧与氧气的浓度有关. D)(外因燃烧是一种化学反应,需考虑两方面因素:反应物(内因)和反应条件9) .学习化学,提高学科核心素养,学会从化学的角度分析问题。
安徽省2019年中考化学真题(含答案)

安徽省2019年初中化学学业水平测试试卷姓名:__________班级:__________考号:__________题号一二三四五六总分评分一、单选题1.下图所示活动体现了我国古代劳动人民的勤劳和智慧。
其中涉及化学变化的是()A.织布B.耕田C.生火D.灌溉2.我国是今年“世界环境日”活动主办国,保护环境,人人有责。
下列做法错误的是()A.生活购物时,用布袋代替塑料袋B.上班上学时,鼓励低碳出行C.工作学习中,提倡纸张双面使用D.农业生产中,禁止使用化肥3.我国科学家最新研制出一种新型石墨烯-铝电池,手机使用这种电池,充电时间短,待机时间长。
碳、铝元素的相关信息如图,有关说法正确的是()A.它们的化学性质相同B.碳在地壳中含量最高C.铝的原子序数为13D.铝的相对原子质量为26.98g4.生活中处处有化学,化学与人体健康密切相关。
下列说法错误的是()A.微量元素与人体健康无关B.新鲜蔬菜、水果中含有丰富的维生素C.食用甲醛浸泡的食物,危害人体健康D.为了自己和他人的健康,不要吸烟5.下列实验操作正确的是()A.滴加液体B.点燃酒精灯C.量取液体D.称量固体6.我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式为25343C),该物质是超高能材料,在航空航天上可做推进剂.下列有关该物质的说法正确的是()A.属于有机物B.由四种非金属元素组成C.25343C中原子总数为62D.氢、氮、氧、氯的原子个数比为1:7:8:17 7.下图是一种处理汽车尾气的反应微观示意图,有关说正确的是()A.反应前后分子总数不变B.反应后原子种类发生变化C.反应前后为纯净物D.该反应可以减少二氧化氮的排放8.某同学用一系列实验探究物质的燃烧,得到下列结论,其中错误的是()A.镁条在氧气和二氧化碳中均能燃烧,说明二氧化碳分子中有氧气B.玻璃棒不能燃烧而火柴棒可以燃烧,说明燃烧与物质本身性质有关C.蜡烛在氧气中比在空气中燃烧更旺,说明燃烧与氧气的浓度有关D.燃烧是一种化学反应,需考虑两方面因素:反应物(内因)和反应条件(外因)9.学习化学,提高学科核心素养,学会从化学的角度分析问题下列说法确的是()A.木炭具有疏松多孔的结构,因此具有吸附性B.盐酸和氢氧化钠溶液混合,无现象,没有发生反应C.随着铁制品的不断锈蚀,自然界中铁元素的含量不断减少D.碳酸氢铵有强烈的味,是氮肥;尿素没有氨味,不是氮肥10.压强为101kPa下,硝酸钾和氨气在不同温度下的溶解度如下表.下列说法正确的是()温度/℃10203060溶解度/g B320.931.645.8110NH3705644.520A.两种物质的溶解度均随温度升高而增大B.20℃时B3饱和溶液中溶质的质量分数为31.6%C.60℃的B3饱和溶液降温至30℃,有晶体析出D.NH3的溶解度与压强大小无关二、填空题11.能源与环境是社会关注的焦点。
2015-2019年安徽省中考化学考试试题分类汇编——选择题之化学基本思维(word版,含解析)
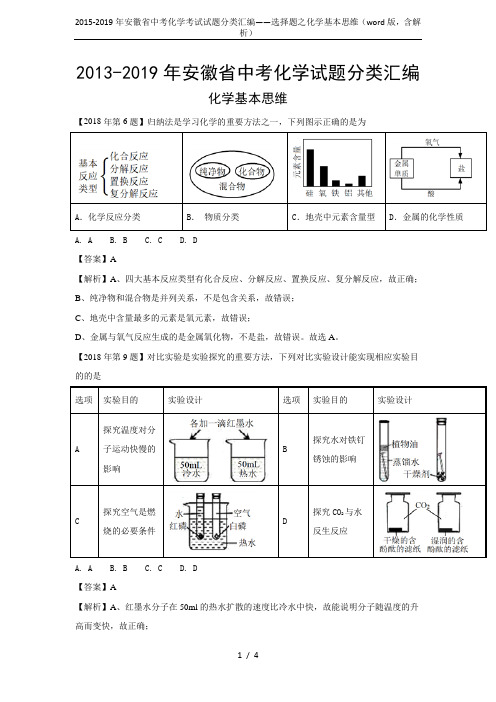
2013-2019年安徽省中考化学试题分类汇编化学基本思维【2018年第6题】归纳法是学习化学的重要方法之一,下列图示正确的是为A.化学反应分类B.物质分类C.地壳中元素含量型D.金属的化学性质A. A B. B C. C D. D【答案】A【解析】A、四大基本反应类型有化合反应、分解反应、置换反应、复分解反应,故正确;B、纯净物和混合物是并列关系,不是包含关系,故错误;C、地壳中含量最多的元素是氧元素,故错误;D、金属与氧气反应生成的是金属氧化物,不是盐,故错误。
故选A。
【2018年第9题】对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是选项实验目的实验设计选项实验目的实验设计A探究温度对分子运动快慢的影响B探究水对铁钉锈蚀的影响C探究空气是燃烧的必要条件D探究CO2与水反生反应A. AB. BC. CD. D【答案】A【解析】A、红墨水分子在50ml的热水扩散的速度比冷水中快,故能说明分子随温度的升高而变快,故正确;B、该实验中缺少铁与氧气和水同时接触的对比实验,故错误;C、该实验中缺少不与氧气接触的白磷的对比实验,故错误;D、酚酞在酸性和中性环境中都不变色,故错误。
故选A。
【2017年第6题】建立模型是学习化学的重要方法,下列有关模型正确的是()A.原子结构模型B.物质分类模型C.燃烧条件模型D.空气组成模型【考点】13:科学探究的基本方法.【分析】A、根据原子核由质子和中子构成分析解答;B、根据纯净物包括化合物和单质分析解答;C、根据燃烧需要可燃物温度达到着火点并与空气接触分析解答;D、根据按体积计算空气由78%N2和21%O2还有1%其他成分组成分析解答;【解答】解:A、原子核由质子和中子构成,模型中质子不在原子核内,故错误;B、纯净物包括化合物和单质,模型中化合物没包括在纯净物中,故错误;C、燃烧需要可燃物温度达到着火点并与空气接触,模型中可燃物专指固体是片面的,对气体未予具体说明,故错误;D、按体积计算空气由78%N2和21%O2还有1%其他成分组成,模型描述与事实相符,故正确.故选D【2017年第9题】下列实验事实不能作为相应观点的证据的是()选项实验事实观点A.A B.B C.C D.D【考点】B9:利用分子与原子的性质分析和解决问题.【分析】A、根据铁丝燃烧的实质及质量守恒定律解答;B、根据化学反应的实质解答;C、根据分子的性质分析解答;D、根据物质是由分子组成的,分子体积小,组成物体的分子间存在间隙解答.【解答】解:A、铁丝燃烧属于化学变化,所以遵守质量守恒定律,铁丝燃烧是铁丝与氧气反应生成四氧化三铁,根据质量守恒定律,反应前铁丝与氧气的质量和,等于生成的四氧化三铁的质量,因此铁丝在氧气中燃烧后质量增加,故正确;B、水电解可得到氢气和氧气,说明水分子是可分的,分解为氢原子和氧原子,原子不能再分,故正确;C、少量白糖加入水中,不久“消失”,说明微粒是不断运动的,故正确;D、5mL苯和5mL冰醋酸混合后体积小于10mL,不是大于10mL,说明微粒间有间隔,故错误.答案:D【2016年第3题】下列选项中的物质所属类别错误的是()A.A B.B C.C D.D【考点】纯净物和混合物的判别;单质和化合物的判别;有机物与无机物的区别;生命活动与六大营养素.【专题】物质的分类.【分析】混合物是由多种物质组成;单质是由一种元素组成的纯净物,有机物是含有碳元素的化合物.【解答】解:A、干冰中只含有二氧化碳一种物质物质,属于化合物,故A对;B、氮气、水银、金刚石都是含有一种元素的物质,都属于单质,故B错;C、糖类、油脂、蛋白质都属于营养素,故C错;D、甲烷、乙醇、塑料都是含有碳元素的化合物,都属于有机物,故D错.故选A.【点评】应抓住概念的要点来判断物质的类别,了解常见物质的组成.【2015年第9题】研究和学习化学,有许多方法。
(完整版)安徽化学中考真题及答案.doc

2015年安徽省初中毕业学业考试化 学(试题卷)注意事项:1.化学试卷共三大题,满分60 分。
化学与物理的考试时间共120 分钟。
2.试题包括 “试题卷 ”和 “答题卷 ”两部分, “试题卷 ”共 4 页, “答题卷 ”共 2 页。
3.请务必在 “答题卷 ”上答题,在 “试题卷 ”上答题是无效的。
4.考试结束后,请将 “试题卷 ”和“答题卷 ”一并交回。
可能用到的相对原子质量:H — 1 C — 12O —16Fe — 56一、本大题包括 10 小题,每小题 2 分,共 20 分。
每小题的 4 个选项中只有 1 个符合题意。
1.下列生产、生活中的变化,属于化学变化的是A .冰雪融化2. 2015 年世界环境日的主题是 B .水的净化“促进可持续的生活方式C .燃料燃烧D .风力发电”,核心是倡导良好的消费习惯。
小明的下列做法符合这一主题的是A .去超市购物,用布质购物装 C .节假日随父母出游经常开私家车 3.学校食堂提供了下列5 种食物:B .网上购买大量闲置物品D .外出就餐超量点菜①青菜②苹果③米饭④猪肉 ⑤鱼小亮为自己安排的午餐食谱中,较合理的是A .①②③B . ①③⑤C .①④⑤D . ③④⑤4.重铬酸钾( KCr O )可用于测定酒驾中的酒精( C HOH )含量。
下列说法正确的是2272 5A . K Cr O中铬元素的化合价为+7B . K Cr O 7 属于氧化物22 722C .C 2H 5OH 的相对分子质量为 46D .C 2H 5OH 中 C 、H 、O 的原子个数比为 2∶ 5∶ 15.钒被誉为 “合金的维生素 ”,钒元素的部分信息如下图。
下列有关钒的说法正确的是A .属于非金属元素23 VB .原子序数为 23钒C .原子核外电子数为 2850.94D .相对原子质量为 50.94g6.“超临界水”因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的液体。
2019年化学中考真题汇编:专题(十五)计算题

2019年化学中考真题汇编:专题(十五)计算题1、实验室模拟高温煅烧石灰石的方法制取二氧化碳,取35g石灰石样品(假设杂质受热不分解且不与酸反应),煅烧一段时间恢复到室温,测得生成1lg二氧化碳。
向剩余固体中逐滴加入某盐酸至不再反应为止,又生成 2.2g二氧化碳,加入盐酸的质量与生成的氯化钙质量关系如图:(1)石灰石样品的质量分数是______(结果保留一位小数,下同);(2)a点溶液的pH______7(填“<”“>”或“=”);(3)求所加盐酸的溶质质量分数(写出计算过程)。
2、某纯碱样品中含有少量氯化钠杂质。
称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。
反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。
试回答:CO的质量______。
(1)生成2(2)22.8g样品中氯化钠的质量为______。
(3)计算所得溶液中溶质的质量分数。
(写岀解题过程,计算结果精确到0.1%)3、黄铜是铜和锌的合金。
某化学兴趣小组的同学欲测定实验室中某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。
称量10g粉末状黄铜样品放入烧杯中,量取45mL稀硫酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:第一次第二次第三次加入稀硫酸的体积(mL) 15 15 15生成氢气的质量(g)m 0.04 0.02 试求:(1)m的数值。
(2)此黄铜样品中铜的质量分数是少?(写出计算过程)Cu OH CO,受热可分解生4、碱式碳酸铜是孔雀石的主要成分,俗称铜绿,化学式为232成CuO、水和二氧化碳。
(1)碱式碳酸铜的相对分子质量是。
(2)铜绿分解生成22g的二氧化碳的同时,生成CuO的质量是多少?5、建造“南昌舰”的特种钢材需要用富铁矿石(含铁量高于50%)来冶炼。
研学实践小组为Fe O)中的含铁量,进行实验;取20g赤铁矿石样品,测出某地赤铁矿石(主要成分是23逐渐加入稀盐酸,充分反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2015-2019年安徽省中考化学试题分类汇编
第16题——计算题
【2019年第16题】(6分)侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下: NaCl+C02+NH3+H20 = NaHC03+NH4Cl,请计算:
(1)氯化铵中氮元素的质量分数。
(2)生产8.4t碳酸氢钠,理论上需要氯化钠的质量。
【解析】
(1)考查根据化学式求元素质量分数:14/53.5×100%=26.2%
(2)考查根据生成物质量求反应物质量
解:设生产8.4t碳酸氢钠,理论上需要氯化钠的质量为x
NaCl+C02+NH3+H20 = NaHC03+NH4Cl
58.5 84
x 8.4t
58.5 84
x 8.4t
x=5.85t
答:设生产8.4t碳酸氢钠,理论上需要氯化钠的质量为5.85t
故答案:
(1)氯化铵中氮元素的质量分数:14/53.5×100%=26.2%
(2)解:设生产8.4t碳酸氢钠,理论上需要氯化钠的质量为x
NaCl+C02+NH3+H20 = NaHC03+NH4Cl
58.5 84
x 8.4t
58.5 84
x 8.4t
x=5.85t
答:设生产8.4t碳酸氢钠,理论上需要氯化钠的质量为5.85t
【2018年第16题】尿素[CO(NH2)2]是一种常见的氮肥,工业上制备反应如下:
CO2+2NH3CO(NH2)2+H2O,请计算:
(1)尿素中氮元素的质量分数_________________。
(2)生产6t尿酸理论上需要氨气的质量是多少________________?
【答案】(1). 46.7%(2). 3.4t。
【解析】(1)尿素中氮元素的质量分数为=46.7%
(2)设生产6t尿酸理论上需要氨气的质量为x
CO2+2NH3CO(NH2)2+H2O
34 60
x 6t
=,解得x=3.4t
答:尿素中氮元素的质量分数为46.7%,生产6t尿酸理论上需要氨气的质量为3.4t。
【2017年第16题】实验室加热氯酸钾(KClO3)和二氧化锰的混合物28.0g制取氧气,完全反应后剩余固体质量为18.4g,请计算:
(1)生成氧气的质量.
(2)原混合物中氯酸钾的质量.
【考点】G6:根据化学反应方程式的计算.
【分析】根据质量守恒定律可知,过程中质量的减少是因为生成了氧气,所以可以求算氧气的质量,根据氧气的质量和对应的化学方程式求算氯酸钾的质量.【解答】解:根据质量守恒定律可得,生成的氧气的质量为28.0g﹣18.4g=9.6g 设氯酸钾的质量为x
2KClO32KCl+3O2↑
245 96
x 9.6g
=
x=24.5g
答:
(1)生成氧气的质量为9.6g.
(2)原混合物中氯酸钾的质量为24.5g.
【2016年第16题】早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱.现有含1.6kg硫酸铜的工业废液,加入铁粉回收铜,请计算:
(1)硫酸铜中铜元素的质量分数.
(2)理论上与硫酸铜反应消耗铁粉的质量.
【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算.
【分析】(1)纯净物中某元素的质量分数=×100% (2)根据硫酸铜的质量,利用反应的化学方程式,列出比例式,就可计算出消耗铁粉的质量即可.
【解答】解:
(1)硫酸铜中铜元素的质量分数=100%=40%;
(2)设理论上与硫酸铜反应消耗铁粉的质量为x
Fe+CuSO4═Cu+FeSO4
56 160
x 1.6Kg
x=0.56Kg
答案:
(1)硫酸铜中铜元素的质量分数为40%;
(2)理论上与硫酸铜反应消耗铁粉的质量为0.56Kg.
【点评】本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
【2015年第16题】(6分)非物质文化遗产“芜湖铁画”(镀金)含有金、铁(同其他成分忽略不计)。
某同学取一定质量的铁画边角料,加入足量稀盐酸,充分反应后,放出0.3gH2,剩余固体质量为0.1g。
(1)求样品中铁的质量。
(2)求样品中金的质量分数。
【答案】(1)设铁画边角料中所含铁的质量为x
Fe+2HCl==FeCl2+H2↑
56 2
x0.3g
56 x=
2 0.3g
解得x=8.4g
(2)金的质量分数=0.1g
8.4g+0.1g×100%≈1.2%
答:铁画中铁的质量为8.4g;金的质量分数约为1.2%。
【解析】根据题意,Fe和HCl反应生成FeCl2和H2气体,由生0.3gH2,结合溶质质量=溶液质量×溶质的质量分数、反应的化学方程式进行分析解答即可。
【点评】本题难度不大,掌握根据化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性。
