药品检验原始记录书写范例
药材检验原始记录样本

XXXXX药业(饮片)有限公司原药材检验报告单XXXXX药业(饮片)有限公司原药材检验记录【性状】结果:【鉴别】(1)显微鉴别横截面:结果:粉末:结果:(2)薄层鉴别供试品溶液的制备:取粉末1g,加乙醇15ml,加热回流1小时,放冷,滤过,滤液蒸干,残渣加乙醇5ml使溶解。
对照药材、对照品溶液配制:取菊花对照药材1g,同法制成对照药材溶液。
再取绿原酸对照品,加乙醇制成每1ml含O.5mg的溶液。
温度:(℃)相对湿度:(%)展开剂:三氯甲烷-丙酮-甲醇-5%浓氨试液(6:1:1:0.1)薄层板:硅胶G显色剂:稀碘化铋钾试液灯光:白光、紫外光灯(365nm)展距:(cm)供试品色谱中,在与对照药材色谱相对应的位置上,显相同颜色的荧光斑点。
S1为对照药材(对照品为中检所提供编号为)S2为对照品(对照品为中检所提供编号为) T为样品结果:【检查】杂质不得过 XX % (附录IX A)杂质称重: g杂质计算结果为: % (标准规定不得过 XX %)结果:膨胀度应不低于4.0(附录IX O)温度:(℃)相对湿度:(%)电子天平型号:CP214 溶剂:水样品编号 1# 2# 3#干燥品称重: g g g第一次样品膨胀后体积: ml ml ml第二次样品膨胀后体积: ml ml ml(两次差异不超过0.1ml)膨胀度计算结果为:(标准规定不低于4.0)结果:水分不得过12.0% (附录Ⅸ H 第一法)。
温度:(℃)相对湿度:(%)烘箱型号:DHG-91012SA型电子天平型号:CP214样品编号 1# 2#第一次称量瓶干燥(105℃ 3h) (g)(g)第二次称量瓶恒重(105℃ 1h) (g)(g)样品称重(g)(g)第一次称量瓶+样品干燥(105℃ 5h) (g)(g)第二次称量瓶+样品恒重(105℃ 1h) (g)(g)水分计算结果为:(%)(标准规定不得过12.0%)结果:总灰分不得过4.0%(附录Ⅸ K)温度:(℃)相对湿度:(%)马福炉型号:SX2.5-10 电子天平型号:CP214样品编号 1# 2#第一次坩锅称重(600℃ 3h) (g)(g)第二次坩锅恒重(600℃ 0.5h) (g)(g)样品称重(g)(g)第一次坩锅+残渣称重(600℃ 3h) (g)(g)第二次坩锅+残渣恒重(600℃ 0.5h) (g)(g)总灰分计算结果为:(%)(标准规定不得过4.0%)结果:酸不溶性灰分不得过3.0%(附录Ⅸ K)。
产品检验原始记录

产品检验原始记录日期:XXXX年XX月XX日检验员:XXX一、产品基本信息产品名称:XXXXX生产日期:XXXX年XX月XX日生产批次:XXXXX生产线号:XXXXX包装规格:XXXXX二、检验项目和要求序号检验项目检验要求1外观检查外包装应完好无损,内包装应清洁无异味;产品表面应无明显划痕、锈蚀等瑕疵。
2规格尺寸产品尺寸应符合标准规定。
3功能性能产品应具备正常的功能性能,能够满足使用要求。
4安全性能产品应符合相关的安全标准,无伤害人体的物质和设计缺陷。
三、检验步骤和结果1.外观检查-检查外包装:外包装完好无损,无破损,符合要求。
-检查内包装:内包装清洁无异味,符合要求。
-检查产品表面:产品表面无明显划痕、锈蚀等瑕疵,符合要求。
2.规格尺寸-使用测量工具对产品进行测量。
-比较测量结果与标准规定,确认产品尺寸是否符合要求。
3.功能性能-连接电源,进行基本功能测试。
-检查产品是否能够正常工作,是否满足预期的功能要求。
4.安全性能-检查产品是否符合相关的安全标准,如防火性能、电气安全等。
-检查产品是否存在可能伤害人体的物质和设计缺陷。
四、检验结论根据对产品的检验结果进行综合评估1.外观检查:合格2.规格尺寸:合格3.功能性能:合格4.安全性能:合格五、总结与建议经过本次产品检验,产品符合相关的质量标准和要求,具备正常的外观、规格、功能和安全性能。
建议在生产过程中继续保持良好的品质控制,确保产品的稳定性和一致性。
六、备注七、检验员签名:。
实验药物研发原始记录表

实验药物研发原始记录表
日期:XXXX年XX月XX日
实验员:XXX
实验项目名称:XXX药物研发实验
实验目标:通过合成和筛选,发现具有潜在治疗作用的全新药物分子。
实验步骤:
1. 按照标准操作程序,将原料化合物与溶剂混合,加热至适当温度。
2. 在设定时间间隔内,通过高效液相色谱仪监测反应进程。
3. 反应完成后,将产物进行分离纯化,并对其进行分析。
4. 使用计算机模拟方法,预测新化合物的生物活性。
5. 通过细胞试验,对新化合物进行初步活性筛选。
实验结果:
1. 成功合成了目标化合物,纯度达到95%。
2. 通过高效液相色谱分析,反应转化率达到80%。
3. 初步计算机模拟显示,新化合物可能具有抗癌活性。
4. 细胞试验结果表明,新化合物对癌细胞具有明显的抑制作用。
数据分析:根据实验结果,新化合物具有较好的合成转化率和潜在的治疗效果。
需要进一步的研究来验证其在临床治疗中的应用价值。
实验结论:本实验成功合成了一种具有潜在抗癌活性的新化合物,为药物研发领域提供了新的候选药物分子。
备注:实验过程中需要注意安全操作,避免对人体和环境造成危害。
建议进一步深入研究新化合物的药理作用和毒理学性质。
药品检验原始记录书写范例

数据,记录可以简略;但应注明检查或含量测定项记录的页码。
同2.6.4 气相色谱法和2.6.5 高效液相色谱法项下的记录要求。
2.2.6 紫外-可见吸收光谱:同2.1.7吸收系数项下的记录要求。
2.2.7 红外吸收光谱:记录仪器型号,环境温度与湿度,供试品的预处理和试样的制备法,对照图谱的来源(或对照品的图谱),并附供试品的红外光吸收图谱。
如常规操作红外图谱与对照图谱不一致时,需详细记录供试品的特殊处理过程。
例:
红外光谱:检验日期:2005.08.05 t:28℃RH :65%
按《中国药典》2005年版二部(附录ⅣC)法检验
仪器型号:AE-240型电子天平(№008)
Avatar330型智能型傅立叶变换红外光谱仪(№)供试品(醋酸泼尼松)的制备(压片法):取供试品0.03~0.2mg,置玛瑙研钵中,加入干燥的溴化钾细粉15~20mg,充分研磨混匀,依法压片。
测定:取制成的供试片,目视检查均匀无明显颗粒。
将供试片置于仪器的样品光路中,扣除用同法制成的空白溴化钾片的背景,录制光谱图。
(红外吸收图谱附后见页)。
(完整版)检验原始记录(纯化水)
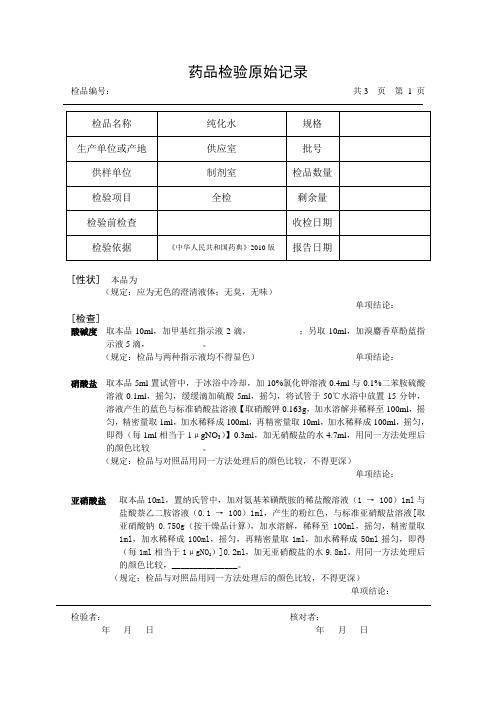
检品编号:共3 页第1 页[性状] 本品为(规定:应为无色的澄清液体;无臭,无味)单项结论:[检查]酸碱度取本品10ml,加甲基红指示液2滴,___________;另取10ml,加溴麝香草酚蓝指示液5滴,____________。
(规定:检品与两种指示液均不得显色)单项结论:硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液【取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)】0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较____________。
(规定:检品与对照品用同一方法处理后的颜色比较,不得更深)单项结论:亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1 → 100)1ml与盐酸萘乙二胺溶液(0.1 → 100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml摇匀,即得(每1ml相当于1μgNO2)]0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,_______________。
(规定:检品与对照品用同一方法处理后的颜色比较,不得更深)单项结论:检验者:核对者:年月日年月日检品编号:共3 页第2 页氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,_________________。
药品检验原始记录书写范例

药品检验原始记录书写范例药品检验原始记录书写范例药品检验是保证药品质量的重要手段,而药品检验原始记录是整个检验过程中重要的一环,对药品的质量控制起着至关重要的作用。
药品检验原始记录必须规范、准确地记录检验结果和检验过程,本文将给出药品检验原始记录书写的范例,以供参考。
1. 各项基本信息的书写药品检验记录中各项基本信息的填写要准确无误,包括药品名称、检验日期、制造厂家、批号、规格、批量、样品编号等。
对于样品批量和批号,即使是重复检验,也必须保持一致。
2. 检验方式当前,药品检验中主要采用荧光分析、气相色谱、液相色谱等方法。
在记录时,需要详细描述采用的检验方法,并注明方法文献的名称、版本和出版日期等信息。
3. 检验设备及工艺药品检验过程中,不同的设备和工艺会对检验结果起着不同的影响,在记录时,必须精准描述检验设备及工艺,如仪器型号、检验温度、检测条件、操作流程等信息。
4. 质量控制进行药品检验时,必须采取质量控制措施,以保证检验结果的精准和准确性。
在记录时,应该详细描述质量控制措施,如内部标准品的采用、浓度的计算及稀释、样品加标、纯化、净化等过程记录。
5. 检验结果药品检验原始记录中检验结果的书写要准确明确,包括结果计算和评价,不合格样品的处理等内容。
对于结果计算,应该详细描述计算过程、计算式的来源和计算结果的含义,对于不同的检验项目,结果评价标准有所不同,必须在记录中明确说明。
6. 仪器及设备校准记录药品检验过程中,仪器及设备的准确性对于检验结果的准确性起着关键作用,因此,周密的校准记录非常重要。
在记录仪器及设备校准时,应该写明校准标准品的来源、浓度以及校准时的操作流程和结果。
7. 附加信息药品检验原始记录中,有些信息不属于必要信息,但是包含这些信息能够使检验结果更可靠、实用。
如样品的来源、样品的保存条件、样品采集时间等。
总的来说,药品检验原始记录的书写要准确、规范,必须包含所有必备信息,同时,需要增加一些附加信息以便于后续分析和判断。
药品研究用原始记录模板
成品检验原始记录(首页)
检验者:复核者:日期:日期:
鉴别检查原始记录
检验者:复核者:日期:日期:
溶出度测定原始记录
日期:日期:
含量均匀度检查原始记录
日期:日期:
有关物质检查原始记录
检验者:复核者:日期:日期:
含量测定原始记录
日期:日期:
微生物限度检查记录
检品名称:批号:
生产单位:检品数量:
规格:包装:
检验日期:报告日期:
检验依据:
供试液制备:
□常规法供试品 g(ml) 0.9%无菌氯化钠-蛋白胨缓冲液 ml
①匀浆仪挡 min ②研钵法③保温振摇法
□非水溶性供试品供试品 g或ml 加乳化剂(g或ml)
□抑菌性供式品处理方法供试品 g或ml 0.9%无菌氯化钠溶液 ml 方法:
结论:按《中国药典2010年版二部》检验上述项目,结果:
检验者:复核者:
日期:日期:。
药品检验记录格式参考模板
%1=16.60×1.005×0.01381/0.2298×100%=100.26%
%1=21.72×1.005×0.01381/0.3006×100%=100.28%
%=100.26%+100.28%/2=100.27%=100.3%符合规定
【性状】为白色结晶性粉末,无臭,味微甜后转不适,水溶液显酸性反应。在乙
醇或乙醚中易溶,沸水中溶解,氯仿中略溶,水中微溶。符合规定
熔点:158.5~160.8℃符合规定
【鉴别】(1)本品水溶液+三氯化铁试液→紫堇色。符合规定
(2)红外图谱与对照图谱一致。符合规定
【检查】苯酚:本品0.10g制成的溶液与同法制成的对照液比较,颜色浅。符合规定
×××公司检测原始记录
No:文件编号:××××
检品名称
水杨酸
检品批号
0801022
规 格
25Kg/袋
包装形式
塑料袋
生产企业
×××药业有限公司
检品数量
160g
送检单位
威海职业学院生化系
检测日期
2008.12.10.
检验依据
《中华人民共和国药典》2005年版二部
报告日期200Leabharlann .12.15.记 录 内 容
检验人:××××××复核人:×××
炽灼残渣:坩埚1:36.2452g,36.2453g坩埚2:28.7638g,28.7637g
样品坩埚1:37.2461g样品坩埚2:29.7624g
恒重后样品坩埚1:36.2454g恒重后样品坩埚2:28.7639g
%1=(36.2454-36.2453)/(37.2461-36.2453)×100%=0.0001/1.0008×100%=0.01%
药物检验原始记录的格式大全
一、化学鉴别法药品检验原始记录检品名称:检验日期:批号:规格:【鉴别】/结果:□呈正反应□不呈正反应结论:□符合规定□不符合规定检验者: 复核者: 第页二、TLC鉴别法药品检验原始记录检品名称:检验日期:批号:规格:[鉴别]供试品溶液的制备:对照品(或对照药材、对照提取物)溶液的制备:对照物质来源:□均为中国药品生物制品检定所提供□其他:No:薄层色谱条件与结果详见附图()。
结论:□符合规定□不符合规定(规定:在供试品色谱中,在与对照品(或对照药材、对照提取物)色谱相应位置上,显相同颜色的斑点。
)检验者: 复核者: 第页三、TLC图薄层色谱检验记录图号:检品名称:检品编号: 检验日期:天气:室温:湿度:薄层板:展开温度:展开剂:显色剂及检视方法:点样量( l):点样顺序: 1 2结论:检验者: 复核者: 第页四、 相对密度药品检验原始记录检品名称: 检品编号: 检验日期: 规格: 批号 室温: 湿度: 相对密度(比重瓶法)照相对密度测定法(中国药典2010年版A V I AV II 二部附录一部附录)测定。
测定方法: □比重瓶法 □韦氏比重称法 (规定测定温度为20℃)。
天平: 实验温度: 空瓶重(W 1): 瓶+供试品重(W 2): 供试品重(W 2-W 1): 瓶+水重(W 3): 水重(W 3-W 1):结果计算:计算公式:相对密度 = 水重量供试品重量结论: (规定 ) 检验者: 复核者: 第 页五、PH值测定法药品检验原始记录检品名称:检品编号: 检验日期:批号:规格:温度:湿度:pH值照pH值测定法(《中国药典》2010年版一部附录VII G)测定。
仪器:校正仪器用标准缓冲液:邻苯二甲酸氢钾标准缓冲液(pH4.00)磷酸盐标准缓冲液(pH6.86)其它:供试品溶液的制备:pH值测定结果:结论:□符合规定□不符合规定(规定: ) 检验者: 复核者: 第页六、重量差异检查之一药品检验原始记录检品名称:检验日期:批号:规格:重量差异按《中国药典》2010年版一部附录I D片剂项下检查法取供试品20片,分别精密称定每片的重量。
药品检验原始记录书写范例
XXX食品药品检验所《质量手册》作业指导书版本号:
执行日期:2005年12月01日
标题检验记录书写范例
共88页第18页
第1版第0次修订
于仪器的样品光路中,扣除用同法制成的空白溴化钾片的背景,录制光谱图。
(红外吸收图谱附后见页)
结果:供试品红外光吸收图谱与《药品红外光谱集》1990年版醋酸泼尼松对照图谱(光谱号549)一致, 符合规定。
2.3【检查】
2.3.1 含氟量:记录氟对照溶液的浓度,供试品的称量(平行试验2份),供试品溶液的制备,对照溶液与供试溶液的吸光度,计算结果。
例:
含氟量:检验日期:2005.08.08 t:28℃
按《中国药典》2005年版二部(附录ⅧE)方法检验
仪器型号:AE-240型电子天平(№008)
UVIKON XL型双光束扫描紫外/可见分光光度计(№。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.3.18崩解(溶散)时限
2.3.19含量均匀度
2.3.20溶出度(释放度)
2.3.21可见异物
2.3.22装量差异
2.3.23最低装量检查
2.3.24不溶性微粒
2.3.25过敏反应检查
2.3.26颗粒剂的粒度
2.3.27微生物限度检查
2.5【浸出物】
2.6【含量测定】
2.6.1容量分析法
2.6.2重量分析法
2.6.3紫外-可见分光光度法
2.6.4气相色谱法
2.6.5高效液相色谱法
2.6.6抗生素微生物检定法
三、检验记录书写范例
“检验记录”是出具检验报告的依据,是进行科学研究和技术总结的原始资料,为保证检验工作的科学性和规范化,检验记录必须做到:记录原始、真实,内容完整、齐全,书写清晰、整洁,删改正确,按页编号,归档保存,内容不得私自泄露。
2 每个检验项目记录的要求和范例
检验记录,可按实验操作的先后,依次记录各检验项目,不要求与标准上的顺序一致。项目名称应按标准规范书写,不能采用习用语,如将片剂的“重量差异”记成“片重差异”,或将“崩解时限”写成“崩解度”等。最后应对该项目的检验结果给出明确的单项结论。以下对一些常见项目的记录内容,提出下述的最低要求(即必不可少的记录内容),检验人员可根据实际情况酌情增加,多记不限。多批号供试品同时进行检验时,如结果相同可只详细记录一个编号(或批号)的情况,其余编号(或批号)可记为同编号(批号)××××××的情况与结论;遇有结果不相同时,则应分别记录。
2.3.4 溶液的澄清度与颜色
2.3.5 氯化物(硫酸盐)
2.3.6 干燥失重
2.3.7 水分(费休氏法)
2.3.8 炽灼残渣(灰分)
2.3.9 重金属(铁盐)
2.3.10 砷盐(硫化物)
2.3.11 异常毒性
2.3.12 热原
2.3.13细菌内毒素
2.3.14 降压物质
2.3.15无菌
2.3.16乙醇量测定法
1.5检验中使用的标准品或对照品,应记录其来源、批号和使用前的处理;用于含量(或效价)测定的,应注明其含量(或效价)和干燥失重(或水分)。
1.6每个检验项目均应写明标准中规定的限度或范围,根据检验结果作出单项结论(符合规定或不符合规定),并签署检验者的姓名。
1.7在整个检验工作完成之后,应将检验记录逐页顺序编号,根据各项检验结果认真填写“检验卡”,并对检品作出明确的结论。检验人员签名后,经主管药师或室主任指定的人员对所采用的标准、内容的完整、齐全,以及计算结果和判断的无误等,进行核校并签名,再经室主任审核后,连同检验卡一并送业务室审核,报主管业务副所长和所长或授权签字人核签后方可打印检验报告,盖章发出。
2.1.8 酸值(皂化值、羟值或碘值)
2.2【鉴别】
2.2.1 中药材的经验鉴别
2.2.2 显微鉴别
2.2.3 显色反应或沉淀反应
2.2.4 薄层色谱(或纸色谱)
2.2.5 气(液)相色谱
2.2.6 紫外-可见吸收光谱
2.2.7 红外吸收光谱
2.3【检查】
2.3.1 含氟量
2.3.2 含氮量
2.3.3 pH值
1.3检验记录中,应先写明检验的依据。凡按《中国药典》、《局(部)颁药品标准》、《地方药品标准》或国外药典检验者,应列出标准名称、版本和页数;凡按送检者所附检验资料或有关文献检验者,应先检查其是否符合要求,并将前述有关资料的影印件附于检验记录之后,或标明归档编码。
1.4检验过程中,可按检验顺序依次记录各检验项目。内容包括:项目名称,检验日期,操作方法(如系完全按1.3检验依据中所载方法,可简略扼要叙述;但如稍有修改,则应将改变部分全部记录),实验条件(如实验温度、仪器名称型号和校正情况等),观察到的现象(不要照抄标准,而应简要记录检验过程中观察到的真实情况;遇有反常的现象,则应详细记录并鲜明标出,以便进一步研究),实验数据,计算(注意有效数字和数值的修约及其运算,详见《中国药品检验标准操作规范2005年版》)和结果判断等;均应及时、完整地记录,严禁事后补记或转抄。如发现记录有误,可用单线划去并保持原有的字迹可辨,不得擦抹涂改,并应在修改处签名或盖章,以示负责。检验或试验结果,无论成败(包括必要的复试),均应详细记录和保存。对废弃的数据或失败的实验,应及时分析其可能的原因,并在原始检验记录上注明。
1 检验记录的基本要求
1.1检验记录应采用统一印制的活页记录纸和各类专用检验记录表格,并用蓝黑墨水或碳素笔书写(显微绘图可用铅笔)。凡用计算机打印的数据与图谱,应剪贴于记录上的适宜处,并有操作者签名;如系用热敏纸打印的数据,为防止日久褪色难以识别,应以蓝黑墨水或碳素笔将主要数据记录于记录纸上。
1.2检验人员在检验前,应注意检品标签与所填检验卡的内容是否相符,逐一核对检品的编号、品名、规格、批号和效期、生产单位和产地,检验目的和收检日期,以及样品的数量和包装情况等,并将检品的编号与品名记录于检验记录纸上。
本《检验记录书写范例》中所引用的生产企业、品种和批号、检验数据等,均为了检验记录书写示例,不是实际检验数据。
二、目录
1 检验记录的基本要求
2 每个检验项目记录的要求和范例
2.1【性状】
2.1.1 外观性状
2.1.2 溶解度
2.1.3 相对密度
2.1.4 熔点
2.1.5 旋光度
2.1.6 折光率
2.1.7 吸收系数
XXX食பைடு நூலகம்药品检验所
检验记录书写范例
一、绪言
食品药品监督管理部门设置或者确定的食品药品检验机构,是国家食品药品监督保证体系的重要组成部分,是国家对食品药品质量监督、检验的法定性专业机构。加强技术监督,为国家和人民把好食品药品质量关,是食品药品检验部门的神圣职责。食品药品检验是保证人民用药安全有效和评价药品质量的重要手段,是贯彻实施《药品管理法》和执行《中国药典》的重要环节。食品药品检验机构出具的检验报告是具有法律效力的技术文件。为保证我所检验数据与结论报告的正确、可靠和一致,实现实验操作的标准化、规范化和管理科学化,根据国家食品药品监督管理局制订的《药品检验所实验室质量管理规范(试行)》和中国药品生物制品检定所编制的《中国药品检验标准操作规范2005年版》(Standard Operation Procedures for Drug Control简称DCSOP),及河南省食品药品检验所检验报告暨检验记录书写要求,总结我所多年来检验工作经验,制定了《检验报告暨检验记录书写范例》,作为我所检验工作者执行检验标准,书写检验报告和检验记录的依据,必将提高全所整体工作质量和工作效率。
