去离子水生产记录
口服液体制剂车间设计概要

⼝服液体制剂车间设计概要⼝服液体制剂车间设计——年产3000万⽀葡萄糖酸钙⼝服制剂车间的设计姓名:李洪⽉班级:⽣实0901学号:200982051⽬录⼀、公司介绍 (4)⼆、实习车间介绍 (4)三、该车间⽣产的⼝服液种类 (4)四、实习岗位 (5)五、葡萄糖酸钙⼝服溶液简介 (5)六、⽣产⼯艺与流程图 (6)1.⼝服液⽣产流程 (6)2.制⽔⼯艺 (7)3.⼯艺流程分析 (7)4.⼯艺特点及难点 (8)七、物料衡算 (9)1.设计规模 (9)2.设计依据 (9)3.年⼯作⽇、班制 (9)4.⽣产流程 (10)6.原材料消耗量⼀览表 (12)⼋、车间平⾯布置图 (12)1.车间布置要求 (12)2.车间⼯艺布置要点 (13)3.车间原布置图(附图1) (14)4.改进的平⾯图(附图2) (14)5.中药提取车间⼯艺布置 (14)九、岗位划分、⼈员配备 (15)1.岗位划分 (15)2.⼝服液车间批⽣产记录 (15)3.操作程序 (16)4.理瓶、洗瓶 (16)5.灭菌 (16)6.灌装、轧盖岗位 (17)7.传递柜操作: (17)8.灯检岗位 (17)9.外包装岗位 (18)10. 做好⽣产记录 (19)11.岗位管理制度 (19)⼗、⼝服液车间⼯资草案 (20)⼝服制剂车间设计⼀、公司介绍⼭东益康药业股份有限公司建有两座⼩容量注射剂车间、两座原料药车间、普通类、青霉素类、头孢类三座⼝服固体制剂车间、⼝服液、中药提取共九座⽣产车间,全部通过了GMP认证。
现有抗⽣素类、⼼脑⾎管类、解热镇痛类、降⾎糖类、维⽣素及矿物质类、消化系统、呼吸系统、肿瘤辅助⽤药81个品种,⼩容量注射剂综合产能位居⼭东省第⼆位,全国前⼗位。
建⽴了省、市、县三级营销⽹络,拥有1200家代理商,以⾼效安全的药品质量畅销国内20多个省市和地区,出⼝南亚、中东和⾮洲地区。
益康药业被评为国家级⾼新技术企业、⼭东国家综合性新药研发技术⼤平台⽰范企业、中国制药⾏业百佳影响⼒品牌企业、⼭东省重点企业技术中⼼、⼭东省专利明星企业、被省政府列为⾸批泰⼭学者⼀药学特聘专家设岗企业、省科技厅确定在益康药业建⽴⼭东省晶型药物⼯程技术研究中⼼,2011年5⽉被省政府评为⼭东省产学研合作创新突出贡献企业,2011年11⽉10⽇改制为股份有限公司,12⽉29⽇在齐鲁证券股权托管中⼼成功挂牌交易,实现了益康药业资本结构、组织形式的⼜⼀转型,促进了企业管理规范化、资本公众化、收益社会化的提升,为企业正式上市打下了坚实的基础。
阳极氧化工艺流程

阳极氧化工艺流程阳极氧化已经慢慢淘汰了,现在已经升级到了微弧氧化,可以做镁和铝合金产品,原理都是一样,通过有机溶剂做为介质,采用尖端放电,在产品表面生成保护膜,类似於陶瓷层。
外观除了一些起跑引起的颜色问题,是很难看出来的,主要通过,盐雾、耐摩擦、电导率、电击穿等测试来判定膜层的好坏。
工艺:除油--水洗--水洗--阳极反应--水洗--封闭--烘烤铝制品阳极氧化工艺流程铝制品阳极氧化通用的工艺流程如下:铝工件→上挂具→脱脂→水洗→碱蚀→水洗→出光→水洗→阳极氧化→水洗→去离子水洗→染色或电解着色→水洗→去离子水洗→封闭→水洗→下挂具对于要求高光亮度的铝制品,可采用如下的工艺流程:铝工件→机械抛光→脱脂→水洗→中和→水洗→化学或电化学抛光→水洗→阳极氧化→水洗→去离子水洗→染色或电解着色→水洗→去离子水洗→封闭→水洗→机械光亮铝及铝合金阳极氧化着色工艺流程(图) 铝及铝合金阳极氧化着色工艺规程1、主题内容与适用范围:本规程规定了铝及铝合金阳极氧化、着色、电泳生产的工艺和操作的技术要求及规范。
2、工艺流程(线路图)基材→装挂→脱脂→碱蚀→中和→阳极氧化→电解着色→封孔→电泳涂漆→固化→卸料包装→入库3、装挂:3.1装挂前的准备。
3.1.1检查导电梁、导电杆等导电部位能否充分导电、并定期打磨、清洗或修理。
3.1.2准备好导电用的铝片和铝丝。
3.1.3检查气动工具及相关设备是否正常。
3.1.4核对流转单或生产任务单的型号、长度、支数、颜色、膜厚等要求是否与订单及实物相符。
3.1.5根据型材规格(外接圆尺寸、外表面积等)确定装挂的支数和间距、色料间距控制在型材水平宽度的1.2倍左右,白料间距控制在型材宽度的1倍左右。
3.1.6选择合适的挂具,确保正、副挂具的挂钩数与型材的装挂支数一致。
3.2 装挂:3.2.1装挂时应先挂最上面一支,再固定最下面一支,然后将其余型材均匀排布在中间、并旋紧所有铝螺丝。
3.2.2装挂前在型材与铝螺丝间夹放铝片,以防型材与挂具间的导电不良而影响氧化、着色或电泳。
WB操作步骤-自己整理

Western Blot 相关实验方法与试剂(湿转法)人工肝实验室学习姚瑶(一)目的蛋白提取:(1)单层贴壁细胞总蛋白的提取:1、倒掉细胞培养液,加入Hanks液洗涤一次后倒掉,根据所用细胞决定是否用胰酶消化,加入适量(约5ml)新鲜细胞培养液后,将贴壁细胞吹起,并转移至4支离心管内,配平后,1500转离心10min。
2、倒掉上清,用4度预冷PBS溶液洗涤沉淀,1500转离心10min。
共洗三次,每次十分钟。
3、倒掉上清,吸净,每管加入50ul 细胞裂解液RIPA,吹散,加入后由于DNA的释放可迅速变粘稠,故应尽快转移至1.5ml EP 管内,-20℃裂解30min。
4、超声波细胞裂解仪上将各管裂解15s。
(可不做)5、4℃,12000转离心10min。
6、将上清转移至0.5ml EP管中,每管100ul,冰浴待用。
(2)组织中总蛋白的提取:1、取约100mg肝组织于研磨器内,加入500ul 细胞裂解液RIPA,研磨后吸出于1.5ml EP管内,再加入500ul RIPA,研磨后吸出于上EP管内。
冰上裂解30min。
2、配平后,4℃,14000转离心10min。
3、将上清分装于0.5ml EP管内,每管100ul,冰浴待用(二)蛋白含量的测定:1、稀释标准品:10ul标准品C液+90ul PBS溶液,混匀。
2、按0、1、2、4、8、12、16、20ul将稀释后的标准品加入于96孔板内,并用PBS将各孔补足20ul。
3、将第2、3排96孔板分别加入样品1ul、0.5ul,(可采用倍比稀释法),并用PBS将各孔补足20ul。
4、配制工作液:按A液:B液=50:1配制适量工作液,每孔加入200ul。
5、37℃水浴30min。
6、酶标仪测定各孔OD值(A570,Mode1)。
7、绘制标准曲线,计算样品蛋白浓度。
(三)SDS-PAGE电泳:(1)清洗玻璃板(2)灌胶与上样:1、配胶:根据目的蛋白的大小,决定分离胶的浓度。
制造业质量控制计划模板
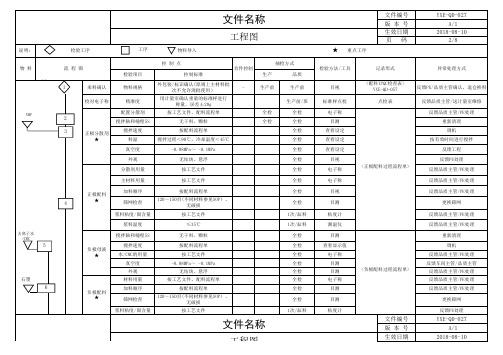
按工艺文件、配料流程单
无干料、颗粒
按配料流程单
搅拌过程<90℃、冷却温度<45℃
-0.08MPa~ -0.1MPa
抽检方式
生产
品质
生产前
生产前
全检 全检
生产前/班
全检 全检 全检 全检 全检
外观
无结块、悬浮
全检
分散剂用量
按工艺文件
全检
主材料用量
按工艺文件
全检
正极配料
加料顺序
按配料流程单
√ 5pcs/5min 3pcs/2h/台
目视
21
刷片
扫粉效果、极片外 观
扫粉作业指导书
卷针尺寸
参照工艺标准
√
3pcs/2h/台 生产前/班目视来自卡尺生产返工 调换卷针
隔膜/胶纸 22
隔膜宽度、厚度
按工艺标准
√
卷芯厚度/宽度/高
卷绕
度
按工艺标准
√
★ 极耳中心距
按工艺标准
√
生产前/班 5pcs/4h 5pcs/4h
反馈品质主管/PE处理 重新清理 调机
按有效时间进行搅拌 反馈工程
反馈PE处理 反馈品质主管/PE处理 反馈品质主管/PE处理 反馈品质主管/PE处理
更换筛网
反馈品质主管/PE处理 反馈品质主管/PE处理
<负极配料过程流程单>
重新清理 调机
反馈品质主管/PE处理 反馈车间主管/品质主管 反馈品质主管/PE处理 反馈品质主管/PE处理 反馈品质主管/PE处理
记录形式
异常处理方式
目视
标准样点校 电子称 目测 查看设定 查看设定 查看设定 目视 电子称 电子称 目视 目测
大输液生产工艺规程

大输液生产工艺规程大输液生产工艺规程部门:生产部题目:大输液生产工艺1/15规起草新订替代STP-PC-99000部门审阅批准审核执行日变更记录及目的批准执修订人日:目的:建立一个大容量注射液(大输液)生产的通用工艺规程,为车间提供一个通用技术标准适用范围:大输液的生产工艺者:生产部经理、输液车间主任、工艺技术员质监员及操作容一产工艺流程图(见下页二作过程及工艺条件制将饮用水(来自青城山)经石英砂过滤和活性碳滤去除水中有机质及微粒,经电渗析初步脱盐(脱75后再经“阳—阴—阴—混离子交换去离子化制得去离子水,再经过切割分子量1000(相当0.00)中空纤维滤材组成的超滤系统滤后制得超纯水(纯化水再经五效蒸馏水机制造馏水,经微孔滤膜(孔0.4)过滤后制得注射用水。
2、洗瓶将检验合格的输液瓶在车间外脱去外包装(麻袋或纸箱),在玻瓶进入口处转入周转箱中,运至理瓶室理瓶机旁,逐一上瓶于转盘上,开动外洗瓶机,淋水下对玻瓶进行外刷洗,同时灌入约100ml自来水,传送至内洗瓶(粗洗)机,先用0.5%NaOH 洗刷,再用自来水洗刷,再用自来水洗刷,最后用纯化水.大输液生产工艺规程部门:生产部题目:大输液生产工艺2/15 规程STP99000文件编号新订替代起草部门审阅审核批准执行日变更记录变更原及目的修订人批准执日:胶塞隔离膜输液瓶原辅料饮用水↓瓶外清洗碱酸处理乙醇浸泡↓称量离子交换清洁剂处理↓饮用水初蒸馏水清刷洗内浓去离子饮用水清蒸馏水煮蒸馏水清过蒸馏去离子水清蒸馏水清注射用水清注射用水清稀注射用注射用水清粗精灌放注射用水清上胶翻盖铝盖铝盖轧口出厂入库包装贴签灯检灭菌注:洁净级别 100级 1万级 10万级大输液生产工艺规程部门:生产部题目:大输液生产工艺3/15规起草新订替代STP-PC-99000部门审阅批准核执行日变更记录及目的批准执行日修订人:药液经中间检验各项指标合格后输送至灌装机,开机灌装入洁净的输液瓶中,立即盖薄膜,膜必须放正,然后对准膜中心,垂直塞入胶塞,经翻塞机翻塞后传送到轧盖。
纯净水检验报告

GB 4789.3-2016检验报告Inspection report产品名称:产品规格:检验单位:检验类别:公司成品检验报告单报告编号:感官指标理化指标微生物指标检验员: 校验员: 审核:年月日- 1 -样品名称: 样品规格:样品状态: 检验环境:室温℃湿度 %检验日期: 商标: 咣一气检验项目: 色度检验类别: 自检检验依据:GB 1929-2014《食品安全国家标准包装饮用水》一、原理百灵达光度计采用光电检测原理对水样的色度进行测量。
测量之前需要对水样进行过滤预处理,去除水样中的悬浮物质,水样色度的测量结果以铂、钴色度Pt/CO表示。
二、仪器百灵达波长自动选择型光度计三、操作步骤1.选择项目编号或项目名称。
2.将去离子水加入试管至10ml刻度线,放入光度计测量室中执行空白设定。
3.用GF/B滤纸过滤待测水样,另取一支试管,加入过滤后的水样至10ml刻度线。
4.将上述试管重新放入测量室中,读取测量值。
5.将测量结果计色度,以mg/hpt为单位显示。
检验员:校验员:审核:年月日- 2 -样品名称: 样品编号:样品状态: 样品规格:检验环境:室温℃,湿度% 商标: 咣一气检验项目: 浊度检验类别: 自检检验依据:GB 19298-2014<<食品安全国家标准包装饮用水>>一、原理百灵达光度计采用光电检测原理对水样浊度进行测量,百灵达浊度量测法与福尔马胼标准浊度溶液进行对比校准,该单位等同于浊度单位NTU。
二、仪器百灵达波长自动选择型光度计三、操作步骤1.选择项目编号或项目名称。
2.将待测水样用GF/B滤纸过滤后,加入试管至10ml刻度线,并将试管放入测量室中执行空白设定。
3.另取一支试管,加入待测水样至10ml刻度线,该试管放入测量室中。
4.读取测量值,测量结果以NTU为单位表示。
检验员: 校验员: 审核:年月日- 3 -样品名称: 样品编号:样品状态: 样品规格:检验环境:室温℃,湿度%商标: 咣一气检验项目: 肉眼可见物检验类别: 自检检验依据:GB 17323-1998<<瓶装饮用纯净水卫生标准>>一、所需仪器250ml烧杯二、原理主要指水中存在的,能以肉眼观察到的颗粒或其它悬浮物质。
GMP认证制药用水标准要求

GMP认证制药用水标准要求在世界许多发达国家如美国,注射用水(Water for Injection, WFI)必须由蒸馏工艺制备这一局限早已被突破,技术更先进、更节能、品质更稳定可靠的高纯水(Highly Purified Water, HPW)及其制备工艺早在1975年已经得到正式确认(美国药典第19版:USP19);现在,美国药典已经在其连续7个版本中明确确认了以反渗透(RO)为基础的HPW 工艺可以作为制取注射用水的法定工艺,并且历经数十年的医药实践,HPW注射用水生产技术已被证明是最先进、可靠的方法之一,以至于在美国的药物专利25条中,反渗透方法是最常用的注射用水生产工艺,由于HPW符合甚至超过WFI的各项理化参数指标,自2002年6月起正式被欧洲认可为第三水质级别。
今天,以RO为基础的HPW已经为代表医药先进技术的世界主要发达国家所确认,成为医用纯化水的标准制备方法之一。
在与国际接轨过程中我国药典亦对医药用水的法定制备方法进行了重新定义。
中国药典(2000年版)中所收载的制药用水,因其使用的范围不同而分为纯化水、注射用水及灭菌注射用水,首次将过去的蒸馏水改为纯化水,并且对纯化水具体定义为“纯化水为采用蒸馏法、离子交换法、反渗透法或其它适宜的方法制得供药用的水”,实际上放弃了对生产工艺“必须为蒸馏法”的限定,为相关企业采用国际上广为流行的反渗透HPW方法制备纯化水奠定了法律基础。
更为重要的是,新的国家药典将注射用水定义为“纯化水经蒸馏所得的水”,从而使RO技术进入注射用水制备过程成为可能。
2000年版国家药典在制约用水技术上朝国际先进领域迈进了一大步。
与传统的蒸馏法相比较,以反渗透法为基础的联合了最新电去离子(EDI)技术的新工艺具有明显的优越性和先进性。
1.高效节能。
蒸馏法系历史最为悠久的医药用水制备工艺,主要有多级蒸馏、高压分级蒸馏和离心净化蒸馏几种工艺。
所有蒸馏方法均在120℃高温状态下进行,所以可以得到完全无菌的水。
审核案例题

环境管理体系内部审核案例题1.审核员刚进工厂就看到门前的宣传栏中写着:"保护环境、造福人类、节能降耗、着眼未来"十六个大字。
站在门口欢迎审核员到来的环境管理者代表说到:"这是我们的环境方针,为方便员工记忆,用十六个字精练地表达出了保护环境的意思。
2.审核员在某污水处理站审核,发现作业指导书规定了要对排放污水的酸碱度(pH值)进行控制,查现场监测记录得知污水pH值变化幅度很大,从3-11不等,询问员工应执行的标准是多少,员工说不清楚,因为文件中并没有作出规定。
3.某企业将其在生产中产生的铬渣委托某运输公司清运,该公司为避免城市污染,将渣运到城郊山坡上掩埋。
4.某公司重大环境因素岗位上帖有环境作业指导书,但体系文件及索引中没有。
5.审核员在某原件厂质管科审核时,发现公司在上一年度内部审核中发现的10个不符合项目前仍有三项示关闭。
6.查某化工厂环境管理部门"相关法律、法规及要求一览表",没有将"化学危险品案例管理条例"列进去。
7.现场抽查机加工车间及装配车间各两名员工,对于所在工作中有无重要环境因素,均未能答出来。
8.现场发现污水处理站有两份污水处理文件,分别由环境管理科和设备科编号,对污水的处理步骤,一份规定加片碱,一份规定加其他化学品。
9.询问公司总经理管理评审的记录,总经理拿出10个月的例会记录解释说,公司领导层对环境问题非常重视,每个月对出现的环境问题都召开例会予以解决,因此没有专门做一份管理评审记录。
10.某分厂"环境管理方案"中写明2月份要建空压机房,以降低噪声排人,现场发现空机房仍露天放置,分厂厂长解释说,现在环保局已经把分厂所在区域由住宅区改为工业区,我们的噪声排放现在是达标的,因此就没有再建空机房的必要。
11.在机加工车间发现操作工未按文件的要求将铜、铁边角料分开放置,员工解释说,反正市废品金属回收公司在收取的时候会分开,文件规定完全是多余的。
