(CX14-03)培训记录表
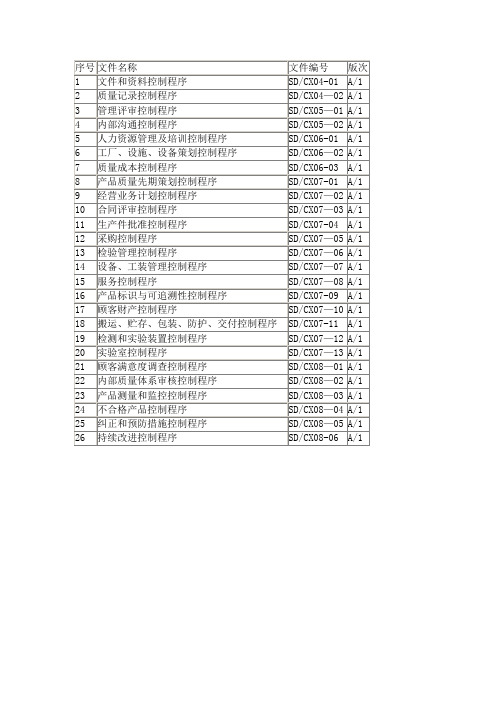
体系文件总表
文件名称
文件编号
版次
1
文件和资料控制程序
SD/CX04-01
A/1
2
质量记录控制程序
SD/CX04—02
A/1
3
管理评审控制程序
SD/CX05—01
A/1
4
内部沟通控制程序
SD/CX05—02
A/1
5
人力资源管理及培训控制程序
SD/CX06-01
A/1
6
工厂、设施、设备策划控制程序
SD/CX06—02
SD/CX07—12
A/1
20
实验室控制程序
SD/CX07—13
A/1
21
顾客满意度调查控制程序
SD/CX08—01
A/1
22
内部质量体系审核控制程序
SD/CX08—02
A/1
23
产品测量和监控控制程序
SD/CX08—03
A/1
24
不合格产品控制程序
SD/CX08—04
A/1
25
纠正和预防措施控制程序
A/1
7
质量成本控制程序
SD/CX06-03
A/1
8
产品质量先期策划控制程序
SD/CX07-01
A/1
9
经营业务计划控制程序
SD/CX序
SD/CX07—03
A/1
11
生产件批准控制程序
SD/CX07-04
A/1
12
采购控制程序
SD/CX07—05
A/1
13
检验管理控制程序
SD/CX07—06
A/1
14
设备、工装管理控制程序
SD/CX07—07
门店值班经理GSP表格培训

规格
单 位
数 量
产品批 号
生产厂家
金 额
销毁原因
合计
待销毁药品共
个品种,个ຫໍສະໝຸດ 号,件,原值元销毁日期
销毁方式
销毁地点
销毁人员
质量管理 员
企业负责 人
监销人
财务人员
广州慈济药业连锁有限公司不合格药品报损审批表
编号:JL-CJ-24-1
商品名 药品通用名 称 生产厂家 生产批 号 金额
规格
供货单 位
数量
编号:JL-CJ-14-1 装斗品种 装斗日期 质量复核情况 验收员 复核人
有质量问题中药明细表 日期 名称 重量 等级 生产日期 供货单位 产地,生产企业 质量情况 复核人
广州慈济药业连锁有限公司药品拆零登记表
编号:JL-CJ-15-1 药品名称 拆零 日期 拆零 规格 批号 有效期 单 位 数 量 生产单位 经手 人 销售完 毕时间
广州慈济药业连锁有限公司中药饮片质量验收记录
编号:JL-CJ-22-1 品名 到货 日期 等级 重量 供货单位 产地、生产企业 产品批号 或生产日期 包装 质量 外观 质量 验收 结论 验收员及验 收日期 备注
广州慈济药业连锁有限公司不合格药品销毁记录
编号:JL-CJ-23-1
编号
药品通用名 称(商品名)
注:每月一次
广州慈济药业连锁有限公司重点养护品种药品养护检查记录(中药饮片)
日期 品名 规格 批号 产地 数量 生产企业 养护方法 养护后情况 养护 人 备注
注:每月一次
重点养护药品确认表
货号 品名 规格 生产企业 有效期至 存放地点 确定理由及养护重点 备注
养护员:
质管员:
(CNAS体系程序文件3)沟通控制程序

广东有限公司检测中心沟通控制程序文件编号:QY/CX-03版本号:B/0受控状态:受控分发号:_____________持有人:_____________编制:日期:审核:日期:批准:日期:为了及时、准确地收集、传递及反馈检测中心相关质量和安全的信息,并对信息进行管理,特制定本程序。
2.0适用范围适用于本检测中心全体员工、各职能部门以及提供外部服务的相关方。
3.0职责和权限3.1 综合部为沟通管理工作归口部门,负责检测中心质量和安全信息的内外部沟通。
3.2 各部门负责工作范围内和对应相关方信息的收集、传递和交流。
4.O工作程序:4.1内部沟通4.1.1内部沟通的信息a.质量方针目标完成情况、测量和监控记录、内部审核与管理评审报告及体系正常运行时的其它记录;b.不符合项报告及纠正预防措施报告;c.紧急信息:安全事故,突发事件信息;d.企业文化信息;e员工建议等。
f.其它信息4.1.2自上而下的沟通:4.1.2.1中心主任根据组织机构和职能运作,通过会议、文件等方式,对管理体系运作的过程,包括顾客和法律法规的要求,方针目标及其完成情况,以及实施的有效性进行沟通,及时采取相应的措施,确保管理体系的正常运作。
4.1.2.2检测中心的例行会议、管理评审会议、内部审核首末次会议、相关的培训讲课等,参加人员应在《会议/培训记录表》上签名,并做好相关会议记录,并根据需要以会议纪要,备忘录、简报等形式对下级相关部门和人员传达。
4.1.2.3检测中心每月至少组织召开一次例会,由中心主任或其受权人主持,对下例各事项进行讨论、交流、汇报:a.质量目标评审及完成情况;b.体系运行监测情况分析;c.合同履行情况汇报d.客户及相关方的投诉处理跟踪;e.不符合项的处理及纠正预防措施的验证f.其它问题4.1.3自下而上的沟通:4.1.3.1各部门建立汇报制度,负责人每月例会汇报本部门工作情况,做为中心主任决策的依据。
4.1.3.2各部门应按有关规定,定期向中心主任上报有关报表。
电梯质量手册及质量体系文件清单

LZHA-A/0-JL-41
42
检验与试验装置台帐
LZHA-A/0-JL-42
43
检验与试验装置领用(归还)记录
LZHA-A/0-JL-43
44
检验与试验装置校准记录
LZHA-A/0-JL-44
45
检验与试验装置周期检定计划表
LZHA-A/0-JL-45
46
检验与试验装置检定报告档案
8
外来文件登记表
LZHA-A/0-JL-08
9
管理评审计划
LZHA-A/0-JL-09
总经理
10
管理评审会议记录
LZHA-A/0-JL-10
11
管理评审报告
LZHA-A/0-JL-11
12
合同评审记录
LZHA-A/0-JL-12
营销部经理
13
合同修订通知单
LZHA-A/0-JL-13
14
合同台账
LZHA-A/0-JL-14
LZHA-A/0-JL-46
47
检验与试验装置定期维护保养计划表
27
焊材验收入库记录
LZHA-A/0-J/0-JL-28
29
焊材领用/回收/报废记录
LZHA-A/0-JL-29
30
曳引电梯安装过程自检记录
LZHA-A/0-JL-30
技质部经理
31
自动扶梯/自动人行道安装过程自检记录
LZHA-A/0-JL-31
32
杂物电梯安装过程自检记录
LZHA-A/0-ZY-11
12
无机房电梯安装工艺文件
LZHA-A/0-ZY-12
13
无脚手架安装电梯工艺文件
(电子行业企业管理)三标管理体系运行相关记录表格电子版

(电子行业企业管理)三标管理体系运行相关记录表格电子版发文登记表集团总部各部门/直属项目部:编号:CX01-01收文登记表集团总部各部门/直属项目部:编号:CX01-02受控文件清单集团总部各部门/直属项目部:编号:CX01-03填表人:日期:部门负责人:日期:文件借阅(复制)登记表集团总部各部门/直属项目部:编号:CX01-04文件领用审批表部门:编号:CX01-05文件销毁登记表部门:编号:CX01-06文件回收记录表部门:编号:CX01-07文件更改审批表部门:编号:CX01-08记录目录清单部门:编号:CX02-01记录目录总清单部门:编号:CX02-02记录归档清单部门:编号:CX02-05记录借阅登记表部门:编号:CX02-04记录处理审批表部门:编号:CX02-03法律法规获取(更新)确认登记表部门:编号:CX03-01法律法规合规性评价登记表部门:编号:CX03-02法律法规和其他要求清单部门:编号:CX03-03法律法规和其他要求总清单部门:编号:CX03-04合规性评价报告部门:编号:CX03-05危害辨识与风险评价结果一览表部门:编号:CX04-01重大危险源清单部门:编号:CX04-02说明:a、培训;b、施工组织设计、施工方案;c、技术、安全交底;d、监督、指挥;e、规范、标准、管理制度;f、管理方案。
重要环境因素清单部门:编号:CX05-01编制/日期:审核/日期批准/日期环境因素识别、排查表部门:编号:CX05-02排查人:评价人:时间:a、发生频率b、排放值与法规标准值之比c、影响范围及程度d、环境影响的可恢复性或持续性e、公众和媒介的关注程度x=am,m=b、c、d、e中的最大值水量消耗节超情况报表部门:编号:CX05-03填报单位:年月计量单位:立方米(m3)单位负责人:制表:填表日期:年月日电量消耗节超情况报表部门:编号:CX05-04单位负责人:制表:填表日期:年月信息交流记录表部门:编号:CX06-01信息交流登记台帐部门:编号:CX06-02年度培训计划编号:CX07-01年月日日期:日期:日期:培训申请表部门:编号:CX07-02外部培训申请表部门:编号:CX07-03培训签到表部门:编号:CX07-04。
HSE全部记录表

健康、安全及环境管理体系记录清单及表样XX有限公司HSE记录清单编号:QPCCCL/HSE—JL—CX—01—01作业活动危害分析记录表作业活动:区域/部位/设备:分析人员:审核人:日期:年月日7 / 130QPCCCL/HSE—JL—CX—01—02安全检查表部门:设备设施:区域:交叉作业:安全资格证:检查人员:审核人:日期:8 / 130QPCCCL/HSE—JL—CX—01—03危险源调查及其风险评价表填报单位:填报人:审核人:9 / 130QPCCCL/HSE—JL—CX—01—04QPCCCL/HSE—JL—CX—02—01环境因素调查登记表QPCCCL/HSE—JL—CX—02—03重要环境因素及控制措施汇总表QPCCCL/HSE—JL—CX—03—01QPCCCL/HSE—JL—CX—03—02适用的法律、法规和其他要求清单重要环境因素法规对照表批准日期:编制日期:QPCCCL/HSE—JL—CX—04—02管理方案编号:中高度风险(重要环境因素):依据法规:项目:起止日期目标:资金责任部门:相关部门措施:123实施计划说明:编制:审核:批准:年月日QPCCCL/HSE—JL—CX—04—03目标、指标、管理方案实施情况检查表检查人:21 / 130QPCCCL/HSE—JL—CX—05—01 HSE培训需求调查表22 / 130QPCCCL/HSE—JL—CX—05—02HSE年度培训计划编号:编制/日期:批准/日期:23 / 13024 / 130QPCCCL/HSE—JL—CX—05—03QPCCCL/HSE—JL—CX—05—04会议(培训)签到表QPCCCL/HSE—JL—CX—05—05 HSE培训考核记录表编号:培训效果评估表QPCCCL/HSE—JL—CX—05—07新员工安全教育卡说明:1、公司级安全教育由安全环保科组织并实施;部门(车间)级安全教育由各个部门(车间)实施;班组级安全教育由各部门组织实施。
核查记录表

查记录清单:共43种记录,在记录清单中规定了保存期限、保管部门和记录编号。保存时用档案袋分类保管,封面有索引目录,便于检索。保护良好。
→查文件内容的清晰明确情况
抽查到《环境与职业健康安全管理手册》、《程序文件汇编》内容清晰、明确,无涂改现象,保持完好。
→查作废文件的管理
查到《文件/记录回收处理记录》,目前无作废文件.
→查文件的保管
在人事办/安全管理办查到各文件保管完好。
公司建立了《记录和资料管理控制程序》XP-02,明确了记录管理的职责,规定了记录的填写、标识、收集、保管、检索、保存期限和处置的规定。
审核内容、方法
审核记录
结果
5.1
7.5.1
7.5.2
5.2
5.4.1
8.1
7.4
9.3
7.1.2
7.1.4
7.1.4
8.1
请介绍部门分管的区域和职责,人员的分工。
公司有哪些文件,包括法律法规,检查现场文件的使用情况,是否使用的有效文件,有无作废文件,作废文件的标识是否清楚。文件是如何保管的。
公司以及部门工作中都有哪些记录产生,检查记录的保存期限、保管人是如何规定的?抽查数份记录,检查其填写是否清楚、真实、及时、正确;保存是否良好,利于检索。
3.管理制度/程序文件,公司以程序文件的形式体现,共有程序文件:17个;
4.管理制度/程序文件的支持性文件:公司作业指导书、管理制》XP-CX-01,明确了文件的管理的范围、职责、流程和方法。
→查文件的批准
在人事办/安全管理办抽查到ES手册和程序文件均经过总经理批准;
3、C版管理评审控制程序(CX03)15-22

标准要求(5.6)管理评审控制程序文件编号:JDFDC/CX031.目的为确保公司质量管理体系的正常运行,保持其特有的适宜性、充分性和有效性,以保证公司质量方针、目标的实现,特制定本程序。
2.适用范围本程序适用于公司最高管理者主持公司各部室对公司质量管理体系运行的适宜性、充分性、有效性的评审。
3.职责3.1公司总经理全面负责主持质量管理体系的评审工作。
3.2体系办公室负责评审的准备工作,编制评审方案、评审计划和评审报告以及措施的跟踪。
3.3各部室按照职能分配表承担的职责和权限提前准备体系运行总结报告和参加评审会议。
4.程序内容4.1管理评审时间安排4.1.1管理评审每年(间隔12个月)至少进行一次,均在内部审核之后进行。
4.1.2如遇以下情况,由总经理决定适时进行管理评审:a)公司组织结构有重大调整;b)公司质量方针及目标需要重大调整时;c)发生重大质量事故或业主有重大质量投诉时;d)ISO9001标准换版和公司体系文件换版时;e)经营管理有重大变化及市场客户有重大调整及变化时;f)针对内部审核结果总经理认为有必要时;g)法律法规发生变化时。
4.2评审输入a)上一次管理评审后对其问题及实施改进的效果;b)内部、外部审核结果的分析;c)售后服务质量及用户满意度情况分析;d)质量方针和质量目标的适宜性及实施情况;e)建筑产品质量状况;f)组织机构和岗位的适宜性;g)纠正/预防措施的落实情况;h)经营的业绩稳定度的评价;i)管理体系文件的符合性和适宜性;j)改进的建议。
4.3管理评审的实施4.3.1体系办公室制定《管理评审方案》﹙JDFDC/CX03-JLO6﹚、《管理评审计划》(JDFDC/CX03-JL01),其内容包括:评审内容、时间安排、参加部门人员、评审方式、管理者代表和各部门需要准备的汇报材料。
4.3.2《管理评审方案》经管理者代表审核后报总经理批准后发放并实施。
4.3.3《管理评审计划》(JDFDC/CX03-JL01)经管理者代表审核,总经理批准后由体系办公室于评审前一周发至各相关部门。
